
- •Методическое пособие Самостоятельная внеаудиторная работа по дисциплине «Химия» для технических специальностей
- •Раздел 1 общая и неорганическая химия Тема 1.1 Основные понятия и законы химии
- •Задание №1. Составьте схему электронного строения, электронную и графическую формулы атомов следующих элементов:
- •Тема 1.3 Строение вещества
- •Тема 1.4 Вода. Растворы. Электролитическая диссоциация
- •Тема 1.5 Классификация неорганических соединений и их свойства
- •Классификация солей
- •Тема 1.6 Химические реакции
- •Правило смещения химического равновесия под влиянием внешних условий Ле Шателье (1884 г.)
- •Задание №2. При повышении температуры на 10ºС скорость химической реакции возрастает в 2 раза. При 20ºС она равна 0,04 . Какова будет скорость этой реакции при: а) 40ºС, б) 10ºС, в) 0ºС, г) 20ºС?
- •Задание №5. Напишите электронные уравнения, расставьте коэффициенты и укажите восстановитель и окислитель в следующих реакциях:
- •Тема 1.7 Металлы и неметаллы
- •1) Металлы реагируют с простыми веществами:
- •Положение в периодической системе
- •1) Взаимодействие неметаллов с простыми веществами
- •2) Взаимодействие со сложными веществами:
- •Задание №1. Напишите уравнение реакций, с помощью которых можно осуществить следующие превращения:
- •Задание №2.Составьте уравнение овр с участием галогенов:
- •Задание №3.Напишите уравнения реакций, с помощью которых можно осуществить цепь следующих превращений:
- •Раздел 2 органическая химия
- •Тема 2.1 Основные понятия органической химии и теория строения органических соединений
- •Тема 2.2 Углеводороды и их природные источники
- •Тема 2.3 Кислородосодержащие органические соединения
- •Тема 2.4 Азотсодержащие органические соединения. Полимеры
- •Раздел 1 «Общая и неорганическая химия»
- •1 Семестр
- •1 Семестр
- •Раздел 2 «Органическая химия»
- •2 Семестр
- •2 Семестр
- •Список использованных источников
Тема 1.6 Химические реакции
Зависимость скорости химической реакции от различных факторов:
1. Скорость химической реакции зависит от концентрации реагирующих веществ.
Закон действующих масс (1867г., Гульдберг, Вааге) для гомогенных систем звучит так:
При постоянной температуре скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ.
![]() ,
,
где а, b – коэффициенты уравнения реакции, k – константа cкорости
3Н2+N2
®
2NH3,
![]() ,
,
Если концентрация водорода увеличится в 3 раза, то скорость возрастёт в 27 раз.
2. Скорость реакции зависит от природы реагирующих веществ.
3. Скорость реакции зависит от температуры (Правило Вант-Гоффа):
При повышении температуры на 10°С скорость гомогенной реакции возрастает от двух до четырех раз
![]()
где g - температурный коэффициент скорости, т.е. число, характеризующее ускорение реакции при нагревании на 10°С.
4. Скорость гетерогенных реакций зависит от площади поверхности соприкосновения реагирующих веществ.
5. Скорость реакции зависит от наличия катализатора.
Правило смещения химического равновесия под влиянием внешних условий Ле Шателье (1884 г.)
Если на систему, находящуюся в равновесии, оказывается внешнее воздействия (изменение С, р, t), то химическое равновесие смещается в ту сторону, которая ослабляет данное воздействие.
Следствия принципа Ле Шателье:
1) при повышении концентрации (С) реагирующего вещества равновесие смещается в сторону образования продуктов реакции,
2) при повышении давления химическое равновесие смещается в сторону той реакции, при которой объем образующихся газов уменьшается,
3) при повышении температуры химическое равновесие смещается в сторону эндотермической реакции,
4) при понижении температуры химическое равновесие смещается в сторону экзотермического процесса.
Алгоритм расчета количества теплоты по термохимическим уравнениям реакции
1. Записать условие задачи.
2. Записать термохимическое уравнение.
3. Подписать формулы веществ известных исходных данных.
4. Над подчеркнутой формулой указать исходные данные, под формулой числовые значения.
5. Рассчитать исходное количество теплоты в кДж.
6. Записать ответ.
Пример: Вычислить, какое количество теплоты выделится при сгорании 6,2 г фосфора.
Термохимическое уравнение реакции:
4Р(тв) +5О2(газ)® 2Р2О5 (тв)+ 3010 кДж
Дано: Решение:
т
 (Р)=6,2
г 6,2г
Q
(Р)=6,2
г 6,2г
Q
Найти: 4Р + 5O2 ® 2Р2O5 + 3010кДж
Q-? 4×31г\моль
![]()
Задание №1. Химической реакции в растворе отвечает уравнение: А+В=С. Как изменится скорость реакции если: а) концентрацию А увеличить в 2 раза, оставив концентрацию В прежней, б) концентрацию одного из веществ увеличить в 2 раза, а другого – в 2 раза уменьшить.
Задание №2. При повышении температуры на 10ºС скорость химической реакции возрастает в 2 раза. При 20ºС она равна 0,04 . Какова будет скорость этой реакции при: а) 40ºС, б) 10ºС, в) 0ºС, г) 20ºС?
Задание
№3. В какую сторону сместится равновесие
системы (влево или вправо) 2SO2+O2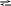 2SO3+Q
2SO3+Q
а) при повышении температуры,
б) при повышении давления.
Задание №4. Вычислите, какое количество теплоты поглощается при окислении 14г азота. Термохимическое уравнение реакции окисления азота:
N2+O2=2NO-180, 8 кДж.
