
- •Методическое пособие Самостоятельная внеаудиторная работа по дисциплине «Химия» для технических специальностей
- •Раздел 1 общая и неорганическая химия Тема 1.1 Основные понятия и законы химии
- •Задание №1. Составьте схему электронного строения, электронную и графическую формулы атомов следующих элементов:
- •Тема 1.3 Строение вещества
- •Тема 1.4 Вода. Растворы. Электролитическая диссоциация
- •Тема 1.5 Классификация неорганических соединений и их свойства
- •Классификация солей
- •Тема 1.6 Химические реакции
- •Правило смещения химического равновесия под влиянием внешних условий Ле Шателье (1884 г.)
- •Задание №2. При повышении температуры на 10ºС скорость химической реакции возрастает в 2 раза. При 20ºС она равна 0,04 . Какова будет скорость этой реакции при: а) 40ºС, б) 10ºС, в) 0ºС, г) 20ºС?
- •Задание №5. Напишите электронные уравнения, расставьте коэффициенты и укажите восстановитель и окислитель в следующих реакциях:
- •Тема 1.7 Металлы и неметаллы
- •1) Металлы реагируют с простыми веществами:
- •Положение в периодической системе
- •1) Взаимодействие неметаллов с простыми веществами
- •2) Взаимодействие со сложными веществами:
- •Задание №1. Напишите уравнение реакций, с помощью которых можно осуществить следующие превращения:
- •Задание №2.Составьте уравнение овр с участием галогенов:
- •Задание №3.Напишите уравнения реакций, с помощью которых можно осуществить цепь следующих превращений:
- •Раздел 2 органическая химия
- •Тема 2.1 Основные понятия органической химии и теория строения органических соединений
- •Тема 2.2 Углеводороды и их природные источники
- •Тема 2.3 Кислородосодержащие органические соединения
- •Тема 2.4 Азотсодержащие органические соединения. Полимеры
- •Раздел 1 «Общая и неорганическая химия»
- •1 Семестр
- •1 Семестр
- •Раздел 2 «Органическая химия»
- •2 Семестр
- •2 Семестр
- •Список использованных источников
Тема 1.4 Вода. Растворы. Электролитическая диссоциация
Концентрация раствора – численная величина, которая показывает содержание растворенного вещества в определенном количестве или объеме раствора.
Массовая доля растворенного вещества – это отношение массы растворенного вещества к общей массе раствора.
![]()
Согласно теории электролитической диссоциации С.Аррениус (1887г.) при растворении в воде электролиты распадаются на свободные ионы.
![]()
Проводниками электрического тока растворы веществ становятся, когда они содержат ионы, которые в электрическом поле приходят в направленное движение.
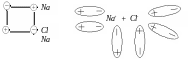
Электролитическая диссоциация – распад электролита на сольватированные (гидратированные) ионы под действием молекул растворителя.
AlCl3 → Al + 3Cl
Р еакциями
ионного обмена
- реакции между ионами. Эти реакции
протекают в растворах и не сопровождаются
изменением степеней
окисления реагирующих веществ.
еакциями
ионного обмена
- реакции между ионами. Эти реакции
протекают в растворах и не сопровождаются
изменением степеней
окисления реагирующих веществ.
Правило Бертолле:
РИО протекает необратимо в случае, если:
1) образуется твердое труднорастворимое вещество - осадок (¯),
2) выделяется летучее вещество - газ (),
3) образуется малодиссоциирующее соединение (слабые электролиты, в том числе Н2О).
Пример РИО:
Al2(SO4)3+3BaCl2 = 2AlCl3+3BaSO4¯ - молекулярная формула
Р р р н
![]()
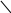 -полное
ионное уравнение
-полное
ионное уравнение
![]() - сокращенное
ионное уравнение.
- сокращенное
ионное уравнение.
Десятичный логарифм концентрации ионов водорода, взятый с обратным знаком, называется водородным показателем.
рН = -lg[Н+] – водородной показатель
10° 107 1014


рН 0 7 14
среда кислая нейтральная щелочная
![]() - среда нейтральная
- среда нейтральная
![]() -
среда кислая
-
среда кислая
![]()
 -
среда щелочная.
-
среда щелочная.
Задание №1. Напишите уравнения диссоциации:
а) нитрата калия, б) хлорида кальция, в) сульфата натрия,
г) йодоводорода, д) гидроксида калия, е) серной кислоты.
Задание №2. Напишите в ионной форме уравнения реакций, представленных следующими схемами:
а) Ca(NO3)2+K2CO3→, б) CaCO3+НNO3 →, в) NaOH+ H2SO4→,
г) MgCO3 + H2SO4 →.
Задание №3. Вычислите массовую долю гидроксида натрия в растворе, полученном растворением 10 граммов NaOH в:
а) 40 г, б) 50 г, в) 250 г, г) 120 г воды.
Задание №4. Вычислите массы карбоната натрия и воды, необходимые для приготовления 50 г. 5-процентного раствора карбоната натрия.
Тема 1.5 Классификация неорганических соединений и их свойства
Оксиды – это сложные вещества, состоящие из атомов кислорода и какого-нибудь другого химического элемента. Оксиды образуют все химические элементы, кроме He, Ne, Ar.
Для составления названия оксида нужно:
1) указать слово «оксид», а затем в родительном падеже название второго элемента: Na2О – оксид натрия
2) если химический элемент может образовать несколько оксидов, то после названия элементов в скобках указывают его валентность: FeO – оксид железа (II), Fe2O3 – оксид железа (III). При написании формул оксидов кислород всегда ставят на второе место, кроме OF2.
Основания – это сложные вещества, которые состоят из атомов металла и одной или нескольких гидроксогрупп Ме(ОН)Х. В названиях оснований в начале указывают слово «гидроксид», а затем название металла, и если металл имеет переменную валентность, то в скобках указывают его валентность: CuOH – гидроксид меди (I), Cu(ОН)2 – гидроксид меди (II).
Щелочи - растворимые в воде основания (NaOH).
Кислоты – это сложные вещества, содержащие в своем составе водород, способный замещаться металлом и образовать соли.
1) Название бескислородной кислоты состоит из названия неметалла с добавлением буквы «-о-» и слова «водородная». H2S – сероводородная кислота.
2) Название
кислородосодержащей кислоты зависит
от валентности элемента, образующего
кислоту: если кислота содержит элемент
с высшей валентностью, но название
состоит из названия этого элемента и
окончания « -ная» или «-вая».
![]() –
серная
кислота.
–
серная
кислота.
3) Название кислоты,
которая содержит элемент с меньшей
валентностью, имеет окончание « -истая».
![]() -
сернистая
кислота.
-
сернистая
кислота.
Соли – сложные вещества, продукт полного или частичного замещения атомов водорода в молекуле кислот на металл или же продукт полного или частичного замещения гидроксогруппы в основании на кислотный остаток.
