- •Методическое пособие Самостоятельная внеаудиторная работа по дисциплине «Химия» для технических специальностей
- •Раздел 1 общая и неорганическая химия Тема 1.1 Основные понятия и законы химии
- •Задание №1. Составьте схему электронного строения, электронную и графическую формулы атомов следующих элементов:
- •Тема 1.3 Строение вещества
- •Тема 1.4 Вода. Растворы. Электролитическая диссоциация
- •Тема 1.5 Классификация неорганических соединений и их свойства
- •Классификация солей
- •Тема 1.6 Химические реакции
- •Правило смещения химического равновесия под влиянием внешних условий Ле Шателье (1884 г.)
- •Задание №2. При повышении температуры на 10ºС скорость химической реакции возрастает в 2 раза. При 20ºС она равна 0,04 . Какова будет скорость этой реакции при: а) 40ºС, б) 10ºС, в) 0ºС, г) 20ºС?
- •Задание №5. Напишите электронные уравнения, расставьте коэффициенты и укажите восстановитель и окислитель в следующих реакциях:
- •Тема 1.7 Металлы и неметаллы
- •1) Металлы реагируют с простыми веществами:
- •Положение в периодической системе
- •1) Взаимодействие неметаллов с простыми веществами
- •2) Взаимодействие со сложными веществами:
- •Задание №1. Напишите уравнение реакций, с помощью которых можно осуществить следующие превращения:
- •Задание №2.Составьте уравнение овр с участием галогенов:
- •Задание №3.Напишите уравнения реакций, с помощью которых можно осуществить цепь следующих превращений:
- •Раздел 2 органическая химия
- •Тема 2.1 Основные понятия органической химии и теория строения органических соединений
- •Тема 2.2 Углеводороды и их природные источники
- •Тема 2.3 Кислородосодержащие органические соединения
- •Тема 2.4 Азотсодержащие органические соединения. Полимеры
- •Раздел 1 «Общая и неорганическая химия»
- •1 Семестр
- •1 Семестр
- •Раздел 2 «Органическая химия»
- •2 Семестр
- •2 Семестр
- •Список использованных источников
Раздел 1 общая и неорганическая химия Тема 1.1 Основные понятия и законы химии
Относительная молекулярная масса (Mr) – безразмерная величина, равная отношению абсолютной массы молекулы к 1/12 массе атома 12С углерода. Относительная молекулярная масса вещества равна сумме относительных атомных масс всех элементов с учетом индексов.
Молярная масса вещества (М) – отношение массы вещества к количеству вещества. Она показывает массу 1 моля вещества.
![]() ,
где ν
(n)–
количество вещества.
,
где ν
(n)–
количество вещества.
Количество вещества (ν, n) означает определенное число структурных элементов (молекул, атомов, ионов).
Моль – единица количества, содержащая столько же структурных единиц данного вещества, сколько атомов содержится в 12 г С, состоящего только из изотопа 12С.
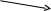 ν
ν
![]()
![]()
![]()
Постоянная Авогадро (NA) – число частиц в одном моле любого вещества одно и тоже и равно 6,02∙1023 моль –1
Молярный объем
газов –
отношение объема газа к количеству
вещества,
![]() ,
при нормальных условиях t
= 273 К,
р = 101 кПа, Vm
= 22,4 л/моль
,
при нормальных условиях t
= 273 К,
р = 101 кПа, Vm
= 22,4 л/моль
Относительная плотность газов (Д) – безразмерная величина, являющаяся отношением молярных масс равных объемов разных газов. Она показывает, во сколько раз 1 моль одного газа тяжелее (или легче) 1 моля другого газа. Плотности газов относятся друг к другу как их молярные массы.
![]()
Задание №1 Чему равна относительная молекулярная масса? Найдите Mr следующих веществ: NaNO3; K2SO4; NH4NO2; Al(OH)3; KAl(SO4)2 .
Задание №2. Какую массу будут иметь 0,24 моль следующих веществ: а) хлорида натрия, б) оксида алюминия, в) гидроксида калия, г) сульфата бария.
Задание №3. Определите массовые доли элементов в следующих соединениях:
а) CaCl2, б) H2SO4 , в) FeCl2 , г) MgCO3 , д) KHS, е) Mn2O7 .
Задание №4. Водород и кремний соединяются в массовом отношении 1:7. Определите формулу этого соединения H и Si.
Задание №5. Плотность газа по воздуху равна 1,17. Определите молярную массу газа.
Тема 1.2 Периодический закон и Периодическая система химических элементов Д.И. Менделеева и строение атома
Современная формулировка периодического закона: свойства химических элементов находятся в периодической зависимости от заряда их атомных ядер.
По мере возрастания зарядов ядер атомов химических элементов периодически изменяется строение их электронных оболочек, что является причиной периодических изменений свойств элементов.
Основные положения современной теории строения атом:
1. атом – электронейтрален,
2. ядро состоит из протонов (р) m=1, q=+1, нейтронов (n) m=1, q=0
число р = порядковый № химического элемента
Порядковый номер химического элемента = число l и p. Число нейтронов (n) = относительная атомная масса (Ar) – число протонов (р).
3. вокруг ядра по сложным орбитам вращаются электроны.
число l = порядковый номер химического элемента, m = 0, q= -1.
В 1927 г. В. Гейзенберг сформулировал принцип неопределенности: невозможно установить местонахождение электрона в атоме, и строго определенная орбита для него никогда не может стать физической реальностью.
4. электронная оболочка любого атома – сложная система, она делится на энергетические уровни, отличающиеся друг от друга расстоянием от ядра и запасом энергии.
число уровней = № периода
-
1
2
3
4
5
6
7
K
L
M
N
O
P
Q
N = максимальное число электронов в квантовом слое = 2n2
где n – целое число, обозначающее № энергетического уровня – главное квантовое число
I период N=2∙12=2l s
II период N=2∙22=8l s p
III период N=2∙32=18l s p d
IV период N=2∙42=32l s p d f
2 6 10 14 электронов
5
 .
энергетические уровни делятся на
подуровни, отличающиеся по формам и
размерам
.
энергетические уровни делятся на
подуровни, отличающиеся по формам и
размерам
s Å p d f
максимальное количество электронов на энергетическом подуровне:
s2 p6 d10 f14
Орбиталь –.область возможного нахождения электрона вокруг атомного ядра, совокупность положений электрона в атоме.
Квантовая механика вводит понятие электронного облака, то есть заряд электрона размазывается, расплывается по всему объему этого облака. Электронные облака имеют разные геометрические формы.
6. на каждой атомной орбитали может разместиться только 2l с противоположными спинами (веретено) – принцип Паули. Он установил, что в атоме не может быть двух электронов с одинаковыми значениями всех 4 квантовых чисел.
7. электроны заполняют атомные орбитали, начиная с подуровней с наименьшей энергией (принцип минимума энергии).
1s<2s<2p<3s<3p<4s£3d<4p<5s …(ряд В. Клечковского).
8. При наличии свободных орбиталей с одинаковым запасом энергии, каждая орбиталь заполняется вначале наполовину электронами с одинаковыми спинами, а затем полностью с образованием электронной пары, так чтобы их сумма была максимальной (правило Гунда).