
- •Позааудиторна самостійна робота №1
- •Методичні рекомендації
- •Позааудиторна самостійна робота № 2
- •Методичні рекомендації
- •І рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 3
- •Методичні рекомендації
- •І рівень
- •І рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота №5
- •Значення рН деяких фізіологічних рідин організму
- •Теорії кислот та основ.
- •Методичні рекомендації
- •Рівень і
- •Рівень іі
- •Рівень ііі
- •Позааудиторна самостійна робота № 6
- •Методичні рекомендації
- •І рівень
- •Іі рівень
- •Позааудиторна самостійна робота № 7
- •Хід роботи
- •Індивідуальний добовий харчовий раціон
- •Дані про хімічний склад та енергетичну цінність харчових продуктів
- •Методичні рекомендації
- •Тести для самоконтролю і рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 8
- •Застосування ферментних препаратів у медицині
- •Методичні рекомендації
- •Рівень і
- •Рівень іі
- •Рівень ііі
- •Позааудиторна самостійна робота № 9
- •Йонний склад нервової клітини
- •Позааудиторна самостійна робота № 10
- •Позааудиторна самостійна робота № 11
- •Тести для самоконтролю і рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 12
- •Тести для самоконтролю і рівень
- •Позааудиторна самостійна робота № 13
- •Способи одержання аерозолів.
- •Методи визначення типу емульсій
- •І рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 14
- •Тести для самоперевірки і рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 15
- •Електронна конфігурація атома Карбону
- •Будова молекули метану
- •-Електронна хмара зв’язку Геометрія молекули
- •Будова молекул альдегідів
- •Будова молекул карбонових кислот
- •І рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 16
- •Методичні рекомендації
- •І рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота №17
- •Методичні рекомендації
- •Тести для самоконтролю і рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 18
- •Методичні рекомендації
- •Тести для самоконтролю і рівень
- •Тести для самоконтролю і рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 20
- •Типи зв’язків у білкових молекулах
- •Ковалентні зв’язки
- •Тести для самоконтролю і рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 21
- •Тести для самоконтролю і рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 22
- •П’ятичленні гетероцикли з одним гетероатомом
- •П’ятичленні гетероцикли з двома гетероатомами
- •Шестичленні гетероцикли
- •Тести для самоконтролю і рівень
- •Іі рівень
- •Ііі рівень
- •Позааудиторна самостійна робота № 23
- •Мал.20.Схема подвійної спіралі днк та її реплікації. Методичні рекомендації
- •Тести для самоконтролю і рівень
- •Іі рівень
- •Ііі рівень
Тести для самоконтролю і рівень
1. Вказати метод хроматографії, який належить до рідинної:
а) паперова; б) афінна; в) тонкошарова; г) газова.
2. За формою проведення процесу розрізняють такі види хроматографії:
а) колонкову; б) капілярну; в) паперову; г) хемосорбційну.
3. Паперову хроматографію поділяють на:
а)афінну; б) розподільну; в) адсорбційну; г) капілярну.
Іі рівень
4.Як експрес – методи використовують:
а) молекулярно – ситову; б) паперову;
в) осадову; г) тонкошарову хроматографії.
5. Хроматографічний метод базується на дослідженні сумішей за допомогою:
а) сорбційних процесів; б) осмотичного тиску;
в) різниці потенціалів; г) різниці температур.
Ііі рівень
У паперовій хроматографії як нерухому фазу використовують:
а) газову колонку; б) скляну пластинку;
в) хроматографічний папір; г) металеву пластинку.
Молекулярно – ситову хроматографію використовують для:
а) виділення і очищення полімерів;
б) визначення молекулярної маси білка;
в) визначення рівня холестерину в крові.
Позааудиторна самостійна робота № 12
Тема: Електрокінетичний потенціал. Електроосмос, електрофорез. Застосування електрокінетичних явищ в медицині.
План
1. Поняття про електрокінетичні явища, їх класифікація.
2. Механізм виникнення електрофорезу та його застосування в медичній практиці.
3. Механізм виникнення електроосмосу та його застосування в медицині.
4. Потенціали течії та седиментації.
Час виконання: 2 години.
Мета роботи: Ознайомитися з електрокінетичними явищами першого та другого роду та їх застосуванням у медичній практиці.
Електрокінетичними називають явища, які грунтуються на взаємозв'язку між електричними та кінетичними властивостями дисперсних систем. Вони полягають у тому, що складові дисперсної системи (дисперсна фаза або дисперсійне середовище) рухаються в електричному полі, або, навпаки, виникає різниця потенціалів під час переміщення частинок або рідини.
Усі електрокінетичні явища пов'язані з існуванням на межі поділу фаз подвійного електричного шару. Їх класифікують таким чином.
1. Електрокінетичні явища першого роду, які пов'язані з переміщенням в електричному полі складових дисперсної системи (дисперсної фази або дисперсійного середовища).До них належать: а) електрофорез;б) електроосмос.
2. Електрокінетичні явища другого роду, які пов'язані з виникненням різниці потенціалів під час переміщення частинок твердої фази (потенціал седиментації або осідання) або рідкого дисперсійного середовища (потенціал течії або перебігу). Це процеси, обернені до електрофорезу та електроосмосу.
Швидкість
руху частинок в електричному полі
залежить від величини їх заряду. Тому
наведені вище електрокінетичні явища
дають змогу виміряти величину
![]() -потенціалу.
-потенціалу.
Наявність електричного заряду у частинок дисперсних систем і електрокінетичні явища були вперше виявлені професором Московського університету Ф. Рейссом 1808 року.
Електрофорез. Електрофорез - це спрямоване переміщення частинок дисперсної фази у постійному електричному полі відносно нерухомого дисперсійного середовища. Вивчаючи електроліз води, Ф. Рейсс пропускав постійний електричний струм у приладі, який складався з двох скляних трубок, заповнених водою, занурених у шар вологої глини (рис.8 а).
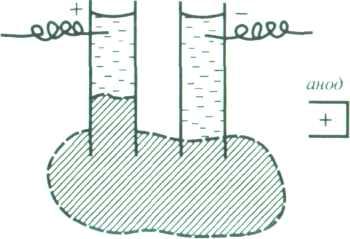
а б
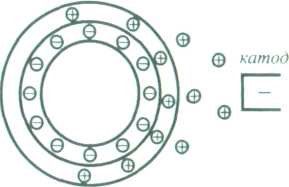
Рис. 8.Схема досліду Рейсса з електрофорезу (а) і рух частинок під
час електрофорезу (б)
При цьому він спостерігав помутніння рідини в трубці з позитивним електродом, очевидно за рахунок переміщення негативно заряджених частинок дисперсної фази (глини) до анода. Таке явище було назване електрофорезом.
Рухливість частинок в електричному полі зумовлена тим, що за умови накладання зовнішньої різниці потенціалів розривається ПЕШ на межі "ковзання", в результаті чого частинка набуває певного заряду і рухається до електрода, знак заряду якого протилежний до заряду частинки. При цьому протиіони дифузного шару переміщуються до протилежно зарядженого електрода (рис.8, б).
Швидкість руху частинок дисперсної фази пропорційна величині їх електрокінетичного потенціалу. Тому, спостерігаючи електрофоретичний рух частинок, можна визначити знак заряду частинок дисперсної фази і величину потенціалу.
За
рівнянням
Гельмгольца-
Смолуховського
,
лінійна
швидкість руху частинок (U0)
прямо пропорційна діелектричній
проникності середовища (![]() ),
величині
-потенціалу,
напруженості
електричного поля (градієнта
потенціалу) (H) і
обернено
пропорційна в'язкості середовища (
),
величині
-потенціалу,
напруженості
електричного поля (градієнта
потенціалу) (H) і
обернено
пропорційна в'язкості середовища (
![]() ):
):
Uo
=
![]()
![]() ,
,
де о - коефіцієнт пропорційності, який дорівнює діелектричній проникності вакууму (8,85 10-12Ф/м).
Оскільки лінійна швидкість змінюється пропорційно до напруженості електричного поля, було введено поняття електрофоретичної рухливості (Uефр) Електрофоретична рухливість дорівнює швидкості руху частинок за градієнта потенціалу 1 В/м:
Uефр
=
![]()
Якщо уявити лінійну швидкість Uo як відношення лінійного зміщення межі золю (S) до часу експерименту ( ):
Uo =S/ ,
а градієнт потенціалу H як відношення напруги зовнішнього поля (Е) до відстані між електродами (l):
Н = Е/1,
то електрофоретичну рухливість в експерименті можна обчислити за такою формулою:
Uефр
=
![]() .
.
З іншого боку,
Uефр
=
=
![]() .
.
Тому
= .
Звідси одержуємо формулу для обчислення -потенціалу методом електрофорезу:
![]() =
=
![]()
Рівняння Гельмгольца - Смолуховського можна застосовувати тоді, коли розміри частинок значно перевищують товщину подвійного електричного шару. Тому воно придатне для визначення характеристики еритроцитів, лейкоцитів, мікроорганізмів та інших мікроскопічних біологічних об'єктів. Для білкових молекул і колоїдних частинок, розмір яких співмірний з товщиною ПЕШ, електрофоретична рухливість залежить від їх розмірів та форми.
Методика проведення електрофорезу. Експериментально електрофорез проводять у приладі, який є U-подібною градуйованою трубкою з боковим відростком (рис.9.).
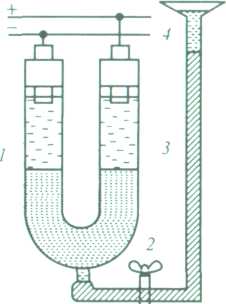
Рис.9. Схема приладу для проведення електрофорезу: 1 -U-подібна трубка; 2 - кран; 3 - гумовий шланг; 4 - скляна лійка
Спочатку в посудину 1 наливають ультрафільтрат допоміжного золю (проміжну рідину) (приблизно 1/3 посудини). Закривають кран 2 і у лійку 4 наливають досліджуваний золь. Обережно відкриваючи кран, випускають забарвлений золь, який займає нижню частину приладу, витісняючи проміжну рідину вверх. Після занурення електродів у рідину кран закривають, вмикають струм і слідкують за переміщенням границі золю S(S =h2 –h1) за певний проміжок часу . Залежно від заряду колоїдних частинок межа золю піднімається до катода чи анода. Обчислюють величину -потенціалу за наведеною вище формулою.
Застосування електрофорезу у медичних дослідженнях
Клітини організму мають різний за величиною заряд, причому кожен тип клітин звичайно характеризується певним, досить стабільним значенням потенціалу. Жива протоплазматична поверхня та всі біологічні поверхні мають негативний заряд. Зокрема, у різних ссавців при рН = 7,4 величина -потенціалу еритроцитів коливається в межах від -7 до -22 мВ. У людини ця величина дорівнює-16,3 мВ.
Низьке значення ізоелектричної точки еритроцитів (рНіет = 1,7), а також їх постійний негативний заряд можна пояснити йонізацією кислотних груп фосфоліпідів на поверхні еритроцитів. Лейкоцити, як і еритроцити, рухаються до анода; їх негативний заряд зумовлений дисоціацією йоногенних груп білків сироватки крові, які адсорбуються на поверхні лейкоцитів.
За електрофоретичною рухливістю клітини крові можна розмістити у такій послідовності: гранулоцити 0,6 ∙ 10-12 м2/ (с ∙В); лімфоцити 0,8 ∙10-12 м2/(с ∙В); еритроцити 1 ∙10-12 м2/(с ∙В).
Впровадження електрофорезу у біохімічні дослідження дало змогу розділити складні суміші біологічних рідин і дослідити їх індивідуальні характеристики, зокрема склад білків сироватки крові та шлункового соку. Серед біологічних рідин найкраще досліджена і викликає найбільший інтерес кров (таблиця 3).
Склад білків плазми крові людини в нормі
Таблиця 3.
-
Білок
Склад, у відсотках
Альбумін
50,0
 -1-глобулін
-1-глобулін4,0
α-2-глобулін
12,0
β-глобулін
13,0
γ-глобулін
13,0
Фібриноген
8,0
одержують електрофореграми, вигляд яких у нормі і за конкретної патології суттєво відрізняється (рис.10).
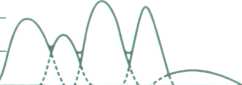
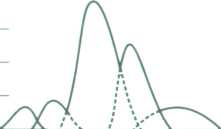
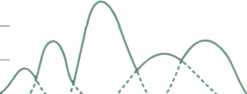
альбумін
а б в
Рис.10. Електрофореграми: а - сироватки крові в нормі; б - при інфекційному гепатиті; в - при ліпідному нефрозі
Таким чином, електрофореграми можуть використовуватись як з діагностичною метою, так і для контролю за нормалізацією складу крові у процесі лікування.
Електрофоретичні методи належать до кращих сучасних способів розділення нуклеїнових кислот, амінокислот, антибіотиків, ферментів, стеринів та методів контролю чистоти лікарських речовин. Електрофорез широко застосовують у техніці для нанесення декоративних антикорозійних або електроізоляційних плівок на поверхню металу, при одержанні напівпровідникових плівок. Цей метод лежить в основі роботи електрофільтрів для уловлювання цінних відходів виробництва та очищення виробничих газів.
Електрофорез - один із фізіотерапевтичних методів лікування, що ґрунтується на безпосередньому введенні лікарських препаратів в уражену ділянку організму крізь шкіру або слизові оболонки. З цією метою прокладку активного електрода змочують розчином необхідного лікарського засобу. Речовину вводять з того електрода, заряд якого вона має: аніони вводять з катода, а катіони - з анода.
Серед сучасних видів електрофорезу слід виділити гель-електрофорез, імуноелектрофорез, диск-електрофорез, ізотахофорез тощо. На рис. 10 зображені електрофореграми, одержані методом гель-електрофорезу.
Електроосмос. Електроосмос - це спрямоване переміщення під дією постійного електричного поля дисперсійного середовища відносно нерухомої дисперсної фази. Як і електрофорез, вперше це явище спостерігав Ф. Рейсс у такому досліді (рис.11, а):
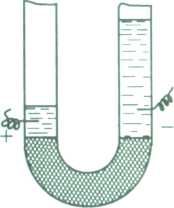
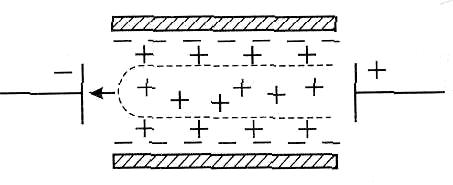
.+.____+. а б
Рис.11. Дослід Рейсса з електроосмосу (а) і рух рідини при електроосмосі (б)
При пропусканні постійного електричного струму в U-подібній трубці, яка заповнена кварцовим піском і водою, біля негативно зарядженого електрода (катода) рівень води підвищувався, а у другому коліні - знижувався. Рух рідини відбувався доти, поки не встановлювалась певна різниця рівнів рідини в U- подібній грубці (рівновага з гідростатичним тиском). Оскільки без поруватої діафрагми переміщення рідини не відбувалось, то Ф. Рейсс дійшов висновку, що при контакті з частинками кварцового піску рідина набувала заряду.
Механізм електроосмосу можна пояснити таким чином (рис.11, б). На внутрішній поверхні капілярів поруватої мембрани виникає подвійний електричний шар. Під дією зовнішнього електричного поля протиіони дифузного шару рухаються до відповідного електрода, захоплюючи частину дисперсійного середовища. При цьому рух відбувається по "поверхні ковзання" відносно нерухомого адсорбційного шару.
Метод електроосмосу мас широке практичне застосування у процесах зневоднення поруватих матеріалів і концентруванні колоїдних систем, для просочування поруватих матеріалів розчинами речовин, які поліпшують їх якість. У медицині його використовують для зневоднення перев'язувального матеріалу.
Потенціали течії і седиментації. У другій половині XIX ст. були відкриті ще два електрокінетичні явища, які протилежні до електрофорезу та електроосмосу.
У 1859 р. Квінке виявив, що при протіканні рідини крізь порувату мембрану виникає різниця потенціалів, яку назвали потенціалом течії або перебігу (рис.12, а). Потенціал течії (перебігу) - це різниця потенціалів, що виникає під час руху дисперсійного середовища відносно нерухомої дисперсної фази.
Це явище пояснюється тим, що в результаті руху рідини під дією гідростатичного тиску крізь капіляри або пори, стінки яких мають електричний заряд, деформується подвійний електричний шар і йони дифузного шару зміщуються у напрямку руху рідини. Перенесення зарядів є причиною виникнення на кінцях капілярів мембрани різниці потенціалів-потенціалу перебігу. Останній є причиною виникнення біопотенціалів. При протіканні крові по капілярах кровоносної системи виникає потенціал перебігу, який фіксується Q-зубцем на кардіограмі людини.
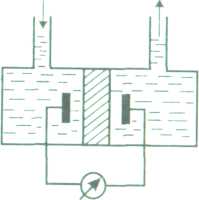
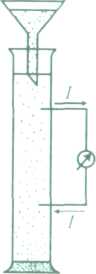
Рис.12. Схема експериментів Квінке потенціалу течії (а) та Дорна з
потенціалу седиментації (б)
У 1878 р. Г. Дорн спостерігав явище, протилежне електрофорезу-виникнення потенціалу седиментації (осідання) - різниці потенціалів, що виникає в процесі осідання частинок дисперсної фази у нерухомому дисперсійному середовищі (рис. 12, б). Суть його полягає в тому, що при осіданні частинок дисперсної фази (наприклад, кварцу) у воді під дією сили тяжіння виникає різниця потенціалів між верхніми і нижніми шарами гетерогенної системи. Ефект Дорна також зумовлений деформацією подвійного електричного шару при терті осідаючих частинок із частинками середовища.
Потенціал седиментації виникає під час осідання формених елементів крові. Еритроцити, лейкоцити, тромбоцити тощо, які мають негативний заряд і питома вага яких більша, ніж плазми, осідають на дно посудини. Протиіони дифузного шару (катіони) відстають від руху формених елементів і тому нижні шари набувають негативного, а верхні - позитивного заряду (рис. 13.).
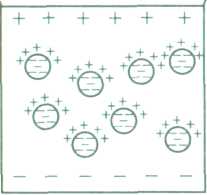
Рис. 13. Схема виникнення потенціалу осідання при стоянні крові
Електрокінетичні явища другого роду спостерігаються і при осіданні дисперсної фази в суспензіях та розділенні фаз в емульсіях. Потенціал седиментації виникає при роботі центрифуги. На кінцях трубопроводів і апаратів виникають високі різниці потенціалів
Методичні рекомендації
При вивченні першого питання записати визначення всіх термінів.
При опрацюванні другого питання розглянути схему приладу для проведення електрофорезу і його застосування в медицині.
Розглядаючи третє питання, дослідити механізм електроосмосу за малюнком .
При розгляді четвертого питання записати визначення електрокінетичних явищ другого роду.
Запитання для самоперевірки:
Які явища відносять до електрокінетичних та як їх класифікують?
Охарактеризувати застосування електрофорезу в медицині.
У яких випадках виникають потенціали течії та седиментації?
