
- •Клиническая фармакология средств лечения пневмонии
- •6.1. Фармакотерапия внебольничных пневмоний
- •6.2. Фармакотерапия госпитальных пневмоний
- •6.3. Аспирационные пневмонии
- •6.4. Пневмония на фоне нейтропении
- •6.5. Краткая характеристика антибактериальных препаратов, используемых в терапии пневмоний
- •I. Антибиотики:
- •II. Синтетические противомикробные средства:
- •I поколение:
- •II поколение (карбоксипенициллины):
- •III поколение (уреидопенициллины):
- •IV поколение (амидинопенициллины):
- •I поколение:
- •II поколение:
- •III поколение:
II поколение (карбоксипенициллины):
• Карбенициллин (Геопен).
• Тикарциллин (Тикар).
• Кариндациллин.
• Карфециллин (Карфексил).
• Флумициллин. Комбинированные:
• Тиментин (тикарциллин + клавулановая кислота).
III поколение (уреидопенициллины):
• Азлоциллин (Секропен).
• Пиперациллин (Пипрацил).
• Мезлоциллин (Байпен).
• Апалциллин. Комбинированные:
|
• Тазоцин (пиперацилин + тазобактам).
IV поколение (амидинопенициллины):
• Мециллинам.
• Пивамдиноциллин.
• Ацидоциллин.
• Амидиноциллин.
• Бакамдиноциллин.
Аминопенициллины - это полусинтетические пенициллины I поколения с широким спектром действия и высокой чувствительнос- тью к пенициллиназам. Спектр действия аминопенициллинов представлен в табл. 6.13. Амоксициллин по сравнению с ампициллином обладает гораздо большей биодоступностью при пероральном приеме, что позволяет создавать более высокие концентрации препарата в тканях (в том числе легочной). Кроме того, амоксициллин имеет больший период полувыведения, что дает возможность назначать его 3 раза в сутки, а не 4, как ампициллин. Это делает назначение амоксициллина более предпочтительным по сравнению с ампициллином.
В случае выявления ампициллинрезистентных штаммов микроорганизмов используются защищенные аминопенициллины, пред- ставляющие собой комбинацию одного из аминопенициллинов с ингибитором β-лактамаз (клавулановой кислотой или сульбактамом). Введение в комбинацию ингибитора β-лактамаз, не обладающего значимой собственной антибактериальной активностью, позволяет расширить спектр действия антибиотика и повысить его активность.
Изоксазолилпенициллины в нашей стране представлены, в первую очередь, оксациллином. Спектр действия препарата узкий, с преобладающим действием на грамположительную микрофлору (см. табл. 6.13). Оксациллин резистентен к действию β-лактамаз и является средством выбора при стафилококковых (MSSA) пневмониях.
Карбоксипенициллины и уреидопенициллины по спектру действия сходны с аминопенициллинами, но обладают более низкой активностью в отношении грамположительных кокков, хотя превосходят их по влиянию на грамотрицательные палочки, в том числе Pseudomonas aeruginosa. Это позволяло рассматривать их как антипсевдомонадные препараты. По активности в отношении Pseudomonas aeruginosa препараты данных групп располагаются в следующем порядке снижения активности: азлоциллин = пиперациллин >тикарциллин >карбенициллин. При этом предпочтительнее является использование защищенных карбокси- и уреидопенициллинов, так как резистентность к монопрепаратам высокая.
|
Амидинопенициллины имеют узкий спектр действия (преимущественно на грамотрицательные палочки), не разрушаются β-лактамазами. Используются в основном при инфекциях мочевыводящих путей.
Распределение цефалоспоринов по поколениям определяется спектром их антимикробной активности (см. табл. 6.13). Препараты I поко-
Таблица 6.13. Спектр антибактериальной активности β-лактамных антибиотиков
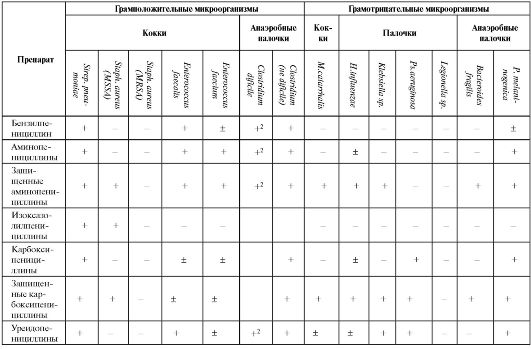
Окончание табл. 6.13
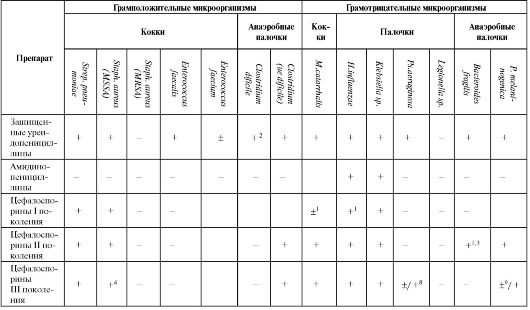
Окончание таблицы 6.13
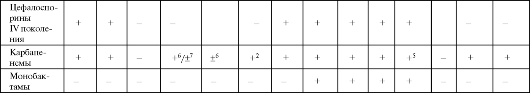
Примечание: 1 - кроме оральных цефалоспоринов; 2 - подавляют при смешанных интраабдоминальных инфекциях и инфекциях малого таза; 3 - кроме цефуроксима; 4 - кроме цефтибутена и цефиксима; 5 - кроме эртапенема; 6 - имипенем; 7 - меропенем, эртапенем; 8 - цефепим, цефтазидим; 9 - цефтриаксон.
Цефалоспорины
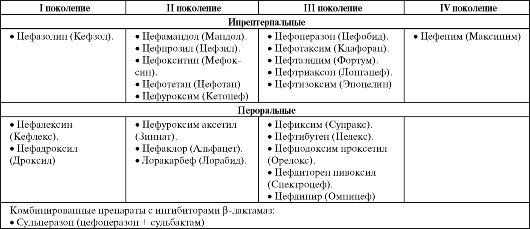
ления активны в отношении грамположительных палочек и кокков, а также грамотрицательных кокков. Наиболее активен цефазолин. Антибактериальная активность парентеральных цефалоспоринов несколько превосходит активность пероральных препаратов, однако все препараты разрушаются β-лактамазами.
По сравнению с цефалоспоринами I поколения, препараты II поколения более активны в отношении грамотрицательных микроор- ганизмов, особенно в отношении гемофильной палочки, сохранив действие на грамположительную микрофлору. Кроме того, они более устойчивы к действию β-лактамаз. Антибактериальная активность пероральных и парентеральных препаратов не различается.
Цефалоспорины III поколения высокоактивны в отношении большинства грамотрицательных микроорганизмов (в том числе неферментирующих микроорганизмов), уступая по действию на грамположительную флору препаратам I и II поколения. К действию большинства β-лактамаз препараты устойчивы. Ряд цефалоспоринов III поколения рассматриваются в качестве антипсевдомонадных препаратов, среди которых наиболее активны цефтазидим и цефоперазон.
|
На сегодняшний день среди цефалоспоринов препараты IV поколения имеют наиболее широкий спектр действия, сочетая высокую активность цефалоспоринов I-II поколений в отношении Staphylococcus aureus и цефалоспоринов III поколения в отношении грамотрицательных микроорганизмов.
Только один цефалоспорин (цефоперазон) применяется в сочетании с ингибиторами β-лактамаз (сульбактам). Данная комбинация позволяет расширить спектр действия цефалоспорина за счет снижения устойчивости грамотрицательных микроорганизмов, в том числе анаэробных.
Карбапенемы
• Имипенем.
• Меропенем (Меронем).
• Эртапенем (Инванз). Комбинированные препараты:
• Тиенам (имипенем + циластатин натрий).
Карбапенемам присущ наиболее широкий спектр антимикробной активности среди всех β-лактамов (см. табл. 6.13). При этом меропенем наиболее активен в отношении Pseudomonas aeruqinosa, превосхо- дя имипенем и цефалоспорины III поколения. К эртапенему данный возбудитель не чувствителен. По антианаэробной активности все карбапенемы сопоставимы с метронидазолом и превосходят линко-
замиды и цефокситин. Устойчивость к β-лактамазам очень высокая. Карбапенемы - единственные из β-лактамов, способные проявлять постантибиотический эффект.
Препараты данной группы могут рассматриваться в качестве оптимальных средств терапии тяжелых госпитальных инфекций, резис- тентных к цефалоспоринам и фторхинолонам.
Имипенем в организме разрушается почечным ферментом дигидропептидазой, что требует применения его совместно с ингибитором данного фермента - циластатином. Меропенем устойчив к действию дигидропептидазы.
Монобактамы
• Азтреонам (Азактам).
Азтреонам активен только в отношении грамотрицательных микроорганизмов (см. табл. 6.13) и имеет ограниченное применение в клинической практике.
|
Лекарственные взаимодействия β-лактамов представлены в табл. 6.14.
Таблица 6.14. Лекарственные взаимодействия β-лактамов
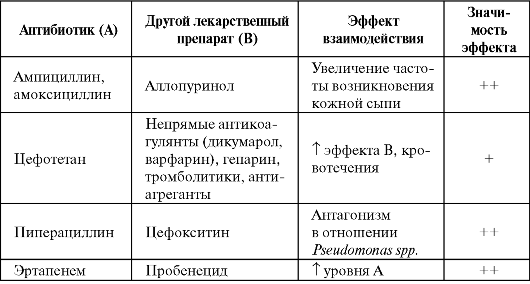
Примечание: «?» - теоретическая возможность; «+» - вероятно значимый; «++» - определенно значимый.
Побочные эффекты β-лактамов
β-лактамы являются одними из наименее токсичных антибиотиков, так как они нарушают синтез микробной стенки, отсутствующей в клетках человека. Тем не менее они могут вызывать следующие по- бочные эффекты:
- аллергические реакции от крапивницы до анафилактического шока (более характерны для биосинтетических пеницилли- нов);
- флебиты при внутривенном введении (все β-лактамы);
- диспепсические явления (тошнота, рвота, диарея) - наиболее часто наблюдаются при применении аминопенициллинов;
- гепатиты, холестаз - для оксациллина, азтреонама;
- нефротоксичность (гематурия, протеинурия) - встречается при применении оксациллина и цефалотина, особенно в комбинации с аминогликозидами;
- неврологические нарушения (головная боль, головокружения, тремор) - возможны при использовании всех β-лактамов;
- суперинфекцию (чаще в виде кандидозов).
Макролиды, азалиды и кетолиды
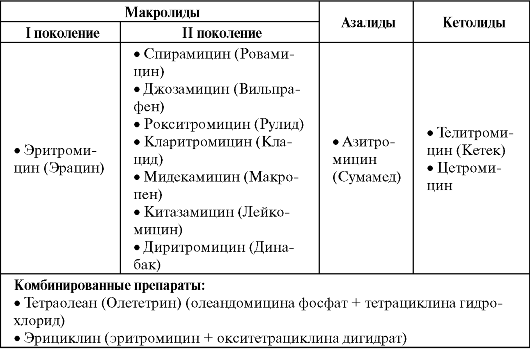
Макролиды, азалиды, кетолиды, линкозамиды и стрептограмины имеют сходный механизм действия, который включает связывание препарата с каталитическим пептидилтрансферазным центром рибосомальной 50S субъединицы, что приводит к нарушению реакции транслокации и транспептидации и, соответственно, прекращению синтеза белка. Кетолиды связываются одновременно с двумя учас-
тками на бактериальной рибосоме, что дает им более высокую, чем у эритромицина, антимикробную активность и способность сохранять ее при резистентности к макролидам, линкозамидам, стрептограминам (MLS-резистентность).
|
Макролидам присущ бактериостатический тип действия, хотя, в некоторых условиях, определяемых видом микроорганизма и бактериальной нагрузкой, эффект может трансформироваться в бактерицидный. Кроме того, для азитромицина характерно так называемое постантибиотическое действие, проявляющееся подавлением бактериального роста на протяжении 5-7 дней после отмены препарата.
Все антибиотики этой группы обладают заметной противовоспалительной активностью за счет снижения индуцированного микро- организмами высвобождения IL-6 и IL-1, а также NO.
Препараты данной группы (в первую очередь азитромицин и кларитромицин) создают высокие концентрации в макрофагах и нейтрофилах и с ними транспортируются в очаг воспаления.
Спектр действия макролидов изменяется в зависимости от принадлежности к тому или иному поколению (табл. 6.15). Так, для препаратов I поколения он сопоставим с биосинтетическими пенициллинами, но при этом важной особенностью является их активность в отношении внутриклеточных атипичных возбудителей (хламидий, микоплазм, легионелл). Макролиды II поколения и азалиды отличаются более высокой антимикробной активностью (в первую очередь в отношении гемофильной палочки), расширенным спектром действия и улучшенной фармакокинетикой.
Кетолиды при близком к макролидам и азалидам антимикробном спектре действия высокоактивны против эритромицинорези- стентных штаммов кокковых микроорганизмов с MLS-резистентнос- тью, которая достаточно широко распространена. Это отличает кетолиды, например, от рокситромицина и азитромицина, которые в случае MLS-резистентности теряют активность подобно эритромицину. Внутри группы резистентность неперекрестная (т. е. микроорганизмы, резистентные к телитромицину, чувствительны к цетромицину).
|
Лекарственные взаимодействия макролидов, азалидов и кетолидов представлены в табл. 6.16.
Побочных эффектов, возникающих при применении макролидов, немного. Чаще всего наблюдаются:
- со стороны ЖКТ: тошнота, рвота, диарея, холестатический гепатит, псевдомембранозный колит;
Таблица 6.15. Спектр антибактериальной активности противомикробных средств, используемых при лечении пневмоний
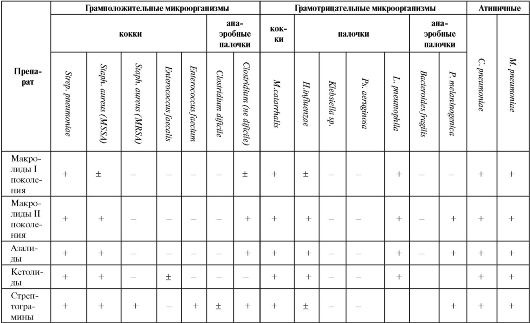
Продолжение табл. 6.15
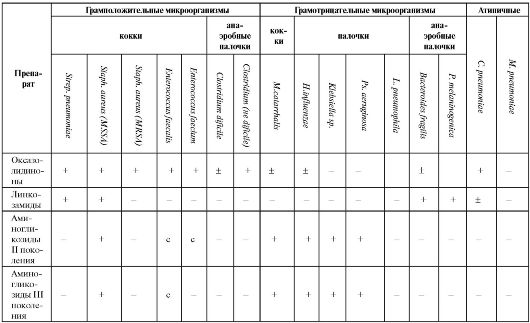
Окончание таблицы 6.15
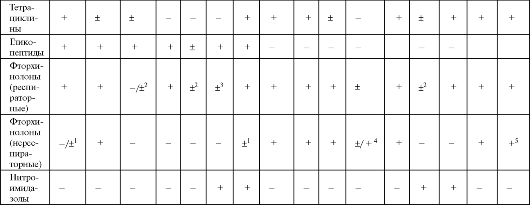
Примечание: С - синергизм с бензилпенициллином, аминопенициллинами, гликопептидами; 1 - офлоксацин, ципрофлоксацин; 2 - моксифлоксацин, гатифлоксацин; 3 - подавляют при смешанных интраабдоминальных инфекциях и инфекциях малого таза; 4 - ципрофлоксацин; 5 - кроме пефлоксацина.
Таблица 6.16. Лекарственные взаимодействия макролидов, азалидов, кетолидов
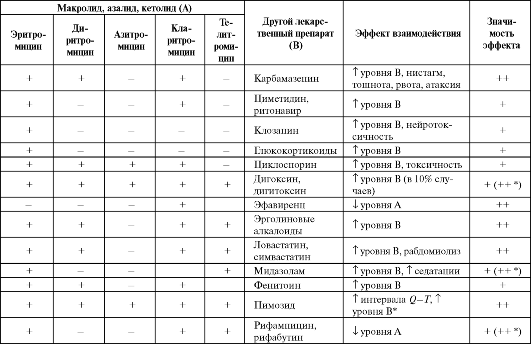
Окончание таблицы 6.16
Примечание: «+» - теоретически возможные; «+» - вероятно значимые; «++» - определенно значимые; * - для телитромицина.
- со стороны сердечно-сосудистой системы: удлинение интервала Q-T, желудочковые тахикардии;
- аллергические реакции.
Стрептограмины
• Квинупристин-дальфопристин (Синерцид).
Синерцид представляет собой комбинацию двух молекул: стрептограмина А (дальфопристин) и В (квинупристин) в соотношении 30/70. Оба компонента имеют синергичный эффект в подавлении синтеза белка микроорганизмом, связываясь с разными участками 50S субъединицы рибосом. Интересно, что по отдельности эти антибиотики обладают бактериостатическим эффектом, а их комбинация бактерицидна.
Этот препарат активен против большинства грамположительных бактерий и атипичных возбудителей, таких как микоплазмы, хламидии, легионеллы (табл. 6.17). 90% стафилококков чувствительны к си- нерциду, в том числе метициллинрезистентные штаммы. В 100% он активен против пневмококков независимо от их чувствительности к пенициллину. Квинупристин-дальфопристин также активен против Enterococcus faecium, включая ампициллингентамицин- и ванкомицинрезистентные штаммы. Только Enterococcus fecalis обладает устойчивостью к стрептограминам.
|
Для предупреждения развития резистентности к квинупристиндальфопристину показанием к его применению является только тяже- лая инфекция, вызванная полирезистентными штаммами Enterococcus faecium и Staphylococcus aureus.
Линкозамиды
• Линкомицин (Линкоцин).
• Клиндамицин (Далацин).
Спектр действия линкозамидов относительно узкий, с преимущественным влиянием на грамположительную микрофлору (см. табл. 6.15). Особое значение имеет их влияние на стафилококки и анаэробы.
Оба препарата практически не отличаются по антибактериальному спектру, но клиндамицин более активен, лучше проникает в ткани (в том числе в легочную) и имеет меньшее число побочных эффектов. Однако период полувыведения клиндамицина короче, чем у линкомицина, что требует либо его более частого назначения (4 раза в сутки), либо увеличения разовой дозы (до 600 мг), что позволяет использовать его 3 раза в сутки.
Наиболее частыми побочными эффектами препаратов являются диспепсические явления, в редких случаях - развитие псевдомембранозного колита.
Аминогликозиды
