
- •Общая характеристика: строение, классификация, номенклатура
- •Изомерия. Номенклатура.
- •Номенклатура
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Поскольку первым присоединяется положительно заряженный ион галогена, реакция называется электрофильным присоединением.
- •Окисление.
- •Применение алкенов
ТЕМА ЛЕКЦИИ: УГЛЕВОДОРОДЫ. АЛКЕНЫ
(этиленовые углеводороды или олефины)
Вопросы:
Общая характеристика: строение, классификация, номенклатура.
Методы получения
Физические свойства
Химические свойства
Отдельные представители. Способы идентификации.
Общая характеристика: строение, классификация, номенклатура
Гомологический ряд алкенов начинается с этилена.
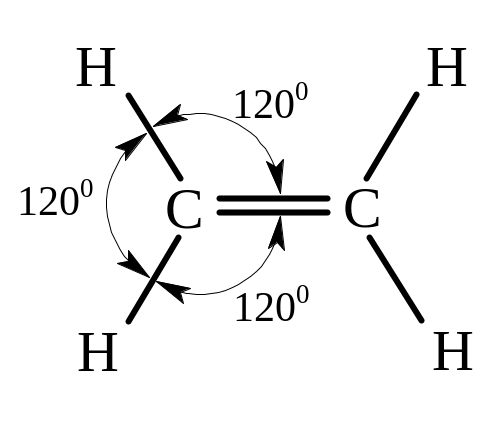
В этиленовых углеводородах обязательно имеются два атома углерода, которые на связь между собой затрачивают по две валентности. Т.е., между ними существует двойная связь, о природе которой упоминалось ранее. Углероды, связанные двойной связью, находятся в sр2-гибридном состоянии и образуют между собой за счет sр2-орбиталей -связь. Перекрывание электронных облаков их р-электронов создает π-связь.
Атомы молекулы этилена лежат в одной плоскости и углы между связями составляют 120о.
Алкены образуют гомологический ряд с общей формулой СnН2n.
Изомерия. Номенклатура.
Как и в ряду предельных углеводородов структурная изомерия алкенов начинается с четвертого члена ряда. Однако число изомеров значительно больше. Изомерия олефинов обусловлена, во-первых, строением углеродной цепи, во-вторых – положением двойной связи в цепи и в-третьих – пространственным расположением атомов или групп при углеродах с двойной связью. Последний вид изомерии носит название геометрической или цис-транс-изомерии. Если вращение вокруг простой -связи требует небольшого количества энергии (8-20 кДж·моль-1), которая сообщается молекуле при комнатной температуре и даже ниже. При вращении вокруг двойной связи должна разрываться π-связь, а это примерно 250 кДж·моль-1. Поэтому поворот вокруг двойной связи возможен лишь при высоких температурах, облучении или присутствии катализаторов, ослабляющих π-связь. По этим причинам в алкенах не существует изомеров вращения вокруг двойной связи, а олефины из-за невозможности вращения вокруг двойной связи при обычных условиях присутствуют в виде стабильных геометрических изомеров. В цис-изомерах – одинаковые атомы или группы при углеродах с двойной связью располагаются по одну сторону от этой связи, в транс-изомерах – по разные стороны.
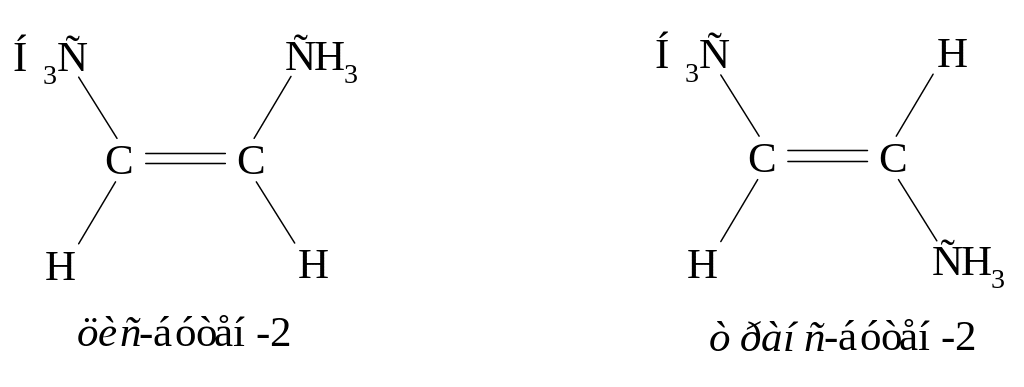
При гидрировании оба бутена-2 дают один и тот же бутан.
Номенклатура
Называют алкены по различным номенклатурам. При обозначении по тривиальной номенклатуре к названию соответствующего радикала предельного углеводорода добавляют суффикс –ен: этилен, пропилен, бутилен, изобутилен, амилен и т.д. По рациональной номенклатуре олефины называются как производные этилена. При составлении названия по номенклатуре ИЮПАК в качестве основной цепи соединения выбирается самая длинная углеродная цепочка, включающая двойную связь. За основу названия берется название алкана с заменой окончания -ан на -ен. Цифрой обозначают номер атома углерода, за которым следует двойная связь. Нумеровать углеродные атомы основной цепи следует с того конца, к которому ближе двойная связь.
Например:

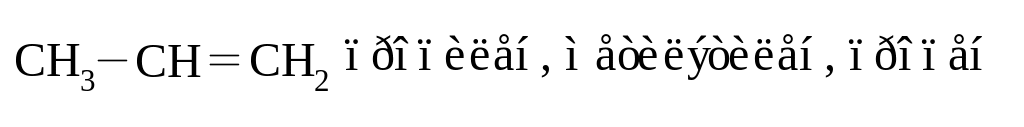
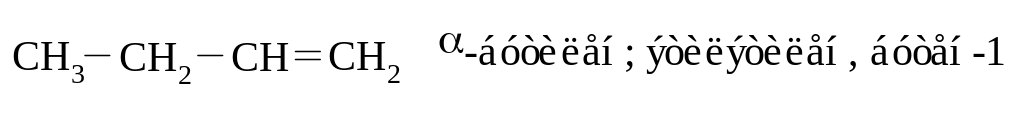

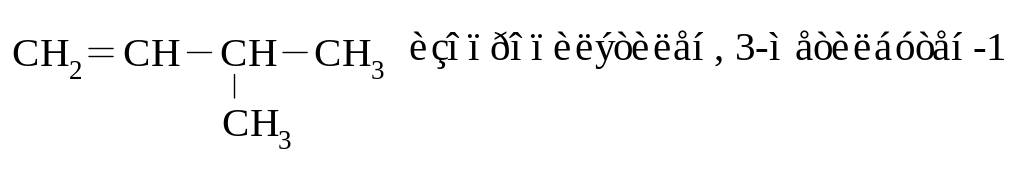

Способы получения
Основным промышленным источником олефинового сырья являются процессы крекинга и пиролиза нефтяных фракций. Эти процессы дают смесь легких газообразных алкенов С2 – С5, которая сжижается при пониженной температуре и повышенном давлении разгоняется на фракции С2, С3, С4. Большое количество олефинов дают газы коксования и процессы дегидривания алканов. Реакция в последнем случае протекает при температуре ~300С на катализаторе оксид хрома.
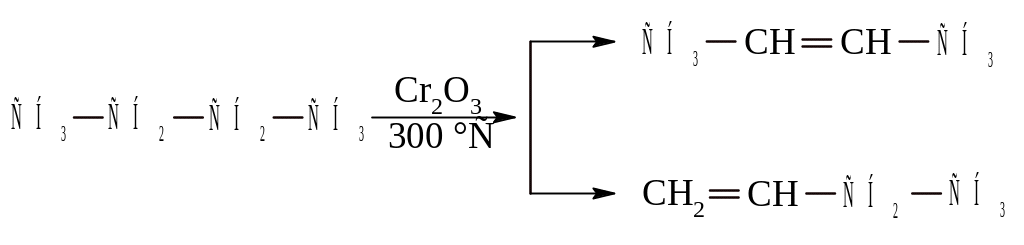
Дегидратация спиртов. Это обычный лабораторный способ получения этиленовых углеводородов.
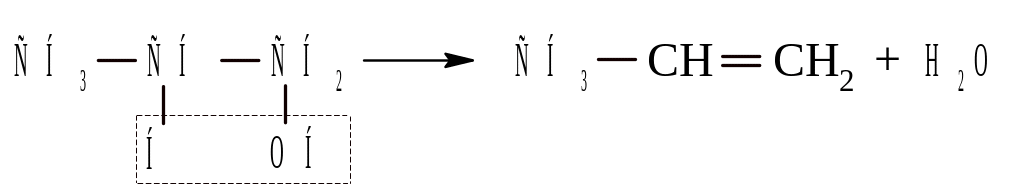
Реакцию можно проводить в паровой фазе при 300-400С на Al2O3 и жидкой фазе с катализаторами H2SO4, H3PO4 и др. В зависимости от природы одни спирты дегидратируются легче, другие – труднее. Так, третичные спирты отщепляют воду уже при перегонке.

Порядок отщепления воды в большинстве случаев определяется правилом Зайцева: при образовании воды наиболее легко водород отщепляется от соседнего наименее гидрогенизированного атома углерода, так как он наиболее подвижен.
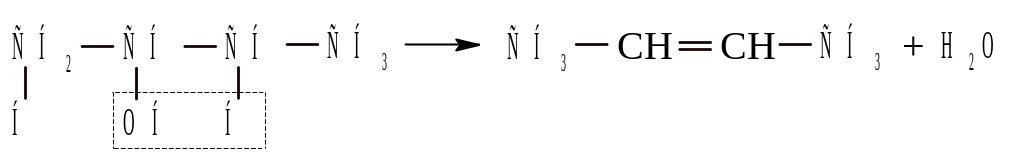
На практике это правило выполняется не строго. Оно лишь указывает на преимущественный порядок отщепления воды.
При дегидратации спиртов С4 и выше может получаться смесь олефинов с различным положением двойной связи и даже изменяться углеродный скелет.
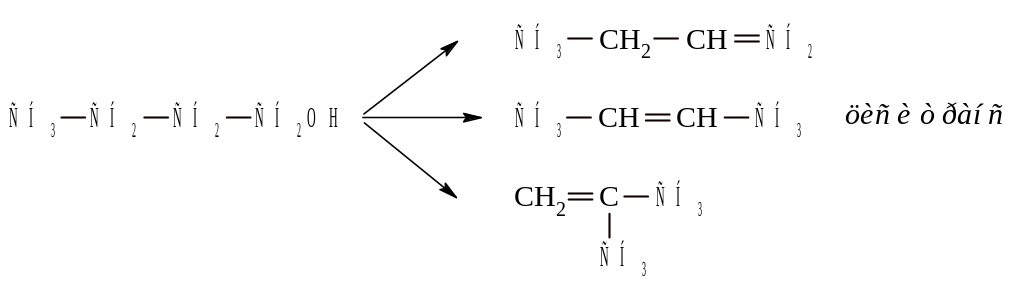
Алкены можно получать из галогенпроизводных отщеплением галогенов или галогеноводородов.
Моногалогенпроизводные дают алкены при действии щелочей в спиртовом растворе или органических оснований (диметиланилин, хинолин).
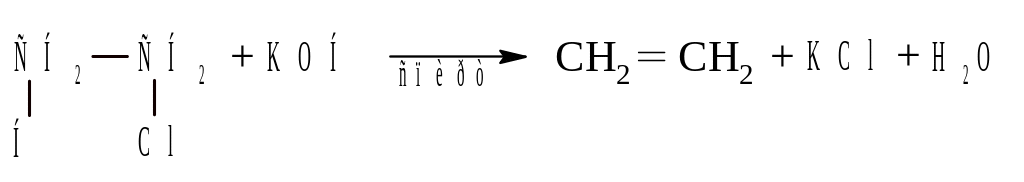
В общем случае направление дегидрогалогенирования соответ-ствует правилу Зайцева.
Алкены получаются также при действии цинковой пыли на дигалогенопроизводные, у которых атомы галогенов расположены у соседних углеродов.
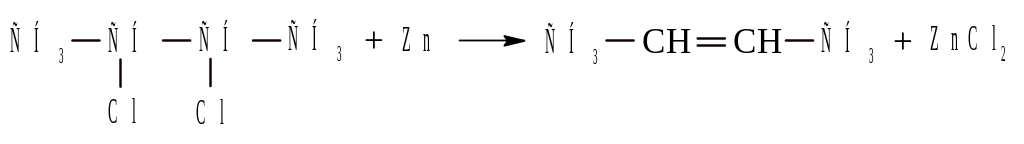
Гидрирование соединений с тройной связью (ацетиленов) над не очень активным катализатором (Fe, частично «отравленные» Pd и Pt).

