
- •37 Лекция 17. Рентгеновское и нейтронное рассеяние. Кристаллография лекция 17. Рентгеновское и нейтронное рассеяние. Кристаллография
- •Рассеяние рентгеновских лучей и нейтронов
- •Поглощение
- •Сечение рассеяния и размер образца
- •Когерентное и некогерентное рассеяние
- •Упругое и неупругое рассеивание
- •Суммирование волн, преобразование Фурье и обратное пространство
- •Фазовая проблема
- •Одномерные кристаллы
- •Двумерные и трёхмерные кристаллы
- •Разупорядоченные системы
- •Разрешающая способность и контраст
- •Комплементарность
- •Источники излучения и измерительные приборы
- •Активная зона с
- •Подвижным отражателем
- •Обогащенный уран u-235
- •Гренобль, Франция
- •Обратная кристаллическая решетка, сфера Эвальда и структурные факторы
- •В случае кристалла f(q) заменяется на g(q), где
- •Симметрия пространственной группы
- •Электронная плотность
- •Технические задачи и кристаллографическая модель
- •Методы кристаллизации
- •Идентификация кристаллов и преципитатов – размеры и форма кристаллов
- •Криокристаллография и криопротекторы
- •Крепление кристалла
- •Мечение
Идентификация кристаллов и преципитатов – размеры и форма кристаллов
При определенных условиях могут появляться солевые кристаллы. Как правило, легко определить, что они не имеют отношения к белку. Наличие прозрачной капли указывает на то, что либо она еще не пришла в равновесие, либо концентрация образца слишком низкая. Наличие выпавшей фазы заставляет предположить слишком высокую концентрацию образца. Обычно опыты повторяются с уменьшением начальной концентрации образца вдвое. Однако при благоприятных обстоятельствах белковые кристаллы способны расти даже в капле с осадителем.
Для сбора данных рентгенографического исследования приходится выращивать достаточно большие кристаллы. С появлением синхротронных источников появилась возможность использовать кристаллы, размер которых приближается к микрону, они выращиваются в каплях 0,2 мкл.
Криокристаллография и криопротекторы
Использование синхротронного излучения является предпочтительным в рентгеновской кристаллографии, поскольку позволяет быстро собрать данные дифракции с высоким разрешением. Однако высокая интенсивность порождает проблемы, так как рентгеновские лучи, поглощаясь в кристалле, вызывают нагрев и радиационные разрушения. Непосредственный ущерб наносится, когда атомы в кристалле поглощают кванты рентгеновского излучения, а косвенное повреждение обуславливается диффузией химически активных радикалов, возникающих при излучении.
Чтобы уменьшить радиационные повреждения, кристалл содержится при низкой температуре (~100 K), тогда косвенное повреждение значительно снижается вследствие меньшей скорости диффузии, что дает достаточно времени для сбора данных. Но образец должен очень быстро охладиться до криогенной температуры (сверхбыстрое охлаждение), чтобы избежать образования льда. Ведь кристаллический лед деформирует как решетку белкового кристалла, так и структуру самого белка. Ключом к успешному применению метода является образование стекловидной водной фазы. Часто добавляются химические вещества с низкой температурой замерзания, чтобы растворитель внутри кристалла оставался неупорядоченным и чтобы способствовать образованию аморфного стекла после замерзания. В число обычно применяемых криопротекторов входят глицерин, 2-метил-2,4-пентандиол (MPD), низкомолекулярный полиэтиленгликоль и жиры. Дальнейшие добавки могут не потребоваться, если раствор, в котором растет кристалл, сам будет криозащищенным.
Всегда важно убедиться, что раствор криопротектора можно мгновенно охладить как аморфное стекло. Затем уже исследуемые белковые кристаллы подвергаются сверхбыстрому охлаждению.
Крепление кристалла
Гониометр
Кристалл устанавливается на гониометре, что дает возможность свободно вращать его вокруг осей в целях изучения большого объема обратного пространства (Рис. E3.4). Во время сбора данных кристалл, как правило, совершает колебания в небольшом угловом диапазоне. Данные, соответствующие каждому угловому положению, называются образом осцилляций.
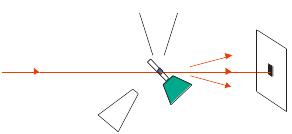
Видеокамера – вместе.
Рис. E3.4. Схема эксперимента по рентгеновской кристаллографии. Пучок (красный) коллимируется и делается монохроматическим. Кристалл (синий) в капилляре или криопетле крепится на гониометре (зеленый) и помещается в центр пучка с помощью видеокамеры. Кристалл непрерывно охлаждается потоком холодного сухого азота.
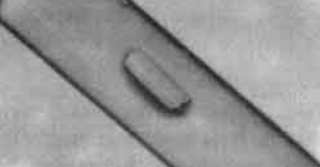
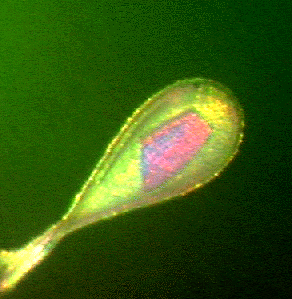
Рис. E3.5 Кристаллы закреплены в: (a) стеклянном капилляре и (б) в крио-петле.
Крепление в капиллярной трубке при комнатной температуре
На заре кристаллографии перед появлением криотехнологий кристаллы подвергались воздействию рентгеновских лучей при комнатной температуре в герметичных стеклянных капиллярных трубках (Рис. E3.5a). Капля маточного раствора заключалась в неё рядом с кристаллом, чтобы предотвратить высыхание. Сбор данных тоже проводился при комнатной температуре, если не удавалось найти подходящие условия охлаждения.
Криопетли
Наиболее распространенный метод замораживания состоит в улавливании кристалла с помощью небольшой петли из волокна (Рис. E3.5б). Тонкая пленка раствора распределяется по всей петле и поддерживает кристалл. Быстрое охлаждение достигается погружением петли в криогенное вещество при низкой температуре (например, поток сухого азота при ~100 K). Затем в течение сбора данных кристалл непрерывно поддерживается в замороженном состоянии.
