
Суммарное уравнение аэробного окисления одной молекулы глюкозы:
1-Глюк + 6 О2 = 6 СО2 + 6 Н2О + 38 АТФ
Прежде чем ПВК вступит на путь ЦТК она подвергается окислительному декарбоксилированию при участии комплекса ферментов. Результатом такого взаимодействия является образование ацетил-КоА. В таком виде это соединение поступает на путь ЦТК
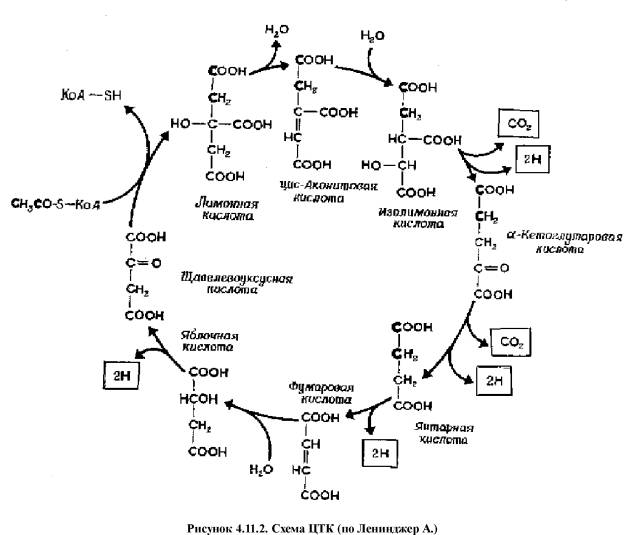
. ацетил-КоА + оксалоацетат (щавелевокуксусная кислота) цитрат (лимонная кислота) + КоА
Е: цитратсинтетаза;
2. цитрат цис-аконитат + Н2О
Е: аконитаза;
3. цис-аконитат + Н2О изоцитрат
Е: изоцитратсинтетаза;
4. изоцитрат + НАД+ альфа-кетоглутарат + СО2 + НАДН2
Е: изоцитратдегидрогеназа / декарбоксилаза;
5. альфа-кетоглутарат + НАД+ сукцинат (янтарная кислота) + СО2 + НАДН2
Е: альфа-кетоглутаратдегидрогеназа / декарбоксилаза;
6. сукцинат + ФАД+ фумарат + ФАДН2
Е: фумаратдегидрогеназа;
7. фумарат + Н2О малат (яблочная кислота)
Е: фумараза;
8. малат + НАД+ оксалоацетат + НАДН2
Е: малатдегидрогеназа.
Регуляторные ферменты:
1) пируватдегидрогеназа (Ингибиторы: АТФ, НАДН, цитрат, Ац-КоА);
2) цтратсинтаза (Ингибиторы: АТФ, НАДН, ВЖК);
3) Изоцитратдегидрогеназа (Ингибиторы: АТФ, НА;ДН);
4) Кетоглутаратдегидрогеназа (Ингибиторы: АТФ, НАДН).
Литература к главе IV.11.
1. Бышевский А. Ш., Терсенов О. А. Биохимия для врача // Екатеринбург: Уральский рабочий, 1994, 384 с.;
2. Кнорре Д. Г., Мызина С. Д. Биологическая химия. – М.: Высш. шк. 1998, 479 с.;
3. Ленинджер А. Биохимия. Молекулярные основы структуры и функций клетки // М.: Мир, 1974, 956 с.;
4. Пустовалова Л.М. Практикум по биохимии // Ростов-на Дону: Феникс, 1999, 540 с.
5. Методы биохимических исследований (липидный и энергетический обмен). Под ред. М.И.Прохоровой // Л.: Изд-во Ленинградского университета, 1982. - 327 с.;
6. Ньюсхолм Э., Старт К. Регуляция метаболизма. Под ред. Э.Г.Ларского. - М.: Мир, 1977. - 407 с.
