
- •Задача 1
- •Задача 2
- •Задача 3
- •Задача 4
- •Задача 5
- •Задача 6
- •Задача 7
- •Задача 8
- •Задача 9
- •Задача 10
- •Задача 11
- •Задача 12
- •Задача 13
- •Задача 14
- •Задача 15
- •Частные реакции на сульфацил-натрия:
- •Задача 16
- •Задача 17
- •Задача 18
- •Задача 20
- •Задача 21
- •Задача 22
- •Задача 23
- •Задача 24
- •Количественное определение
- •Задача 28
- •Задача 30
- •Задача 31
- •Задача 32
- •Задача 33
- •Задача 34
- •Задача 35
- •Задача 36
- •Задача 37
- •Задача 38
- •Задача 39
- •Задача 40
Задача 9
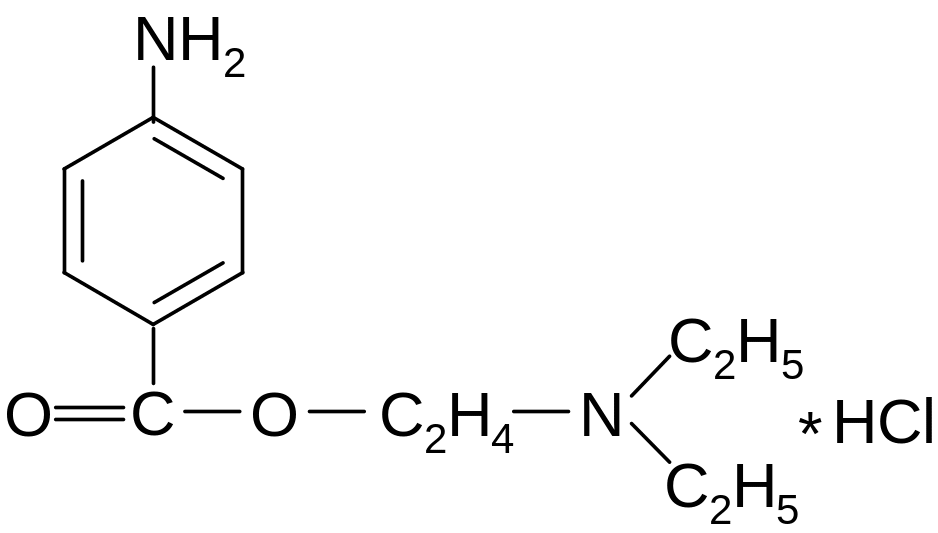
Новокаин. Novocainum
Прокаина гидрохлорид (МНН)
β-диэтиламиноэтилового эфира п-аминобензойной кислоты гидрохлорид
1. Местноанестезирующее средство. Применяют для инфильтрационной, спинномозговой и местной анестезии в виде 0,25% - 0,5% водных растворов для инъекций.
2. По химической структуре является сложным эфиром п-аминобензойной кислоты. Представляет собой белый кристаллический порошок без запаха, горького вкуса, очень легко растворим в воде, легко растворим в этаноле. Обладает светопоглощением в УФ области оптического спектра, что также можно использовать для идентификации. Оптический спектр новокаина имеет максимум светопоглощения при 298 нм (растворитель – вода).
3. Новокаин содержит в молекуле следующие функциональные группы, которые обусловливают его химические свойства: первичную ароматическую аминогруппу, бензольный цикл, сложноэфирную и третичную аминогруппу, является солью органического основания. Свойствами этих функциональных групп обусловлены реакции: диазотирования и азосочетания, замещения (галогенирования), гидролиза, комплексообразования.
Все эти типы реакций можно использовать для идентификации новокаина:
а) реакция диазотирования и азосочетания (на первичную ароматическую аминогруппу) [см. задачу № 1].
б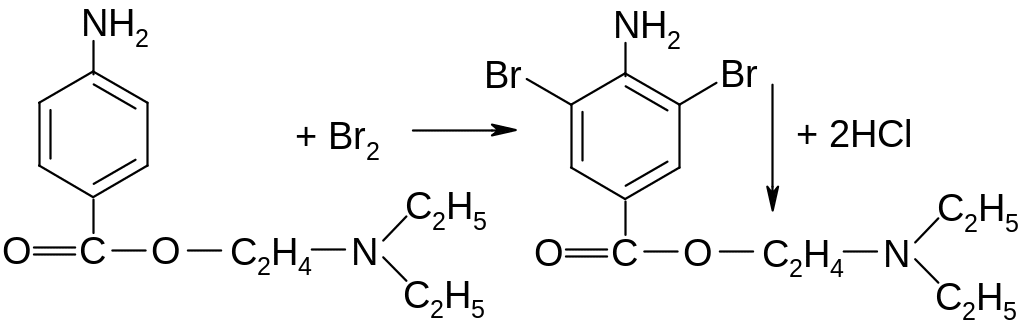 )
реакция галогенирования (ароматический
цикл):
)
реакция галогенирования (ароматический
цикл):
белый осадок
в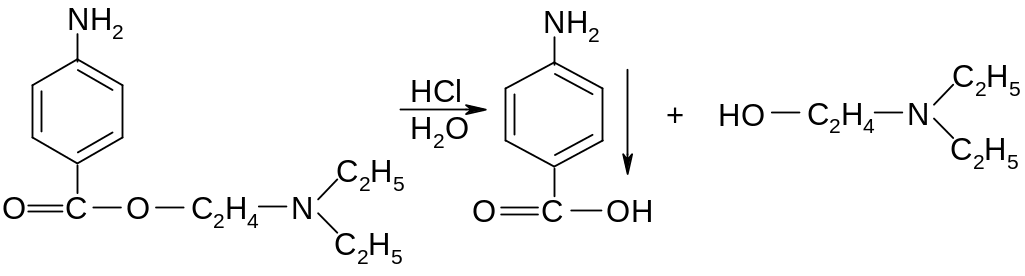 )
реакция гидролиза (сложноэфирная
группа):
)
реакция гидролиза (сложноэфирная
группа):
п-аминобензойная диэтиламиноэтанол
кислота
г) реакции комплексообразования (на третичную аминогруппу) с осадительными общеалкалоидными реактивами (пикриновая, фосфорномолибденовая кислоты и др.).
д) для идентификации хлорид-иона проводят реакцию с нитратом серебра.
4. Указанные реакции используются также и для количественного определения.
Для количественного определения новокаина в субстанции рекомендуется метод нитритометрии:
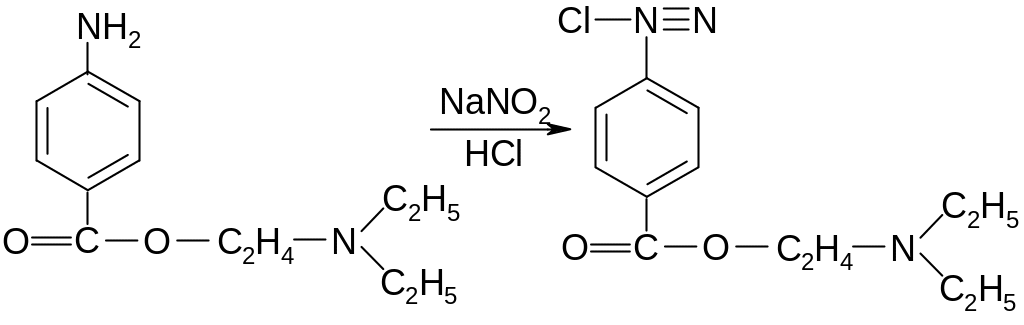
соль диазония
Индикаторы: тропеолин 00 или его смесь с метиленовым синим.
Известны методики броматометрического и иодхлорметрического определения, основанные на образовании дибром- и дийод-производных (см. подлинность – реакция «б»).
Известны методики неводного титрования в среде безводной уксусной кислоты. Титрант – хлорная кислота, индикатор – кристаллический фиолетовый.
В лекарственных формах возможно алкалиметрическое титрование, т. к. новокаин является гидрохлоридом. Титрование проводят в присутствии хлороформа, который извлекает выделяющееся основание:
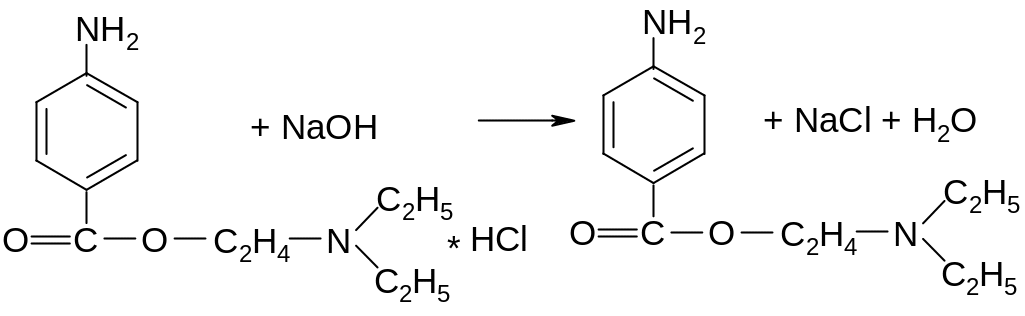
В лекарственных формах с компонентами кислотного характера применяется аргентометрический или меркуриметрический методы.
Количественное определение новокаина в лекарственных формах можно провести спектрофотометрическим методом в максимуме светопоглощения при длине волны 272 нм (растворитель – вода).
Образование азокрасителя и гидроксамовую пробу используют для фотоколориметрического определения.
При титриметрическом определении новокаина (Х%) расчет проводят по формуле:
![]() ,
,
где: V – объем титранта, мл;
К – поправочный коэффициент;
Т – количество новокаина (г), соответствующее 1 мл 0,1 М раствора нитрита натрия, г;
а – масса навески, г.
При спектрофотометрическом и фотоколориметрическом определении используют формулу:
![]() ,
,
где: Ах и Аст – оптические плотности анализируемого и стандартного образца соответственно;
Сст – концентрация стандартного образца, г/мл;
W – объем колбы, используемой для разведения навески, мл;
Р – общая масса лекарственной формы, г;
а – масса навески, г.
5. Для инъекционных растворов используются различные виды стабилизации: химическая, физическая и микробиологическая. Химическую стабилизацию проводят путем добавления хлористоводородной кислоты, создающей такое значение рН среды, при котором гидролиз минимален. Кроме того, выщелачивание стекла может вызвать выпадение оснований органических солей. Процессы разложения лекарственных веществ усиливаются на свету, который является катализатором. Для подавления влияния этого физического фактора, инъекционные растворы следует хранить в темноте. Для микробиологической стабилизации инъекционные растворы подвергают стерилизации.
6. Гидролиз – это процесс разложения вещества с участием воды. Гидролизу подвергаются соли, образованные сильным основанием и слабой кислотой и наоборот. Первые гидролизуются по аниону, вторые – по катиону.
Гидролизу подвергаются и органические соединения, например, галогенангидриды (образуются две кислоты – галогенводородная и кислородсодержащая), сложные эфиры распадаются на кислоту и спирт, ацетпроизводные – на уксусную кислоту и органическое соединение.
Гидролиз ускоряется в присутствии кислот и оснований, а также ионов металлов, способных связываться с одним из продуктов реакции.
Окислительно-восстановительные реакции сопровождаются изменением зарядов элементов за счет отдачи и присоединения электронов. Соединения, в которых элементы отдают электроны, называются восстановителями, а в которых присоединяют – окислителями.
7. На устойчивость лекарственных веществ в растворах влияют: значение рН среды, температура стерилизации, наличие кислорода и углекислого газа в воде, присутствие ионов металлов, микробная загрязненность, воздействие света.
Причиной помутнения раствора новокаина для инъекций при его приготовлении явилось изменение значения рН раствора. За счет выщелачивания стекла раствор приобретает щелочную среду (рН > 7). Это привело к нейтрализации хлористоводородной кислоты, основание новокаина в воде нерастворимо, что и привело к помутнению. Поэтому для стабилизации данного раствора необходимо сдвинуть рН в кислую сторону путем добавления хлористоводородной кислоты. Растворы, подвергающиеся разложению, следует предохранять от действия света. Они должны быть хорошо укупоренными.
