
- •Задача 1
- •Задача 2
- •Задача 3
- •Задача 4
- •Задача 5
- •Задача 6
- •Задача 7
- •Задача 8
- •Задача 9
- •Задача 10
- •Задача 11
- •Задача 12
- •Задача 13
- •Задача 14
- •Задача 15
- •Частные реакции на сульфацил-натрия:
- •Задача 16
- •Задача 17
- •Задача 18
- •Задача 20
- •Задача 21
- •Задача 22
- •Задача 23
- •Задача 24
- •Количественное определение
- •Задача 28
- •Задача 30
- •Задача 31
- •Задача 32
- •Задача 33
- •Задача 34
- •Задача 35
- •Задача 36
- •Задача 37
- •Задача 38
- •Задача 39
- •Задача 40
Задача 40
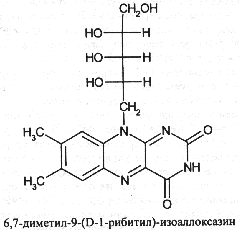
Рибофлавин (МНН). Riboflavinum
Витамин В2
1. Рибофлавин восполняет недостаток витамина В2 в организме. Особенно он важен для нормальной функции зрения. Назначают внутрь в таблетках и драже по 0,005-0,01 г и глазных каплях (0,01% раствор) при гипо- и авитаминозе, различных глазных заболеваниях, длительно незаживающих ранах и язвах, лучевой болезни, болезни Боткина и т.д.
Рибофлавин является производным изоаллоксазина, который включает пиримидин, пиразин и бензол:
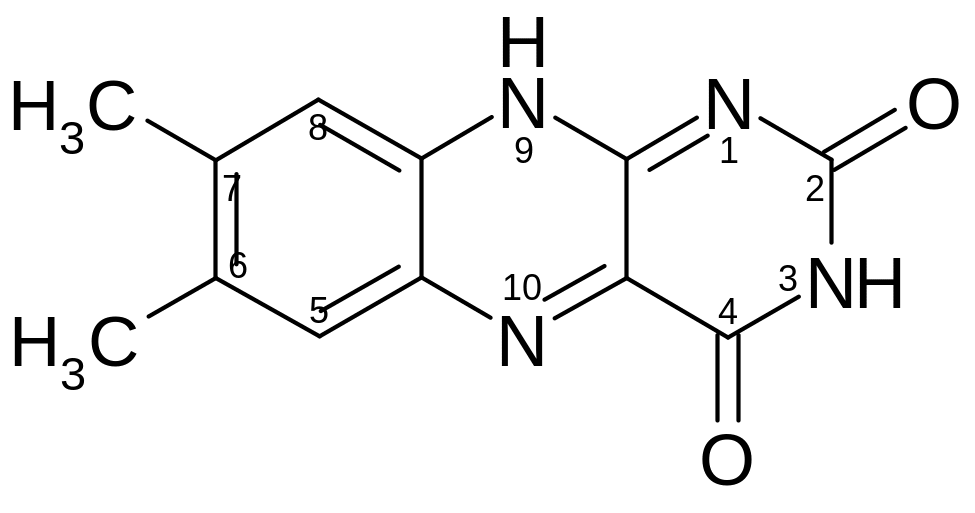
Изоаллоксазиновый цикл в молекуле рибофлавина связан с остатком рибитола.
Рибофлавин имеет характерную желто-оранжевую окраску, обусловленную несколькими сопряженными связями в молекуле. Рибофлавин имеет слабый специфический запах и горький вкус. Он мало растворим в воде, нерастворим в этиловом спирте, эфире, ацетоне, хлороформе. Растворим в растворах гидроксидов щелочных металлов и кислот, т.к. является амфотерным соединением. Его кислотные свойства обусловлены наличием подвижного атома водорода имидной группы, а основные – наличием нескольких гетероциклических атомов азота.
Нейтральные водные растворы рибофлавина имеют яркую зеленовато-жёлтую окраску, вследствие чего становится возможным для проведения анализа использование спектро- и фотометрических методов.
Рибофлавин оптически активен. Оптическая активность рибофлавина обусловлена наличием в рибитильной цепочке трёх асимметричных атомов углерода. Поэтому ГФ рекомендует в качестве константы, характеризующей подлинность и чистоту, определять удельное вращение щелочного раствора (определённой концентрации) рибофлавина, которое должно быть от -115 до -135°.
Рибофлавин можно идентифицировать по ИК-спектру, который должен соответствовать спектру его стандартного образца или спектру сравнения.
2. Проявление витаминной активности во флавиновой системе связано с наличием в молекуле чрезвычайно лабильной азадиеновой группировки. Эта группировка обусловливает окислительно-восстановительные свойства рибофлавина.
При восстановлении рибофлавин, теряя желтую окраску, переходит в бесцветный лейкорибофлавин. Последующее окисление обусловливает обратный процесс:

Рибофлавин устойчив к окислителям и нагреванию, но при нагревании в щелочных растворах рибофлавин быстро разрушается. Под влиянием света неустойчив он и в кислой, и щелочной средах. Например, под действием света рибофлавин в щелочной среде образует люмифлавин, а в нейтральной и слабокислой – люмихром, в этом случае физиологическая активность рибофлавина исчезает.
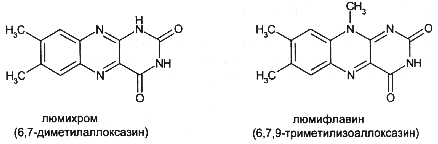
Люмифлавин в растворах имеет окрашивание и флуоресценцию, аналогичные рибофлавину, но отличается от него тем, что растворяется в хлороформе. Это свойство используют для обнаружения примеси люмифлавина в рибофлавине.
Для испытаний производных изоаллоксазина используют химические реакции, основанные на окислительно-восстановительных свойствах сопряженных двойных связей, окислении, комплексообразовании аминогруппы.
Подлинность рибофлавина устанавливают по характерной яркой зеленовато-желтой окраске и интенсивной зеленой флуоресценции водного раствора (в ультрафиолетовом излучении), которая обусловлена наличием в молекуле свободной иминной группы в положении 3 изоаллоксазинового цикла. Флуоресценция исчезает при добавлении растворов кислоты хлористоводородной или щелочи. Если к водному раствору рибофлавина прибавить натрия гидросульфит (сильный восстановитель), то окраска и флуоресценция исчезают вследствие образования лейкорибофлавина. Свойство флуоресцировать используют для флуориметрического определения рибофлавина.
Как азотсодержащее органическое основание, рибофлавин дает положительную реакцию с реактивом Драгендорфа и другими общеалкалоидными (осадительными) реактивами. С солями металлов (серебра, кобальта, меди, ртути и др.) рибофлавин образует нерастворимые окрашенные комплексные соединения. Эти реакции используют для фотоколориметрического определения рибофлавина в лекарственных формах.
Для количественного определения рибофлавина в настоящее время используются в основном биологические и физико-химические методы: флуориметрический, колориметрический и спектрофотометрический.
Для качественного и количественного анализа применяют спектрофотометрию в УФ-области. Все испытания выполняют, защищая испытуемое лекарственное вещество от попадания прямого солнечного света. В водных растворах рибофлавин имеет 4 максимума поглощения. Количественное содержание рассчитывают по удельному показателю поглощения рибофлавина.
Способы количественного определения титриметрическими методами основаны на использовании кислотно-основных и окислительно-восстановительных свойств.
Для количественного определения применяют алкалиметрическое определение рибофлавина после его реакции с серебра нитратом, а также цериметрию и метод Кьельдаля.
Рибофлавин необходимо хранить в хорошо укупоренных банках оранжевого стекла, учитывая его свойство легко окисляться и разлагаться под действием света с образованием биологически неактивных люмихрома и люмифлавина.
В рибофлавине устанавливают допустимое содержание примеси лю-мифлавина путем извлечения его хлороформом. Затем измеряют его оптическую плотность относительно хлороформа при длине волны 440 нм.
Растворы, приготовленные для количественного спектрофотометрического определения, используют для установления в рибофлавине допустимого содержания светопоглощающих примесей. Отношения оптических плотностей растворов рибофлавина, измеренных при определённых длинах волн, должны находиться в интервалах, приведенных в НД.
.
