- •6. Схема катаболизма
- •22.Цикл трикарбоновых кислот. Связь между общими путями катаболизма и цепью переноса электронов и протонов.
- •23.Регуляция общих путей катаболизма. Анаболические функции цикла Кребса
- •25. Переваривание и всасывание продуктов переваривания углеводов.
- •27. Аэробный дихотомический путь распада углеводов: химизм и биологическая роль.
- •36)Биосинтез и мобилизация гликогена. Биологическая роль этого процесса.
- •37) Регуляция катехоламинами и глюкагоном мобилизации гликогена.
1)Методы изучения обмена веществ. Изучение состояния обмена в-в можно проводить на отдельно взятой клетке в опытах in vitro, на субклеточных фракциях , полученных при гомогенизации клеток какой-либо ткани. Либо оценивать состояние метаболизма по промежуточным и конечным метаболитам, определяя скорость из образования или разрушения in vivo методами энзимного анализа, их содержание в биожидкостях человека в крови, лимфе, ликворе и моче различными биохимическими методами, в том числе радиоиммунного (метод количественного определения биологически активных веществ в биологических жидкостях, основанный на конкурентном связывании искомых стабильных и аналогичных им меченных радионуклидом веществ со специфическими связывающими системами, с последующей детекцией на специальных счетчиках — радиоспектрометрах.) иммуноферментного анализа (лабораторный иммунологический метод качественного или количественного определения различных соединений, макромолекул, вирусов и пр., в основе которого лежит специфическая реакция антиген-антитело. Выявление образовавшегося комплекса проводят с использованием фермента в качестве метки для регистрации сигнала.). При решении фундаментальных проблем, для изучения неясных метаболических механизмов в эксперименте на животных создаются модельные состояния и последовательно, начиная с целостного организма и органов, затем на уровне тканевых срезов, клеток и субклеточных структур, изучаются все звенья, все интересующиеся звенья метаболизма.
2 Состав пищи человека Пища, продукты питания, которые может использовать человек растительного и животного происхождения. Основные химические компоненты пищи: белки, жиры, углеводы, витамины. По содержанию аминокислот различают полноценные и неполноценные белки. К полноценным белкам относятся белки, содержащие все незаменимые аминокислоты. Это белки животного происхождения и некоторые бобовых культур. В пищевом отношении биологически ценными являются легкоплавкие липиды, к которым относятся растительные масла. В их составе содержаться полиненасыщенные жирные кислоты и среди них незаменимая линолевая кислота. В состав пищи должны входит минеральные в-ва и вода. Вода – это самое распространенное минеральное в-во в живых организмах. Нет ни одного организма, который мог бы обходиться без нее. Являясь неотъемлемым пищи, вода выполняет: является растворителем и стабилизатором биомолекул и ионов; явл-ся регулятором теплового баланса организма; обеспечивает транспортную функцию; способствует сохранению внутриклеточного давления, поддерживает форму клеток; явл-ся структурным компонентом клеточных мембран; используется для синтеза биомолекул; обеспечивает катаболизм биомолекул реакциями гидролиза. Минеральные в-ва находятся в организме человека в неодинаковом количестве. Макроэлементы – Ca, P, Mg, K, Na, Fe. Микроэлементы – I, F, Cu, Co, Mn, Zn. Все минеральные в-ва в организме находятся в виде соединений образующие ионы. Мин в-ва определяют величину осмотического и гидроосмотического давления. Они используются для построения опорных тканей. Короче, минеральные вещества выполняют биоэлектрическую, осмотическую, структурную, регуляторную, транспортную, энергетическую, опорную и синтетическую функции. При недостатке йода разрастается щитовидная железа (эндемический зоб), при недостатке фтора – кариес, недостаток цинка – задержка роста и специфический гиперкераноз. Отсутствие меди и кобальта – анемия.
3)Витамины – низкомолекулярные органические соединения, не синтезируемые в организме человека, но, присутствуя в небольших количествах в некоторых продуктах питания, при поступлении в организм обеспечивают нормальный метаболизм и выполнение клетками функции. Витамины делятся на две группы по физико-химическим функциям: жирорастворимые, водорастворимые.
Витамин А ( ретинол)
– антигемеролагический витамин. По
химической приподе это циклический
непредельный одноатомный спирт. Различают
2 формы: А1,
![]()
А2
![]() Много
витамина А содержится в печени рыб, в
говяжей печени, в молоке, желтке яиц. В
растительных продуктах в мокровке,
томат, свекла, салат. Все формы витамина
А оказывают влияние на белковый, липидный
и углеводный обмены. В белковом обмене
вит. А ускоряет превращение фенилаланина
в тирозин и синтез адреналина. В липидном
обмене – ускоряет синтез КоА и
сфингомиэлинов мозга, снижает синтез
холестерина. В углеводном обмене –
ускоряет синтез гликогена, путем
активации глюкоза-6-дегидрагеназы
активирует пентозный путь распада
глюкозы. Повышает проницаемость мембран.
Оказывает антигемералгический эффект,
участвует в фотохимическом акте зрения.
Много
витамина А содержится в печени рыб, в
говяжей печени, в молоке, желтке яиц. В
растительных продуктах в мокровке,
томат, свекла, салат. Все формы витамина
А оказывают влияние на белковый, липидный
и углеводный обмены. В белковом обмене
вит. А ускоряет превращение фенилаланина
в тирозин и синтез адреналина. В липидном
обмене – ускоряет синтез КоА и
сфингомиэлинов мозга, снижает синтез
холестерина. В углеводном обмене –
ускоряет синтез гликогена, путем
активации глюкоза-6-дегидрагеназы
активирует пентозный путь распада
глюкозы. Повышает проницаемость мембран.
Оказывает антигемералгический эффект,
участвует в фотохимическом акте зрения.
Витамин Д ( кальциферолы) – антирахитические витамины. По химической природе ненасыщенные одноатомные вторичные спирты. Различают – Д2-эргокальциферол
![]() и
витамин Д3-холекальциферол
и
витамин Д3-холекальциферол
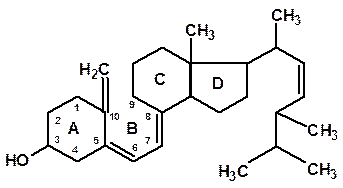
Витамин Д содержится в ряде продуктов животного происхождения ) печень, сливочное масло, молоко), в растительных маслах, в дрожжах. Очень много его в печени рыб. Основная функция – регуляция фосфо-кальциевого обмена, в частности транспорт кальция и фосфатов через клеточные мембраны. В костной ткани контролирует процесс мобилизации и отложения фосфорнокислых кальциевых солей.
Витамин Е(токоферолы) – витамины размножения.
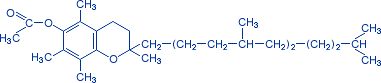
Источники – растительное масла, зародыши пшеницы. Обладают антиоксидантным действием, припятствуют развитию серии неуправляемых процессов пероксидного окисления ненасыщенных жирных кислот, липидов, мембран клеток. Ускоряет созревание сперматозоидов, улучшает их подвижность, нормализирует менструальный цикл.
Витамин К(нафтохинолы) – антигеммарогические витамины. Различают 2 вида: К1 (филлохинол) и К2 (менахинон):
![]()
![]()
Содержатся в капусте, шпинат, корнеплоды, фрукты, печень животного. Синтезируются бактериями тонкого кишечника. Регулирует процесс свертывания крови путем стимуляции синтеза протромбина. Стимулирует тканевое дыхание и окислительное фосфорилирование, повышают сократительную активность мышц.
ВОДОРАСТВОРИМЫЕ ВИТАМИНЫ:
Витамин В1(тиамин) антиневритный витамин.
![]()
два кольца – пиримидиновое и тиазоловое, объединенные метиленовой связью. Содержится в муке грубого помола, в горохе, фасоли, в мясных продуктах. Биологическая роль – кофермент(ТПФ) следующих ферментов: перуватдегадрогеназный комплекс, альфа-кетоглуторатдегидрагеназный комплекс, тренкетолаза. Тиаминтрифосфат принимает участие в транспортировке ионов калия и натрия, снижает активность ацетилхолинэстеразы, что обеспечивает высокий тонус парасимпатического отдела НС.
Витамин В2(рибофлавин)
![]()
гетероциклическое соединение – изоаллоксазин (сочетание бензольного, пиразинового и пиримидинового колец), к которому в положении 9 присоединен пятиатомный спирт рибитол. Содержится в молоке, твороге, в желтке, печени, в сердце, в дрожжах. Витамин В2 выполняет коферментную функцию, входит в состав ФМН и ФАД, принимает участие в фун-х след. ферментов: аэробные дегидрагеназы митохондрии, оксидаз аминокислот, моноаминоксидаз, диаминоксидаз, ксантиноксидаз.
Витамин В5(РР)(ниацин) – антиаллергический витамин
![]()
соединение пиридинового ряда, содержащее амидную группу. Основные источники – мясо, печень, дрожжи, рисовые отруби. Основные биофункции РР связаны с коферментами НАД, НАДФ: коферменты аэробных дегидрогеназ, синтез ДНК, аллостерическая регуляция ферментов в цикле Кребса и глюконеогенеза. Кроме кофермент фун-й: стимулирует синтез соляной кислоты, улучшает фун-ю печени и органов кроветворения, сосудорасширяющее действие.
Витамин В6(пиродоксин) – антидермативный витамин.
![]() производное
3-оксипиридина. Производные отличаются
природой замещающей группы в положении
4 пиридинового ядра. Источник – мясо
рыба, зерновые, бобовые культуры, кишечные
бактерии. Биофук-и связаны с пиродоксаль
зависимыми ферментами: трансаминаза
аминокислот, аминоферазы иодтиронинов,
декарбоксилаза аминокислот, аминофераза
гамма-аминомаслянной кислоты, синтетаза
дельта аминолевулиновой к-ты, фосфорилаза
гликогена. Кроме этого, стимулирует
всасывание аминокислот, ненасыщенных
жирных кислот, улучшает работу сердечной
мышцы, стимулирует гемопоэз.
производное
3-оксипиридина. Производные отличаются
природой замещающей группы в положении
4 пиридинового ядра. Источник – мясо
рыба, зерновые, бобовые культуры, кишечные
бактерии. Биофук-и связаны с пиродоксаль
зависимыми ферментами: трансаминаза
аминокислот, аминоферазы иодтиронинов,
декарбоксилаза аминокислот, аминофераза
гамма-аминомаслянной кислоты, синтетаза
дельта аминолевулиновой к-ты, фосфорилаза
гликогена. Кроме этого, стимулирует
всасывание аминокислот, ненасыщенных
жирных кислот, улучшает работу сердечной
мышцы, стимулирует гемопоэз.
Витамин Н(биотин, биос2) – антисеборейный витамин.
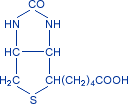
циклическое производное мочевины (имидазоловое и тиоэфирные кольца), боковая цепь которого представлена валериановой кислотой. Источники – яичный желток, печень, горох, соя. Биофун-я: определяет каталитическую активность биотиновых ферментов: пируваткарбоксилаза, ацетил-КоА-карбоксилаза, пропионил-КоА-карбоксилаза, карбомоилфосфатситетаза.
Витимин В3(пантотеновая к-та) β-аланин и 2,4-дигидрокси-диметил-масляная кислота.
![]()
Коферментная форма: HS-KoA (кофермент или коэнзим А - кофермент ацилирования). Строение КоА: а) тиоэтиламин б) пантотеновая кислота в) 3’-фосфоаденозин-5’-дифосфат. Участие в метаболизме: HSКоА - кофермент ацилирования, то есть входит в состав ферментов, которые катализируют перенос ацильных остатков. Поэтому В3 участвует:
а) в β-окислении жирных кислот и их биосинтезе
б)в окислительном декарбоксилировании α-кетокислот (пируват, α-кетоглутарат)
в) в биосинтезе нейтрального жира, липоидов, стероидов, гема гемоглобина, ацетилхолина.
Витамин В9(фолиевая к-та) Химическая природа: 3 структурных единицы – остаток птеридина, ПАБК (парааминобензойная кислота) и глутаминовая кислота.
![]()
Коферментная форма: тетрагидрофолиевая кислота (ТГФК)
Участие в метаболизме:
а)ТГФК является коферментом ферментов, переносящих одноуглеродные радикалы (формильную –СНО, метильную –СН3, метиленовую –СН2-, метенильную –СН=, оксиметильную –СН2ОН, формиминогруппу –СН=NН).
б) переносит одноуглеродистые фрагменты при биосинтезе метионина и тимина, серина, образовании пуриновых нуклеотидов и т.д.
Витамин В12(цианобламин) порфириноподобное корриновое ядро, содержащее центральный атом кобальта, соединенный с атомами азота четырех восстановленных пиррольных колец и с атомом азота 5,6-диметилбензимидазола.
( ФОРМУЛА ПРОСТО ОХУЕТЬ КАКАЯ БОЛЬШАЯ)
Коферментные формы: метилкобаламин (CH3-B12), дезоксиаденозилкобаламин (дАВ12)
Участие в метаболизме: а) реакции трансметилирования – метилкобаламин выполняет роль промежуточного переносчика метильной группы (синтез метионина и ацетата;) б) перенос водорода в реакциях изомеризации (глутаматмутазная реакция – взаимопревращения глутаминовой и β-метиласпарагиновой кислот и т.д.); в) предполагается участие в реакциях трансметилирования и дезаминирования
Витамин С – аскорбиновая кислота. лактон кислоты со структурой, близкой к структуре L-глюкозы. Является сильной кислотой. Природные изомеры, обладающие витаминной активностью, относятся к L-ряду.
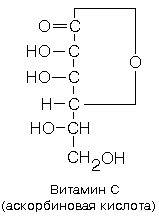
Источники – цитрусы, ягоды шиповника, смородины. Участие в метаболизме: биологическая роль связана с его участием в окислительно-восстановительных реакциях:
1. Витамин С, являясь сильным восстановителем, играет роль кофактора в реакциях окислительного гидроксилирования, что необходимо для окисления аминокислот пролина и лизина в оксипролин и в оксилизин в процессе биосинтеза коллагена.
2. Участвует в синтезе стероидных гормонов коры надпочечников (кортикостероидов).
3. Участвует в синтезе аминокислоты триптофана.
4. Способствует распаду тирозина и гемоглобина в тканях.
5. Необходим для всасывания железа.
6. Участвует в неспецифической иммунной защите организма.
4)Витаминоподобные вещества. При недостаточном поступлении витаминов в организм возможно возникновение патологического состояния (гиповитаминоз, авитаминоз). При этих состояниях, в зависимости от фун-й витаминов, нарушаетсякакой-либо этап метаболизма, проявляющейся соответствующими симптомами. Гиповитаминоз или авитаминоз возникает при недостатке витамина в пище, это так называемый алиментарный гипо- и авитаминоз. Возможны и вторичные гиповитаминозные состояния. Они связаны либо с нарушение всасывания витаминов, либо с нарушением их транспорта. При повышенном употреблении витаминов в организме могут возникнуть патологические состояния –
гипервитаминозы.
5. Обмен в-в и энергии – закономерный порядок превращения в-в и энерг. в живых системах направленная на их сохранение и самовоспроизведение. Обмен веществ стадии: - переваривание (ЖКТ) с высокомолекулярного до низкомолекулярного, устраняется межвидовая специф. белка; -всасывание продуктов гидролиза; - промежуточный обмен(метаболизм); выделение конечных продуктов. Катаболизм – это расщепление сложных молекул, как поступивших с пищей, так и входящих в состав клетки , до простых компонентов; конечные продукты(вода,СО2, мочевинв, мочевая кислота, креатинин, индикан и минеральные соли) свободная энергия(дых. цепь) используется для работы , для сокращения мышц, проведение нервных импульса, биосинтеза, активный транспорт веществ, поддержания осмотического давления, АТФ и НАДФН2. Катаболизм специфические пути общие пути(окис-ое декорбоксилирование пирувата) Цикл Кребса. При катаболизме образуется промежуточные субстраты от которых возможно отщепление двух атомов водорода – этот процесс дегидрирование( при наличии соответствующей дегидрогензы например изоцитрат, сукцинат, малат, альфакетаглутарат). Далее эти атомы водорода при участии дыхательной цепи вост. кислород до воды – строение митохондрии. Этот процесс сопровождается выделением свободной энергии особенно значительна в 3 пунктах т.к значительна разность редокса-потенциала. За счет этого образуется 3 молекулы АТФ: АДФ+Рн= АТФ; 3 мол АТФ – ионная дыхательная цепь а 2-1 молекула АТФ – неполная дыхательная цепь. Анаболизм- биосинтез компонентов клетки кроме незаменимых факторов (витамины, жирные кислоты) с использованием свободной энергии.
6. Схема катаболизма
Липиды Гликоген-крахмал Белки
Жирные Глицерин Глюкоза Аминокислоты
Ацето глицерофосфат Фруктоза – 1,6 дифосфат
цетил-КоА
Глицеральдегид – 3 фосфат
Пируват Пируват
СО2 Н2О +3 АТФ
Ацетио – КоА Ацетил –КоА Ацетил- КоА
+
Оксалоацетат Оксалоацетат
-Н2О+ 3 АТФ
Цитрил- КоА Малат
Цитрат Фумарат
- Н2О+ 2 АТФ
Изоцитрат Сукцинат
Н2О + 3 АТФ ГТФ
Оксалосукцинат Сукцинил- КоА
-Н2О+ 3АТФ
СО2 Альфа-кетоглутарат
7. Общие принципы регуляции метаболизма. Регуляция метаболизма на клеточном и субклеточном уровнях осуществляется прежде всего путем регуляции синтеза и каталитической активности ферментов. К таким регуляторным механизмам относятся: подавление синтеза ферментов. К таким регуляторным механизмам относятся: подавление синтеза ферментов конечным продуктом метаболич.пути , индукция синтеза одного или более ферментов субстратами, модуляция активности уже присутствующих молекул ферментов, в том числе алоостерическая регуляция. Большое значение имеет также регуляция скорости поступления метаболитов в клетку, где ведущую роль играют био.мембраны , окружающие цитоплазму и находящиеся в ней ядро, митохондрии, лизосомы и другие субклточные органеллы. Важнейшим средством, с помощью которого осущ-ся регуляция обмена веществ в живых организмах, являются гормоны. Особая роль в механизме действия гормонов принадлежит циклическим нуклеотидам.
8Основные конечные продукты метаболизма.В ходе многочисленных реакции метаболизма в клетках накапливаются вещества, которые оказываются непригодными для дальнейшего использования и подлежат выведению из организма. Эти вещества называют конечными продуктами обмена веществ. К ним относятся (вода,СО2, мочевинв, мочевая кислота, креатинин, индикан и минеральные соли). Выведение конечных продуктов обмена из организма человека происходит главным образом почками с мочей. Углекислый газ и вода выводятся из организма через легкие с выдыхаемым воздухом. Частично, вода и минеральные соли могут выводиться через кожу при потоотделении. Продукты распада гема (биллирубин, стеркобилин), холестерини другие стеройды(половые гормоны) , некоторе мин.в-ва выводятся из организма печенью в состав желчи. В норме за сутки организма взрослогочеловека выводится около 1000 грамм СО2 2,0-2,5 литра воды, до 30 грамм минеральных солей, 35-40 грамм органических низкомолекулярных азотсодержащих соединений. За сутки с мочой выводится 25-30 мочевины, 0.7-0.8 грамм мочевой кислоты, 1.5 грамма креатинина, 0.7гр гиппуровой кислоты, 5- 25 мкг индикана. При патологических состояниях выедение конечных продуктов может быть увеличено, например воды при несахарном и сахарном диабете, мочевой кислоты при подагре, кальций и фосфор при рахите и тд. В ряде случаев может иметь место задержка конечных продуктов обмена в-в в организме повышениеих концентрации в крови и в тканях. Например при нефрите уменьшается выведение воды и азотсодержащих конечных метаболитов(мочевина, мочевая кислота, аммонийные соли и др) с мочой, что приводит к отравлению организма,к уремии.
9. Основные типы окисления Микросомальное окисление осущ-ся ферментнми системами, локализованными преимущественно во фракциях микросом печени и надпочечников. В процессах микросомального окисления активированный кислород непосредственно внедряется в окисляемое вещество. Микросомальное окисление- механизм использования кислорода с «пластическими» целями. Ферментативные системы, локализованные в микросомной фракции и способные использовать молекулярный кислород для окисления специфичесих органических соединений, делятся на 2 группы: диоксегеназы и монооксигеназы. Диоксегеназы катализируют реакции, в которых в мелкулу органического субстрата вкл.оба атома молекулы кислорода А+О2 АО2 . Монооксигеназы присоединяют к субстрату только 1 из двух атомов кислорода. Обычно поставщиком атомов водорода для восстановления второго атома килорода до воды служит НАДФН» анпример: RH + O2 + НАДФН2 RОH+ Н2О + НАДФ.
Оксидазного типа происходит на мемранах эндоплазматического ретикулума и во внутр.мембране митохондрии.Ферменты- Оксидазы. По строению яв-ся металлофлавопротеинами.Находятся оксидахы в пероксисомах. Отнимают Н2 от субстрата и передают его на О2 с образованием Н2О2-перикиси водорода. Эти ферменты обычно обладают широкой субстратной специфичностью и невысокой активностью.
Пероксидное окисление липидов (ПОЛ) — один из наиболее важных окислительных процессов в организме. Это естественный метаболический процесс. Он необходим для осуществления процессов обновления липидов мембран, синтеза метаболитов арахидоновой
кислоты, являющихся биорегуляторами; активации макрофагов, разрушения чужеродных веществ, попавших в организм, уничтожения переродившихся клеток и т. д. При ряде патологических состояний (хроническом стрессе, действии жесткого ультрафиолетового света, ионизирующего излучения, лучевой болезни, канцерогенезе и др.) происходит активация ПОЛ.
10Макроэргические соединения. К макроэргическим соединения относятся АТФ и другие нуклеотид- 5- трифосфат, креатинфосфат, 1,3- дифофоглицерат, фосфоенолпируват. Из всех макроэргов Атф- главный хим.посредник клетки, связывающий между собой процессы идущие с выдлением и поглощением энергии(катаболизма, анаболизма), служит общим промежуточным продуктом в реакиях переноса энергии с фосфатными группами, используется для обеспечения энергией мышечного сокращения, для активного транспорта через мембраны, поставляет энергию для биолюминесценции и др. АТФ – постоянный универсальный носитель энергии для клетки. Роль АТФ можно сравнить с ролью аккумулятора. Он мобилен и может доставлять хим.энергию в любую часть клетки. Когда клетка нуждается в энергии, единственное, что требуется для ее получения- это гидролиз АТФ. АТФ+ Н2О АТФ-аза АДФ+Н3РО4 + своб.энерг идет на работу
11) Понятие о тканевом дыхании и биологическом окислении. Высвобождение свободной энергии при катаболизме углеводов, липидов и аминокислот может происходить в животном организме в аэробных и анаэробных условиях. Энергетически более выгоден аэробный путь катаболизма, который сопровождается в обязательном порядке поглощением тканями кислорода и выделением углекислого газа, т.е явление называемое тканевое дыхание или внутреннее, клеточное дыхание. В основе биологического окисления различных энергетических субстратов, как показали исследования, лежат три след. Типа реакций:1.перенос электронов2.перенос атомов водорода3.перенос атомов кислорода Основными энергетическими субстратами служат углеводы и жиры. Так клетки головного мозга млекопитающих вообще не способны использовать для клеточного дыхания, ничего кроме глюкозы. Окисление глюкозы в клетке, как главного энергетического субстрата, происходит путем последовательных реакций дегидрирования. При этом в анаэробных условиях окисление глюкозы завершается образованием двух молекул пирувата, которые восстанавливаются в две молекулы лактата. В аэробных условиях, образующиеся в цитозоле при гликолизе две молекулы пирувата подвергаются в митохондриях окислительному декарбоксилированию с образованием двух молекул ацетил КоА, которые разрушаются в цикле Кребса до углекислого газа и воды с высвобождением свободной энергии, трансформируемой ферментами дыхательной цепи митохондрий в макроэргические связи АТФ.
12. Дегидрирование субстратов и окисление водорода как источник энергии в клетке. Биологическое окисление это процесс дегидрирования субстрата с помощью промежуточных переносчиков водорода и его конечного акцептора. Если в роли конечного акцептора выступает кислород, процесс называется аэробным окислением или тканевым дыханием, если конечный акцептор представлен не кислородом анаэробным окислением. Анаэробное окисление имеет ограниченное значение в организме человека. Основная функция биологического окисления обеспечение клетки энергией в доступной форме. Тканевое дыхание процесс окисления водорода кислородом до воды ферментами цепи тканевого дыхания. Оно протекает по следующей схеме: Вещество окисляется, если отдает электроны или одновременно электроны и протоны (атомы водорода), или присоединяет кислород. Способность молекулы отдавать электроны другой молекуле определяется окислительно-восстановительным потенциалом (редокс-потенциалом). Любое соединение может отдавать электроны только веществу с более высоким окислительно-восстановительным потенциалом. Окислитель и восстановитель всегда образуют сопряженную пару.
13.Строение митохондрий и структурная организация цепи переноса электронов и протонов. Митохондрии имеются во всех эукариотических клетках. Эти органеллы главное место аэробной дыхательной активности клетки. Число митохондрий в клетке очень непостоянно и зависит от вида и природы клеток. Чрезвычайно варьируют размеры и форма митохондрий. Они могут быть овальными, округлыми, вытянутыми, спиральными и даже разветвленными. Длина митохондрий колеблется в пределах 1,5-10 мкм, а ширина 0,25-1,0 мкм . Митохондрии могут изменить свою форму. Каждая митохондрия окружена двумя мембранами. Наружную мембрану отделяет от внутренней расстояние в 6-10нм. Внутренняя мембрана заключаетя себе полужесткий матрикс митохондрий и образует многочисленные гребневые складки кристы. Внутренняя мембрана отличается избирательной проницаемостью. Митохондрии любой клетки быстро и очень экономно осуществляют процесс окисления различных субстратов путем отщепления атома водорода, разбивают его на протон и электрон и тем самым обеспечивают трансформацию химической энергии субстратов вначале в электрохимический потенциал градиента концентрации протонов на мембране, затем на процесс окислительного фосфорилирования, завершающийся синтезом АТФ. Этот процесс включает несколько этапов, в котором участвует ряд промежуточных ферментов переносчиков протонов и электронов на конечный акцептор-кислород, образующих дыхательную митохондриальную цепь. Путь протонов и электронов атома расходится. Перенос электронов осуществляется с помощью цитохромов b,c1,c,a и a3. Комплекс цитохромов b и c1 функционирует как КоQH- дегидрогеназа, которая осуществляет перенос электронов на цитохром c. Протоны при этом переходят в раствор. Перемещение электронов и протонов происходит по градиенту окислительно-восстановительного потенциала, который отражает величину свободной энергии окисления в соответствующей редокс-системе.
14. Дегидрогеназы и первичные акцепторы водорода - НАД и флавопротеиды; НАДН-дегидрогеназы. В тканях никатиновая кислота и никотинамид используется для синтеза коферментов НАД и НАДФ. Синтез НАД может идти непосредственно из триптофана через стадию образования кинуренина, 3-гидрооксикинунерина идр. НАД используется как субстрат ДНК-лигазной реакйции, т.е синтеза ДНК. НАД и НАДФ являются аллостерическими регуляторами ферментов цикла Кребса, ключевых ферментов глюконеогенеза. Никотинамидадениндинуклеоти́д (НАД, NAD) — кофермент, присутствующий во всех живых клетках, входит в состав ферментов группы дегидрогеназ, катализирующих окислительно-восстановительные реакции; выполняет функцию переносчика электронов и водорода, которые принимает от окисляемых веществ. Восстановленная форма (NADH) способна переносить их на другие вещества. Представляет собой динуклеотид, молекула которого построена из амида никотиновой кислоты и аденина, соединённых между собой цепочкой, состоящей из двух остатков D-рибозы и двух остатков фосфорной кислоты; применяется в клинической биохимии при определении активности ферментов крови. Отличие его от другого важнейшего кофермента — никотинамидадениндинуклеотидфосфата, или NADP, в том, что последний содержит в молекуле ещё один остаток фосфорной кислоты, связанной с 21-углеродным атомом рибозы. НАДН дегидрогеназа) окисляет НАД-Н, отбирая у него два электрона и перенося их на растворимый в липидах убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 4 протона из матрикса в межмембранное пространство митохондрии.
15. Терминальное окисление: убихинон, цитохромы. Цитохромоксидаза. Цитохромы — это гемопротеины — белки, содержащие в качестве прочно связанной простетической группы гем:
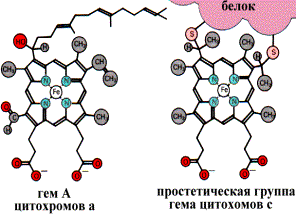
Убихинон (как окисленный, так и восстановленный) совершенно нерастворим в воде, но хорошо растворяется в средах с низкой диэлектрической постоянной ("жирные" среды). Длинный хвост убихинона, по-видимому, вытянут в плоскости гидрофобного слоя мембраны, а активная голова может располагаться либо в той же плоскости, либо приближаться к поверхностям мембраны, контактирующим с водными фазами. Важное свойство убихинона, которое понадобится нам при дальнейшем рассмотрении, состоит в том, что его голова может восстанавливаться ступенчато, принимая последовательно по одному электрону (и протону).
Убихинон (кофермент Q) — производное изопрена:
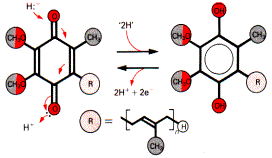
Цитохромоксидаза включает комплекс цитохромов а и а3 (комплекс IV). Цитохромоксидаза кроме гема содержит ионы меди, которые способны менять валентность и таким способом участвовать в переносе электронов:
![]()
Цитохромоксидаза переносит электроны с цитохрома С на кислород. В переносе электронов участвуют сначала ионы железа цитохромов а и а3, а затем ион меди цитохрома а3. Молекула кислорода связывается с железом в геме цитохрома а3. Следовательно, переход электронов на кислород с иона меди цитохрома а3, происходит на молекуле фермента. Каждый из атомов молекулы кислорода присоединяет по два электрона и протона, образуя при этом молекулу воды. Белки, содержащие негеминовое железо. Некоторое количество атомов железа в митохондриях связано не в геме цитохромов, а образует комплексы с другими белками. Эти белки называют также железосерными, так как атомы железа связаны с атомами серы цистеиновых остатков. Белки, содержащие негеминовое железо, участвуют в переносе электронов на нескольких стадиях, однако, не совсем ясны их локализация и механизм действия.
16.Механизмы трансформации энергии в клетке Согласно предложенной П. Митчеллом гипотезе, движущей силой фосфорилирования АДФ служит энергия разности редокс-потенциалов, возникающая при переносе электронов от окисляемого субстрата по дыхательной цепи к кислороду трансформируемая в энергию протонного электрохимического потенциала ( dM H+) , возникающая на внутренней мембране митохондрий. За счет протонов отщепляемых от окисляемых субстратов и накопления их тна наружной стороне мембраны митохондрий, она оказывается электроположительной , а со стороны митохондриального матрикса заряжается элктроотрицательно. Ионы Н+ , выведенный наружу , под воздействием электроосмотических сил устремляются внутрь , в митохондриальный матрикс через специальные протонный каналы , в которых функционирует Н+ - АТФ синтетаза . Переход ионов Н+ с более высокой в зону с более низкой их концентрацией сопровождается выделением свободной энергии , за счет которой и сетезируется АТФ. До определенного времени считалось что АТФ и только АТФ выполняет универсальную аккумулирующую энергию функцию в клетке. Однако исследованиями В,П Скулачева и другими биоэнергетиками было устанолено что трансмембранный электрохимический потенциал , возникающий на мембране за счет Н+ градиента является универсальной формой энергии в клетке и может быть использован : -для синтеза АТФ ; - для транспорта ионов кальция и др. ионов; - для транспорта фосфатов; - для транспорта АДФ и АТФ; - для теплообразования ; - для сократительной и двигательной активности.В нормальной функционирующей клетке процесс трансформации энергии и степень окислительного фосфорилирования зависит от целого ряда факторов : от целостности митохондриальной мембраны , от типа окисляемого субстрата , от уровня кислорода , доставки неорганического фосфата и уровня АДФ.
17.Регуляция цепи переноса электронов и протонов (дыхательный контроль).Согласно предложенной Митчелом гипотезе, движущей силой фосфорилирования АДФ служит энергия разности редокс-потенциалов, возникающая при переносе электронов от окисляемого субстрата по дыхательной цепи к кислороду и трансформируемой в энергию протонного электрохимического потенциала (dMH+), возникающего на внутренней мембране митохондрий.За счет протонов отщепляемых от окисляемых субстратов и накопления их на наружной стороне мембраны митохондрий, она оказывается электроположительной, а со стороны митохондриального матрикс через специальные протонные каналы, в которых функционирует H+-АТФ синтетаза
18Окислительное фосфорилирование.При окислении одной молекулы субстрата на один атом поглощенного митохондриями кислорода может использоваться от одного до трех молекул фосфорной кислоты и синтезироваться при этом 1, 2 или 3 молекулы АТФ. Это процесс - процесс синтеза АТФ в реакциях биологического окисления субстратов получил название - окислительное фосфорилирование. Для его количественной оценки был введен показатель окислительного фосфорилирования - коэффициент Р/О . Коэффициент Р/О (АДФ/О) - это есть отношение количества молекул фосфорной кислоты (АДФ) к количеству атомов кислорода использованных митохондриями при окислении какого-либо субстрата.
19Разобщение тканевого дыхания и окис.фосфор.е.Окисление субстратов и фосфорилирование АДФ в митохондриях прочно сопряжены. Скорость использования АТФ регулирует скорость потока электронов в ЦПЭ. Если АТФ не используется и его концентрация в клетках возрастает, то прекращается и поток электронов к кислороду. С другой стороны, расход АТФ и превращение его в АДФ увеличивает окисление субстратов и поглощение кислорода. Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. Некоторые химические вещества (протонофоры) могут переносить протоны и другие ионы (ионофоры) из мембранного пространста через мембрану в матрикс, минуя протонные каналы АТФ-синтазы. В результате этого исчезает электрохимический потенциал и прекращается синтез АТФ. Это называют разобщением дыхания и фосфорилирования. В результате разобщения количество АТФ снижается, а АДФ увеличивается, что приводит к возрастанию скорости окисления НАДН и ФАДН2, возрастает и количество поглощенного кислорода, но энергия выделяется в виде тепла, и коэффициент Р/О резко снижается (свободное окисление). Разобщители – липофильные вещества, легко проходящие через липидный слой мембраны: - 2,4-динитрофенол, - дикумарол (антивитамин вит. К); - билирубин (продукт распада гема); - тироксин (гормон щитовидной железы). Все эти вещества проявляют разобщающее действие только при их высокой концентрации.
20.Терморегуляторная функция тканевого дыхания. Гипоэнергетические состояния возникают: 1) при нарушении поступления субстратов для дегидрирования ( на всех этапах от пищи до матрикса митохондрий); 2) при нарушении поступления О2 в митохондрии ( на всех этапах от дыхания, связь с НЬ, транспорт и др.); 3) при нарушении мембран митохондрий, композиции липидного бислоя и ферментативных ансамблей внутренней мембраны митохондрий. Живая клетка нуждается в АТФ непрерывно, поскольку разнообразные процессы, связанные с использованием АТФ, в клетке никогда не прекращаются. Например, для обновления белков расходуется около 15 % всей энергии основного обмена (т. е. обмена в состоянии покоя), на поддержание трансмембранного градиента концентраций ионов натрия и калия — около 30 %. При переходе к мышечной активности потребность в АТФ многократно увеличивается. Запасов АТФ в клетке практически не создается. Например, в сердечной мышце АТФ истощается за несколько секунд, если блокирован его синтез. Следовательно, клетка непрерывно должна получать пищевые вещества (доноры водорода) и кислород для поддержания синтеза АТФ. При голодании в качестве источников энергии используются собственные вещества тканей. Энергетический обмен в этих условиях снижен: через две недели голодания потребление кислорода уменьшается на 40 % (алиментарная форма гипоэнергетического состояния). Резервов пищевых веществ в организме хватает на несколько недель полного голодания, запасов же кислорода нет, поэтому при лишении кислорода уже через 2-3 мин наступает смерть. Гипоксия — наиболее частая причина гипоэнергетических состояний (табл. 8.5), а гипоксия мозга — наиболее частая непосредственная (последняя) причина смерти. Поэтому среди реанимационных процедур ведущее место занимают меры, направленные на восстановление снабжения органов кислородом.
21) .Понятие о специфических и общих путях катаболизма. Окислительное декарбоксилирование пировиноградной кислоты. Специфические и общие пути катаболизма . В катаболических процессах можно выделить два звена: - специфические пути катаболизма, разные для различных классов соединений (белков, жиров, углеводов и др.), - общие пути катаболизма - единые пути катаболизма для различных классов веществ, являющиеся продолжением специфических путей. С общими путями катаболизма, в основном, связаны главные биоэнергетические процессы, сопряженные с высвобождением и накоплением энергии в клетке.К специфическим путям катаболизма относятся реакции гидролиза белков, углеводов, липидов происходящие в желудочно-кишечном тракте или в тканях, реакции разрушения моносахаридов, аминокислот, жирных кислот, спиртов, происходящие в клетках и, в конце концов, завершающиеся образованием пировиноградной кислоты или ацетильным радикалом в форме ацетил-КоА.
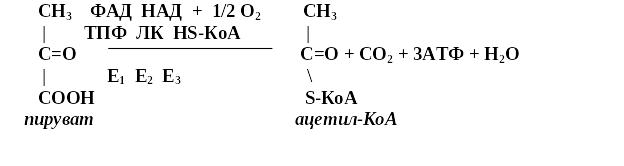
Окислительное декарбоксилирование пировиноградной кислоты
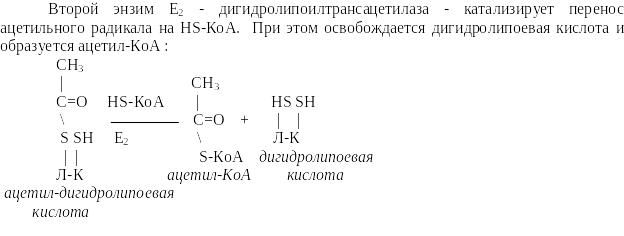
Окислительное декарбоксилирование пирувата катализируется мультиэнзимным пируват-дегидрогеназным комплексом, локализованным на внутренней мембране митохондрий со стороны матрикса. Пируват-дегидрогеназный комплекс (окислительная декарбоксилаза пировиноградной кислоты) состоит из трех ферментов (Е1,Е2,Е3): Е1-пируватдекарбоксилаза с коферментом ТПФ (тиаминпирофосфат), Е2-дигидролипоил-трансацетилаза с коферментом липоевая кислота (ЛК) и кофактором - НS-КоА, Е3-дигидролипоил-дегидрогеназа с коферментом ФАД и кофактор -НАД Пировиноградная кислота (пируват) и ацетил-КоА являются теми метаболитами, которые, включаясь в общие пути катаболизма, разрушаются до углекислого газа и воды, поставляют энергию для синтеза АТФ в митохондриях. К общим путям катаболизма относятся следующие метаболические процессы (оба эти процесса локализованы в митохондриях): - окислительное декарбоксилирования пировиноградной кислоты; - превращение ацетил-КоА в цикле трикарбоновых кислот Кребса (Ц Т К ).Пируват (пировиноградная кислота) является одним из центральных метаболитов углеводного обмена. При окислительном декарбоксилировании пирувата образуется ацетил-КоА - ключевой субтсрат цикла трикарбоновых кислот Кребса. В анаэробных условиях из пирувата образуется молочная кислота. В процессе глюконеогенеза из пируват синтезируется глюкоза. Повышение уровня пирувата наблюдается при гиповитаминозе В1, при интенсивной мышечной работе, при сердечной декомпенсации, сахарном диабете, при гепатитах. В ликворе концентрация пирувата резко повышается после черепно-мозговой травмы, при менингите, абсцессе мозга.
Окисление пирувата