
- •Л.Й. Дворкін, і.Г. Скрипник фізико-хімічні і фізичні методи досліджень будівельних матеріалів
- •Передмова
- •1. Основні поняття та визначення
- •1.1. Фізико-хімічний аналіз
- •1.2. Хімічні, фізичні і фізико-хімічні методи аналізу
- •1.З. Фізико-хімічні і фізичні методи досліджень
- •Фігуровського
- •2.1.1. Опис експериментальної установки
- •2.1.2. Порядок обробки результатів вимірювань
- •2.1.3. Питання самоконтролю
- •2.2. Визначення питомої поверхні дисперсних матеріалів
- •2.2.1. Суть методу та опис приладу псх-2. Робоча формула
- •2.2.2. Прилад Блейна
- •2.2.3. Питання самоконтролю
- •Література
- •3. Методи дослідження структури порового простору будівельних матеріалів
- •3.1. Будова пористого матеріалу
- •3.1.1. Пікнометричний метод визначення істинної густини речовини
- •3.1.2. Визначення середньої густини твердих тіл за допомогою гідростатичного зважування
- •3.1.3. Визначення загальної, відкритої та закритої пористості твердих тіл
- •3.1.4. Питання самоконтролю
- •Література
- •3.2. Метод визначення показників пористості матеріалів за кінетикою їх водопоглинання
- •3.2.1. Порядок обробки результатів вимірювань
- •3.2.2 .Питання самоконтролю
- •Література
- •4. Визначення в’язкості речовин в рідкому стані та дослідження реологічних властивостей структурованих дисперсних систем
- •4.1. Визначення умовної в'язкості рідин
- •4 Рис. 4.2. Віскозиметр .1.1. Опис експериментальної установки
- •4.2. Дослідження в’язкості рідин методом Пуазейля і Стокса
- •4.3. Дослідження в’язкості рідин методом Швидковського
- •4.3.1. Опис експериментальної установки
- •Ампула зі зразком
- •Кінематичної в'язкості
- •4.4. Дослідження реологічних властивостей структурованих дисперсних систем
- •4.4.1. Опис експериментальної установки
- •4.5. Визначення граничної напруги зсуву формовочних мас конічним пластоміром
- •4.5.1. Опис експериментальної установки
- •4.6. Питання самоконтролю
- •Література
- •5. Термічні методи дослідження матеріалів
- •5.1. Простий термічний аналіз (та)
- •5.2. Диференціальний термічний аналіз (дта)
- •5.3. Термогравіметричний аналіз (тг) та диференціальнотермогравіметричний аналіз (дтг) матеріалів
- •5.4. Ідентифікація олігомерів та полімерів як приклад застосування термографії
- •5.5. Питання самоконтролю
- •Література
- •6. Методи дослідження теплофізичних властивостей матеріалів
- •6.1. Теплопровідність як явище переносу енергії
- •6.1.1 .Вимірювання теплопровідності методом відносного горизонтального шару
- •6.1.2. Опис експериментальної установки
- •6.2. Питома теплоємність будівельних матеріалів
- •6.2.1. Визначення питомої теплоємності матеріалів калориметричним методом змішування
- •6.2.2. Опис експериментальної установки
- •6.3. Калориметричні методи
- •6.3.1. Тепловиділення
- •6.3.2. Теплота гідратацій цементу
- •(За о.В. Ушеровим-Маршаком):
- •6.3.3. Види калориметрії
- •6.3.4. Термосний метод калориметрії
- •6.3.5. Ізотермічний метод калориметрії
- •6.3.6. Адіабатичний метод калориметрії
- •6.3.7. Метод розчинення
- •6.3.8. Диференціальна мікрокалориметрія
- •6.4. Питання самоконтролю
- •Література
- •7. Ультразвукові методи дослідження властивостей матеріалів
- •7.1. Основні положення
- •7.2. Суть та застосування ультразвукового імпульсного методу для дослідження міцності бетону
- •7.3. Питання самоконтролю
- •Література
- •8. Дослідження електрофізичних властивостей сировини та матеріалів
- •8.1. Метод електропровідності
- •8.1.1. Вимірювання електропровідності матеріалів контактним методом
- •8.2. Метод діелектрометрії
- •8.2.1. Відносна діелектрична проникність речовини та діелектричні втрати
- •8.2.2. Застосування методу діелектрометрії
- •8.2.3. Установка для вимірювання ємності та діелектричних втрат на змінному струмі
- •8.3. Питання самоконтролю
- •Література
- •9. Застосування методу термо-е.Р.С. Для визначення вмісту вуглецю в сталях і чавунах та фізичні основи теорії і практики термоелектричної термометрії
- •9.1. Фізичні основи термоелектричних ефектів
- •9.1.1. Ефект Пельтьє
- •9.1.2.Ефект Томсона
- •9.1.3. Ефект Зеебека
- •9.2. Закони термоелектричних ефектів та їх застосування
- •9.3. Конструкція приладу експрес-методу термо-е.Р.С. Для визначення вмісту вуглецю в сталях і чавунах та виробах із них
- •9.3.1. Принципова і електровимірювальна схема та функціональна робота приладу.
- •9.3.2. Електрична схема тиристорного регулятора температур робочих електродів
- •9.3.3. Механічна частина приладу
- •9.3.4. Обґрунтування вибору матеріалів для виготовлення робочих електродів, наконечників, термопар і нагрівних елементів
- •Значення коефіцієнтів а, в і с та е0100 для Cu і Ag, в контакті із Fe
- •Фізичні властивості для Сu, Аg, Fe і ніхрома
- •Термоелектрична характеристика гілок тха
- •9.3.5. Калібровка приладу та його апробація
- •9.3.6. Основні конструкційні і технічні характеристики приладу
- •9.4. Області застосування методу термо-е.Р.С.
- •9.5. Питання самоконтролю
- •Література
- •10. Метод рентгенографічного дослідження фазового складу сировини та матеріалів
- •10.1. Структура кристалічних речовин, дифракція рентгенівських променів та суть методу рентгенографії
- •10.2. Застосування методу рентгенографії
- •10.3. Якісний рентгенфазовий аналіз
- •10.4. Питання самоконтролю
- •Література
- •11. Оптична спектроскопія
- •11.1. Атомна спектроскопія
- •11.1.1. Емісійний спектральний аналіз
- •11.1.2. Фотометрія полум'я
- •11.1.3. Атомно-абсорбційний спектральний аналіз
- •11.2. Молекулярна спектроскопія
- •11.2.1. Спектроскопія комбінаційного розсіювання
- •11.2.2. Застосування інфрачервоної спектроскопії
- •11.3. Питання самоконтролю
- •Література
- •12. Метод інфрачервоної спектроскопії у дослідженні органічних і неорганічних речовин
- •12.1. Взаємодія інфрачервоного випромінювання з речовиною
- •12.2. Способи зображення спектрів пропускання та поглинання
- •12.3. Апаратура та приготування досліджуваних зразків
- •12.3.1. Спектрометр
- •12.3.2. Джерела інфрачервоного випромінювання
- •12.3.3. Монохроматори та їх оптичні характеристики
- •12.3.4. Приймачі випромінювання
- •12.3.5. Приготування досліджуваних зразків
- •12.3.6.Інфрачервоний спектрофотометр типу ur -20
- •12.4. Розшифровка інфрачервоного спектру поглинання
- •Спектри каолініту:
- •12.5. Питання самоконтролю
- •Література
- •13. Оптична мікроскопія
- •13.1. Застосування оптичної мікроскопії
- •13.2.Оптична схема і принцип дії мікроскопа та основні його характеристики
- •13.3. Вимірювання лінійних розмірів об'єкта за допомогою мікроскопа
- •13.4. Методи мікроскопії
- •13.4.1. Дослідження матеріалів у прохідному світлі
- •Мікроскопа
- •13.4.2. Дослідження матеріалів у відбитому світлі
- •Мікроскопа
- •13.4.3. Метод ультрамікроскопії
- •13.4.4. Метод спостереження об'єктів у поляризованому світлі
- •13.4.5. Метод дослідження у люмінесцентному світлі та флуоресцентна мікроскопія
- •13.4.6. Методи спостереження в ультрафіолетових та інфрачервоних променях
- •13.4.7. Методи фазового та інтерференційного контрасту
- •13.4.8. Високо- і низькотемпературна мікроскопія
- •13.4.9. Телевізійна мікроскопія
- •13.5. Питання самоконтролю
- •Література
- •14. Електронна мікроскопія
- •14.1. Оптична схема та вузли електронного мікроскопа
- •14.2. Роздільна здатність і збільшення електронного мікроскопа
- •14.3.Типи електронних мікроскопів
- •14.4. Методи досліджень в електронній мікроскопії
- •14.5. Методи препарування зразків для досліджень
- •14.6. Растрова електронна мікроскопія
- •14.6.1. Суть методу електронної растрової мікроскопії
- •14.6.2. Електронні растрові мікроскопи на просвічування і відбивання
- •Р ис. 14.7. Принципова схема растрового електронного мікроскопа на просвічування:
- •14.6.3. Растрова мікроскопія спеціального призначення
- •14.7. Приклади використання електронної мікроскопії
- •14.8. Питання самоконтролю
- •Література
6.2. Питома теплоємність будівельних матеріалів
По відношенню до впливу теплоти визначають технологічні та експлуатаційні характеристики матеріалів. Окрім теплопровідності, до теплофізичних властивостей відноситься питома теплоємність, яка залежить від хімічного складу і будови матеріалів, їх температури та вологості.
За визначенням питома теплоємність речовини С дорівнює кількості теплоти Q , яку необхідно передати тілу одиничної маси, щоб нагріти його на один градус:
c = Q / m( Т – Т ) = Q/(m ΔT) (6.18)
Питома теплоємність С в системі одиниць СІ вимірюється в Дж/кгК. При необхідності можна скористатись співвідношенням 1ккал/кгС = 4,1868 кДж/кгК.
Знання значень питомої теплоємності будівельних матеріалів потрібні для теплотехнічних розрахунків. Так питома теплоємність скла знаходиться в досить широких межах - від 0,335 до 1,047 кДж/кгК, природних й штучних кам'яних матеріалів від 0,754 до 0,921 кДж/кгК. Для органічних матеріалів вона, значно вища, ніж для неорганічних.
Підвищення теплоємності із зростанням температури виражається лінійною залежністю:
с = с0(1+αT) (6.19)
де с - питома теплоємність при 0°С; α - константа; T - абсолютна температура.
Для матеріалів, які нагрівають до дуже високих температур, користуюся залежністю:
с
= a
+ вT
+с΄T![]() (6.20)
(6.20)
де а, в, с' - емпіричні коефіцієнти.
6.2.1. Визначення питомої теплоємності матеріалів калориметричним методом змішування
М
Рис. 6.5.
Калориметр
змішування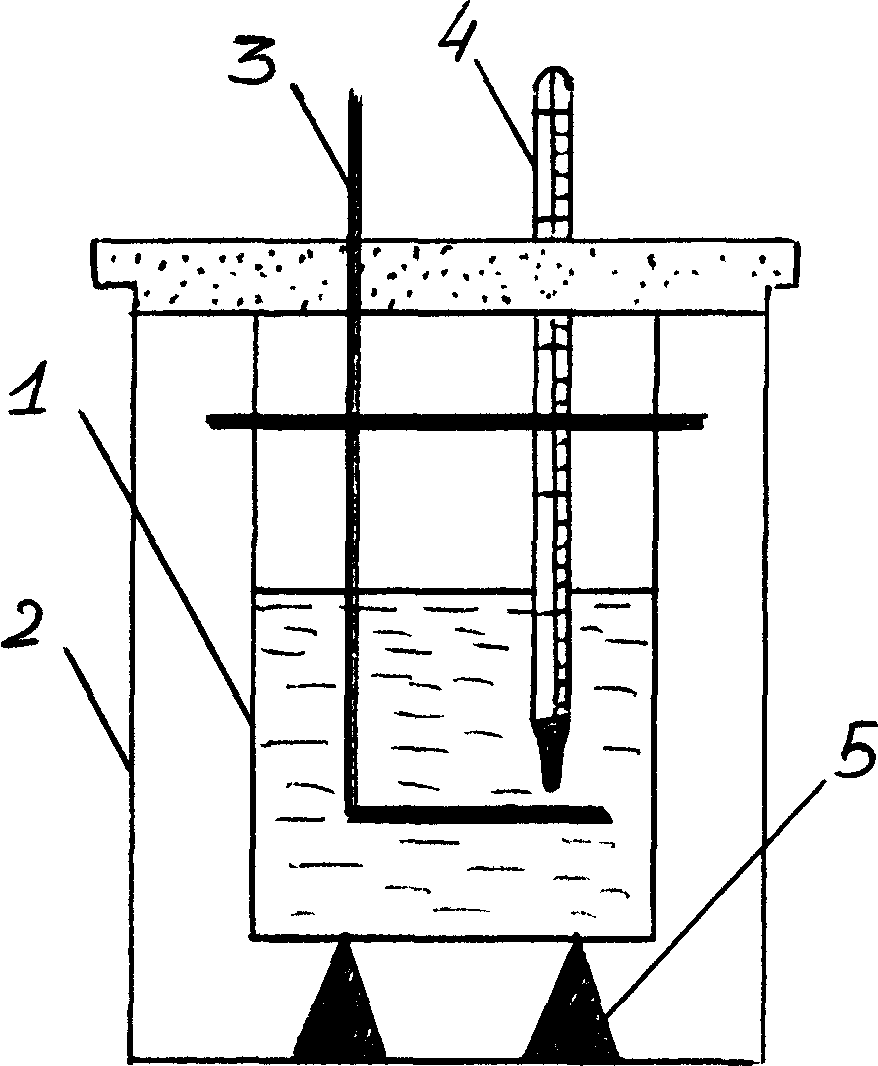
При калориметричних вимірюваннях теплових сталих різних речовин енергія витрачається не лише на забезпечення протікання досліджуваного процесу, а й на нагрівання калориметра, термометра, мішалки та інших частин калориметричної установки. Ці затрати теплової енергії необхідно визначати та враховувати при обчисленні сталих речовин. Нерідко безпосереднє визначення затрат теплової енергії ускладнюється відсутністю відомостей про природу і масу матеріалів, з яких виготовлені частини установки. Тому в практиці калориметричних вимірювань широко використовуються так звані водяні еквіваленти різних тіл.
Під водяним еквівалентом К будь-якого тіла розуміють кількість теплової енергії, необхідної для нагрівання його на 1°С, яка чисельно дорівнює масі води, для нагрівання якої на 1°С потрібна така ж кількість теплової енергії, як і для нагрівання тіла.
Якщо К калориметра, мішалки і термометра незначні порівняно з кількістю теплоти, яка витрачається на протікання досліджуваних процесів, і вимірювання теплових сталих цих процесів не забезпечують достатньої точності результатів, то їх не визначають і не беруть до уваги при остаточних підрахунках. В інших випадках водяні еквіваленти обчислюють або знаходять дослідним шляхом (калориметричним методом).
При певних вимірюваннях можна вважати , що рідина, калориметр і його допоміжні частини за час досліду не встигнуть віддати помітну кількість теплоти зовнішньому середовищі. При прецизійних калориметричних вимірюваннях необхідно вносити відповідні поправки.
Водяний еквівалент ртутного термометра можна визначати як дослідним, так і розрахунковим шляхом, спиртових термометрів - лише дослідним, оскільки водяні еквіваленти скла та спирту, взятих в однакових об'ємах, значно відрізняються між собою. Відомо, що водяний еквівалент ртутного термометра можна визначити за виміряним об'ємом його зануреної частини, прийнявши, що водяний еквівалент одиниці об'єму ртутного термометра становить 0,46 кал/градсм3. Об'єм зануреної частини термометра V знаходять за допомогою мензурки. Тоді водяний еквівалент ртутного термометра становить:
Кт = 0,46V кал/град. (6.21)
Визначення питомої теплоємності речовин методом змішування ґрунтується на термодинамічному принципі, за яким тіла при контакті обмінюються теплом до моменту досягнення однакової температури.
Для визначення питомої теплоємності твердого тіла його нагрівають у спеціальному нагрівнику та занурюють у калориметр з холодною водою.
Нехай маса тіла m , початкова температура t , його кінцева температура t. Тоді кількість тепла, яку віддасть тіло при охолодженні:
Q = mc (t – t) (6.22)
Якщо втрати в зовнішнє середовище дуже малі, ними можна знехтувати. Тоді кількість теплоти на нагрівання води та калориметра:
Q = (m c + m c + 0,46V)(t –t ) (6.23)
де m - маса води в калориметрі; t - її температура до експерименту; c1 - її теплоємність; m2 - маса калориметра з мішалкою; c2 - питома теплоємність калориметра з мішалкою; 0,46 V - водяний еквівалент термометра (V - об'єм зануреного термометра).
Користуючись законом збереження і перетворення енергії та нехтуючи обміном теплоти з зовнішнім середовищем, на підставі рівностей (6.22) та (6.23) записуємо:
mc (t – t) = (m c + m c + 0,46V)(t –t ) (6.24)
звідки
c = (m c + m c + 0,46V)(t –t ) / m(t – t) (6.25)
