
- •Павлоцька л.Ф., дуденко н.В., димитрієвич л.Р., божко н.В. Біологічна хімія суми – 2008
- •Передмова
- •Розділ 1. Біохімічна характеристика живих організмів
- •1. 1. Хімічний склад організму людини
- •1. 2. Структура клітини
- •1.3. Роль обміну речовин у життєдіяльності організму
- •1.4. Значення харчових факторів у забезпеченні процесів життєдіяльності
- •Контрольні питання і завдання.
- •Тести для контролю знань і самопідготовки
- •6. Які елементи складають понад 98% маси біосфери?
- •Розділ 2. Хімія білків
- •2.1. Біологічна роль білків
- •2. 2. Амінокислоти
- •Стереоізомерія амінокислот
- •Фізико-хімічні властивості амінокислот
- •Амінокислотний склад білків
- •2.3. Біологічна роль окремих амінокислот
- •2.4. Будова й структурна організація білкової молекули Поліпептидна будова білків
- •Типи хімічних зв'язків у білковій молекулі
- •Рівні організації білкової молекули
- •2.5. Фізико-хімічні властивості білків
- •Амфотерні властивості білків
- •Розчинність білків
- •Денатурація білків
- •2.6. Класифікація й характеристика білків
- •Прості білки
- •Складні білки
- •2.7. Біологічна цінність білків
- •2.8. Білки харчової сировини
- •Білки субпродуктів
- •Білки молока
- •Контрольні питання і завдання:
- •Тести для контролю знань і самопідготовки
- •Яка ак має таку формулу:
- •Які ак мають такі формули :
- •Формула треоніну:
- •Формула гістидину:
- •Із яких компонентів складаються хромопротеіни?
- •Фактори, що викликають незворотні зміни білків:
- •Яка з структур білка тіла людини є найбільш поширена:
- •Формула лізину:
- •Розділ 3. Хімія нуклеїнових кислот Загальна характеристика
- •Хімічний склад і будова
- •Тести для контролю знань і самопідготовки
- •Які азотисті основи мають такі формули?
- •Розділ 4. Ферменти
- •4.1. Загальне поняття про ферменти
- •4.2. Будова ферментів
- •4.3. Властивості ферментів
- •4.4. Загальні уявлення про механізм дії ферментів
- •4.5. Регуляція ферментативних реакцій
- •4.6. Номенклатура й класифікація ферментів
- •4.7. Використання ферментів в харчовій промисловості
- •Характеристика оксидоредуктаз і використання ферментів у виробництві харчової продукції
- •Використання ферментів в технологіях харчових речовин
- •Тести для контролю знань і самопідготовки
- •50. Який кофермент має таку формулу?
- •Розділ 5. Хімія ліпідів
- •5.1. Біологічна роль, будова й властивості ліпідів й їхніх похідних
- •5.2. Прості ліпіди
- •5.3. Складні ліпіди
- •Тести для контролю знань і самопідготовки
- •2. Чим відрізняються складні ліпіди від простих?
- •4. Який ліпід має таку формулу?
- •5. Які функції виконують ліпіди?
- •До складу яких фосфоліпідів входять таки азотисті основи:
- •Розділ 6. Хімія вуглеводів
- •6.1. Біологічна роль, будова, властивості вуглеводів й їхніх похідних
- •6.2. Утворення вуглеводів у процесах фотосинтезу
- •6.3. Використання вуглеводів у харчовій промисловості
- •Тести для контролю знань і самопідготовки
- •Який моносахарид належить до тріоз?
- •8. Які формули мають пентози?
- •Які олігосахариди є дисахаридами?
- •Який дисахарид має таку формулу?
- •Який дисахарид має таку формулу?
- •Який олігосахарид утворюється під час ферментативного гідролізу крохмалю?
- •Які вуглеводи належать до полісахаридів?
- •Розділ 7. Енергетичні процеси в організмі
- •7.1. Біологічне окиснювання
- •7.2. Роль окислювально-відновних ферментів у біологічному окиснюванні
- •7.3. Транспорт електронів і протонів при біологічному окиснюванні
- •7. 4. Окисне фосфорилюванння
- •Контрольні питання і завдання:
- •Тести для контролю знань і самопідготовки
- •Розділ 8. Вітаміни
- •8. 1. Загальне поняття про вітаміни і їхня класифікація
- •Класифікація вітамінів
- •8. 2. Водорозчинні вітаміни
- •8. 3. Жиророзчинні вітаміни
- •8. 4. Вітаміноподібні сполуки
- •Контрольні питання і завдання:
- •Тести для контролю знань і самопідготовки
- •Розділ 9. Регуляція обміну речовин в організмі
- •9.1. Загальні уявлення про регуляцію обміну речовин
- •9.2. Роль нервової системи в регуляції обміну речовин
- •9.3. Роль гормонів у регуляції обміну речовин
- •9.4. Класифікація гормонів
- •Контрольні питання і завдання:
- •Тести для контролю знань і самопідготовки
- •Яка сполука має таку формулу?
- •Яка речовина має таку формулу?
- •Яку формулу має гістамін?
- •6. Які процеси регулюють мінералокортикоіди?
- •Яка речовина має таку формулу:
- •Яку формулу має серотонін?
- •Розділ 10. Обмін білків
- •10.1. Біологічне значення білкового обміну
- •10.2. Переварювання білків у травному тракті
- •10.3. Утворення в кишечнику отрутних продуктів розпаду білків й їхнє знешкодження
- •Шляхи обміну амінокислот
- •Дезамінування амінокислот
- •Трансамінування (переамінування) амінокислот
- •Декарбоксилювання амінокислот
- •10.5. Процеси знешкодження аміаку
- •10.6. Обмін хромопротеїнів
- •10.7. Обмін нуклеїнових кислот в організмі
- •Утворення сечової кислоти
- •10.8. Біосинтез білка
- •10.9. Регуляція біосинтезу білка
- •Контрольні питання і завдання:
- •Тести для контролю знань і самопідготовки
- •Яка сполука утворюється з амінокислот при відбудовному дезамінуванні?
- •Розділ 11. Обмін вуглеводів
- •11.1. Розщеплення вуглеводів у травному тракті людини
- •11.2. Регуляція обміну вуглеводів і його порушення
- •11.3. Проміжний обмін вуглеводів
- •Аеробне окиснювання вуглеводів
- •Цикл трикарбонових кислот (цикл Кребса)
- •Пентозний цикл окиснювання вуглеводів
- •Види бродіння
- •Контрольні завдання і питання
- •Тести для контролю знань і самопідготовки
- •Яким чином утворилася така сполука?
- •Яка сполука має таку формулу?
- •Які сполуки мають такі формули:
- •Розділ 12. Обмін ліпідів
- •12.1. Розщеплення ліпідів у травному тракті людини
- •12.2. Обмін ліпідів у тканинах
- •Метаболізм кетонових (ацетонових) тіл
- •12.3. Біосинтез ліпідів
- •12.4. Регуляція обміну ліпідів і його порушення
- •12.5. Псування ліпідів
- •Контрольні питання і завдання:
- •Тести для контролю знань і самопідготовки
- •Розділ 13. Біохімічні та інші зміни, що відбуваються з основними речовинами в процесі зберігання і технологічної обробки харчової продукції
- •13.1.Зміна стану та вмісту води
- •13.2. Зміни вмісту мінеральних речовин
- •Втрати мікроелементів при варінні бобових
- •13.3. Зміни стану та вмісту білків
- •Вплив тривалості варіння на перехід колагену в глютин, %
- •Вплив температури і тривалості варіння на перехід колагену в глютин, %
- •Чинники, що впливають на емульгування жиру
- •Кількість отриманого жиру в залежності від режимів обробки кістки
- •Температура димоутворення різних жирів
- •13.5. Зміни углеводів
- •Контрольні питання і завдання:
- •Тести для контролю знань і самопідготовки
- •6. Які структурні компоненти харчових продуктів скорочують втрати вологи в сировині при тепловій обробці ?
- •31. Під дією яких процесів утворюється інвертний цукор?
- •Список рекомендованої літератури
Розділ 7. Енергетичні процеси в організмі
7.1. Біологічне окиснювання
У процесі життєдіяльності організми поглинають з навколишнього середовища енергію в адекватній формі, а потім повертають її еквівалентну кількість, але вже в іншому виді.
Основним носієм енергії є електрон (е-). Одержавши визначену кількість енергії, він збуджується: переходить на більш високий енергетичний рівень. Роблячи зворотний шлях на нижню орбіту, електрон вивільняє таку ж кількість енергії.
Для всіх організмів, що живуть на Землі, основним джерелом енергії служить сонячне випромінювання. Існує дві групи організмів, що розрізняються за способом харчування - аутотрофи і гетеротрофи.
Аутотрофи (зелені рослини) здатні безпосередньо уловлювати сонячну енергію і використовувати її для створення органічних сполук.
Гетеротрофи - це організми, що асимілюють готові органічні речовини, які мають визначений запас потенційної енергії. У процесі їхньої життєдіяльності енергія вивільняється.
Великий художник, вчений і натураліст епохи Ренесансу Леонардо Да Вінчі писав: "Життя можливе там, де може горіти вогонь". Іншими словами, процеси життєдіяльності здійснюються тільки при наявності енергії, отриманої при окиснюванні.
Ще в стародавності було відомо, що вугілля або дерево, згоряючи, виділяють теплову енергію, причому для цього необхідне повітря. М. В. Ломоносов вперше в 1756 показав, що при прожарюванні на повітрі метали збільшуються у своїй масі. Звідси був зроблений висновок, що повітря приєднується до металів. Результати дослідів М. В. Ломоносова спростували теорію флогістону (від грец. phlogіstos - займистий). За уявленнями хіміків кінця XVІІ - початку XVІІІ століття, флогістон - це "початок горючості", гіпотетична складова частина речовини, що вони нібито втрачають при горінні і випалі.
У 1774 році, французький хімік А. Лавуазьє довів, що при згорянні органічної речовини в організмі і поза ним утворюються ті самі продукти - СО2 і Н2О і в обох випадках виділяється теплота. Цей факт мав важливе значення не тільки для вивчення механізмів вивільнення енергії в організмі, але й у методологічному плані, оскільки була доведена єдність процесів, що відбуваються в живій і неживій природі.
У живих організмах енергія, що вивільняється при окиснюванні, запасається в основному у виді хімічної енергії, що після використання переходить у теплоту.
При окиснюванні в неживій природі відбувається пряме приєднання кисню:
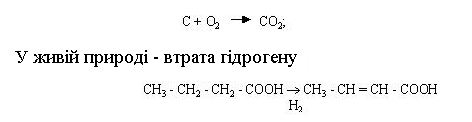
Такий процес можливий лише в тому випадку, якщо в реакційній суміші міститься речовина, що з'єднується з гідрогеном, який вивільнився. Цю речовину називають акцептором гідрогену, а сполуку, що є джерелом гідрогену, - донором цього елемента. Універсальним акцептором гідрогену виступає оксиген повітря.
Загальна умова окиснювання - віддача електрона:
Fe2+ → Fe3+
–e
Процес вивільнення енергії в живому організмі забезпечує усі форми життєдіяльності (у тому числі перетворення речовин їжі в компоненти клітини), а також підтримку організму в стані динамічної рівноваги, незважаючи на постійні зміни умов зовнішнього середовища.
Типовим прикладом окиснювання в неживій природі є горіння. Воно супроводжується значним підвищенням температури. При горінні виділяється величезна кількість енергії, утворюється суміш різноманітних речовин непостійного складу. Характер виділення енергії, що з'являється при горінні, можна порівняти з нищівною силою водоспаду, що падає з високої гори. Якщо розділити його на кілька водоспадів, що падають з невеликої висоти, то кожний з них буде мати менший напір.
У процесі еволюції в живих організмах виробилися механізми перетворення могутнього потоку енергії, що вивільняється при повному окиснюванні харчових речовин, у невеликі порції, що запасаються, приблизно на 50 %, у виді хімічної енергії, використовуваної для процесів синтезу, інші 50 % виділяються у виді теплоти.
Встановлено, що універсальним резервом хімічної енергії, що утворюється в процесі окиснювання органічних речовин у клітинах, є аденозинтрифосфат (АТФ). Ця сполука складається з аденіну, рибози і трьох залишків фосфорної кислоти. Таким чином, вивільнення енергії при окиснюванні органічних речовин, на відміну від горіння, відбувається поступово. При цьому не виникають ті значні перепади температури, що характерні для горіння. Незалежно від окремих етапів окисного розщеплення органічних речовин у кінцевому рахунку утворюються ті ж продукти розпаду (СО2 і Н2О) і виділяється стільки ж енергії.
Оксиген з повітря надходить в організм через дихальні шляхи в легені і кров, що транспортує його до всіх клітин. Однак оксиген у тканинах не приєднується безпосередньо до вихідного джерела енергії - будь то карбоген, амінокислота або жирна кислота. Ці сполуки поступово деградують, втрачаючи гідроген, електрони, що і реагують з оксигеном.
Таким чином, джерелом енергії в організмі стає реакція між гідрогеном і оксигеном, у результаті чого утворюється вода.
Оксид карбогену, що є обов'язковим продуктом окиснювання, відщеплюється тканинними ферментами від кислотних груп - СООН амінокислот, жирних кислот і ін.
На вивчення шляхів взаємодії органічних речовин і оксигену в клітинах були спрямовані зусилля багатьох дослідників, що висували гіпотези, які часом заперечували одна одну. Роль кисню для життя не викликала сумнівів. Задача полягала в тому, щоб з'ясувати, чому оксиген повітря не окисляє організм і сам процес окиснювання відбувається тільки в тканинах, а не на шляху до них. Виявилося, що в тканинах відбувається активація оксигену, яку потребує цей елемент для швидкої взаємодії з речовинами, що окисляються (те ж спостерігається і поза організмом).
На рубежі XІ і XX ст. російський вчений А. Н. Бах і незалежно від нього в Німеччині К. Емглер і В. Вілд висунули гіпотезу про утворення пероксидів органічних сполук як початкового етапу біологічного окиснювання. Відповідно до цієї гіпотези молекула кисню переходить в активний стан за рахунок розриву в ній подвійного зв'язку за допомогою "внутрішньої коливальної енергії" самої сполуки, що окислюється, і при участі ферментів-оксидаз.
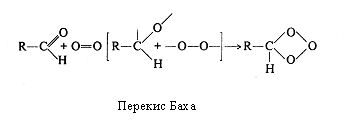
Під впливом ферментів легкоокислювані речовини, наприклад, феноли або сполуки, що містять подвійні зв'язки, утворюють перекиси (пероксиди), що у свою чергу під впливом ферментів пероксидаз розщеплюються, виділяючи атомарний оскиген (так звана "перекісна теорія"). В наступні роки теорія А. Н. Баха знайшла підтвердження в роботах О. Варбурга, Д. Кейліна, де було показано, що пероксиди органічних сполук, що утворилися, як і пероксид водню, можуть окисляти інші речовини.
Однак не всі біологічні субстрати окислюються оксигеном у присутності легкоокислюваних речовин і пероксидази.
На підставі результатів досліджень російський хімік В. І. Паладін у 1908 році розробив теорію, відповідно до якої головну роль у біологічному окиснюванні грають ферменти, які каталізують відщіплення гідрогену від органічних речовин клітин, тобто дегідрогенази. Функція оксигену, за цією теорією, полягає в окиснюванні гідрогену з утворенням води.
Теорія В. І. Паладіна одержала подальший розвиток у працях Г. Віланда, що описав, як відбувається окиснювання речовин, що не є безпосередніми субстратами для дії дегідрогеназ. Такою речовиною був названий, наприклад , оцтовий альдегід.
На початку XX сторіччя склалися дві концепції: біологічного активування оксигену і активування гідрогену. Однак протистояння їхніх прихильників продовжувалося недовго. У 1925 р. Д. Кейлін відкрив в аеробних біологічних об'єктах цитохроми, тобто ферменти, що дозволило вченим декількома роками пізніше зв'язати активування оксигену і гідрогену воєдино. Цьому сприяло виявлення О. Варбургом (1928 р.) цитохромоксидази, що називають "дихальним ферментом Варбурга". Саме цитохромоксидаза виявилася тим ферментом, що безпосередньо активує гідроген, а цитохроми - ферментами, що "знімають" електрони у гідрогену і передають їх цитохромоксидазі.
Сучасна теорія біологічного окиснювання об'єднала теорії Баха - Варбурга і Паладіна - Віланда на новому рівні розвитку досліджень цієї наукової проблеми. Отже, біологічне окиснювання - це процес відщіплення атомів водню або електронів від субстрату і передача їх через ряд проміжних етапів на молекулярний кисень. У цьому процесі беруть участь ферменти: пирідинозалежні дегідрогенази (їх коферментну функцію виконує нікотинамідаденіндинуклеотид-НАД або нікотинамідаденіндинуклеотидфосфат - НАДФ), флавінозалежні дегідрогенази - флавінові ферменти (до складу їхньої простетичної групи входить флавінаденіндинуклеотид - ФАД або флавінаденінфосфат - ФАДФ); цитохроми (містять у якості простетичної групи залізопорфіринову кільцеву систему), а також убіхінон (коензим Q) і білки, що містять негемінове залізо.
