
- •Поверхность раздела твердое тело-газ
- •1. Адсорбционные методы исследования пористых материалов (адсорбентов и катализаторов)
- •1.1. Общая характеристика пористых тел
- •1.1.1. Пористость
- •1.1.2. Удельная поверхность и методы ее определения
- •1.2. Адсорбционно-структурный анализ пористых твердых тел
- •1.2.1. Определение величины удельной поверхности скелета по методу бэт
- •1.2.2. Определение поверхности адсорбционной пленки
- •1.2.3. Раздельное определение объемов микро- и мезопор
- •1.2.4. Построение кривой распределения объема пор по радиусам
- •Лабораторная работа № 1 Определение удельной поверхности адсорбентов методом тепловой десорбции азота
- •Сущность метода тепловой десорбции азота (аргона)
- •Порядок выполнения работы
- •Обработка результатов измерений
- •Лабораторная работа № 2 Определение пористой структуры адсорбентов
- •Порядок выполнения работы
- •1.2.5. Адсорбционная способность пористых тел
- •Лабораторная работа № 3 Адсорбционная активность силикагеля
- •Порядок выполнения работы
- •Порядок работы на рефрактометре рл-2
- •Обработка результатов измерений
- •II. Поверхность раздела твердое тело - жидкость
- •2.1. Межфазные взаимодействия между конденсированными фазами.
- •2.2. Управление смачиванием.
- •Лабораторная работа № 4. Изучение влияния природы материала на смачивание его поверхности.
- •Порядок выполнения работы.
- •Обработка результатов
- •Контрольные вопросы и задания
- •Лабораторная работа № 5 Определение теплоты смачивания
- •Обработка полученных результатов
- •Экспериментальная часть
- •Вариант № 1
- •Вариант № 2
- •Опыт № 1. Влияние рН на набухание и определение изоэлектрической точки желатина
- •Опыт № 1.1. Влияние рН на набухание
- •Опыт № 2. Влияние электролитов на набухание
- •Контрольные вопросы и задания
- •Лабораторная работа № 7 Изучение устойчивости лиофобных золей Краткие теоретические сведения
- •Коагуляция лиофобных дисперсных систем
- •Экспериментальная часть
- •Изучение устойчивости коллоидных систем.
- •Порядок выполнения работы
- •1. Получение золя «берлинской лазури» с отрицательно заряженными частицами.
- •4. Получение золя Fе(он)3 методом пептизации.
- •Определение знака заряда коллоидных частиц
- •Вариант № 1 Опыт № 1. Определение порога коагуляции гидрозоля железа (III)
- •Вариант № 2
- •Опыт № 2. Исследование процесса коагуляции золя «берлинской лазури» с отрицательно заряженными частицами.
- •Порядок выполнения работы
- •Контрольные вопросы и задания
- •Лабораторная работа № 8 Адсорбция на границе раздела твердое тело–раствор. Избирательность адсорбции.
- •Экспериментальная часть
- •Избирательность адсорбции
- •Порядок выполнения работы:
- •2. Адсорбционная хроматография
- •Порядок выполнения работы:
- •3.Ионообменная хроматография
- •Хроматография на бумаге
- •Распределительная хроматография на бумаге
- •Контрольные вопросы
- •Рекомендуемая литература
Обработка результатов измерений
1. Рассчитать парциальное давление азота РN2 в газовой смеси по уравнению:

где Рбар- барометрическое давление, WN2 и WHe – скорости подачи азота и гелия соответственно.
2. Зная барометрическое давление, найти по номограмме температуру кипения азота. Затем по кривой упругости найти давление насыщенных паров азота PS.
3. Рассчитать
относительное давление азота:
 .
Данные представить в виде таблицы.
.
Данные представить в виде таблицы.
Таблица 1
№ |
WHe, мл/мин |
WN2, мл/мин |
Wсмеси, мл/мин |
РN2, мм. рт. ст. |
PS |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4. По десорбционным пикам на хроматограммах рассчитать площади десорбированного азота при различных относительных давлениях:
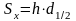
где Sx – площадь пика, h – высота пика, d1/2 – ширина на полувысоте (полуширина).
5. Аналогичным образом найти площади пиков от известного объема азота (SN2).
6. Привести объем от известного количества азота VN2 к нормальным условиям:
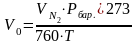
где V0 – объем азота (при калибровке), приведенный к нормальным условиям; Т – комнатная температура.
7. Рассчитать объемы адсорбированного азота Vx при различных относительных давлениях:

8. Рассчитать объем азота, адсорбированного 1 г адсорбента при различных относительных давлениях V, мл/г:

где m – масса адсорбента, г.
9. Найти емкость мономолекулярного слоя Vm (мл/г) по методу БЭТ графическим способом. Для этого использовать уравнение адсорбции БЭТ:

в линеаризованной форме:

где V – удельная величина адсорбции (мл/г); C – энергетическая константа.
Построить график зависимости:
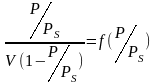 .
.
Найти
отрезок, отсекаемый по оси ординат,
который равен
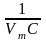 и тангенс угла наклона прямой к оси
абсцисс:
и тангенс угла наклона прямой к оси
абсцисс:
tgα
=
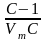 .
.
Решив систему уравнений, найти емкость мономолекулярного слоя Vm (мл/г) и энергетическую константу С.
10. Найти емкость мономолекулярного слоя Vm расчетным путем по методу Темкина, приняв, что энергетическая константа равна 60:
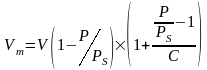
11.
Найти удельную поверхность адсорбента
Sуд. по уравнению 12, зная, что для азота
q=16,2•10-20
м2.
Т.к. емкость мономолекулярного слоя
была вычислена в мл/г, то при переводе
ее в моль/г, используя уравнение
Клапейрона-Менделеева
 ,
можно показать, что
,
можно показать, что
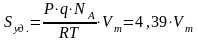
где 4,39 – это площадь, занимаемая 1 мл адсорбата при нормальных условиях, м2/см3.
12. Полученные данные свести в таблицу:
Таблица
№ |
P/PS |
SN2 |
Sx |
V0, мл |
Vx, мл |
V, мл/г |
Vm, мл/г |
Sуд., м2/г |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
13. Рассчитать среднее значение удельной поверхности адсорбента.
14. Сравнить значение удельной поверхности, найденной с использованием графического и расчетного методов.
15. Представить отчет с указанием подробного расчета всех требуемых адсорбционных параметров.
