
- •Поверхность раздела твердое тело-газ
- •1. Адсорбционные методы исследования пористых материалов (адсорбентов и катализаторов)
- •1.1. Общая характеристика пористых тел
- •1.1.1. Пористость
- •1.1.2. Удельная поверхность и методы ее определения
- •1.2. Адсорбционно-структурный анализ пористых твердых тел
- •1.2.1. Определение величины удельной поверхности скелета по методу бэт
- •1.2.2. Определение поверхности адсорбционной пленки
- •1.2.3. Раздельное определение объемов микро- и мезопор
- •1.2.4. Построение кривой распределения объема пор по радиусам
- •Лабораторная работа № 1 Определение удельной поверхности адсорбентов методом тепловой десорбции азота
- •Сущность метода тепловой десорбции азота (аргона)
- •Порядок выполнения работы
- •Обработка результатов измерений
- •Лабораторная работа № 2 Определение пористой структуры адсорбентов
- •Порядок выполнения работы
- •1.2.5. Адсорбционная способность пористых тел
- •Лабораторная работа № 3 Адсорбционная активность силикагеля
- •Порядок выполнения работы
- •Порядок работы на рефрактометре рл-2
- •Обработка результатов измерений
- •II. Поверхность раздела твердое тело - жидкость
- •2.1. Межфазные взаимодействия между конденсированными фазами.
- •2.2. Управление смачиванием.
- •Лабораторная работа № 4. Изучение влияния природы материала на смачивание его поверхности.
- •Порядок выполнения работы.
- •Обработка результатов
- •Контрольные вопросы и задания
- •Лабораторная работа № 5 Определение теплоты смачивания
- •Обработка полученных результатов
- •Экспериментальная часть
- •Вариант № 1
- •Вариант № 2
- •Опыт № 1. Влияние рН на набухание и определение изоэлектрической точки желатина
- •Опыт № 1.1. Влияние рН на набухание
- •Опыт № 2. Влияние электролитов на набухание
- •Контрольные вопросы и задания
- •Лабораторная работа № 7 Изучение устойчивости лиофобных золей Краткие теоретические сведения
- •Коагуляция лиофобных дисперсных систем
- •Экспериментальная часть
- •Изучение устойчивости коллоидных систем.
- •Порядок выполнения работы
- •1. Получение золя «берлинской лазури» с отрицательно заряженными частицами.
- •4. Получение золя Fе(он)3 методом пептизации.
- •Определение знака заряда коллоидных частиц
- •Вариант № 1 Опыт № 1. Определение порога коагуляции гидрозоля железа (III)
- •Вариант № 2
- •Опыт № 2. Исследование процесса коагуляции золя «берлинской лазури» с отрицательно заряженными частицами.
- •Порядок выполнения работы
- •Контрольные вопросы и задания
- •Лабораторная работа № 8 Адсорбция на границе раздела твердое тело–раствор. Избирательность адсорбции.
- •Экспериментальная часть
- •Избирательность адсорбции
- •Порядок выполнения работы:
- •2. Адсорбционная хроматография
- •Порядок выполнения работы:
- •3.Ионообменная хроматография
- •Хроматография на бумаге
- •Распределительная хроматография на бумаге
- •Контрольные вопросы
- •Рекомендуемая литература
Вариант № 2
Опыт № 1. Исследование процесса коагуляции золя «берлинской лазури» с отрицательно заряженными частицами
Поскольку полученный коллоидный раствор «берлинской лазури» имеет отрицательно заряженные коллоидные частицы, то коагуляцию должны вызывать катионы, причем, тем быстрее, чем выше заряд катиона. В качестве электролитов – коагуляторов используют растворы: 1,0 М КCl, 0,01 М СаCl2 (ВаСl2, MgCl2) и 0,005 М AlCl3.
1. Первый опыт проводят с электролитом 1,0 М раствором KCl. В пять пробирок первого штатива наливают указанное количество раствора 1,0 М КCl и разбавляют дистиллированной водой до 5,0 мл. Необходимые объемы раствора электролита – коагулятора и воды указаны в таблице 1.
Таблица 1
№ пробирки |
1 |
2 |
3 |
4 |
5 |
Объем электролита, мл |
1,0 |
2,0 |
3,0 |
4,0 |
5,0 |
Объем воды, мл |
4.0 |
3.0 |
2.0 |
1.0 |
0.0 |
Помутнение (+, –) |
|
|
|
|
|
В каждую пробирку быстро приливают по 5,0 мл полученного золя «берлинской лазури». Следят за тем, чтобы общий объем раствора в каждой пробирке оставался постоянным (Vобщ = 10,0 мл). Через 30-40 минут отмечают, в каких пробирках прошла явная коагуляция. При «помутнении» раствора в таблице 1 ставят знак «+».
2. Аналогично исследуют процесс коагуляции золя электролитами 0,01 М CaCl2 и 0,005 М AlCl3, проводя второй и третий опыт с соответствующими электролитами. Для этого в пять пробирок второго и третьего штативов наливают растворы электролитов 0,01 М CaCl2 и 0,005 М AlCl3 в количестве, указанном в таблице 1.
В каждую из пяти пробирок приливают по 5,0 мл полученного золя «берлинской лазури». Следят за тем, чтобы общий объем раствора оставался постоянным. Через 30-40 минут отмечают, в каких пробирках прошла явная коагуляция. При «помутнении» раствора в пробирках в таблице 2 ставят знак «+».
3. Рассчитывают порог коагуляции (γ, моль/л) по следующему уравнению:
γ
=

где V– объем электролита, вызывающего коагуляцию, мл; С- концентрация электролита, моль/л; W- объем золя, мл.
4.
Проверяют правило Шульце – Гарди.
Значение показателя степени заряда
иона-коагулятора (n) рассчитывают
графическим способом. Для этого
уравнение γ =
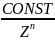 приводят к линейному виду (логарифмируют).
приводят к линейному виду (логарифмируют).
lg γ = lg const- nlg z
Строят график в координатах lg γ = f (lg z). Тогда тангенс угла наклона прямой равен tg(π -ψ) = n .
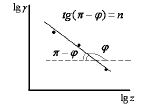
Рассчитывают значение показателя степени заряда иона- коагулятора и сравнивают его с теоретическим значением.
Опыт № 2. Исследование процесса коагуляции золя «берлинской лазури» с отрицательно заряженными частицами.
Цель работы: определить порог коагуляции золя берлинской лазури поддействием различных электролитов; проверить выполнимость правила Шульце – Гарди для данной системы.
Реактивы: золь берлинской лазури, полученный в первой части работы; растворы электролитов: 1N KCl, 0.06N BaCl2, 0.015N AlCl3
