
- •Содержание
- •Инструкция по технике безопасности и противопожарной безопасности при работе в лаборатории кафедры тппм и ик
- •Введение
- •Практическая часть
- •1. Используемые реактивы, посуда и оборудование
- •2. Порядок выполнения работы а) Проведение суспензионной полимеризации
- •Б). Исследование свойств полученного продукта
- •Отчет о выполнении работы
- •Контрольные вопросы и задания:
- •Полиамиды
- •Практическая часть
- •1. Используемые реактивы, посуда и оборудование
- •2. Порядок выполнения работы а) Синтез полимера
- •Б) Исследование свойств полученного продукта
- •3. Отчет о выполнении работы
- •1. Синтез полимера
- •2. Результаты исследования полученного продукта:
- •Контрольные вопросы и задания:
- •Поливиниловый спирт
- •Практическая часть
- •1. Используемые реактивы, посуда и оборудование
- •2. Порядок выполнения работы а) Получение водонерастворимых волокон из раствора поливинилового спирта
- •Б) Исследование свойств полученного продукта
- •3. Отчет о выполнении работы
- •1. Получение волокон
- •2. Результаты исследования полученного продукта:
- •Контрольные вопросы и задания
- •Практическая часть
- •1. Используемые реактивы, посуда и оборудование
- •2. Порядок выполнения работы
- •3. Отчет о выполнении работы
- •Контрольные вопросы и задания:
- •Практическая часть
- •1. Используемые материалы и оборудование
- •2. Устройство прибора пмэ-1
- •3. Порядок выполнения работы
- •4. Обработка результатов эксперимента
- •5. Отчет о выполнении работы
- •5. Деформации, проявленные образцами в процессе испытаний.
- •Контрольные вопросы и задания:
- •Вопросы коллоквиумов
- •Домашнее задание
- •Описание каждого полимера приводят строго по следующей схеме:
- •Литература
- •Учебное издание
- •Лабораторный практикум
- •117997, Москва, ул. Садовническая, 33, стр.1
Введение
Искусственные и синтетические кожи, полиуретаны, термоэластопласты, ткани и трикотаж из синтетических и искусственных волокон, пленки, клеи и многие другие полимерные материалы широко используются в обувной, кожгалантерейной, швейной и других отраслях промышленности.
Правильный выбор полимерных материалов для конкретного изделия, предсказание их поведения при физико-механических, тепловых и других воздействиях, осуществляемых при изготовлении изделий, невозможны без знания методов получения и строения полимеров, их свойств, зависимости этих свойств от химической природы полимеров, их структуры, специально вводимых компонентов и многих других факторов.
Основной задачей дисциплины «Химия и физика высокомолекулярных соединений» является приобретение и развитие студентами систематических знаний в области строения и методов получения полимеров, их химических свойств, агрегатных, физических и фазовых состояний, особенностей механического и релаксационного поведения, физико-химических основ переработки полимеров, а также особенностей свойств полимеров, наиболее широко используемых при производстве изделий легкой промышленности и в быту.
Кроме освоения теоретического материала, в ходе изучения дисциплины студенты выполняют по четыре лабораторные работы, по одному домашнему заданию и сдают по три коллоквиума, что позволяет им закрепить лекционный материал, наглядно ознакомиться со способами получения полимеров и их основными свойствами.
«Химия и физика высокомолекулярных соединений» входит в естественнонаучный цикл» ФГОС ВПО, базируется на ранее освоенных разделах дисциплин «Физика» и «Химия», способствует формированию умений и навыков, необходимых для изучения дисциплин «Экология» и «Технология изделий легкой промышленности».
Лабораторная работа № 1
РАДИКАЛЬНАЯ ПОЛИМЕРИЗАЦИЯ ЭФИРОВ
АКРИЛОВОЙ ИЛИ МЕТАКРИЛОВОЙ КИСЛОТ
Цель работы: Ознакомление студентов с полимеризационными методами синтеза высокомолекулярных соединений на примере получения полиэфиров акриловой или метакриловой кислот.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Общие положения. Полимеризация – это процесс получения высокомолекулярных соединений, при котором рост макромолекул происходит путем последовательного присоединения молекул мономера к активным растущим центрам.
Мономерами для реакций полимеризации служат вещества, имеющие кратные связи и/или неустойчивые циклы: алкены и их производные (например, этилен, пропилен, изобутилен, винилхлорид, винилиденхлорид, винилацетат, стирол), алкадиены и их производные (например, бутадиен, изопрен, хлоропрен), алкины (например, ацетилен), ненасыщенные кислоты и их производные (например, акриловая кислота, метакриловая кислота, эфиры и нитрилы акриловой и метакриловой кислот), лактамы, лактоны, оксиды углеводородов и многие другие соединения.
Структурные формулы акриловой кислоты, метакриловой кислоты и некоторых их эфиров, которые могут быть использованы в качестве мономеров в лабораторной работе, имеют следующий вид:
CH2=CH | C=O
акриловая кислота |
CH2=CH | C=O OCH3
метилакрилат
|
CH2=CH | C=O OC2H5
этилакрилат |
CH2=CH | C=O OC3H7
пропилакрилат |
CH2=CH | C=O OC4H9
бутилакрилат |
CH3 | CH2=C | C=O OH метакриловая кислота |
CH3 | CH2=C | C=O OCH3
метилметакрилат
|
CH3 | CH2=C | C=O OC2H5
этилметакрилат |
CH3 | CH2=C | C=O OC4H9
бутилметакрилат |
Классификация реакций полимеризации. По времени жизни промежуточных продуктов, образующихся в процессе реакции, полимеризация может протекать по цепному или ступенчатому механизму. Ступенчатой называют такую полимеризацию, при которой промежуточными продуктами являются достаточно стабильные соединения, которые в любой момент могут быть выведены из зоны реакции. Если промежуточные продукты нестабильны, полимеризацию называют цепной.
В зависимости от природы активных центров и механизма присоединения к ним мономеров, полимеризацию делят на радикальную и ионную. При радикальной полимеризации активные центры и растущие цепи представляют собой свободные радикалы - молекулы, концевые С-атомы которых содержат неспаренные электроны. При ионной полимеризации активные центры и растущие цепи представляют собой либо анионы (анионная полимеризация), либо катионы (катионная полимеризация).
При радикальной полимеризации для образования начальных активных центров используют как непосредственное энергетическое воздействие на мономер (нагревание, облучение светом, воздействие излучением с высокой энергией и т.п.), так и независимые источники свободных радикалов: инициаторы (пероксиды, азо- и диазосоединения, дисульфиды, металлоорганические соединения и некоторые другие) или окислительно-восстановительные системы.
Стадии полимеризации. Весь процесс радикальной (как и любой иной цепной) полимеризации делят на несколько стадий.
Первая стадия - это стадия образования активных центров, или стадия инициирования. При радикальной инициированной полимеризации в нее входят:
реакция разложения инициатора;
реакция присоединения к образовавшемуся радикалу первой молекулы мономера.
Соединения, образующиеся на этой стадии полимеризации, называются активными центрами.
Вторая стадия носит название «рост цепи». При радикальной полимеризации на этой стадии в результате последовательного присоединения мономеров к активным растущим центрам последние постепенно превращаются в макрорадикалы.
Третья стадия - стадия обрыва цепи. При радикальной полимеризации на этой стадии макрорадикалы, образовавшиеся в процессе роста цепей, утрачивают свою реакционную способность и превращаются в нейтральные (по иному – «мертвые») макромолекулы - макромолекулы, не способные самопроизвольно продолжать свой рост.
Потеря реакционной способности радикала происходит в том случае, если его неспаренный электрон образует общую электронную пару с другим неспаренным электроном. Этот другой неспаренный электрон может принадлежать любому радикалу, находящемуся в реакционной смеси (активному центру, олиго- или макрорадикалу и т.п.) или протону, по той или иной причине оказавшемуся в зоне реакции. В зависимости от механизма потери реакционной способности радикалами и количества образующихся при этом макромолекул различают два вида реакций обрыва цепи: рекомбинацию и диспропорционирование.
Если в результате образования общей электронной пары два реагирующих радикала превращаются в одну нейтральную макромолекулу, то такая реакция называется реакцией рекомбинации. Если один из реагирующих макрорадикалов присоединяет к себе протон, оторвавшийся от другого макрорадикала, и эти два макрорадикала превращаются в две нейтральные макромолекулы, то такая реакция обрыва цепи называется реакцией диспропорционирования. При диспропорционировании одна из вновь образовавшихся макромолекул (именно та, которая получается из радикала, от которого отрывается протон) имеет на конце цепи двойную связь.
Помимо указанных реакций, при радикальной полимеризации возможно протекание еще одного вида реакций, получивших название реакций передачи цепи. Это реакции, при которых растущий радикал «забирает» у оказавшегося рядом соединения (у нейтральной макромолекулы, молекулы мономера, молекулы растворителя или у какого-либо другого) атом водорода и превращается в «мертвую» молекулу, а атакованное им соединение превращается в радикал. Вновь образованный радикал реагирует с молекулами мономера, продолжая тем самым реакцию полимеризации. При этом если радикалом стала линейная макромолекула, то в результате присоединения к ней молекул мономера у нее постепенно вырастает ответвление.
Реакции передачи цепи иногда рассматривают как 4-ю стадию цепной полимеризации, иногда – как 3-ю стадию (передвигая стадию обрыва цепи на четвертое место), иногда – как один из вариантов обрыва цепи, иногда объединяют с реакциями обрыва цепи под общим названием: реакции ограничения роста цепи.
Следует отметить, что при радикальной полимеризации, как правило, образуются макромолекулы нерегулярного строения (т.е. на второй стадии реакции нет регулярности присоединения «голова-хвост», «1-4» и т.д.), причем с широким молекулярно-массовым распределением. При ионной полимеризации всегда образуются макромолекулы регулярного строения со значительно более узким молекулярно-массовым распределением.
Ниже, в качестве примера, приведены реакции, описывающие процесс радикальной инициированной полимеризации бутилметакрилата (в качестве инициатора использован пероксид бензоила).
I. Образование активных центров:
Разложение инициатора:
О
||
C6H5 – C
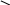 О
О
| 2 C6H5COO· 2 C6H5· + 2 CO2
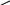 О
О
C6H5 – C Радикал Радикал
||
О
Пероксид бензоила
2. Взаимодействие образовавшихся радикалов (радикала C6H5COO· и радикала C6H5·) с молекулами мономера. Для радикала C6H5· эта реакция может быть описана следующим уравнением:
CH3 CH3
| |
C6H5· + CH2 = C C6H5 – CH2 – C·
| |
COOC4H9 COOC4H9
Мономер Активный центр
II. Рост цепи:
CH3 CH3 CH3 CH3
| | | |
C6H5 – CH2 – C · + n CH2 = C C6H5 –[– CH2 – C –]n– CH2 – C ·
| | | |
COOC4H9 COOC4H9 COOC4H9 COOC4H9 Макрорадикал
III. Обрыв цепи:
а) реакция рекомбинации. В результате таких реакций два радикала превращаются в одну нейтральную макромолекулу, например:
CH3 CH3 CH3 CH3
| | | |
C6H5 –[– CH2 – C –]n– CH2 – C · + · C – CH2–[– C –CH2 –]m– ООСC6H5
| | | |
COOC4H9 COOC4H9 COOC4H9 COOC4H9
Макрорадикал Макрорадикал
CH3 CH3 CH3 CH3
| | | |
C6H5–[–CH2–C–]n–CH2–C C– CH2–[–C –CH2–]m –ООСC6H5
| | | |
COOC4H9 COOC4H9 COOC4H9 COOC4H9
Макромолекула
б) реакция диспропорционирования. В результате таких реакций два радикала превращаются в две нейтральные макромолекулы, одна из которых имеет на конце цепи двойную связь. Например:
CH3 CH3 CH3 CH3
| | | |
C6H5 –[– CH2 – C –]n– CH2 – C · + · C – CH2 –[– C– C H2 –]m–ООСC6H5
| | | |
COOC4H9 COOC4H9 COOC4H9 COOC4H9
CH3 CH3 CH3 CH3
| | | |
C6H5–[–CH2–C–]n –CH = C + CH – CH2 –[– C– C H2 –]m–ООСC6H5
| | | |
COOC4H9 COOC4H9 COOC4H9 COOC4H9
Макромолекула Макромолекула
Реакция передачи цепи на мономер выглядит так:
CH3 CH3 CH3
| | |
C6H5 –[– CH2–C –]n – CH2 – C· + CH2 = C
| | |
COOC4H9 COOC4H9 COOC4H9
CH3 CH3 CH3
| | |
C6H5–[– CH2–C –]n –CH2–CН + · CH = C
| | |
COOC4H9 COOC4H9 COOC4H9
макромолекула радикал
CH3 CH3 CH3 CH3
| | | |
C = CH · + CH2 = C C = CH – CH2 –C · и т.д.
| | | |
COOC4H9 COOC4H9 COOC4H9 COOC4H9
Можно отметить, что в результате реакций рекомбинации, диспропорционирования и передачи цепи образуются макромолекулы разной длины, вследствие чего получаемые методом радикальной полимеризации высокомолекулярные соединения имеют широкое ММР.
Технические способы проведения полимеризации. В зависимости от химической природы мономера, требований, предъявляемых к готовому продукту, и некоторых других факторов радикальную полимеризацию чаще всего осуществляют одним из следующих технических способов: блочным (в массе), в растворе, эмульсионным или суспензионным.
Каждый из этих способов имеет свои преимущества и недостатки. Так, блочный способ, при котором в реакционном сосуде нагревают только мономер и инициатор, позволяет получать чистый, без примесей полимер, причем непосредственно в виде готового изделия (например, листа, необходимой формы блока, шестерни). Основной недостаток способа - сложность отвода выделяющегося на второй стадии полимеризации тепла и неравномерность, в связи с этим, свойств изделия по толщине.
При суспензионном методе мономер с растворенным в нем инициатором диспергируют в нерастворителе (чаще всего воде) интенсивным перемешиванием. Во избежание слияния образующихся при этом капель мономера в реакционный сосуд дополнительно вводят поверхностно-активные вещества - диспергаторы. Перемешивание осуществляют в течение нескольких часов при нагревании. В процессе полимеризации капли мономера постепенно превращаются в твердые частицы (гранулы). В связи с этим такую полимеризацию называют также гранульной, микроблочной, бисерной или жемчужной. При таком методе проведения реакций проблема теплоотвода решается относительно легко, получающийся полимер более однороден по свойствам. Однако одновременно возникают проблемы освобождения полимера от эмульгатора и очистки сточных вод.
Подобные проблемы возникают и при эмульсионном способе полимеризации.
Полимер, полученный в растворе, нуждается, как правило, в очистке от растворителя.

 OH
OH