
- •Министерство образования и науки рф
- •Иркутский государственный технический университет
- •Введение
- •Краткие методические указания к выполнению лабораторных работ
- •Термохимия Теоретическое введение
- •Определение константы калориметра и теплоты нейтрализации
- •Теоретические основы второй части работы
- •Определение средней теплоемкости вещества
- •Теоретические основы работы
- •Равновесие жидкость-пар: давление насыщенного пара жидкостей Теоретическое введение
- •Определение давления насыщенного пара индивидуальной жидкости
- •Порядок выполнения работы
- •Физико-химический анализ Теоретическое введение
- •Визуально-политермический метод
- •Термографический метод
- •Контрольные вопросы
- •Построение диаграммы плавкости бинарной системы фенол −нафталин термографическим методом
- •Теоретические основы работы
- •Порядок выполнения работы
- •Методика экспериментального определения электрической проводимости растворов
- •Удельная электрическая проводимость растворов хлорида калия при различных температурах, См∙см-1
- •Определение постоянной электролитической ячейки
- •Экспериментальные данные по измерению сопротивления стандартных растворов хлорида калия
- •Определение удельной электропроводности, константы и степени электролитической диссоциации слабого электролита
- •Результаты опыта и расчетные величины
- •Электродное равновесие Теоретическое введение
- •Методика измерения эдс
- •Определение стандартного потенциала ферри-ферро электрода
- •Порядок выполнения работы
- •Формальная кинетика химических реакций Краткое теоретическое введение
- •Изучение зависимости скорости химической реакции от температуры
- •Этилацетата щелочью
- •Порядок выполнения работы
- •Экспериментальные и расчетные данные
- •Контрольные вопросы
- •Изменения относительного количества реагентов
- •Порядок выполнения работы
- •Соотношения объемов растворов в опытах и экспериментальные данные
- •Контрольные вопросы
- •Определение константы скорости гетерогенной реакции
- •Экспериментальные и расчетные данные
- •Не забывать после каждого отбора пробы опускать брусок мрамора в раствор так, чтобы площадь контакта его с раствором оставалась постоянной
- •Краткое описание метода
- •Краткое описание методов
- •Термодинамика поверхностных явлений. Адсорбция Теоретическое введение
- •Поверхности и в глубине фазы
- •Определение поверхностного натяжения и расчёт характеристик адсорбционного мономолекулярного слоя
- •(См. Теоретическое введение)
- •Метод максимального давления пузырька
- •Методом максимального давления пузырьков
- •Порядок выполнения работы
- •Работа 11 определение величины адсорбции
- •Теоретические основы работы
- •П орядок выполнения работы
- •Дисперсные системы Теоретическое введение
- •Классификация дисперсных систем по агрегатному состоянию фаз
- •Получение дисперсных систем
- •Р ис. 33. Строение мицеллы золя AgI
- •Порядок выполнения работы
- •Зависимость показателя степени п при длине волны λ от размера частиц r
- •Порядок выполнения работы
- •Седиментационный анализ грубодисперсных систем
- •Теоретические основы работы
- •Порядок выполнения работы
- •Электрокинетические явления Теоретическое введение
- •Электрического напряжения
- •Электрофорез в золе гидроксида железа
- •Теоретические основы работы См. Теоретическое введение – Электрокинетические явления
- •Порядок выполнения работы
- •Мицеллярнорастворимые поверхностно-активные вещества Теоретическое введение
- •Определение критической концентрации мицеллообразования в растворах поверхностно-активных веществ
- •Библиографический список
Равновесие жидкость-пар: давление насыщенного пара жидкостей Теоретическое введение
При кипении жидкости происходит ее испарение. При этом поглощаемая теплота расходуется на преодоление сил взаимодействия между молекулами в жидкости. Связь между теплотой испарения жидкости, температурой и давлением насыщенного пара выражается уравнением Клаузиуса-Клапейрона в дифференциальной форме:

где
Р
– давление насыщенного пара, Т –
термодинамическая температура;
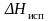 −
мольная теплота испарения; R
– универсальная газовая постоянная.
−
мольная теплота испарения; R
– универсальная газовая постоянная.
Интегральная форма уравнения Клаузиуса-Клапейрона будет:
 ,
(6)
,
(6)
где В – постоянная интегрирования.
Уравнение (6) является уравнением прямой линии. Имея ряд экспериментальных значений зависимости давления насыщенного пара жидкости от температуры, можно построить график в координатах lnР = f(1/Т). Соответствующий график показан на рис. 3.
П о
тангенсу угла наклона прямой находят
мольную теплоту испарения жидкости:
о
тангенсу угла наклона прямой находят
мольную теплоту испарения жидкости:
 ;
;

Постоянная
интегрирования имеет простой физический
смысл. Если взять Т=Ткип
и Р
= 1 атм, то
 =
const ∙ R
=
=
const ∙ R
= .
Таким образом,
.
Таким образом,
 и уравнение (6) приобретает вид
и уравнение (6) приобретает вид
 .
(7)
.
(7)
Зная мольную теплоту испарения жидкости, находят ее удельную теплоту испарения:
 ,
(8)
,
(8)
где lисп – удельная теплота испарения; М – молярная масса жидкости.
Отношение теплоты к температуре в изотермическом процессе равно изменению энтропии. Следовательно, изменение энтропии при испарении жидкости
 ,
(9)
,
(9)
где
−
изменение энтропии при испарении 1 моля
жидкости; К
– постоянная Труттона;
 −
температура кипения жидкости при
нормальном давлении.
−
температура кипения жидкости при
нормальном давлении.
По значению удельной теплоты испарения жидкости можно найти еще одну величину – эбуллиоскопическую константу:
 .
(10)
.
(10)
Работа 3
Определение давления насыщенного пара индивидуальной жидкости
Цель работы: ознакомление с методикой определения давления насыщенного пара жидкости и расчет некоторых термодинамических величин.
Теоретические основы работы
(см. теоретическое введение)
Эксперимент выполняется на установке, схема которой показана на рис. 8.
Приборы и материалы: колба с исследуемой жидкостью, вакуумметр, электронагреватель с водяной баней, водоструйный насос.
Порядок выполнения работы
1. Поместить колбу с исследуемой жидкостью на водяную баню так, что бы уровень водяной бани был выше уровня исследуемой жидкости в колбе (Рис. 3).
. 2.
Открыть
кран 1,
при закрытом кране 2
и водоструйным насосом 3
создать в системе разряжение до отметки
на вакуумметре 75 − 80, что соответствует
0,25 − 0,20 атм. Если установка герметична,
то стрелка вакуумметра должна держаться
на постоянном уровне. В противном случае
надо найти место подсоса и добиться
герметичности (смазать шлифы, проверить
все соединения в установке).
2.
Открыть
кран 1,
при закрытом кране 2
и водоструйным насосом 3
создать в системе разряжение до отметки
на вакуумметре 75 − 80, что соответствует
0,25 − 0,20 атм. Если установка герметична,
то стрелка вакуумметра должна держаться
на постоянном уровне. В противном случае
надо найти место подсоса и добиться
герметичности (смазать шлифы, проверить
все соединения в установке).
3. Осторожно пустить воду в холодильник от водопроводного крана 4. Включить электронагреватель и следить за жидкостью в колбе. Когда начнется интенсивное кипение жидкости, записать ее температуру кипения и показания вакуумметра РВ.
4. Осторожно открыть кран 2, соединяющий прибор с атмосферой, чтобы давление увеличилось приблизительно на 0,1 атм, и аналогично измерить температуру кипения при новом давлении.
Таким образом, давление доводят до атмосферного, сделав 10 – 12 отсчетов.
5. Результаты опытов занести в табл. 3 и показать преподавателю.
Таблица 3
Опыт |
t, 0С |
Т, К |
1/Т |
Показания вакуумметра РВ |
Давление в колбе РК = (1-РВ), атм. |
lnРК |
1 2 3 . . . и т.д. |
|
|
|
|
|
|
6. На миллиметровой бумаге построить график, отложив на оси ординат lnР, а на оси абсцисс – 1/Т. По уравнениям (7 – 10) рассчитать молярную и удельную теплоту испарения жидкости, постоянную Труттона и эбуллиоскопическую константу для изученной жидкости.
Контрольные вопросы
Что называется насыщенным паром?
Что характеризует уравнение Клаузиуса-Клапейрона?
Как определить константы уравнения Клаузиуса-Клапейрона?
Какой физический смысл константы интегрирования в уравнении Клаузиуса-Клапейрона?
Что характеризует эбуллиоскопическая константа и в каких единицах измерения выражается?
Что характеризует постоянная Труттона?
