
- •Ферменты
- •1. История открытия и изучения ферментов
- •2. Особенности ферментов как биокатализаторов
- •3. Классификации ферментов и номенклатура.
- •3.1. Классификация ферментов по строению ферменты
- •3.2. Ферменты по уровню организации белковых молекул
- •3.3. Классификация ферментов по типу катализируемой реакции и номенклатура ферментов
- •3.4. Принципы построения рабочего названия фермента
- •3.5. Список ферментов
- •4. Механизм действия ферментов.
- •4.1 Активный центр ферментов
- •4.2. Механизм действия ферментов (на примере фермента холинэстеразы)
- •4.3. Причины высокой каталитической активности.
- •5. Специфичность ферментов
- •5.1. Субстратная специфичность
- •5.2. Специфичность пути превращения
 ерменты
ерменты
Ферменты
1. История открытия и изучения ферментов
Ферменты - это биокатализаторы, образующиеся в клетке, и представляющие собой простые или сложные белки. Слово фермент происходит от латинского - fermentum -закваска; другое название ферментов - энзимы - происходит от греческого- enzyme - в дрожжах. В 30-х годах XX века некоторые ферменты были выделены в высокоочищенном кристаллическом состоянии. По химической природе кристаллы оказались белковыми.
История изучения ферментов тесно переплетается с историей катализа. Катализом называют ускорение химической реакции, вызванное добавлением малых нестехиометрических количеств катализатора. Катализатор ускоряет реакцию не просто своим присутствием, а взаимодействием с веществом, подвергающимся превращению, но при этом регенерируется в ходе реакции. Ферменты - биокатализаторы - не являются исключением.
Ферменты - это белки, и подобно всем белкам, они могут избирательно присоединять определенные вещества - лиганды. Лиганд, подвергающийся химическому превращению под действием фермента, называют субстратом (S), продукты (P) реакции освобождаются в раствор. Ферменты являются наиболее изученным классом белков. Это объясняется той важной ролью, которую играют ферменты: любое химическое превращение в организме происходит с их участием. К тому же, ферменты, в отличие от других белков, сравнительно легко обнаруживать и измерять их количество по катализируемой реакции.
2. Особенности ферментов как биокатализаторов
Ферменты как катализаторы имеют ряд особенностей:
Высокоэффективные катализаторы - ускоряют реакцию в 1010раз:
1 моль каталазы при 00 С обеспечивает разложение за 1 мин 5 млн. H2O2, в то время как 1 моль Pt катализирует только 250- 2000 молекул H2O2.
Высокоспецифичны - катализируют, как правило, реакцию одного типа или воздействуют на один субстрат. Это наиболее важное свойство ферментов.
Эффективно работают в мягких условиях.
Синтез аммиака по реакции: N2 + 3H2 = 2NH3 проводят при t = 500-5500C, p = 107-108Па, ферменты, содержащиеся в бобовых культурах обеспечивают протекание подобного процесса при обычных условиях.
Ферменты - это катализаторы, работу которых можно регулировать.
3. Классификации ферментов и номенклатура.
3.1. Классификация ферментов по строению ферменты
|
|
|
простые- состоят только из полипептидных цепей |
сложные- в состав сложных входят группы небелковой природы |
|
|
|
|
|
кофермент или простетическая группа (группа небелковой природы) |
апофермент (белковая часть фермента) |
3.2. Ферменты по уровню организации белковых молекул
могут иметь только третичную структуру (одну полипептидную цепь) и четвертичную структуру (несколько полипептидных цепей). Последние - аллостерические ферменты.
3.3. Классификация ферментов по типу катализируемой реакции и номенклатура ферментов
В номенклатуре ферментов, введенной Международным биохимическим союзом (IUB) используется принцип классификации ферментов по типу катализируемой реакции и ее механизму. Основные принципы номенклатуры следующие:
Выделяют 6 классов ферментов, катализирующих 6 типов реакций:
Оксидоредуктазы.
Трансферазы.
Гидролазы.
Лиазы
Изомеразы.
Лигазы.
В каждом из 6 классов имеется несколько подклассов (от 4 до 13).
Систематическое название фермента состоит из 2-х частей: названия субстрата, типа катализируемой реакции и части слова -аза.
Дополнительная информация, если она необходима для уточнения, заключается в скобках.
Н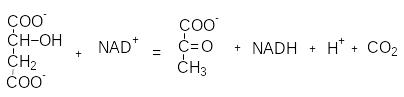 апример:
апример:
L-малат пируват
Фермент L-малат:NAD+оксидоредуктаза (декарбоксилаза)
Каждый фермент обозначается специальным шифром, указывающим номер класса, подкласса, подподкласса и номер фермента в подподклассе. Например: 2.6.1.2 - аланин:оксоглутарат-аминотрасфераза.
Помимо систематического названия указывается рабочее название фермента.
