
- •Морфологічна диференціація інших мікроорганізмів
- •Фізіологія та біохімія мікроорганізмів
- •Живлення мікроорганізмів
- •Розділ 3 .Вплив факторів зовнішнього середовища на мікроорганізми
- •Фізичні фактори
- •Біологічні фактори
- •Контрольні питання
- •Анаеробне розкладання (бродіння) безазотистих речовин
- •Аеробне розкладання
- •Контрольні питання
- •Розділ 5 перетворення мікроорганізмами сполук азоту
- •Фіксація молекулярного азоту
- •Амоніфікація білкових речовин
- •Розкладання сечовини та цианаміду
- •Амоніфікація гумусу
- •Нітрифікація
- •Денітрифікація
- •Контрольні питання
- •Розділ 6 Перетворення сполук сірки, фосфору і заліза.
- •Контрольні питання
- •Розділ 7 синтез мікроорганізмами білка і біологічно активних речовин
- •Контрольні питання
- •Глава 8. Мікробіологія борошна, круп, комбікормів
- •3.1. Сапрофітна мікрофлора зерна
- •3.2. Мікрофлора дефектного зерна
- •3.3. Фітопатогенні і патогенні мікроорганізми у зерновій масі
- •3.4. Зміни складу сапрофітної мікрофлори зерна при зберіганні
- •3. 4. Вплив сапрофітної мікрофлори на насіннєві, продовольчі та кормові властивості зерна
- •3.6. Роль мікроорганізмів у самозігріванні зерна
- •3.7. Вплів різних способів сушки на мікрофлору зерна
- •3.8. Вплив нестачі кисню на якість і мікрофлору зерна при зберіганні
- •3.9. Способи хімічної консервації
- •3. 10. Мікрофлора борошна та круп
- •3.11. Мікрофлора комбікормів
Аеробне розкладання
Д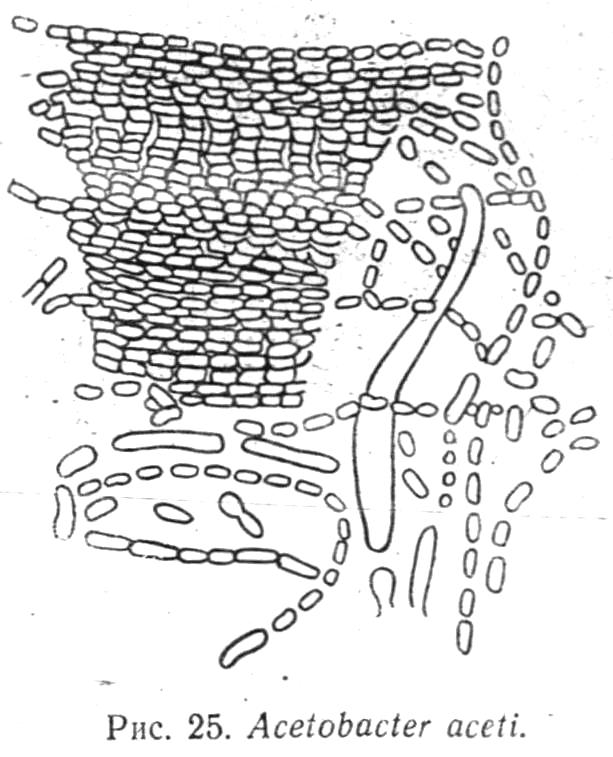 о
нього відносяться окислювальні біохімічні
процеси, пов'язані з диханням мікроорганізмів
в аеробних умовах.
Кінцевими
продуктами дихання часто можуть бути
не тільки вуглекислий газ і вода, а й
продукти неповного або часткового
окислення органічних речовин (лимонна
кислота, оцтова кислота і т. д.).
В
природі ці речовини використовують
інші мікроби і піддають їх подальшому
окисленню
до
СО2
і Н
2
0.
о
нього відносяться окислювальні біохімічні
процеси, пов'язані з диханням мікроорганізмів
в аеробних умовах.
Кінцевими
продуктами дихання часто можуть бути
не тільки вуглекислий газ і вода, а й
продукти неповного або часткового
окислення органічних речовин (лимонна
кислота, оцтова кислота і т. д.).
В
природі ці речовини використовують
інші мікроби і піддають їх подальшому
окисленню
до
СО2
і Н
2
0.
В природних умовах до окислення схильні не тільки органічні речовини, але і багато неорганічних: водень, сірководень, аміак, закис заліза, відновлені з'єднання. Найпростішим типом окислення є окислення молекулярного водню до води:
2Н 2 + 0 2 = 2Н 2 0 + 579 600 Дж.
Окислювальні процеси відіграють важливу роль, особливо в умовах зрошення, де надлишок води часто пов'язаний з анаеробними процесами і накопиченням отруйних сполук (FeO, FeS, MnO, СН 4 ). Заходи, спрямовані на підвищення аерації, будуть сприяти окисленню - переводу FeO в Fe 20 3 , H 2 S в H 2 S 0 4 і т. д., тобто в з'єднання, не токсичні для рослин.
Окислення етилового спирту в оцтову кислоту. Цей процес здійснюється групою оцтовокислих бактерій по рівнянню.
СН3СН2ОН+О2=СН3СООН+Н2О
етиловий оцтова
спирт кислота
Збудниками є аеробні бактерії. Серед них зустрічаються рухомі і нерухомі. З роду Acetobacter описаний ряд найважливіших видів типових оцтовокислих бактерій, таких як Acetobacter aceti (Рис. 25), Acetobacter pasteiirianum, Acetobacter oreeanes schutzenbachii.
Бактерії цього роду - грамнегативні палички розміром від 0,5 до 8 мкм, іноді з'єднані в ланцюжки. Спор не утворюють. Одні види бактерій відрізняються від інших розмірами, різною стійкістю до спирту, здатністю накопичувати в середовищі більшу або меншу кількість кислоти (від 6 до 11,5%).
Для промислового приготування оцтової кислоти використовують виноградне вино або оцтово-спиртовий розчин (10-12% спирту і 1% оцтової кислоти). Для оцтовокислих бактерій в субстрат додають необхідні мінеральні солі та вітаміни. Оптимальна температура для розвитку цих бактерій 20-35 ° С. Багато оцтовокислих бактерій на субстраті утворюють характерні міцні товсті плівки.
Оцтовокислі бактерії широко поширені в природі, зустрічаються на зрілих плодах, ягодах, в квашених овочах, вині, пиві, квасі.
Окислення вуглеводів до лимонної кислоти. Лимонну кислоту отримують з допомогою пліснявих грибів Aspergillus, які широко поширені в природі і виявляються в самих різних субстратах.
Основною сировиною для виробництва лимонної кислоти служить меляса. (чорна патока). Розчин її, що містить приблизно 15% цукру з додаванням різних мінеральних солей, в плоских відкритих кюветах засівають спорами гриба. При хорошій аерації в спеціальних камерах процес триває 6-7 днів при температурі близько 30 ° С. Вихід лимонної кислоти становить 50-60% витраченого цукру. При недостатній кількості цукру гриби споживають саму лимонну кислоту.
Останнім часом починає впроваджуватися «глибинний» метод культивування гриба в спеціальних закритих ємностях (ферментерах) з інтенсивною аерацією. Цей метод підвищує продуктивність процесу і не допускає забруднення рідини сторонньою мікрофлорою.
Лимонну кислоту широко використовують в медицині, а також при виготовленні кондитерських виробів, безалкогольних напоїв, в кулінарії.
Окислення жирів і жирних кислот. Потрапляючи в грунт разом з тваринними і рослинними залишками, жири повністю руйнуються (гідролізуються) різними мікроорганізмами. При цьому утворюються гліцерин і жирні кислоти. Процес протікає під дією ферменту ліпази при звичайній температурі в присутності води. Мікробів, що виділяють цей фермент, досить багато. Серед аеробних бактерій він виявлений у Васteria coli, Proteus vulgaris, Bacillus mycoides, Вас. megatherium, Salmonella, а також у стафілококів, пневмококів і стрептококів. Найбільш енергійно розщеплюють жири деякі пігментні і флуоресціюючі бактерії (Bact. prodigiosum, Bact. pyocyanerum, Bact. fluorescens), актиноміцети і цвілеві гриби. Із грибів високою ліполітичною здатністю володіють Oidium lactis, багато видів з родів Aspergillus і Реnicillium.
Гідроліз жирів мікроорганізмами відбувається постійно і грає істотну роль в загальному круговороті речовин у природі.
Отримані в процесі гідролізу гліцерин і вільні жирні кислоти поступово окислюються в ґрунті різними мікробами і перетворюються в перегнійні кислоти, вуглекислий газ і воду.
Окислення вуглеводнів. Ґрунтові мікроорганізми використовують ці речовини як джерело енергії.
Багато бактерій окислюють бензол, нафталін, кисневі феноли, поліфеноли і креозоли.
Ксилол, толуол і бензин беруть участь в обмінних реакціях багатьох видів мікробів, зокрема Pseudomonas і мікобактерій.
Існує велика група мікроорганізмів, що здатні розщеплювати вуглеводні нафти. Метан може бути окислений в ґрунті короткою паличкою Bact. metanicum з утворенням органічних сполук і С0 2 . Цією здатністю володіють також Bact. руосуапеіт, Bact. fluorescens.
Інші мікроорганізми, широко поширені в грунті поблизу нафтових свердловин, енергійно окислюють етан, пропан (Pseudomonas, Propanica), мінеральні масла, що містяться в нафті і парафіні ( Desulfovibrio).
Вуглеводні розщеплюють не тільки бактерії, але і багато актиноміцетів і деякі гриби.
Розкладання целюлози (клітковини). Серед хімічних безазотистих речовин рослинних залишків відносно повільно розкладаються під дією мікроорганізмів целюлоза, лігнін і пектинові речовини.
В природі целюлоза під впливом ферменту целюлози перетворюється спочатку в дисахарид целобіозу, а потім під дією ферменту целлобіази переходить в глюкозу. Мікроорганізми, що розкладають клітковину, поширені найбільше в ґрунті, а також зустрічаються в мулі, гної і навіть в травному тракті багатьох тварин.
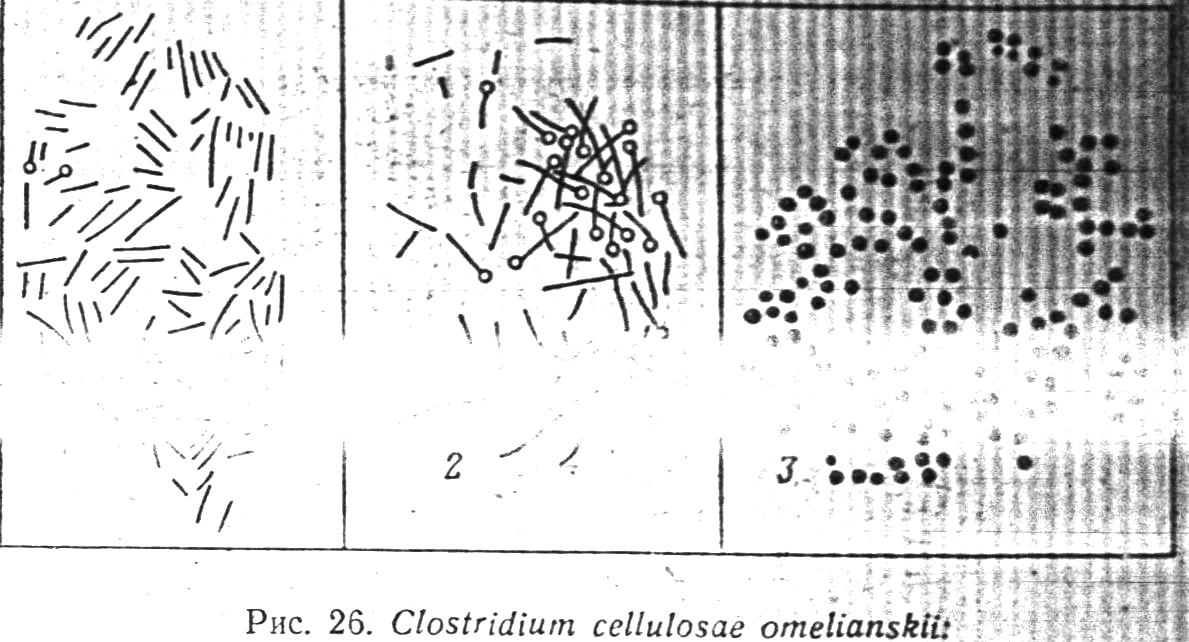
Типовий представник анаеробних бактерій, які розщеплюють клітковину Clostridium cellulosae omelianskii (Рис. 26). Вперше вона виділена В.Л.Омельянським в 1902 г. Це паличкоподібна рухома бактерія завдовжки. 4 -7 мкм при спороутворенні приймає вид барабанної палички. У природі зустрічаються розкладаючі целюлозу термофільні бактерії: Clostr. thermocellum - невелика грамнегативна спороутворююча паличка та Bacillus cellulosae dissolvens - паличка довжиною 12 мкм. Оптимальна температура для них 55 - 56 ° С, реакція середовища - близька до нейтрального.
З аеробних бактерій, що розкладають целюлозу, особливою активністю володіють бактерії роду Cytophaga (Рис. 27) з класу Myxobacteriae. Це довгі вигнуті, грамнегативні клітини без оболонки.
З інших видів бактерій, що активно розкладають целюлозу, можна назвати наступні:
1. Cellvibrio – дрібні, злегка вигнуті паличкоподібні бактерії з заокругленими кінцями, розміром в середньому 1,5 мкм (рис. 28), частіше монотрихи або лофотрихи, грампозитивні. При культивуванні на папері утворюють жовтий пігмент. Оптимальна температура для їх розвитку 28-30 ° С. Розщеплення клітковини протікає краще при нейтральній або слабколужній реакції.
2. Cellfacicula – паличка у вигляді серпа з загостреними кінцями, рухлива. При вирощуванні на фільтрувальному папері виділяє зелений пігмент.
Під впливом аеробних форм бактерій клітковина перетворюється в драглисту речовину, дуже стійку до дії мікробів.

Крім бактерій, розкладати клітковину можуть окремі різні види проактиноміцетів, актиноміцетів (Streptomyces) і грибів (Trichoderma, Botritis, Aspergillus та ін.).
У кислих ґрунтах руйнують целюлозу головним чином гриби.
У ґрунті при гідролізі клітковини мікроорганізмами утворюється гумус. У травному тракті травоїдних тварин до 70% прийнятої з кормом клітковини розкладається мікробами, що сприяє кращій перетравності грубих кормів.
Розщеплення лігніну. Лігнін руйнується дуже небагатьма мікроорганізмами, переважно актиноміцетами, грибами і деякими бактеріями. З грибів, що розщеплюють лігнін в ґрунті, можна зазначити Merulius, Coniphofa, Fusarium, Mucor.
Розщеплення лігніну - завжди результат симбіозу або асоціації бактерій. Так як ця речовина володіє великою стійкістю, то процес його руйнування протікає порівняно повільно. Тому лігнін має i тенденцію накопичуватися в ґрунті і служить основою утворення гумусових комплексів.
Розпад пектинових речовин. Пектинові речовини являють собою складні полісахариди. Вони мовби склеюють між собою клітини в рослинних тканинах. Їхня назва надається через здатність давати драглисту масу при кип'ятінні.
П овне
розщеплення пектину здійснюється під
впливом ферментів протопектинази,
пектинази і пектази до органічних
кислот, спиртів і газу.
Пектинолітичними властивостями володіють
численні анаеробні бактерії, цвілеві
гриби, актиноміцети.
овне
розщеплення пектину здійснюється під
впливом ферментів протопектинази,
пектинази і пектази до органічних
кислот, спиртів і газу.
Пектинолітичними властивостями володіють
численні анаеробні бактерії, цвілеві
гриби, актиноміцети.
До збудників пектинового бродіння в анаеробних умовах відносяться спороутворюючі рухомі грампозитивні бактерії розміром 10-15 мкм. З них найбільш відомі Clostridium pectinovorum (Рис. 29) і Clost. felsineiis. До аеробних бактерій, здатних розкладати пектинові речовини, належать Bacillus subtilis, Вас. mesentericus, Pseudomotias fluorescens. Серед цвілевих грибів найбільш активні Aspergillus niger, Penicillium і Botritis cinerea.
Процес розпаду пектинових речовин широко використовується при виділенні з стебел луб'яних рослин (льон, конопля, джут та ін.) волокон, що йдуть на виготовлення пряжи. Для руйнування пектинових речовин, луб'яних рослин застосовують анаеробну водяну мочку.
Після руйнування пектинових речовин зв'язок між луб'яними волокнами і клітинами інших тканин стебла слабшає і після висушування легко відокремлюється механічним шляхом.
