
- •Содержание
- •1 Производство чугуна
- •1.1 Исходные материалы и подготовка их к плавке
- •1.2 Основные физико-химические процессы в современных доменных печах
- •1.3 Продукты доменного производства и области их применения:
- •2 Производство стали
- •2.1 Физико-химические процессы получения стали
- •2.2 Процессы производства стали
- •3 Производство цветных металлов
- •3.1 Производство магния
- •3.2 Производство меди
- •3.3 Производство титана
- •4 Охрана труда и окружающей среды в металлургическом производстве
- •5 Строение и основные свойства металлов и сплавов
- •5.1 Атомно-кристаллическое строение металлов
- •5.2 Понятие о строении сплавов
- •5.3 Нагрузки, напряжения и деформации
- •5.4 Механические свойства
- •5.5 Теоретическая и техническая прочность
- •6 Железо и его сплавы
- •6.1 Влияние легирующих элементов на свойства стали
- •6.2 Конструкционные легированные стали, их маркировка и области применения
- •6.3 Инструментальные стали, их маркировка и области применения
- •6.4 Твердые сплавы и композиционные материалы
- •7 Цветные металлы и сплавы
- •7.1.Алюминий и его сплавы
- •7.2 Магний и его сплавы
- •7.3.Медь и ее сплавы
- •7.4 Титан и его сплавы
- •7.5 Подшипниковые сплавы и материалы
- •8 Неметаллические материалы
- •8.1 Классификация, строение и свойства неметаллических материалов
- •8.2 Типовые термопластичные материалы
- •8.3 Типовые термореактивные материалы
- •8.4 Резиновые материалы, области их применения
- •9 Основные конструктивные и технологические характеристики изделия
- •9.1 Определение детали, размера и понятие о взаимозаменяемости
- •9.2 Точность обработки и качество обработанной поверхности
- •10 Основы технологии термической обработки стали
- •10.1 Виды термической обработки
- •10.2 Виды отжига. Нормализация стали
- •10.3 Закалка и отпуск стали
- •10.4 Термомеханическая обработка стали
- •10.5 Химико-термическая обработка стали
- •11 Литейное производство
- •11.1 Классификация способов изготовления отливок
- •11.2 Эффективность использования металла
- •11.3 Сведения о литейных сплавах
- •11.4 Изготовление отливок из серого, высокопрочного и ковкого чугунов
- •11.5 Особенности изготовления стальных отливок
- •11.6 Особенности изготовления отливов из цветных металлов
- •11.7 Контроль качества отливок. Способы исправления литейных дефектов
- •12 Основы технологии обработки металлов давлением
- •12.1. Классификация способов обработки металлов давлением
- •12.2 Пластичность металлов и сопротивление деформированию
- •13 Прокатка, прессование и волочение
- •13.1 Сущность процесса прокатки
- •13.2 Технологический процесс прокатки
- •14 Ковка и штамповка
- •14.1 Сущность процесса ковки
- •14.2 Сущность процесса горячей объемной штамповки
- •14.3 Классификация способов холодной штамповки
- •15 Основы технологии сварочного производства
- •15.1 Физическая сущность и классификация способов сварки
- •15.2 Свариваемость однородных и разнородных материалов
- •15.3 Сварка углеродистых и легированных сталей и чугунов
- •15.4 Сварка меди, алюминия, титана и их сплавов
- •16 Пайка металлов и сплавов
- •16.1 Сущность и схема процесса
- •16.2. Способы пайки
- •16.3 Контроль качества сварных и паяных соединений
- •17 Технология изготовления изделий из пластмасс
- •17.1 Способы переработки пластмасс в вязкотекучем состоянии
- •17.2 Классификация резинотехнических изделий
- •17.3 Понятие о технологии изготовления изделий из резины
- •18 Основы технологии обработки конструкционных материалов резанием
- •18.1 Способы обработки металлов резанием и классификация движений в металлорежущих станках
- •18.2.Физические явления, сопровождающие процесс резания. Износ и стойкость режущего инструмента
- •18.3 Принцип классификации металлорежущих станков
- •18.4 Характеристика метода обработки сверлением и растачиванием
- •18.5 Характеристика методов обработки фрезерованием
- •18.6 Характеристика методов обработки заготовок зубчатых колёс
- •19 Обработка заготовок на шлифовальных и отделочных станках
- •19.1 Характеристика метода обработки шлифованием
- •19.2 Технология обработки шлифованием
- •19.3 Методы отделки поверхностей
- •20 Механизация и автоматизация технологических процессов механической обработки
- •20.1 Автоматизация металлорежущих станков и производства
- •20.2 Автоматические линии и комплексная автоматизация производства
- •21 Основы технологии упрочняющей обработки деталей машин
- •21.1 Качество машин
- •21.2 Технологические способы упрочняющей обработки деталей машин
- •21.3.Технологические способы упрочняющей обработки наплавкой, напылением, нанесением покрытий на рабочие поверхности деталей
- •Список литературы
5 Строение и основные свойства металлов и сплавов
5.1 Атомно-кристаллическое строение металлов
Твердые тела в зависимости от скорости охлаждения при кристаллизации делят на аморфные и кристаллические.
Аморфный металл получается при скоростях охлаждения Ю6...107°С/с и более в виде тонких лент или мелких частиц. Атомы при этом не располагаются в правильном порядке, не образуют кристаллов. Аморфное твердое тело является изотропным, т.е. обладает одинаковыми свойствами во всех направлениях. Кроме того, ему присущи высокая твердость, хорошая коррозионная стойкость и другие свойства. Если такое тело нагреть до определенной температуры, которая приведет к значительному повышению тепловой активности атомов, то аморфное состояние его перейдет в кристаллическое. Можно получить и смешанную структуру: аморфная основа и образовавшиеся в ней кристаллы.
В кристаллических твёрдых телах (при меньших скоростях охлаждения) атомы расположены в геометрически правильном порядке, образуя кристаллы и создавая кристаллическую решетку или воображаемую пространственную сетку. Кристаллическим веществам свойственна анизотропия свойств, они имеют различные свойства в разных направлениях. Это объясняется тем, что число атомов, приходящееся на то или иное плоское сечение кристаллической решетки, неодинаково.
В кристаллических твёрдых телах ростях охлаждения) атомы расположены в геометрически правильном порядке, образуя кристаллы и создавая кристаллическую решетку или воображаемую пространственную сетку.
Кристаллическим веществам свойственна анизотропия свойств, они имеют различные свойства в разных направлениях. Это объясняется тем, что число атомов, приходящееся на то или иное плоское сечение кристаллической решетки, неодинаково.
Металлы имеют кристаллические решетки различных типов. Чаще всего встречаются три типа: кубическая объемно-центрированная (ОЦК), кубическая гране- центрированная (ГЦК) и гексагональная плотноупакованная (ГПУ) кристаллические решетки. Показанные на рисунке 3,а...в наименьшие объемы кристаллов называются элементарными кристаллическими ячейками, с помощью которых представляют атомное строение металлов.
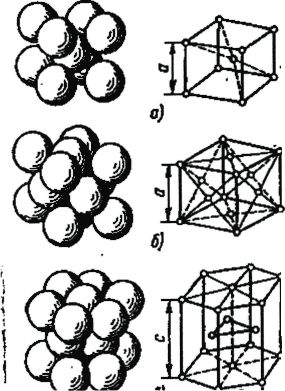
Рисунок 3
В элементарной ячейке кубической объемно-центрированной решетки (рисунок 3, а) содержится девять атомов: восемь располагаются по узлам ячейки и один атом – в центре. Такой тип решетки имеют литий, натрий, калий, рубидий, ванадий, молибден, вольфрам, ниобий, тантал, железо, церий, «-кальций и др. В элементарной ячейке гексагональной плотноупакованной решетки (рисунок 3, в) содержится семнадцать атомов, которые расположены в углах ячейки и центрах шестигранных оснований призмы и три атома в средней плоскости призмы. Такую решетку имеют магний, цинк, кадмий, рений, бериллий, гафний, титан - фаза), осмий и др.
Размеры кристаллической решетки характеризуются расстоянием между центрами соседних атомов, находящихся в вершинах элементарных ячеек, называемым параметром или периодом решетки. Кубическую решетку характеризует один параметр – длина ребра куба а, а гексогональную — два параметра а и с или их отношение с/а.
Плотность различных кристаллических решеток разная и характеризуется координационным числом К, под которым понимают число атомов, находящихся на равном и наименьшем расстоянии от данного атома. Координационное число для кубической объемно-центрированной решетки равно восьми (К8), и коэффициент заполнения (отношение объема, занятого атомами, к объему всей ячейки) равен 68 %. Для гранецентрированной и гексагональной кристаллических решеток координационное число равно двенадцати (К 12), а коэффициент заполнения – 74%.
В кристаллах всегда имеются дефекты (несовершенства) строения, вызванные нарушением расположения атомов в кристаллической решетке. Характер и степень нарушения правильности кристаллического строения определенным образом сказываются на свойствах металлов. Дефекты кристаллического строения по геометрическим признакам подразделяют на точечные, линейные и поверхностные.
К точечным дефектам относят вакансии и межузельные атомы. Известно, что атомы находятся в колебательном движении около узлов решетки. Нагревание увеличивает амплитуду этих колебаний. Большинство атомов металла в данной решетке обладает одинаковой энергией (средней), однако отдельные атомы имеют энергию, превосходящую среднюю и могут перемещаться из одного места в другое. Такие атомы, особенно расположенные ближе к поверхности, выходят на поверхность, а их место могут занять атомы, находящиеся дальше от поверхности. Освободившееся место, где находился переместившийся атом, называется вакансией (рисунок 3, г). Число вакансий увеличивается с повышением температуры, при обработке давлением, облучении и других видах обработки. Вакансии играют важную роль в диффузиойных процессах, происходящих в металлах и сплавах. Межузельные дефекты образуются в результате перехода атома из узла решетка в межузлие кристаллической решетки. Точечные дефекты приводят к искажению кристаллической решетки (рисунок 3).
Линейные дефекты называются дислокациями. Различают два вида дислокаций – краевые и винтовые.
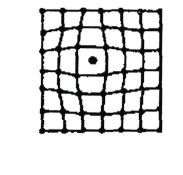
Рисунок 4 – Дефекты кристаллической решотки атома
Краевая дислокация представляет собой местное искажение кристаллической решетки; винтовая дислокация образуется при неполном сдвиге кристалла по плоскости. Дислокации образуются в процессе кристаллизации, при термической и химико-термической обработках, пластической деформации и других видах воздействий на структуру сплавов.
Для дислокации характерна большая подвижность. Это связано с тем, что кристаллическая решетка в зоне нахождения дислокации упруго искажена, а смещенные атомы стремятся переместиться в равновесное положение. На свойства металлов влияет не только плотность дислокаций, но и их расположение в объеме.
Поверхностные дефекты представляют собой поверхности раздела между отдельными кристаллитами или их блоками. На границахзерен расположение атомов менее правильное, чем в зерне.
Вакансии, дислокации и другие дефекты атомно-криссталлического строения оказывают существенное влияние на свойства металлов и сплавов. Как известно, металлы и сплавы находятся в трех агрегатных состояниях – твердом, жидком и газообразном. Переход металла из жидкого состояния в твердое (кристаллическое) называется кристаллизацией. Этот вид кристаллизации называется первичной в отличие от вторичной кристаллизации (перекристаллизации), которая имеет место в твердом металле. В чистых металлах твердое состояние переходит в жидкое при температуре плавления, жидкое в газообразное – при температуре кипения. Температура плавления металлов колеблется от –39°С (для ртути, самого легкоплавкого металла + 3390 °С (для самого тугоплавкого металла вольфрама).
На рисунке 4 приведена схема кристаллизации металла. До тех пор, пока формирующийся вокруг центра кристаллизации кристалл окружен жидким расплавом металла, он имеет правильную геометрическую форму, но при столкновении и срастании кристаллов их правильная форма нарушается и образуются так называемые кристаллиты – зерна.

Рисунок 5 Схема дендранта Д.К. Чернова
Величина зерна зависит от числа центров кристаллизации и скорости роста. На образование центров кристаллизации влияет скорость охлаждения. Чем больше степень охлаждения, тем больше центров кристаллизации и меньше размер зерна. Чем мельче зерно, тем выше механические свойства металла (сплава); особенно это сказывается на пластичности. На процесс кристаллизации оказывает влияние ультразвук; модифицирование; введение порошков, частицы которых служат центрами кристаллизации; поверхностно-активные вещества, облегчающие образование зародышей и др.
Строению металлического слитка посвящены работы Д. К. Чернова, А.А. Бочвара, Л.П. Гуляева, Н.Т. Гудцова, В.Н. Добаткина, И.Н.Фриндлера и др.
Обычно механизм образования кристаллов носит дендритный характер. Это связано с тем, что развитие зародышей протекает главным образом в тех направлениях решетки, которые имеют наибольшую плотность упаковки атомов и минимальное расстояние между ними. В этих направлениях образуются ветви – оси первого порядка (рисунок 5) От осей первого порядка начинают расти новые оси второго порядка – оси третьего порядка III и т.д
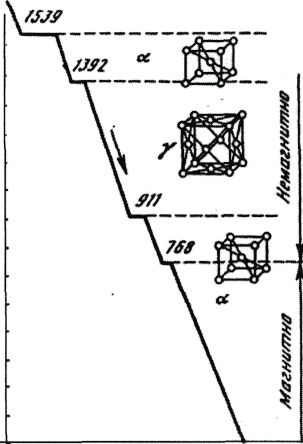
Рисунок 6 График полиморфных
Полиморфизмом или аллотропией называют способность металла в твердом состоянии олиморфные превращения сопровождаются выделением или поглощением теплоты, а также изменением свойств металла Различные аллотропические состояния называют модификациями. Каждой модификации свойственно оставаться устойчивой лишь в пределах определенного для данного металла интервала температур. Аллотропические формы обозначаются греческими буквами а, и т. д. На кривых охлаждения и нагрева превращений железа переход из одного состояния в другое характеризуется остановкой (для чистых металлов) или изменением характера кривой (для сплавов). При аллотропических превращениях кроме изменения свойств (теплопроводности, электропроводности, механических, магнитных и др.) наблюдают изменения объема металла и растворимости (например, углерода в железе). Аллотропические превращения свойственны многим металлам (железу, олову, титану и др.).
Железо
известно в двух полиморфных модификациях
– а
и
![]() .На
рисунке 6 приведена кривая охлаждения,
характеризующая его аллотропические
превращения. Как видно, в интервале
температур 911.... 13920С железо имеет
кубическую гранецентрированную решётку
У
-
железа (Fe),
а в интервале от 0 до 91 ЮС и от 1392 до 15390С
- объёмно центрированную решётку а-
железа
(Fe).
Железо меняет свои магнитные свойства:
выше 7680С железо немагнитно, а ниже -
магнитно.
.На
рисунке 6 приведена кривая охлаждения,
характеризующая его аллотропические
превращения. Как видно, в интервале
температур 911.... 13920С железо имеет
кубическую гранецентрированную решётку
У
-
железа (Fe),
а в интервале от 0 до 91 ЮС и от 1392 до 15390С
- объёмно центрированную решётку а-
железа
(Fe).
Железо меняет свои магнитные свойства:
выше 7680С железо немагнитно, а ниже -
магнитно.
