
- •Раздел 1. Введение
- •Раздел 2. Равновесие сложных гетерогенных систем
- •Тема 1. Правило фаз Гиббса
- •§ 1 Основные определения
- •§ 2 Вывод правила фаз Гиббса
- •§ 3 Условная вариантность.
- •Тема 2. Однокомпонентные системы
- •§1. Общие положения
- •§2. Равновесие двух фаз однокомпонентной системы.
- •§3. Диаграммы состояния однокомпонентных систем
- •Тема 3. Двухкомпонентные системы
- •§1. Общие положения
- •§2. Диаграмма плавкости при неограниченной растворимости в жидком состоянии и полной нерастворимости в твердом
- •§3. Диаграмма плавкости бинарной системы с неограниченной растворимостью компонентов в жидком и твердом состояниях
- •§4. Диаграмма плавкости бинарной системы с устойчивым химическим соединением
- •§5. Диаграмма плавкости бинарной системы с химическим соединением, плавящимся инконгруэнтно
- •Тема 4. Трёхкомпонентные системы
- •§1. Общие положения
- •§2. Геометрические образы фазовых равновесий в тройных сплавах
- •§3. Диаграмма состояния с тройной эвтектикой (растворимость компонентов в твёрдом состоянии отсутствует)
- •3.1. Строение пространственной диаграммы
- •3.2. Кристаллизация типичных сплавов
- •3.3. Реальная диаграмма с тройной эвтектикой
- •3.4. Диаграмма плавкости системы CaO – SiO2 – Al2o3
3.3. Реальная диаграмма с тройной эвтектикой
В качестве примера реальной тройной диаграммы эвтектического типа можно привести систему свинец – олово – кадмий, проекция, которой показана на рисунке.
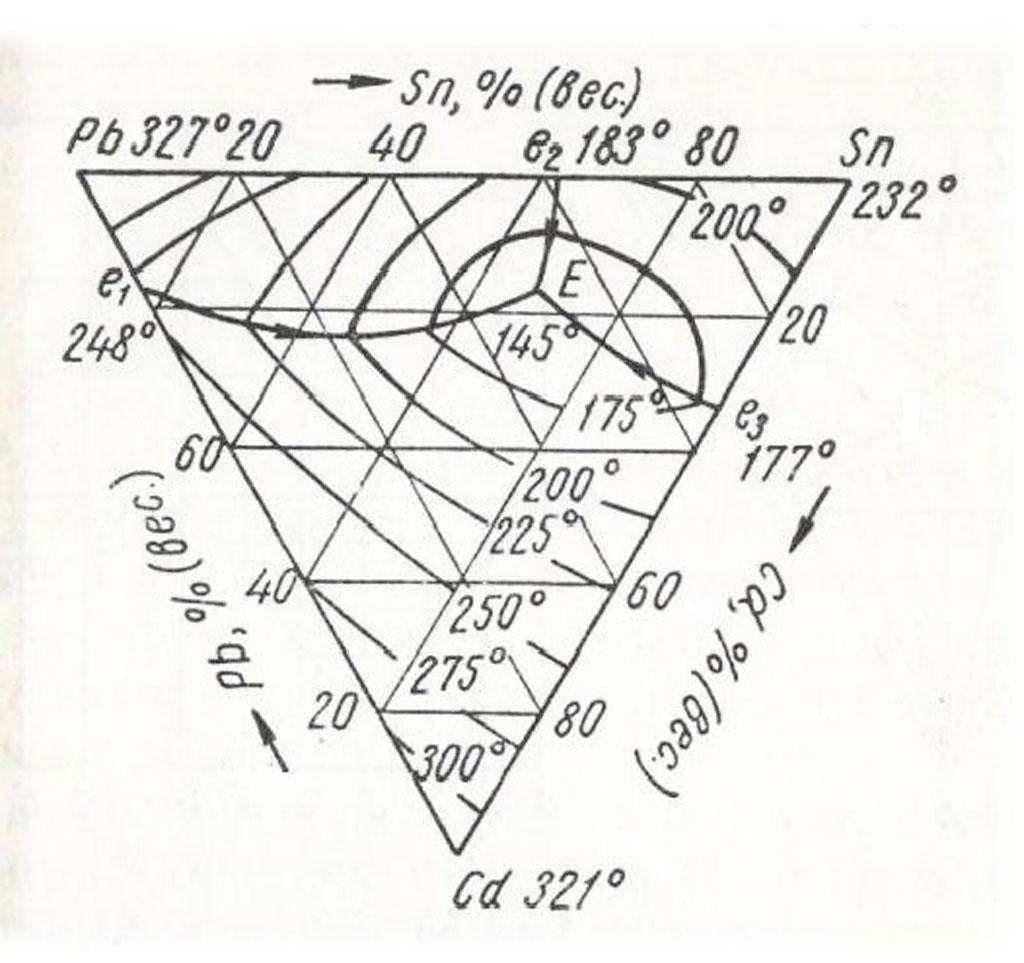
Кривые е1Е, е2Е, е3Е представляют собой линии кристаллизации двойных эвтектик Pb + Cd, Sn + Pb, Sn + Cd. Эти кривые сходятся в точке тройной эвтектики Е (Pb + Sn + Cd), которая плавится при температуре около 145°С. Кроме кривых кристаллизации двойных эвтектик, на рисунке показаны изотермы поверхности ликвидуса через каждые 25°.
3.4. Диаграмма плавкости системы CaO – SiO2 – Al2o3
Диаграмма плавкости системы CaO – SiO2 – Al2O3 (рисунок) имеет большое значение для различных областей техники, так как компоненты системы входят в состав многих материалов.
В данной системе
имеется 5 конгруэнтно плавящихся двойных
соединений, как это следует из двойных
диаграмм состояния и 5 инконгруэнтно
плавящихся двойных соединений. Кроме
того, нужно отметить два тройных
конгруэнтных

соединения: CaO∙Al2O3∙2SiO2 – анортит и 2CaO∙Al2O3∙SiO2 – геленит. Устойчивые двойные и тройные химические соединения на диаграмме обозначены точками (1), инконгруэнтно плавящиеся соединения – точками (2). На поле диаграммы нанесены несколько типов линий. Сплошные линии с одной стрелкой обозначают линии двойных эвтектик (3). Линии с двумя стрелками (4) – линии двойных перитектик. Точки пересечения сплошных линий могут быть охарактеризованы следующим образом. Если стрелки трёх линий направлены в точку пересечения (5), то это точка тройной эвтектики. Если одна из трёх стрелок направлена от точки пересечения (6), то это точка тройной перитектики. Сплошные линии на диаграмме ограничивают области кристаллизации тех или иных соединений. Штрих-пунктирная линия (7) показывает полиморфное превращение кристобалита в тридимит, линя (8) разграничивает области расслаивания жидкости на два несмешивающихся расплава, пунктирные линии (9) являются неточно установленными (предполагаемыми). Изотермы поверхности ликвидуса на диаграмме проведены через каждые 100°.
Рассматривать процессы затвердевания расплавов в такой довольно сложной тройной диаграмме в ряде случаев затруднительно. В связи с этим диаграмму разбивают на ряд более простых (частных) треугольников. Такая процедура носит название триангуляции. При триангуляции в вершинах новых треугольников находятся конгруэнтно плавящиеся химические соединения. Элементарные треугольники позволяют свести анализ затвердевания шлаков в этой сложной системе к рассмотрению более простых случаев.
Например, если мы выделим частный треугольник волластонит – геленит – анортит, то увидим, что полученная частная тройная система ничем не отличается от рассмотренной нами выше тройной диаграммы состояния эвтектического типа. Любой состав, обозначенный фигуративной точкой внутри этого частного треугольника будет окончательно затвердевать при температуре около 1200 °С с образованием тройной эвтектики.
