
- •Физическая химия
- •2. Химическое равновесие
- •2.1. Характеристика химического равновесия
- •2.2. Константа равновесия
- •Принцип Ле Шателье
- •Уравнение изотермы химической реакции Вант-Гоффа
- •Нормальное (стандартное) химическое сродство
- •Вывод уравнения изобары и изохоры химической реакции
- •Зависимость константы равновесия от температуры. Интегрирование уравнения изобары химической реакции
- •3. Фазовые равновесия м свойства растворов
- •3.1. Понятия фаза, компонент, независимые компоненты, степень свободы. Правило фаз Гиббса
- •Диаграмма состояния однокомпонентных систем в координатах «давление – температура». Применение правила фаз для анализа состояния однокомпонентных систем (пояснение на диаграмме состояния).
- •3.3. Предельные законы Рауля. Закон Вант-Гоффа
- •Законы Коновалова
- •I Закон:
- •3.6. Взаимосвязь диаграмм “общее давление – состав” и
- •3.7.Дисциляция (перегонка) двойных смесей, азеотропные смеси
- •3.8.Особенности равновесия в двухкомпонентных системах “кристаллы – жидкость (расплав)”. Диаграммы плавкости двухкомпонентных систем, термический анализ, кривые охлаждения
- •Двухкомпонентная система с эвтектикой.
- •Д иаграмма с простой эвтектикой
- •4.Электрохимия
- •4.1.Растворы электролитов
- •4.1.1.Сильные и слабые электролиты, свойства растворов слабых электролитов. Изотонический коэффициент. Степень диссоциации, её зависимость от концентрации, температуры, посторонних электролитов.
- •4.1.2.Применение закона действия масс к слабым электролитам. Константа диссоциации. Закон разбавления Оствальда
- •4.1.4.Удельная электропроводимость, её зависимость от концентрации и от темперетуры
- •4.1.5.Эквивалентная электропроводность и связь с удельной электропроводностью, её зависимость от концентрации. Предельная эквивалентная электрическая проводимость, её определение
- •4.1.6.Подвижность ионов. Закон независимого движения ионов. Уравнение Кольрауша для электролитов
- •4.2.Термодинамическая теория эдс
- •4.2.1. Возникновение электродных потенциалов и 2го электрического слоя. Гальванический элемент и его эдс. Обратимые гальванические элементы
- •4.2.2.Электродные потенциалы, нормальный водородный электрод. Вычисление эдс элемента
- •4.2.3.Термодинамический вывод уравнения, выражающего зависимость эдс гальванического элемента от активности (Ур-е Нернста)
- •4.2.7.Применения измерений эдс для определения рH раствора. Электроды сравнения, элемент Вестана
- •4.2.8. Применения измерений эдс для аналитических цепей. Потенциометрические тестирования
- •Применение эдс для определения измерения тд функций при электродных реакциях и констант равновесий ( )
- •5.Химическая кинетика
- •5.1.Основные понятия формальной кинетики: скорость реакции, порядок
- •Зависимость скорости от концентрации, константа скорости
- •5.4.Экспериментальные методы определения порядка реакции и константы скорости
- •Метод подстановки (подбора уравнений)
- •Графические методы
- •Метод определения по периоду полураспада.
- •Метод изоляции или избытка реагентов.
- •Определение константы и с для реакции I порядка графическим методом.
- •5.5.Зависимость скорости и константы скорости химической реакции от температуры. Уравнение Аррениуса
- •Теории химической кинетики (активных столкновений переходного состояния или активированного комплекса)
4.2.7.Применения измерений эдс для определения рH раствора. Электроды сравнения, элемент Вестана
Для определения pH собирается гальванический элемент, один из электродов которого обратим по отношению ионов водорода (водородные, стеклянные, хингидродные). Второй электрод – это электрод сравнения, т.е. электрод с известным потенциалом постоянным.
Определение pH с водородным электродом.
(-) Pt, H2 | p-p || KCl | Hg Cl , Hg (+)
ЭДС
=  -
;
=
b lg a
=
- bpH; pH=-lg a
-
;
=
b lg a
=
- bpH; pH=-lg a
Э ДС
=
+ bpH;
ДС
=
+ bpH;
p H
=
H
=

О
Pt
пределение pH с хингидронным электродом.
( -)
Hg, Hg2 Cl
| KCl || p-p
| Pt (+)
-)
Hg, Hg2 Cl
| KCl || p-p
| Pt (+)
C
Исслед р-р
хингидрон
 H
O
*
C
H
(OH)
H
O
*
C
H
(OH)
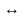 C
H
O
+
C
H
O
+
+C H O +
+ C
H
(OH)
C
H
(OH)
хингидрон – это эквимолекулярный комплекс хинона и гпдрохинона.
C H O + 2H +2e C H (OH)
О О OH
+2е +2H
О хенон О OH гидрохенон
Потенциал
хингедрона  =
=
 +
+
 lg
lg
 ;
a
;
a =const
=const
В
кислотной среде
 1;
1;
В щелочной среде отношение активностей 1
Применять хингедр. электрод только в кислой среде.
lga =
2lga
=
+
b lna
j
= j
-
bpH
=
2lga
=
+
b lna
j
= j
-
bpH
E =j - j E=j - bpH - j
pH
=
 ;
;
4.2.8. Применения измерений эдс для аналитических цепей. Потенциометрические тестирования
Применяется для определения концентрации раствора при титровании составляется гальванический элемент один электрод называется индикаторный его потенциал меняется при титровании, т.е он должен быть обратим по отношению к тем ионам, концентрация которых изменяется при титровании.
Исследуемый раствор помещается в индикаторный электрод, прикасается порциями после каждого титрования, измеряется ЭДС элемента, строится кривая титрования.
ЭДС это функция от объема приливания раствора.
Резкое изменения от количества приливаемого раствора наблюдают точки эквивалентности.
Пимер: титруем кислоту HCl с щелочью NaOH
(-)
Hg, Hg2Cl2
 Pt
(+)
Pt
(+)
 ,
где
,
где
 ,
,

-
HCl + NaOH NaCl + H2O
Vк С = Vщ Сн,щ.
Применение эдс для определения измерения тд функций при электродных реакциях и констант равновесий ( )
G = -nFE.


Тепловой эффект химической реакции:




Измерив ЭДС можно вычислить константу равновесия электрохимической реакции.




5.Химическая кинетика
Основные понятия формальной кинетики: скорость реакции, порядок.
Зависимость скорости от концентрации, константа скорости
.Кинетическая классификация гомогенных необратимых химических реакций. Реакции I и II порядков. Кинетические уравнения. Дифференциальные (интегральные) этих реакций, уравнение, выражающее зависимость концентраций от продолжительности этих реакций, период полупревращения.
Экспериментальные методы определения порядка реакции и константы скорости.
Зависимость скорости и константы скорости химической реакции от температуры. Уравнение Аррениуса.
Теории химической кинетики (активных столкновений переходного состояния или активированного комплекса).
