
Биологическое окисление
Это совокупность окислительных процессов протекающих в живых организмах.
Оно выполняет ряд важных функций:
Энергетическая – сменные процессы снабжают биологические процессы энергией.
Биосинтетическая – путем окислительных реакций могут синтезироваться новые вещества необходимые для организма.
Обезвреживающая (детоксикационная) заключается в том, что путем окислительных реакций многие вещества лишаются своей токсичности.
По современным представлениям процесс окисления сводится к потере электрона. Вещество теряющее электрон – донор, вещество присоединяющее электрон – акцептор. Все живые организмы в зависимости от того, что является конечным акцептором делятся на аэробные и анаэробные. У аэробов конечным акцептором электронов служит кислород. У анаэробных организмов электрон присоединяется не на кислород, а на какое-то другое вещество, акцептор.
История. Теории:
Теория активации кислорода, она предполагает какой-то механизм активации кислорода, так как кислород в организме является окислителем.
П
ерекисная теория Баха 1847. Согласно ей в организме есть вещества, которые взаимодействуя с молекулярным кислородом образуют перекисные вещества, в которых кислород становится более активным.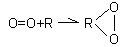
В последствии эта перекись окисляет субстрат. В результате окисленное вещество восстанавливается и к нему присоединяется кислород. Эта теория носит частный характер.
3. Теория дегидрирования Палладина. Согласно ей вещества окисляются не путем присоединения кислорода, а путем потери атомов водорода.
![]()
По теории Палладина допускалось участие в окислительных процессах кислорода воды. Теория Палладина универсальна и она легла в основу современного представления о биологическом окислении.
Процессы биологического окисления могут протекать в разных отсеках клетки. Принято выделять 2 вида окисления: внутримитохондриальное и внемитохондриальное.
Внутримитохондриальное протекает на внутренней мембране митохондрий, оно выполняет энергетическую функцию.
Внемитохондриальное протекает в цитозоле, ЭПС, пероксисомах и на внешней мембране митохондрий. Оно в основном участвует в биосинтетических и детоксикационных процессах.
В обоих окислениях участвует большое количество ферментов, коферментов, переносчики электронов. К ферментам участвующим в биологическом окислении относятся: дегидрогеназы, оксигеназы, пероксидазы.
Дегидрогеназы
Двух видов. В зависимости от небелковой части делят на никотинзависимые и флавиновые.
Никотинзависимые – сложные белки состоящие из белковой и небелковой части. Небелковая часть представлена 2 нуклеотидами НАД, НАДФ. Белковая часть определяет специфичность фермента, имеет молекулярную массу =70 тыс. В активном центре присутствуют SH группы. Кофермент представлен динуклеотидами.
НАД – никотинамид аденин динуклеотид
НАДФ – никотинамид аденин динуклеотид фосфат.
Состав НАД включает два нуклеотида:
аденин – рибоза – Н3 РО4
Никотинамид – рибоза - Н3 РО4
Состав НАДФ:
рибоза (Н3 РО4) - Н3 РО4
НАД и НАДФ определяют третичную структуру дегидрогеназ, придают активность белковой части и участвуют в переносе кислорода. Могут встречаться дегидрогеназы активные только в присутствии НАД: лактатдегидрогеназа, малатдегидрогеназа. Есть ферменты где коферментом является только НАДФ: глюкоза-6-фосфат ДГ, 6-фосфоглюконат ДГ.
Общий вид реакции катализирующие НАД (НАДФДГ):
Субстрат Н2 + кофермент (НАД,НАДФ)→ субстрат + НАДН2 (водород отрывается от субстрата, а кофермент восстанавливается).
НАД и НАДФ отщепляются от белковой части легко. В этой реакции из НАДФ непосредственным акцептором протонов и электронов в составе НАД или НАДФ являются частью никотинамида.
Механизм окисления
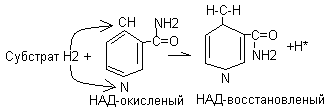
В последующем НАДН2 используется в энергетических процессах, а НАДН используется как источник Н2 для восстановительных синтезов (синтез ЖК).
В составе НАД и НАДФ содержится витамин РР (никотиновая кислота) – противопеллагрический .Содержится в злаках, суточная потребность до 10мг.
Биологическая роль – входит в состав НАД и НАДФ участвует в процессах биологического окисления. Авитаминоз проявляется в заболевании пеллагра (шершавая кожа), симптомы дерматит, слабоумие, расстройства функций кишечника, диарея, болезнь трех Д.
Флавопротеиды
Это сложные белки, состоящие из белка и небелковой части представленной ФМН (ФАД). Белковая часть имеет большую молекулярную массу=200тыс и прочно связывается с небелковой частью. Нуклеотиды: ФМН – флавин моно нуклеотид. Он состоит из флавина, рибитола, Н3 РО4. ФАД – флавин аденин динуклеотид
Общий вид реакции:
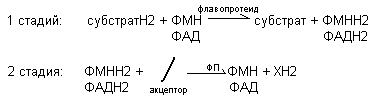
В качестве субстратов для флавопротеидов является янтарная кислота, активные формы жирных кислот. В этом случае Флавопротеиды являются первичными акцепторами протонов и электронов для этих веществ. Донором Н2 для флавопротеидов является молекула НАДН2. В этом случае Флавопротеиды являются промежуточными акцепторами протонов и электронов. В качестве акцепторов могут быть убихинон, или непосредственно кислород. Переносчиком протонов и электронов в составе флавопротеидов служит флавил.
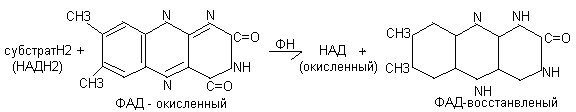
В составе ФМН и ФАД содержится витамин В2 (рибофлавин) – витамин роста. Он включает флавин и рибитол. Распространен в оболочке злаков, дрожжах. Суточная потребность 1-2мг. Биологическая роль – входит в состав ФМН и ФАД, участвует в биологическом окислении.
Авитаминоз – дерматит, катаракта, анемия, поражение сердечной мышцы.
