
- •1)Інтерференція світлових хвиль. Когерентність світлових хвиль.
- •2)Методи спостереження інтерференції світла.
- •5)Метод графічного додавання амплітуд світлових хвиль.
- •6)Дифракція Френеля від круглого отвору.
- •7)Дифракція Фраунгофера від щілини.
- •8)Дифракція Фраунгофера на дифракційній решетці.
- •3)Принцип Гюйгенса-Френеля.
- •4)Дифракція світла. Метод зон Френеля.
- •9)Поляризація світла. Закон Малюса.
- •10)Види поляризованого світла. Ступінь поляризації.
- •11) Поляризація світла при заломленні та відбитті. Закон Брюстера.
- •12) Природна оптична активність речовини
- •13) Магнітне обертання площини поляризації.
- •14) Дисперсія світла. Області нормальної і аномальної дисперсії
- •15) Електронна теорія дисперсії світла
- •16) Теплове випромінювання. Закон Кірхгофа
- •17. Закон Стефана-Больцмана. Закон Віна
- •18)Формула Релєя-Джинса для функції Кірхгофа
- •19) Квантова гіпотеза і формула Планка
- •20) Рентгенівське віпромінювання
- •27) Рівняння Шредінгера
- •28) Властивості хвильової функції. Квантування енергії.
- •30) Частинка в одномірній прямокутній «потенціальній ямі».
- •31. Проходження частинки крізь потенціальний бар”єр. «Тунельний ефект».
- •32. Атом водню. Головне, азимутне і магнітне квантові числа. Спін електрона. Спінове квантове число.
- •33. Розподіл електронів в атомі по енергетичним рівням. Принцип Паулі.
- •35. Склад і характеристика атомного ядра. Состав и характеристика атомного ядра
- •36. Маса і енергія зв’язку ядра.
- •38. Реакція поділу ядра. Ланцюгова реакція.
- •39. Радіоактивність. Альфа-, бета-, гама-випромінювання атомних ядер.
- •40. Термоядерні реакції
31. Проходження частинки крізь потенціальний бар”єр. «Тунельний ефект».
32. Атом водню. Головне, азимутне і магнітне квантові числа. Спін електрона. Спінове квантове число.
Спін (англ. spin — веретено) — фундаментальна характеристика частинки (наприклад атомного ядра чи елементарної частки), яка в деякому відношенні аналогічна «власному моменту імпульсу частинки». Спін є квантовою властивістю частинок і не має аналогів у класичній фізиці. Тоді як класичний момент імпульсу виникає внаслідок обертання масивного тіла зі скінченними розмірами, спін властивий навіть частинкам, які на сьогодні вважаються точковими, і не пов’язаний із жодним обертанням мас всередині такої частки. (Спін неточкових частинок, наприклад атомних ядер чи адронів, є векторною сумою спінів та орбітального моменту імпульсу її складових. Тобто і у цьому випадку спін лише частково пов’язаний з обертальним рухом всередині частинки.)Спін може набувати лише певні (квантовані) значення:
цілі: 0,1,2,3 ...
напівцілі: 1/2, 3/2, ...Спін є важливою характеристокю елементарних часток.
Головне, орбітальне і квантове число .Для атома водню поняття „власний стан атома” і „стан електрона в атомі” еквівалентні, оскільки у ньому є тільки 1 електрон. Тому квантові числа в атомі водню однозначно характеризують як стан внутрішнього руху атома, так і стан електрона.
1. n – головне квантове число, набуває цілих позитивних значень (n=1,2,3,…,
 ). Вказує на повну енергію електронів
атомів:
). Вказує на повну енергію електронів
атомів:
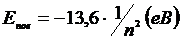 . Вказує на номер енергетичного рівня.
Також головне квантове число вказує
на розміри електронної хмарки і
кількість підрівнів на енергетичному
рівні. У випадку коли n не ціле гамільтоніан
немає рішення. Власні значення для
атома водню для його дискретної частини
визначається наступними співвідношеннями:
. Вказує на номер енергетичного рівня.
Також головне квантове число вказує
на розміри електронної хмарки і
кількість підрівнів на енергетичному
рівні. У випадку коли n не ціле гамільтоніан
немає рішення. Власні значення для
атома водню для його дискретної частини
визначається наступними співвідношеннями:l – орбітальне квантове число. Вказує на форму електронної хмарки та механічний момент електрона навколо ядра. Із теорії Бора – електрон рухаючись по орбіті, повинен мати дискретний момент імпульса
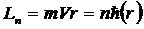
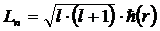 Орбітальне
квантове число може приймати значення:
l=0,1,2,3,…,n-1
Орбітальне
квантове число може приймати значення:
l=0,1,2,3,…,n-1Квантове число l визначає розмір орбітального моменту, але не визначає напрямок орбітального моменту це є скаляр.

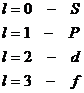 . Магнітне
квантове число – ml, що описує орієнтацію
електронної хмарки в навколо ядерного
просторі.
. Магнітне
квантове число – ml, що описує орієнтацію
електронної хмарки в навколо ядерного
просторі.
33. Розподіл електронів в атомі по енергетичним рівням. Принцип Паулі.
34. Аквнтові явища в твердих тілах. Утворенняенергетичних зон в кристалах
