
- •Химия и технология синтетических лекарственных средств.
- •Производные алифатического ряда.
- •Побочные реакции, протекающие при окислении иас в ивк в кислой среде:
- •Получение ментилового эфира ивк
- •Получение этилового эфира α-бромизовалериановой кислоты
- •Получение Бромизовала
- •Аминокислоты и их производные, используемые в качестве лекарственных средств
- •Исходные вещества для получения ω-аминокислот
- •Получение пирролидона
- •Получение капролактама
- •Получение β-аланина
- •Получение Ацемина
- •Лекарственные средства – производные соединений ароматического ряда. Производные ароматических аминов.
- •Получение парацетамола и фенацетина
- •Производные мезидина и 2-м-ксилидина
- •Бромгексин и Амброксол
- •Лекарственные средства – производные n – аминобензойной кислоты.
- •Сульфаниламидные препараты
- •Примеры сульфаниламидных препаратов.
- •Исходные вещества для получения сульфаниламидных препаратов
- •Синтез сульфаниламидных препаратов
- •Лекарственные средства – производные фенолов Общие способы получения фенолов
- •Лекарственные средства – производные фенолов
- •Производные галоген фенолов
- •Лекарственные средства, производные салициловой кислоты.
- •Методы получения салициловой кислоты и ее производных.
- •Общие подходы к синтезу «сложных» лекарственных средств – производных салициловой кислоты
- •Лекарственные средства – производные гетероциклических соединений Производные пиридина
- •Некоторые лекарственные средства, получаемые на основе β-пиколина
- •Некоторые лекарственные средства, получаемые на основе γ-пиколина
- •Реакции характерные для соединений пиридинового ряда.
- •Нуклеофильные реакции пиридинового кольца. Реакции n-окисей пиридинов.
- •Лекарственные средства – производные пиридина, получаемые путем синтеза пиридинового кольца.
- •Производные фентиазина
- •Лекарственные средства производные фентиазина
- •Лекарственные средства – производные бенздиазепина
- •Методы синтеза о-аминобензофенонов
- •Общие методы синтеза бенздиазепинов
Бромгексин и Амброксол
|
|
В качестве исходных соединений в синтезе можно использовать; для получения первого исходного соединения:
|
|
В качестве второго исходного соединения используют:
|
|
Метил циклогексиламин получают из циклогексанола восстановительным аминированием:

4-Аминоциклогексанол в промышленности получают каталитическим гидрированием 4-аминофенола:

Вторую часть молекулы «собирают» одним из двух методов:

Восстановление антраниловой кислоты в о-аминобензиловый спирт проводят электрохимически в диафрагменных электролизерах, когда катодные и анодные пространства разделены пористой перегородкой.
Из о-аминобензилового спирта реакцией с фосгеном получают циклический уретан. Последний используют для алкилирования аминов:

Полученный на первой стадии продукт бромируют бромом в уксусной кислоте:

Существует другой способ, в котором в качестве исходного соединения используют о-нитротолуол:

Бромирование полученного амина проводят в тех же условиях, описанных в примере выше.
При алкилировании используют избыток амина для того, чтобы предотвратить кватернизацию (образование четвертичных аммониевых солей) и тем самым повысить выход продукта алкилирования.
Реакционную массу последовательно промывают: сначала подкисляют и экстрагируют нейтральные примеси, затем подщелачивают и выделяют основание. Его восстанавливают либо каталитически, либо металлами. Амброксол получают аналогично.
Лекарственные средства – производные n – аминобензойной кислоты.

Исходным соединением для получения n-аминобензойной кислоты и ее производных служит n-нитротолуол, который получают нитрованием толуола серно-азотной нитрующей смесью, при этом соотношение изомеров о- : n- = 2:1. В качестве примеси образуется до 4% м-нитротолуола.
Смесь после нитрования промывают водой для удаления основного количества минеральных кислот, затем содой и снова водой. Обработанную массу подвергают ректификации. Фракцию, содержащую преимущественно n-изомер подвергают вымораживанию. В результате чего получают чистый n-нитротолуол.
Окислением n-нитротолуола получают n-нитробензойную кислоту:

В качестве окислителей обычно используют:KMnO4; K2Cr2O7; HNO3; [NaOCl].
Относительная стоимость 1 г атома кислорода: 20; 3,5; 1,5; 1,0.
Недостатки окислителей: NaOCl – практически не окисляет n-нитротолуол; HNO3 – может быть использована в качестве окислителя, однако для окисления необходима высокая температура (окисление проводят в автоклавах под избыточным давлением). Для окисления используется разбавленная азотная кислота, температура процесса довольно высокая, поэтому в качестве конструкционного материала для изготовления автоклава должен быть использован титан.
При окислении выделяется смесь окислов азота (NO и NO2), следовательно, необходимо предусматривать их абсорбцию. Это приводит к большим эксплуатационным затратам.
K2Cr2O7 – самый приемлемый с точки зрения производства окислитель: легко дозируется, не дает газовых выбросов, аппаратурно легко оформляется.
Недостатки: очень низкие ПДК поVI и III валентному хрому в сточных водах, поэтому обработанную после окисления реакционную массу необходимо обязательно подвергать регенерации. Регенерация хромовых отходов довольно дорогостоящее мероприятие (соединения VI валентного хрома вызывают рак желудка).
KMnO4 – является лучшим окислителем, с точки зрения безопасности. Работает в нейтральной или щелочной среде. В качестве отходов выделяется двуокись марганца, которая легко отделяется фильтрованием.
Перманганат калия используется для получения дорогостоящих продуктов, для которых затраты на окислитель существенным не является.
Нитротолуол можно окислять Na2Cr2O7 в нейтральной среде. Недостаток метода – очень высокая температура 250С. Однако выход n-нитробензойной кислоты по этому методу составляет 82%.
В ходе окисления выделяется щелочь, но защелачивание реакционной массы не происходит, т.к. щелочь взаимодействует с бихроматом переходя в хромат натрия, поэтому при окислении водными растворами Na2Cr2O7 в качестве отхода производства образуется Cr2O3, который хорошо отделяется фильтрованием.

n-Нитробензойную кислоту отфильтровывают после подкисления, фильтрат упаривают при охлаждении до ≈60 из него выпадает Na2SO4, который отфильтровывают. Фильтрат, содержащий бихромат натрия передают на первую стадию для окисления n-нитротолуола.
В настоящее время получение производных n-аминобензойной кислоты проводят через n-нитробензойную кислоту.
n-Нитробензойная кислота легко этерефицируется этиловым спиртом в присутствии H2SO4.

Для повышения выхода эфира, а также для сокращения времени процесса в качестве растворителя можно использовать растворители, которые дают с водой гетероазетропы (системы, которые дают в парах смесь стабильного состава, но при охлаждении делятся на две фазы, одна из которых вода). Бензол, толуол легче воды, поэтому вода в ловушке осаждается на дно, а верхний слой носителя возвращается в реакционную массу.
Лучшим растворителем для проведения этого процесса является толуол, который имеет большую емкость азеотропа и обеспечивает более высокую температуру проведения процесса.
После завершения этерефикации реакционную массу промывают водным раствором щелочи или соды, затем водой. После этого растворитель отгоняют, а эфир очищают либо перегонкой под вакуумом, либо кристаллизацией.
Э тиловый
эфир n-нитробензойной
кислоты является исходным соединением
для получения анестезина. Его получают
каталитическим гидрированием при
атмосферном давлении:
тиловый
эфир n-нитробензойной
кислоты является исходным соединением
для получения анестезина. Его получают
каталитическим гидрированием при
атмосферном давлении:

После завершения процесса катализатор отфильтровывают, спиртовой раствор анестезина упаривают. Выход при гидрировании практически количественный.
Анастезин полученный таким способом отвечает требованиям фармакопейной статьи. Основание используют для приготовления лекарственных средств.
Анастезин используется в качестве исходного соединения в производстве новокаина. Для его получения используется реакция переэтерефикации. В качестве катализатора используют соду (Na2CO3).

Процесс проводят при температуре 120С, выделяющийся в ходе реакции этанол непрерывно отгоняется из реакционной массы. После завершения реакции массу фильтруют, растворяют в спирте, обесцвечивают углем и подкисляют соляной кислотой. При этом выпадает гидрохлорид новокаина, который отфильтровывают, промывают спиртом и сушат. При необходимости кристаллизуют из спирта с добавлением угля.
Технический новокаин, полученный в результате переэтерефикации используется в качестве исходного соединения для получения дикаина.
Для этого спиртовой раствор основания конденсирует с масляным альдегидом:

Далее спиртовой раствор без выделения основания Шиффа подвергают каталитическому гидрированию до n-бутилновокаина. Метод называется восстановительное аминирование. Он является наиболее простым и позволяет получить большой суммарный выход дикаина.
В качестве примесей дикаин может содержать новокаин. Хлоргидрат дикаина получают так же, как и новокаина.
Новокаинамид получают из n-нитробензойной кислоты через хлорангидрид. Хлорангидрид получают реакцией с SOCl2 .

Хлорангидрид – желтое кристаллическое вещество, которое можно либо перегнать под вакуумом, либо перекристаллизовать из неполярного растворителя (бензол, толуол, дихлорэтан, гексан).
Полученный хлорангидрид используют для ацилирования несимметричного N,N-диэтилэтилендиамина. Ацилирование можно проводить в неполярном растворителе. На последней стадии нитропроизводное восстанавливают.
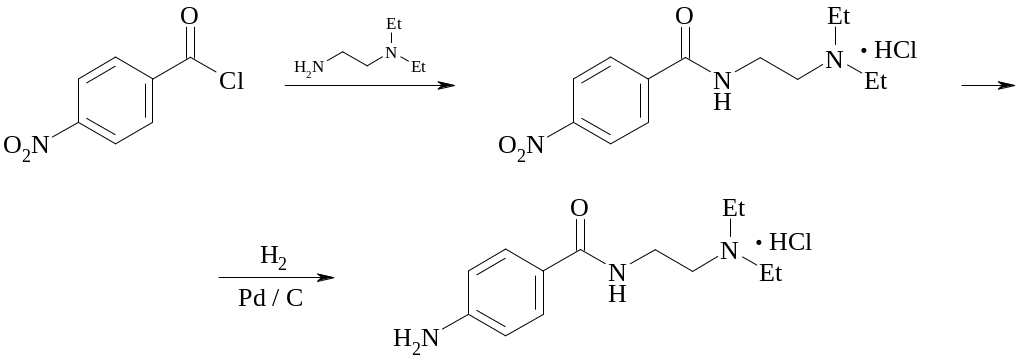
Выделившийся новокаинамид гидрохлорид очищают кипячением с углем его водного раствора с добавлением HCl. Обесцвеченный раствор кристаллизуют с добавлением спирта.






