
- •Химический факультет
- •Введение
- •Ознакомительная часть
- •История оао «Каустик»
- •Общая характеристика производства пвх на предприятии «Каустик»
- •Пиролиз углеводородного сырья и очистка пирогазов
- •Гидрохлорирование ацетилена и выделение винилхлорида
- •Хлорирование этилена
- •Крекинг дихлорэтана
- •Производство инициаторов полимеризации винилхлорида
- •Получение β-бутоксиэтилхлорформиата
- •Получение пероксида натрия
- •Синтез н-бутоксиэтилпероксидикарбоната
- •Синтез хлорсодержащей композиции и пероксидной инициирующей композиции.
- •Полимеризация винилхлорида
- •Исследовательская часть
- •Получение алкил- и полифторалкилхлорформиатов – полупродуктов производства инициирующих перекисных композиций - из фосгена (литературный обзор)
- •О возможности замены пероксида лауроила в инициирующей композиции на 1,1,5-тригидроперфторпентилпероксидикарбонат
- •Уравнения и параметры кинетической модели суспензионной полимеризации винилхлорида
- •Оптимизация загрузки и соотношения инициаторов в композиции, состоящей из фторированного пероксидикарбоната и kcs
- •Список литературы.
О возможности замены пероксида лауроила в инициирующей композиции на 1,1,5-тригидроперфторпентилпероксидикарбонат
Обычно при полимеризации винилхлорида суспензионным способом используется смесь как минимум двух инициаторов. Более активный инициатор (имеющий большую константу скорости распада) применяется для «запуска» процесса полимеризации, в то время как инициатор с меньшей константой скорости распада позволяет довести реакцию до высоких конверсий уже после того, как основная часть более активного инициатора разложилась [1]. Одним из примеров такой комбинации инициаторов, использующейся для полимеризации винилхлорида, является смесь н-бутоксиэтилпероксидикарбоната (KCS) и пероксида лауроила. Последний имеет константу скорости распада в 30 раз меньшую, чем у KCS (при 60°С). Известно, что полифторированные пероксидикарбонаты имеют меньшую константу устойчивости по сравнению с нефторированными, а применение их в качестве инициаторов полимеризации винилхлорида позволяет получать полимер, обладающей повышенной термостабильностью и светостойкостью [21]. Улучшение характеристик полимера связано с введением в макромолекулы в качестве концевых групп полифторалкильных фрагментов, а также с причинами, рассмотренными в предыдущем разделе. С учётом сказанного представляет научный интерес изучение возможности замены пероксида лауроила в инициирующей композиции на фторированный пероксидикарбонат. Для проведения такого исследования на основании литературных данных была предложена математическая модель, описывающая зависимость конверсии винилхлорида от времени и тепловыделения от времени при различных концентрациях инициаторов в полимеризационной смеси.
Уравнения и параметры кинетической модели суспензионной полимеризации винилхлорида
В процессе суспензионной полимеризации винилхлорид диспергируется в воде до мелких капель диаметром от микрометра до миллиметра. Каждая такая капля ведёт себя как система, в которой протекает блочная полимеризация. Через очень непродолжительное время после начала реакции в каждой такой капле сосуществуют две фазы: обогащённая мономером фаза (и практически полностью из него состоящая ввиду практически полной нерастворимости полимера в винилхлориде) и фаза, в основном содержащая полимер. Можно предположить, что первая фаза состоит исключительно из мономера, а во второй фазе содержится мономер в количестве, определяемом его растворимостью в полимере. По мере протекания процесса масса фазы 1 уменьшается, в то время как масса фазы 2 увеличивается. Когда конверсия достигает заданного значения Xf, фаза 1 исчезает и начинается поглощение мономера, находящегося в газовой фазе, а, значит, и падение давления в реакторе. Таким образом, кинетическая модель включает в себя два этапа полимеризации, описываемых различными уравнениями. Для описания участка с конверсиями X<Xf использована основанная на работе [24]. Ниже приведён список допущений и уравнений, используемых в применённой модели:
При X<Xf:
Процесс полимеризации проводится при постоянной температуре T
Рассматривается одновременное действие трёх инициаторов
Эффективность инициирования f для каждого из инициаторов принята равной единице
Концентрация и константа диссоциации каждого инициатора принята одинаковой в обеих рассматриваемых фазах.
Последнее условие выражается следующими уравнениями:
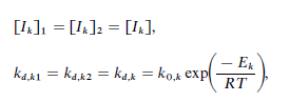
Где k = 1,2,3, индекс 1 обозначает фазу мономера, индекс 2 – полимерную фазу.
Концентрация k-го инициатора в зависимости от времени выражается соотношением:
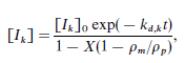
Знаменатель этого выражения отражает изменение объёма системы по мере протекания реакции, ρm/ρp – отношение плотностей мономера и полимера.
Общая концентрация свободных радикалов в каждой фазе при выполнении условия квазистационарности определяется следующими уравнениями:
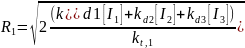
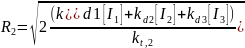
где kt,1 и kt,2 – константы скорости обрыва в фазах 1 и 2 соответственно. Их зависимость от температуры задаётся следующими соотношениями:
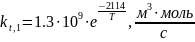
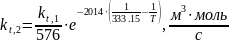
Выражение для kt,2 взято из работы [25].
Концентрация мономера в каждой из фаз:
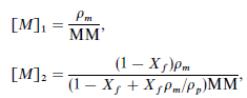 где
MM
– молярная масса мономера.
где
MM
– молярная масса мономера.
Основное кинетическое уравнение для конверсии:
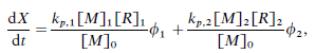
где kp,1 и kp,2 – константы скорости роста цепи, [M]0 – начальная концентрация мономера, равная концентрации мономера в первой фазе (т.к. она не меняется со временем – объём фазы 1 пропорционален количеству вещества мономера в ней), φ1 и φ2 – объёмная доля фаз 1 и 2 соответственно.
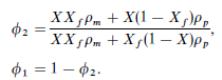
Константы скорости роста цепи полагаются равными для фаз 1 и 2 и определяются соотношением из работы [25]
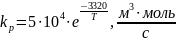
Критическое значение конверсии Xf задаётся соотношением
![]()
Плотности мономера и полимера в зависимости от температуры определяются соотношениями
![]() ,
где θ – температура в °C
,
где θ – температура в °C
![]()
Полученное
дифференциальное уравнение вида
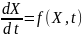 решалось
численным методом Рунге – Кутта
четвёртого порядка.
решалось
численным методом Рунге – Кутта
четвёртого порядка.
Для высоких конверсий X>Xf применена более простая модель, описанная и параметризованная в работах [26,27] и модифицированная на случай использования нескольких инициаторов.
Суть её в следующем. Поскольку в области значений X>Xf эффективность инициирования, константа скорости обрыва цепей и константа скорости роста цепи падают с ростом конверсии, в работе [26] предложено учесть этот эффект, полагая, что комбинация этих величин пропорциональна (1-X). Уравнения модели следующие:
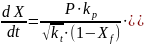
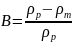
Параметризация для P дана в работе [27]:
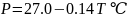
Для
согласования двух моделей в точке X=Xf,
пользуясь условием равенства производной
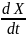 ,
определяемой
из двух моделей, в выражение для
при
X>Xf
введён дополнительный множитель,
численно равный 1,55 при всех температурах.
,
определяемой
из двух моделей, в выражение для
при
X>Xf
введён дополнительный множитель,
численно равный 1,55 при всех температурах.
Скорость изменения конверсии связана со скоростью выделения теплоты в любой момент времени следующим соотношением:
![]() ,
где mD
– общая масса загружаемого винилхлорида,
-ΔH=25,33
ккал/моль.
,
где mD
– общая масса загружаемого винилхлорида,
-ΔH=25,33
ккал/моль.
