
- •2.Электронное и пространственное строение органических вещест
- •2. Адсорбция. Применение в медицине.
- •1.Теория а. М. Бутлерова.
- •2. Углеводы. Применение в медицине
- •2. Аминокислоты. (Строение, состав, получение, применение в медицине).
- •1.Окислительно-востановительные реакции. Применение в медицине.
- •2. Альдегиды и кетоны. (Строение, состав, получение, применение в медицине).
- •15 Билет
- •2. Белки. Применение в медицине.
- •16 Билет
- •1.Липиды. Применение а медицине.
- •17 Билет
- •18 Билет
- •1 Растворы. Применение в медицине.
- •19 Билет
- •20 Билет
- •1 Энтальпия. Применение в медицине.
- •20 Билет
- •1.Тэд. Степень диссоциации
- •21 Билет
- •1 Закон Гесса. Применение в медицине.
- •22Билет
- •23 Билет
- •24 Билет
- •2Факторы, влияющие на смещение равновесия
- •2. Кислоты
- •2. Нуклеиновые кислоты. Применение в медицине.
2. Аминокислоты. (Строение, состав, получение, применение в медицине).
Аминокислоты, класс органических соединений, объединяющих в себе свойства кислот и аминов, т. е. содержащих наряду с карбоксильной группой -COOH аминогруппу -NH2. играют очень большую роль в жизни организмов, т. к. все белковые вещества построены из Аминокислоты. бесцветные кристаллические вещества, растворимые в воде
Состав:
Все природные Аминокислоты, кроме глицина, содержат асимметричные атомы углерода, существуют в оптически активных модификациях и, как правило, относятся к L-ряду. Аминокислоты D-ряда содержатся только в некоторых антибиотиках и в оболочках бактерий.
Применение в медецине:
• При лечении сердечных заболеваний.
• Для снижения артериального давления.
• Для повышения иммунитета.
При некоторых нарушениях работы нервов.
Билет№7
1.Окислительно-востановительные реакции. Применение в медицине.
Окислительно-восстановительные реакции (ОВР) — это встречно-параллельные химические реакции, протекающие с изменением степеней окисления атомов, входящих в состав реагирующих веществ, реализующихся путём перераспределения электронов между атомом-окислителем и атомом-восстановителем.
В процессе окислительно-восстановительной реакции восстановитель отдаёт электроны, то есть окисляется; окислитель присоединяет электроны, то есть восстанавливается. Причём любая окислительно-восстановительная реакция представляет собой единство двух противоположных превращений — окисления и восстановления, происходящих одновременно и без отрыва одного от другого.
Виды окислительно-восстановительных реакций: 1. Межмолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах разных веществ, например:
Н2S + Cl2 → S + 2HCl.
2. Внутримолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах одного и того же вещества, например: NH4NO3 → N2O + 2H2O
3. Диспропорционирование (самоокисление-самовосстановление) — реакции, в которых атомы с промежуточной степенью окисления превращаются в эквимолярную смесь атомов с более высокой и более низкой степенями окисления, например: Cl2 + H2O → HClO + HCl.
4.Репропорционирование (контрпропорционирование) — реакции, в которых из двух различных степеней окисления одного и того же элемента получается одна степень окисления, например: NH4NO3 → N2O + 2H2O.
2. Альдегиды и кетоны. (Строение, состав, получение, применение в медицине).
Альдегиды и кетоны относятся к карбонильным органическим соединениям. Альдегиды – органические соединения, в молекулах которых атом углерода карбонильной группы связан с атомом водорода. Общая формула: R–CН=O.
Кетоны
– органические вещества, молекулы
которых содержат карбонильную группу,
соединенную с двумя углеводородными
радикалами. Общие формулы: 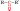 .
.
Систематические названия альдегидов строят по названию соответствующего углеводорода с добавлением суффикса –аль, а кетонов –он.
Применение: Формальдегид Н2С=О (его водный раствор называют формалином) используют как дубитель кожи и консервант биологических препаратов.
Метаналь (муравьиный альдегид) CH2=O - синтез лекарственных средств (уротропин); дезинфицирующее средство;
Билет№8
1.Электрические свойства твердых дисперсных систем определяются их физико-химическими свойствами. Диэлектрическая проницаемость большинства порошкообразных лекарственных веществ невелика и находится в пределах 4,12-6,85, что говорит о сравнительно малой их поляризации и проводимости. По этим значениям таблетируемые вещества можно отнести к категории характерных твердых диэлектриков - асимметричных кристаллов с молекулярной связью и определенным содержанием полярных групп, в частности гидроксилов ОН-, входящих в структуру молекулы или в состав адсорбционной пленки воды.
2. ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ (полимеры), характеризуются мол. массой от неск. тысяч до неск. (иногда многих) миллионов. В состав молекул высокомолекулярных соединений (макромолекул)входят тысячи атомов, соединенных хим. связями. Любые атом или группа атомов, входящие в состав цепи полимера или олигомера, наз. составным звеном. Наим. составное звено, повторением к-рого м. б. описано строение регулярного (см. ниже) полимера, наз. составным повторяющимся звеном. Составное звено, к-рое образуется из одной молекулы мономера при полимеризации, наз. мономерным звеном (ранее иногда наз. элементарным звеном). Напр., в полиэтилене [-СН2СН2-]n повторяющееся составное звено - СН2, мономерное -СН2СН2.
Билет9
1.Комплексные соединения - сочетание, обхват или координационные соединения частицы ,нейтральные молекулы или ионы, которые образуются в результате присоединения к данному иону или атому, называемому комплексообразователем, нейтральных молекул или других ионов, называемых лигандами.
НОМЕНКЛОТИУРА:
1) В названии комплексного соединения первым указывают анион|отрицательно заряженную часть — анион, затем положительную часть — катион.
2) Название комплексной части начинают с указания состава внутренней сферы. Во внутренней сфере прежде всего называют лиганды — анионы, прибавляя к их латинскому названию окончание «о». Например: Cl− — хлоро, CN− — циано, SCN− — тиоцианато, NO3− — нитрато, SO32− — сульфито, OH− — гидроксо и т. д. При этом пользуются терминами: для координированного аммиака — аммин, для воды — аква, для оксида углерода(II) — карбонил.
3) Число монодентатных лигандов указывают греческими числительными: 1 — моно (часто не приводится), 2 — ди, 3 — три, 4 — тетра, 5 — пента, 6 — гекса. Дляполидентатных лигандов (например, этилендиамин, оксалат) используют бис-, трис-, тетракис- и т. д.
4) Затем называют комплексообразователь, используя корень его латинского названия и окончание -ат, после чего римскими цифрами указывают (в скобках) степень окисления комплексообразователя.
5) После обозначения состава внутренней сферы называют внешнюю сферу.
6) В названии нейтральных комплексных частиц комплексообразователь указывается в именительном падеже, а степень его не указывается, так как она однозначно определяется, исходя из электронейтральности комплекса.
Примеры:
K3[Fe(CN)6] — гексацианоферрат(III) калия
(NH4)2[PtCl4(OH)2] — дигидроксотетрахлороплатинат(IV) аммония
[Сr(H2O)3F3] — трифторотриаквахром
СОСТАВ:
в комплексных соединениях различают комплексообразователь,внешнюю и внутреннюю сферы. Комплексообразователем обычно является катион или нейтральный атом. Внутреннюю сферу составляет определенное число ионов или нейтральных молекул, которые прочно связаны с комплексообразователем. Их называют лигандами. Число лигандов определяет координационное число (КЧ) комплексообразователя.
2.Ами́ны — органические соединения, являющиеся производными аммиака, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы.
Хинин - обладающий жаропонижающим и обезболивающим свойствами
Анилин
В России он в основном применяется в качестве полупродукта в производстве ~лекарственных средств (сульфаниламидные препараты)
Сульфаниламидные препараты (сульфаниламиды)- в готовом виде представляют собой белые или слегка желтоватые порошки без запаха и вкуса, плохо растворимые в воде. Их противомикробное действие связано главным образом с тем, что они нарушают процесс получения микробами необходимых для их жизни и развития "ростовых" факторов - фолиевой кислоты и других веществ
Билет 10
а- и у-Пираны представляют собой неустойчивые соединения. В отличие от аиупирана, их оксопроизводные являются довольно устойчивыми ароматическими соединениями. а-Пирон — бесцветная жидкость с запахом свежего сена, перон — бесцветное кристаллическое вещество. В молекулах а- и у-пиронов неподеленная пара электронов циклического атома кислорода находится в сопряжении с л-электронам и двойной связи оксогруппы
Фенол-Терапевтическое применение. Смазывание концентрированными растворами вызывает побеление кожи, ощущение боли; белое пятно состоит из весьма непостоянного соединения карболовой кислоты с тканью верхней кожицы; участки кожи становятся после смазываний 3-5-процентн. растворами, вследствие пропитывания карболовой кислотой окончаний чувствительных, нечувствительными, в них испытывается чувство онемения в течение нескольких часов. На этих свойствах карболовой кислоты основано наружное применение ее в слабых растворах как болеутоляющего средства и в концентрированных растворах как прижигающего и разрушающего вещества. Благодаря противогнилостным свойствам фенол находит широкое применение для обеззараживания предметов и помещений, в которых могут оставаться после заразных больных вредоносные бактерии, а также при противогнилостном способе лечения ран; с этой же целью растворами фенола еще и до настоящего времени пропитывают перевязочные средства (марлю, вату, юту и др.), хотя "противогнилостный" способ теперь стараются заменить"безгнилостным", т. е. способом, при котором не допускают микроорганизмов к ране, так как при этом получаются лучшие результаты. Внутрь фенол назначается, обыкновенно в пилюлях, по 0,02—0,04 несколько раз в день, против ненормальных процессов брожения или гниения в желудке или в кишечнике
БИЛЕТ 11
1.Буферные растворы (англ. buffer, от buff — смягчать удар) — растворы с определённой устойчивой концентрацией водородных ионов; смесь слабой кислоты и её соли(напр., СН3СООН и CH3COONa) или слабого основания и его соли (напр., NH3 и NH4CI). Величина рН буферного раствора мало изменяется при добавлении небольших количеств свободной сильной кислоты или щёлочи, при разбавлении или концентрировании. Буферные растворы широко используют в различных химических исследованиях.
Буферные растворы имеют большое значение для протекания процессов в живых организмах. Например, в крови постоянство водородного показателя рН поддерживается буферными смесями, состоящими из карбонатов и фосфатов. Известно большое число буферных растворов (ацетатно-аммиачный буферный раствор,фосфатный буферный раствор, боратный буферный раствор, формиатный буферный раствор и др.)
2Липи́ды (от греч. λίπος, lípos — жир) — широкая группа органических соединений, включающая жирные кислоты, а также их производные, как по радикалу, так и покарбоксильной группе.
БИЛЕТ12
О́смос (от греч. ὄσμος — толчок, давление) — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону бо́льшей концентрации растворённого вещества (меньшей концентрации растворителя.Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый от чистого растворителя полупроницаемой мембраной, при котором прекращается диффузия растворителя через мембрану. Это давление стремится уравнять концентрации обоих растворов вследствие встречной диффузии молекул растворённого вещества и растворителя
Оксикислоты (оксикарбоновые кислоты, гидрокискарбоновые кислоты) — карбоновые кислоты, в которых одновременно содержатся карбоксильная и гидроксильная группы, например молочная кислота: СН3-СН(ОН)-СООН. Оксикислоты проявляют все свойства, характерные для кислот (диссоциация, образование солей, сложных эфиров и т. д.), и свойства, характерные дляспиртов (окисление, образование простых эфиров и т. д.).
БИЛЕТ13
2.Сложные эфиры — производные оксокислот (как карбоновых так и минеральных) RkE(=O)l(OH)m, (l ≠ 0), формально являющиеся продуктами замещения атомов водорода гидроксилов —OH кислотной функции на углеводородный остаток (алифатический, алкенильный, ароматический или гетероароматический); рассматриваются также как ацилпроизводные спиртов. В номенклатуре IUPAC к сложным эфирам относят также ацилпроизводные халькогенидных аналогов спиртов (тиолов, селенолов и теллуролов)[1]Жиры, или триглицериды — природные органические соединения, полные сложные эфиры глицерина и одноосновныхжирных кислот; входят в класс липидов. В живых организмах выполняют структурную, энергетическую и др. функции.
Наряду с углеводами и белками, жиры — один из главных компонентов питания. Жидкие жиры растительного происхождения обычно называют маслами — так же, как и сливочное масло
БИЛЕТ14
1.Диспе́рсная систе́ма — это система, образования из двух или более фаз (тел), которые совершенно или практически не смешиваются и не реагируют друг с другом химически. Первое из веществ (дисперсная фаза) мелко распределено во втором (дисперсионная среда). Если фаз несколько, их можно отделить друг от друга физическим способом (центрифугировать, сепарировать и т. д.).Обозначение Дисперсионная среда Дисперсная фаза Название и пример Ж/Ж Жидкая Жидкая Эмульсии: нефть, крем, молоко Т/Ж Жидкая Твёрдая Суспензии и золи: пульпа, ил, взвесь, паста Г/Ж Жидкая Газообразная Газовые эмульсии и пены Ж/Т Твёрдая Жидкая Капиллярные системы: жидкость в пористых телах, грунт, почва Т/Т Твёрдая Твёрдая Твёрдые гетерогенные системы: сплавы, бетон, ситаллы, композиционные материалы Г/Т Твёрдая Газообразная Пористые тела Ж/Г Газообразная Жидкая Аэрозоли: туманы, облака Т/Г Газообразная Твёрдая Аэрозоли (пыли, дымы), порошки Г/Г Газообразная Газообразная Дисперсная система не образуется
2.Этано́л (эти́ловый спирт, метилкарбино́л, ви́нный спирт, часто в просторечии просто «спирт» или алкого́ль) — одноатомный спирт с формулой C2H5OH (эмпирическая формула C2H6O), другой вариант: CH3-CH2-OH, второй представитель гомологического рядаодноатомных спиртов, при стандартных условиях летучая, горючая, бесцветная прозрачная жидкостьМедицинский спирт содержит 95% спирта. Это бесцветная легковоспламеняющаяся жидкость, которая горит синим пламенем и хорошо смешивается со всеми веществами.
По своим фармакологическим качествам этиловый спирт является наркотическим веществом, к воздействию компонентов которого особенно чувствительна центральная нервная система и клетки коры головного мозга. Поэтому применение спирта в качестве алкогольного средства всегда вызывала ответную реакцию.
В медицинской практике спирт этиловый находит самое широкое применение в качестве дезинфицирующего, антисептического средства, имеющего к тому же раздражающий эффект, что в некоторых случаях требуется для проведения манипуляций. Если задаться вопросом – как правильно делать укол, то окажется, что без спирта делать их невозможно.
На базе этилового, или медицинского спирта производятся многие лекарства, настойки, экстракты для наружного примененияВ медицинской практике спирт применяется как противовоспалительное средство для проведения противовоспалительной терапии при нарывах внешнего кожного покрова, фурункулов, маститов, различных инфильтратов. Также спирт применяется для обеззараживания операционных полей, при протирании рук хирурга перед операциями.
