
- •Давление кровотока. Скорость кровотока. Схема сердечно-сосудистой системы ( ссс ).
- •Белковый обмен
- •Углеводный обмен
- •Жировой обмен
- •Пигментный обмен
- •Образование билирубина
- •По биологическому значению
- •По расположению рецепторов, раздражение которых вызывает данный рефлекторный акт
- •По месту расположения нейронов, участвующих в рефлексе
- •По характеру ответной реакции, в зависимости от того, какие органы в ней участвуют
Пигментный обмен
Возникновение желтухи всегда обусловлено нарушением обмена билирубина, который образуется в результате распада гемоглобина эритроцитов и разрушения гема. Этот процесс является естественной составной частью постоянного обновления красной крови в организме.
Образование билирубина
Гемоглобин превращается в билирубин в ретикулоэндотелиальной системе, главным образом в печени, селезенке и костном мозге посредством сложного комплекса окислительно-восстановительных реакций. Конечным продуктом распада является биливердин, не содержащий железа и белковой части. Клетки ретикулоэндотелиальной системы выделяют в кровь непрямой, свободный билирубин. За сутки у человека распадается около 1% циркулирующих эритроцитов с образованием 100 - 250 мг билирубина, при этом 5 - 20% билирубина образуется из гемоглобина не зрелых, а преждевременно разрушенных эритроцитов и из других гемсодержащих веществ. Это так называемый шунтовои или ранний билирубин.
Исследованиями с введением в организм изотопных предшественников гема (15N- и 14С-глицин) установлено, что большинство образующихся меченых желчных пигментов выделяются с калом в виде уробилина или стеркобилина в период между 90-м и 150-м днем после введения изотопа, что соответствует продолжительности жизни эритроцитов [Gray С. Н., 1950, 1959; London J. М., 1950].
Выявлено незначительное содержание меченого пигмента в кале сразу же после применения изотопного предшественника, составляющее от 10 до 20% всей меченой пигментной экскреции, что соответствует раннему, или шунтовому, билирубину.
Значительное увеличение образования раннего билирубина обнаружено при болезнях, связанных с неэффективным эритропоэзом, таких, как железодефицитная анемия, пернициозная анемия, талассемия, сидеробластическая анемия, эритропоэтическая порфирия, свинцовое отравление. При этих состояниях количество раннего пигмента колеблется от 30 до 80% всех желчных пигментов. Больные с этой патологией имеют значительно увеличенную фекальную уробилиногенную экскрецию как следствие увеличенного тотального желчного пигментного оборота, но без укорочения жизни эритроцитов периферической крови.
Существование второго неэритроцитного компонента раннего билирубина доказано с применением меченой аминолевулиновой кислоты, являющейся маркером гема из других источников. Наиболее вероятным источником неэритроцитного гема служат печеночные протеиды: миоглобин, цитохромы, каталаза и триптофанпирролаза печени.
Экспериментально установлено, что печеночная часть раннего билирубина может увеличиваться после анестезии, применения фенобарбитала. Этим может объясняться повышение сывороточного билирубина, часто наблюдаемое непосредственно после операции [Israels L. G., 1970].
Пищеварение в ротовой полости и желудке. Изменения в процессе пищеварения при мышечной деятельности.
В ротовой полости осуществляется анализ вкусовых свойств веществ и разделение их на пищевые и отвергаемые: защита пищеварительного тракта от попадания некачественных пищевых веществ и экзогенной микрофлоры; измельчение, смачивание слюной пиши, начальный гидролиз углеводов и формирование пищевого комка; раздражение механо-, хемо-, терморецепторов, вызывающее возбуждение деятельности не только собственных, но и пищеварительных желез желудка, поджелудочной железы, печени, двенадцатиперстной кишки. Защиту организма от патогенной микрофлоры ротовая полость выполняет благодаря наличию в слюне бактерицидного вещества лизоцима. антивирусному действию нуклеазы слюны, способности IgA слюны связывать эндотоксины, а также в результате фагоцитоза лейкоцитов и угнетения патогенной микрофлоры нормальной микрофлорой полости рта.
Слюнными железами вырабатываются гормоноподобные вещества, участвующие в регуляции фосфорно-калышевого обмена костей и зубов, в регенерации эпителии слизистой оболочки ротовой полости, пищевода, желудка и регенерации нервных волокон при их повреждении.
Пища находится в ротовой полости 16—18 с, и за это время слюной смачиваются сухие вещества, растворяются растворимые и обволакиваются твердые вещества, нейтрализуются раздражающие жидкости или уменьшаемся их концентрация и т.д.
Из пищевода пища попадает в желудок — мешкообразное расширение пищеварительного канала емкостью около 2–3 л. В его слизистой оболочке расположено около 14 млн. желез, выделяющих желудочный сок. За сутки у человека выделяется от 1,5 до 2,5 л желудочного сока, содержание 0,5% соляной кислоты и ферменты (пепсин), которые расщепляют белки, вызывая их набухание и денатурацию, и способствуют створаживанию молока (репин). Ферменты желудочного сока, расщепляющие белки (пепсин) и створаживающие молоко (ренин), действуют только при температуре 37 ° и в кислой среде.
Желудочный сок, как и слюна, выделяется рефлекторно. Раздражение пищей рецепторов ротовой полости и желудка вызывает сокоотделительный рефлекс.
Импульсы от этих рецепторов проводятся в продолговатый мозг. Оттуда они направляются по центробежному нерву к железам желудка, вызывая обильное отделение желудочного сока. Желудочный сок выделяется не только при попадании пиши в полость рта или в желудок, но и при виде и запахе пиши. Эту очень важную для пищеварения особенность изучил И. П. Павлов. Важность в том, что нища попадает в желудок, когда в нем уже есть сок, который сразу же начинает расщеплять питательные вещества. И. П. Павлов назвал сок, выделяющийся на вид и запах пищи, «аппетитным». Эта сложнорефлекторная фаза желудочной секреции длится около 2 часов, а пища переваривается в желудке в течение 4-8 часок
С поступлением пищи в желудок начинается нервно-гуморальная фаза желудочной секреции. Пища, поступающая в желудок, механически раздражает нервные рецепторы его слизистой оболочки, возбуждение которых усиливает выделение желудочного сока. Кроме того, во время пищеварения в кровь поступают химические вещества — продукты расщепления пищи, физиологически активные вещества (гистамин, гормон гастрит и др.), которые приносятся кровью к железам пищеварительной системы и усиливают секреторную деятельность. Таким образом, осуществляется гуморальная регуляция желудочного сокоотделения.
Основной обмен энергии, методики его определения. Изменение основного обмена в процессе тренировки.
В организме интенсивность обменных процессов в разных условиях существования во многих органах находится на уровне, который отличается от состояния готовности. Так, в дыхательных мышцах, сердце, печени, почках, ЦНС, эндокринных железах процессы обмена всегда должны превышать уровень, необходимый для самоподдержания их структур. Эти органы выполняют работу даже в условиях абсолютного покоя, поскольку от их функций зависит жизнеспособность организма. Поэтому указанные органы постоянно находятся в активном состоянии. Другие органы (скелетные мышцы, органы пищеварения) в течение более или менее длительного времени могут быть в состоянии готовности без особого вреда для организма. Суммарная интенсивность обменных процессов, определенная в условиях покоя, характеризует так называемый основной обмен. Для определения уровня основного обмена необходимо соблюдать следующие условия: исследование проводить утром натощак в состоянии физического и психического покоя, в положении лежа, в условиях температурного комфорта (25-26 ° С). При этом учитываются те основные факторы, которые могут влиять на интенсивность обменных процессов. Даже при строгом соблюдении условий определения основного обмена показатели его отличаются у разных людей. Прежде всего это обусловлено разницей по возрасту, роста, массы тела, пола, а также активности механизмов регуляции обмена веществ. За основу может быть взята величина, равная 1 ккал / (кг • ч), или 42 кДж / (кг • ч). Около 50% основного обмена приходится на энергопотребление печенью и скелетными мышцами. Во время сна при минимальном тонусе скелетных мышц обмен веществ становится ниже уровня основного обмена. При голодании, когда функциональная активность печени снижена, основной обмен также уменьшается. Интенсивность основного обмена в течение суток колеблется? утром он постепенно повышается, а в ночное время снижается. В связи с различной массой тела лучше определить удельную величину основного обмена на 1 кг массы тела. Было отмечено, что не только люди, но и животные находятся гораздо ближе друг к другу по Энергообразование в пересчете на единицу массы тела, а на единицу его поверхности. Предложено правило, согласно которому уровень обменных процессов пропорциональна поверхности тела, то есть той части, в которой происходит теплоотдача. При некоторых заболеваниях, особенно обусловленных нарушением функции щитовидной железы, уровень основного обмена меняется. При гиперфункции он повышается, а при гипофункции - понижается.
Энергия в организме может быть получена в результате окислительных процессов. В связи с этим существует возможность определить энергообмен на основе потребления кислорода. При «сгорании» отдельных пищевых веществ образуется различное количество тепла на 1 л использованного кислорода: углеводы дают 21,23 кДж (5,08 ккал), жиры — 19,56 кДж (4,68 ккал) и белки — 18,73 кДж (4,48 ккал). Процентная доля энергии, получаемой при углеводном и жировом обмене, рассчитывается из соотношения выделения углекислого газа и потребления кислорода (дыхательный коэффициент). Он составляет: при сгорании чистых углеводов — 1, чистых жиров — 0,7, а при обычной у нас в стране смешанной пище — 0,85. То есть, каждой величине дыхательного коэффициента соответствует определенный эквивалент в джоулях (калориях).
В основном обмене спортсменов обнаруживаются сезонные изменения, которые связаны с величиной физической нагрузки при тренировках. В периоды большого объема тренировок основной обмен увеличивается, так как интенсивность обмена веществ при этом значительно повышается.
Второй после основного обмена составляющей энерготрат организма являются так называемые регулируемые затраты энергии. Они соответствуют потребности энергии, используемой на работу сверх основного обмена. Любой вид мышечной деятельности, даже изменение положения тела (из положения лежа в положение сидя), увеличивает энергозатраты организма. Изменение величины потребления энергии определяется продолжительностью, интенсивностью и характером мышечной работы. Поскольку физическая нагрузка может иметь различный характер, энерготраты подвержены значительным колебаниям.
Расход энергии в состоянии покоя и при разных видах спортивной и трудовой деятельности.
Основным обменом называется количество энергии, которое тратит организм при полном мышечном покое, через 12—14 часов после приема пищи и при окружающей температуре 20—22 °С. У взрослого человека он в среднем равен 1 ккал на 1 кг массы тела в 1 час. У людей при массе тела в 70 кг основной обмен в среднем равен около 1700 ккал. Нормальные его колебания составляют ±10 %. У женщин основной обмен несколько ниже, чем у мужчин; у детей он выше, чем у взрослых. ^ Энерготраты в состоянии относительного покоя превышают величину основного обмена. Это обусловлено влиянием на энергообмен процессов пищеварения, терморегуляции вне зоны комфорта и тратами энергии на поддержание позы тела человека. ^ Энерготраты при различных видах труда определяются характером деятельности человека. Суточный расход энергии в таких случаях включает величину основного обмена и энергию, необходимую для выполнения конкретного вида труда. По характеру производственной деятельности и величине энерготрат взрослое население может быть разделено на четыре группы: 1) люди умственного труда, чей суточный расход энергии составляет 2200—3000 ккал; 2) люди, выполняющие механизированную работу и расходующие за сутки 2300—3200 ккал; 3) люди частично механизированного труда с суточным расходом энергии 2500—3400 ккал; 4) люди немеханизированного тяжелого физического труда, энерготраты которых достигают 3000—4000 ккал. При спортивной деятельности расход энергии может составлять 4500—5000 ккал и более. Это обстоятельство следует учитывать при составлении пищевого рациона спортсменов, который должен обеспечивать восполнение расходуемой энергии. На механическую работу тратится не вся освобождающаяся в организме энергия. Большая ее часть превращается в тепло. То количество энергии, которое идет на выполнение работы, называетсякоэффициентом полезного действия (КПД). У человека КПД не превышает 20—25 %. КПД при мышечной деятельности зависит от мощности, структуры и темпа движений, от количества вовлекаемых в работу мышц и степени тренированности человека.
Белковый обмен в организме и его регуляция. Биологическая ценность белков. Азотистый баланс.
Белки являются основным пластическим материалом, из которого построены клетки и ткани организма. Они являются составной частью мышц, ферментов, гормонов, гемоглобина, антител и других жизненно важных образований. В состав белков входят различные аминокислоты, которые подразделяются на заменимые и незаменимые. Заменимые аминокислоты могут синтезироваться в организме, а незаменимые(валин, лейцин, изолейцин, лизин, метионин, триптофан, фенилаланин, аргинин и гистидин) поступают только с пищей. Поступившие в организм белки расщепляются в кишечнике до аминокислот и в таком виде всасываются в кровь и транспортируются в печень. При избыточном поступлении белков с пищей, после отщепления от них аминогрупп, они превращаются в организме в углеводы и жиры. Белковых депо в организме человека нет. Наряду с основной, пластической функцией, белки могут играть роль источников энергии. ^ При окислении в организме 1 г белка выделяется 4,1 ккал энергии. Конечными продуктами расщепления белков в тканях являются мочевина, мочевая кислота, аммиак, креатин, креатинин и некоторые другие вещества. Они выводятся из организма почками и частично потовыми железами. О состоянии белкового обмена в организме судят по азотистому балансу, т. е. по соотношению количества азота, поступившего в организм, и его количества, выведенного из организма. Если это количество одинаково, то состояние называется азотистым равновесием. Состояние, при котором усвоение азота превышает его выведение, называется положительным азотистым балансом. Оно характерно для растущего организма, спортсменов в период их тренировки и лиц, перенесших заболевания. При полном или частичном белковом голодании, а также во время некоторых заболеваний азота усваивается меньше, чем выделяется. Такое состояние называется отрицательным азотистым балансом. При голодании белки одних органов могут использоваться для поддержания жизнедеятельности других, более важных. При этом расходуются в первую очередь белки печени и скелетных мышц; содержание белков в миокарде и тканях мозга остается почти без изменений. Нормальная жизнедеятельность организма возможна лишь при азотистом равновесии, или положительном азотистом балансе. Такие состояния достигаются, если организм получает около 100 г белка в сутки; при больших физических нагрузках потребность в белках возрастает до 120—150 г. Всемирная Организация Здравоохранения рекомендует употреблять не менее 0,75 г белка на 1 кг массы тела в сутки. Богаты белками мясо, рыба, печень, грибы, бобовые, соя и т. п.
Углеводный обмен в организме и его регуляция. Значение углеводов при мышечной деятельности.
Углеводы служат в организме основным источником энергии. При окислении 1 г углеводов освобождается 4,1 ккал энергии. Для окисления углеводов требуется значительно меньше кислорода, чем при окислении жиров. При уменьшении концентрации глюкозы в крови резко снижается физическая работоспособность. Большое значение углеводы имеют для нормальной деятельности нервной системы. При голодании запасы гликогена в печени и концентрация глюкозы в крови уменьшаются. То же происходит при длительной и напряженной физической работе без дополнительного приема углеводов. Снижение содержания глюкозы в крови до 0,06—0,07 % (нормальная концентрация 0,08—0,12 %) приводит к развитию гипогликемии, что проявляется мышечной слабостью, падением температуры тела, а в дальнейшем — судорогами и потерей сознания. При гипергликемии (содержание сахара в крови достигает 0,15 % и более) избыток глюкозы быстро выводится почками. Такое состояние может возникать при эмоциональном возбуждении, после приема пищи, богатой легкоусвояемыми углеводами, а также при заболеваниях поджелудочной железы. При истощении запасов гликогена усиливается синтез ферментов, обеспечивающих реакцию глюконеогенеза, т. е. синтеза глюкозы из лактата или аминокислот. Конечными продуктами обмена углеводов являются вода, углекислый газ и АТФ. Суточная потребность в углеводах около 450 г. ^
Обмен липидов в организме. Значение жиров в энергообеспечении двигательной деятельности.
Физиологическая роль липидов, к которым относят нейтральные жиры, фосфатиды и стерины, в организме заключается в том, что они входят в состав клеточных структур, выполняя пластическую функцию и являясь источниками энергии. Общее количество жира в организме человека колеблется в широких пределах и составляет 10—20 % массы тела, при ожирении оно может достигать 40—50 %. Жировые депо в организме непрерывно обновляются. При обильном углеводном питании и отсутствии жиров в пище синтез жира в организме может происходить из углеводов. Нейтральные жиры, поступающие в ткани из кишечника и жировых депо, окисляются и используются какисточник энергии. При окислении 1 г жира освобождается 9,3 ккал энергии. В связи с тем, что в молекуле жира содержится относительно мало кислорода, последнего требуется для окисления жиров больше, чем при окислении углеводов. Как энергетический материал жиры используются главным образом в состоянии покоя и при выполнении длительной малоинтенсивной физической работы. В начале более напряженной мышечной деятельности используются преимущественно углеводы, которые в дальнейшем в связи с уменьшением их запасов замещаются жирами. При длительной работе до 80 % всей энергии расходуется в результате окисления жиров. ^ Жировая ткань, покрывающая различные органы, предохраняет их от механических воздействий.Скопление жира в брюшной полости обеспечивает фиксацию внутренних органов, а подкожная жировая клетчатка защищает организм от излишних теплопотерь. Секрет сальных желез предохраняет кожу от высыхания и излишнего смачивания водой. Важная физиологическая роль принадлежит стеринам, в частности, холестерину. Эти вещества являются источником образования в организме желчных кислот, а также гормонов коры надпочечников и половых желез. При избытке холестерина в организме развивается патологический процесс — атеросклероз. Некоторые стерины пищи, например, витамин Д, также обладают большой физиологической активностью. Обмен липидов тесно связан с обменом белков и углеводов. Поступающие в организм в избытке белки и углеводы превращаются в жир. Наоборот, при голодании жиры, расщепляясь, служат источником углеводов. Конечные продукты обмена липидов — вода и углекислый газ. Суточная потребность в жирах составляет 70—100 г. ^
Функции почек. Механизм мочеобразования. Влияние мышечной работы на мочеобразование.
Ф-ции почек: 1. Поддержание норма-льного содержания в организме воды, солей и некоторых в-в (глюкоза, аминокислоты); 2. Регуляция рН крови, осмотического давления, ион-ного состава и кислотно-щелочного состояния; 3. Экскреция из организ-ма продуктов белкового обмена и чу-жеродных в-в; 4. Регуляция кровяно-го давления, эритропоэза и сверты-вания крови; 5. Секреция ферментов и биологически активных в-в (ренин, брадикинин, простагландин и др.) Почка обеспечивает 2 процесса – мочеобразов-ый и гомеостатический.
В каждой почке человека около 1 млн нефронов, являющихся ее функцио-нальными единицами и включающими мальпигиево (почечное) тельце и мочевые канальцы.Мальпигиево тель-це состоит из капсулы Шумлянского –Боумана, внутри которой находится сосудистый клубочек. Внутренняя стенка капсулы соприкасается со стенками капилляров сосудистого клубочка, образуя базальную фильт-рующую мембрану. Между ней и наруж-ной стенкой капсулы находится щеле-видная полость, в которую поступает плазма крови, фильтрующаяся через базальную мембрану из капилляров клубочка.Клубочек состоит из при-носящей артерии, сложной сети арте-риальных капилляров и выносящей ар-терии. Диаметр выносящей артериолы меньше, чем приносящей, что способ-ствует поддержанию в капиллярах клубочка высокого кровяного давле-ния. Мочевые канальцы начинаются от щелевидной полости капсулы, которая переходит в проксимальный извитой каналец (каналец первого порядка). Затем проксимальный каналец выпрям-ляется и образует петлю Генле, пе-реходящую в дистальный извитой ка-налец (каналец 2-го порядка), отк-рывающийся в собирательную трубку. Собирательные трубки проходят через мозговой слой почки и открываются на верхушках сосочков.
Воды и низкомолекулярные компоненты плазмы фильтруются через стенки капилляров клубочка. Фильтрат, пос-тупивший в капсулу Шумлянского-Боумена, составляет первичную мочу, которая по своему содержанию отли-чается от состава плазмы только от-сутствием белков. Из каждых 10 л крови, проходящей через капилляры клубочков, образуется около 1 л фильтрата, что составляет в течение суток 150-180 л первичной мочи.
Регуляция мочеобразования осущ-ся нейрогуморальным путем. Высший под-корковый центр регуляции мочеобра-зования – гипоталамус. Импульсы от рецепторов почек по симпатическим нервам поступают в гипоталамус, где вырабатыв-ся антидиуретический гор-мон или вазопрессин, усиливающий реабсорбацию воды из первичной мочи и явл-ся основным компонентом гумо-ральной регуляции
Физиологические механизмы теплообразования и теплоотдачи. Особенности терморегуляции при мышечной деятельности.
Терморегуляция это совокупность физиологических процессов теплообразования и теплоотдачи, обеспечивающих поддержание нормальной температуры тела. В основе терморегуляции лежит баланс этих процессов. Регуляция температуры тела посредством изменения интенсивности обмена веществ, называется химической терморегуляцией. Образование тепла усиливается путем интенсификации обменных процессов, это называется недрожательным термогенезом. Он обеспечивается за счет бурого жира. Его клетки содержат много митохондрий и специальный пептид, вызывающий разобщение процессов окисления и фософрилирования и стимулирующий распад липидов с выделением тепла. Кроме того термогенез усиливает непроизвольная мышечной активность в виде дрожи, произвольная моторной активность. Наиболее интенсивно теплообразование идет в работающих мышцах. При тяжелой физической работе оно возрастает на 500%.
Теплоотдача служит для выделения избытка образующегося тепла и называется физической терморегуляцией. Посредством теплоизлучения выделяется 60% тепла, конвекции (15%), теплопроводности (3 %), испарения воды с поверхности тела и из легких (20%).
Баланс процессов теплообразования и теплоотдачи обеспечивается нервными и гуморальными механизмами. При отклонении температуры тела от нормальной величины, возбуждаются терморецепторы кожи, сосудов, внутренних органов, верхних дыхательных путях. Этими рецепторами являются специализированные окончания дендритов сенсорных нейронов, а также тонкие волокна типа С. Холодовых рецепторов в коже больше, чем тепловых и они расположены более поверхностно. Нервные импульсы от этих нейронов по спиноталамическим трактам поступают в таламус, гипоталамус и кору больших полушарий. Формируется ощущение холода или тепла. В заднем гипоталамусе и преоптической области переднего, находится центр терморегуляции. Нейроны заднего гипоталамуса в основном обеспечивают химическую терморегуляцию, а переднего физическую. В центре имеется три типа нейронов. Первый термочувствительные нейроны. Они расположены в преоптической области и реагируют на изменение температуры крови, проходящей через мозг. Меньшее количество таких же нейронов имеется в спинном и продолговатом мозге. Вторая группа – интернейроны. Они получают информацию от периферических температурных рецепторов и терморецепторных нейронов. Эта группа нейронов служат для поддержания установочной точки, т.е. определенной температуры тела. Одна часть данных нейронов получает информацию от холодовых, другая от тепловых периферических рецепторов и терморецепторных нейронов. Третий тип нейронов – эфферентные. Они находятся в заднем гипоталамусе и обеспечивают регуляцию механизмов теплообразования.
Свои влияния на исполнительные механизмы, центр терморегуляции осуществляет через симпатическую и соматическую нервную системы, железы внутренней секреции. При повышении температуры тела возбуждаются периферические тепловые рецепторы и терморецепторные нейроны. Импульсы от них поступают к интернейронам, а затем к эффекторным. Эффекторными являются нейроны симпатических центров гипоталамуса. В результате их возбуждения активируются симпатические нервы, которые расширяют сосуды кожи и стимулируют потоотделение. При возбуждении холодовых рецепторов наблюдается обратная картина. Частота нервных импульсов идущих к кожным сосудам и потовым железам уменьшается, сосуды суживаются, потоотделение тормозится. Одновременно расширяются сосуды внутренних органов. Если это не приводит к восстановлению температурного гомеостаза, включаются другие механизмы. Во-первых, симпатические нервная система усиливает процессы катаболизма, а следовательно теплопродукцию. Выделяющийся из окончаний симпатических нервов норадреналин стимулирует процессы липолиза. Особую роль в этом играет бурый жир. Это явление называется не дрожательным термогенезом. Во-вторых, от нейронов заднего гипоталамуса начинают идти нервные импульсы к двигательным центрам среднего и продолговатого мозга. Они возбуждаются и активируют a-мотонейроны спинного мозга. Возникает непроизвольная мышечная активность в виде холодовой дрожи. Третий путь – это усиление произвольной двигательной активности. Большое значение имеет соответствующее изменение поведения, которое обеспечивается корой. Из гуморальных факторов наибольшее значение имеют адреналин, норадреналин и тиреоидные гормоны. Первые два гормона вызывают кратковременное повышение теплопродукции за счет усиления липолиза и гликолиза. При адаптации к длительному охлаждению усиливается синтез тироксина и трийодтиронина. Они значительно повышают энергетический обмен и теплопродукцию посредством увеличения количества ферментов в митохондриях.
Понижение температуры тела называется гипотермией, повышение гипертермией. Гипотермия возникает при переохлаждении. Гипотермия организма или мозга используется в клинике для продления жизнеспособности организма или мозга человека при проведении реанимационных мероприятий. Гипертермия возникает при тепловом ударе, когда температура повышается до 40-41о. Одним из нарушений механизмов терморегуляции является лихорадка. Она развивается в результате усиления теплообразования и снижения теплоотдачи. Теплоотдача падает из-за сужения периферических сосудов и уменьшения потоотделения. Теплообразование возрастает вследствие воздействия на центр терморегуляции гипоталамуса бактериального и лейкоцитарного пирогенов, являющихся липополисахаридами. Это воздействие сопровождается и лихорадочной дрожью. В период выздоровления нормальная температура восстанавливается за счет расширения сосудов кожи и проливного пота.
Гормоны гипофиза. Их значение для роста, жизнедеятельности организма и при стрессовых ситуациях.
Питуитарная железа, называемая также гипофизом, — это мелкая железа около 1 см в диаметре и массой от 0,5 до 1 г, которая лежит в турецком седле (костном образовании основания черепа) и связана с гипоталамусом посредством питуитарного, или гипофизарного, стебля. Физиологически питуитарная железа подразделяется на две независимые части: переднюю долю гипофиза, или аденогипофиз, и заднюю долю гипофиза, или нейрогипофиз. Между ними есть промежуточная доля, относительно плохо васкуляризированная, практически не выраженная у человека и более заметная как структурно, так и функционально у низкоорганизованных организмов.
В эмбриогенезе эти две доли гипофиза развиваются из разных источников: передняя доля — из кармана Ратке, который эмбриологически является инвагинацией фарингеального эпителия, а задняя доля — из нервной ткани, являющейся выростом гипоталамуса. Происхождением передней доли гипофиза из фарингеального эпителия объясняется эпителиоидная структура ее клеток, а наличие глиального типа клеток в задней доле гипофиза — его нейрогенной природой. Передним гипофизом продуцируются 6 важных гормонов-пептидов и несколько менее существенных, в заднем гипофизе содержатся 2 гормона-пептида. Гормоны аденогипофиза играют важную роль в контроле метаболических функций организма: • гормон роста обеспечивает рост организма, увеличение количества клеток и их дифференцировку, стимулируя образование белков; • адренокортикотропный гормон (кортикотропин) управляет секрецией некоторых гормонов коры надпочечников, которые, в свою очередь, влияют на метаболизм глюкозы, белков и жиров; • тиреотропный гормон (тиреотропин, ТТГ) контролирует скорость секреции тироксина и трийодтиронина щитовидной железой. В свою очередь, они регулируют в организме скорость основных химических реакций; • пролактин обеспечивает развитие молочных желез и продукцию молока;
• два самостоятельных гонадотропных гормона — фолликулостимулирующий и лютеинизирующий — контролируют рост яичников и семенников, их гормональную и репродуктивную активность. Роль гормонов заднего гипофиза иная: • антидиуретический гормон (также называемый вазопрессином) контролирует скорость экскреции воды с мочой, помогая регулировать количество воды в организме; • окситоцин стимулирует роды и способствует молокоотделению из молочных желез во время кормления ребенка.
Передняя доля гипофиза содержит много различных типов клеток, синтезирующих и высвобождающих гормоны. Для синтеза определенного типа гормонов в аденогипофизе существует определенный тип клеток. С помощью специальных красителей, реагирующих с комплексом антиген-антитело, где антигеном является определенный гормон, смогли выделить пять разных типов клеток. 1. Соматотропы — гормон роста человека. 2. Кортикотропы — адренокортикотропин. 3. Тиреотропы — тиреотропный гормон. 4. Гонадотропы — гонадотропные гормоны, включая лютеинизирующий гормон, фолликулостимулирующий гормон. 5. Лактотропы — пролактин.
Гормоны щитовидной железы. Их значение для роста и развития организма.
Щитовидная железа, расположенная сразу ниже гортани, кпереди и но обе стороны от трахеи, является одной из наиболее крупных эндокринных желез (ее масса — от 15 до 20 г у взрослых в норме). Щитовидная железа секретирует два важных гормона: тирозин и трийодтиронин, обычно обозначаемых соответственно как Т3 и Т4. Оба эти гормона резко увеличивают скорость обменных процессов в организме. Полное отсутствие секреции щитовидных желез снижает основной обмен на 40-50% относительно нор мы, а чрезвычайно высокий уровень активности железы может повышать его на 60-100%. Секреция щитовидных желез регулируется главным образом тирсотропным гормоном, продуцируемым передней долей гипофиза. Щитовидные железы синтезируют также кальцитонин — важный гормон, регулирующий обмен кальция.
Цель статей нашего сайта — рассмотрение образования и секреции гормонов щитовидной железы и их метаболических функций, а также регуляции функций щитовидной железы.
Почти 93% активности гормонов щитовидной железы, влияющих на обменные процессы, обусловлены тироксином и лишь 7% — трийод-тиронином. Однако почти весь тироксин в тканях в итоге превращается в трийодтиронин, поэтому оба эти гормона функционально важны. Эффекты действия этих гормонов практически одинаковы, но различаются по скорости и интенсивности. Трийодтиронин почти в 4 раза активнее тироксина, но присутствует в крови в гораздо меньшем количестве, и время его пребывания в крови заметно короче, чем тироксина.
Для образования нормального количества тироксина необходимо поступление в организм почти 50 мг йода в виде йодидов в течение года, или около 1 мг в неделю. Для предотвращения дефицита йода обычная столовая соль йодируется: к каждым 100000 частям хлорида натрия добавляют 1 часть йоди-да натрия.
Потребление с пищей йодидов. Йодиды, попавшие с пищей в желудочно-кишечный тракт, всасываются в кровь точно так же, как хлориды. Большинство йодидов в норме быстро экскретируются почками, и лишь менее 1/5 избирательно извлекаются из циркулирующей крови клетками щитовидной железы и используются для синтеза тиреоидных гормонов.
Первой стадией образования гормонов щитовидной железы, является транспорт йодидов из крови в клетки и фолликулы щитовидной железы. Базальная мембрана клеток щитовидной железы обладает специфической способностью активно закачивать йодиды внутрь клеток. Этот процесс называют йодной «ловушкой». В норме концентрация йода в щитовидной железе в 30 раз выше, чем в крови, а при максимальной активности железы концентрация йода увеличивается в 250 раз по сравнению с концентрацией в крови. Скорость захвата йода щитовидной железой зависит от ряда факторов, наиболее важным из которых является концентрация тиреотропного гормона; ТТГ стимулирует, а гипофизэктомия резко снижает активность йодного насоса.
Гормоны мозгового и коркового слоя надпочечников. Их роль при мышечной деятельности и в повышении устойчивости к неблагоприятным воздействиям.
Мозговой слой надпочечников состоит из хромафинной ткани, в которой есть два вида клеток: те, которые образуют адреналин, и те, которые образуют норадреналин. Мозговое вещество вместе с симпатичными ганглиями, в которых также содержатся хромаффинными клетки, относится к так называемой адреналовой системы. Надпочечники интенсивно снабжаются кровью. Иннервация их осуществляется главным образом за счет ветвей брюшного сплетения и ветвей великого брюшного нерва. Кроме того, надпочечники еще получают ветку от нижнего диафрагмального сплетения, Вопрос о иннервацию надпочечников ветвями блуждающего нерва еще не решен. Корковый и мозговой слои надпочечников имеют разное происхождение их можно рассматривать как две самостоятельные железы внутренней секреции, вырабатывающих различные гормоны и выполняют разные функции. Гормоны коры надпочечников. Из коры надпочечников выделено более 40 кортикостероидов. Физиологически активными является только 8 из них. ГКС делят на три группы: 1) глюкокортикоиды (гидрокортизон, кортизон и кортикостерон) 2) минералокортикоиды (альдостерон, дезоксикортикостерон) 3) половые гормоны (андрогены, эстрогены, прогестерон). Считают, что настоящими гормонами являются кортикостерон и гидрокортизон, которые определяют все функции этих желез. Остальные вещества е продуктами обмена гормонов. Глюкокортикоиды образуются в клетках пучковой зоны коры надпочечников, минералокортикоиды - в клубочковой зоне, половые гормоны - в сетчатой. По составу гормоны надпочечников е стероидами. Процесс их образования начинается от холестерина. Для их биосинтеза требуется также аскорбиновая кислота. Глюкокортикоиды влияют на обмен углеводов, белков и жиров, усиливают процессы образования глюкозы из белков (глюконеогенез), а также откладывание гликогена в печени, являются антагонистами инсулина по регуляции углеводного обмена. ГКС вызывают распад тканевых белков, задерживают включения аминокислот в белки организма и ускоряют процесс выделения азота (катаболический эффект). Глюкокортикоиды способны проявлять противовоспалительное действие. Это связано с тем, что названные гормоны снижают проницаемость стенки сосудов за счет снижения активности фермента гиалуронидазы, блокируют секрецию серотонина и гистамина, кининов и систему плазмин - фибринолизин. Под влиянием глюкокортикоидов производятся липокортины, тормозящие влияние фосфолипазы А2 и тем самым подавляют образование из арахидоновой кислоты простагландинов и лейкотриенов, стимулирующих воспалительный процесс. Противовоспалительное действие глюкокортикоидов используется в клинической практике, например, для лечения больных с ревматическими процессами. ГКС осуществляют значительное влияние на клеточный и гуморальный иммунитет. Доказано, что выше (фармакологические) дозы гидрокортизона обусловливают обратное развитие (инволюцию) пидгрудиннои железы и лимфатических узлов, подавляют выработку антител, тормозящие реакцию взаимодействия чужеродного белка (антигена) с антителом. При этом в периферической крови уменьшается количество лимфоцитов и эозинофилов. Именно иммуносупрессорной действие глюкокортикоидов используется для лечения аллергических заболеваний (например, бронхиальной астмы). ГКС с другими гормонами (АКТГ) способствуют адаптации организма к новым условиям существования, а также к воздействию различных неблагоприятных факторов (резко выраженные холод и сп? Ка, кислородное голодание, травмы, эмоциональное перенапряжение и т.д.). Поэтому их называют защитными (адаптивными) гормонами. Минералокортикоиды участвуют в регуляции минерального обмена (баланса электролитов). Активным минералокортикоиды является альдостерон. Под его влиянием усиливается реабсорбция Na + в канальцах почек и уменьшается реабсорбция К +, что приводит к задержке Na + и Сl-в организме и увеличение выделения К +, Н +. В отличие от глюкокортикоидов, минералокортикоидов способствуют развитию воспалительных процессов. Это объясняется их способностью к повышению проницаемости капилляров и серозных оболочек. Минералокортикоиды участвуют также в регуляции тонуса кровеносных сосудов. Доказано, что альдостерон повышает тонус сосудов и способствует повышению артериального давления. Избыток альдостерона в организме ведет к повышению содержания натрия и снижение уровня калия, к развитию алкалоза и увеличение объема внеклеточной жидкости. Напротив, недостаточность альдостерона в организме обусловливает потерю натрия, дегидратацию тканей и снижение АД (гипотензия). Влияние половых гормонов надпочечников. Эти гормоны имеют значение для развития половых органов в раннем детском возрасте и появления вторичных половых признаков в тот период, когда внутрищньосекреторна функция половых желез еще незначительна. Кроме специфического воздействия, половые гормоны (эстрогены) оказывают еще и антисклеротическое эффект, прежде у женщин, благодаря высокой их концентрации. Они (особенно андрогены) также способствуют обмену белков, стимулируя их синтез в организме. Вместе с этим половые гормоны влияют на эмоциональный статус и поведение человека.
Гормоны поджелудочной железы. Их значение в углеводном и жировом обмене.
непосредственно в кровь и доставляется к органам-мишеням.
Основными гормонами поджелудочной железы являются следующие соединения:
Инсулин
Глюкагон
С-пептид
За синтез инсулина отвечают бета-клетки островков Лангерганса, его основная функция в организме состоит в понижении уровня сахара в крови. Это достигается с помощью одновременного действия по трем направлениям. Инсулин приостанавливает образование глюкозы в печени и повышает количество сахара, который усваивается тканями организма за счет увеличения проницаемости клеточных мембран. В то же время он тормозит распад глюкагона, ведь тот является полимерной цепочкой, состоящей из молекул глюкозы, и может быть использован для увеличения ее концентрации в крови. Под действием ряда факторов в организме возникает недостаток инсулина, ведущий к развитию сахарного диабета.
Выработкой глюкагона занимаются альфа-клетки островков Лангерганса, он отвечает за увеличение концентрации глюкозы в кровяном русле. Это достигается путем стимулирования ее образования в печени. Кроме того, он способствует расщепление липидов в жировой ткани. Таким образом, два описанных выше гормона поджелудочной железы выполняют противоположные функции. Однако в поддержании нормального уровня сахара в крови участвуют и другие биологически активные соединения, вырабатываемые эндокринной системой — соматотропин (гормон роста), кортизол, адреналин.
В диагностике таких заболеваний, как сахарный диабет, ожирение, акромегалия и различные патологии печени, используют анализ крови на инсулин. С-пептид, строго говоря, не является гормоном поджелудочной железы. Он представляет собой часть молекулы проинсулина, которая отделяется от нее в процессе синтеза и оказывается в кровяном русле. Поэтому количество С-пептида в сыворотке крови эквивалентно количеству инсулина, которое секретируется поджелудочной железой. Этот показатель более точен, ведь белковый фрагмент не обладает биологической активностью и не вступает в химические реакции.
В настоящее время его используют в диагностике сахарного диабета I и II типа, опухоли поджелудочной железы и заболеваний печени. Повышенное содержание С-пептида свидетельствует о наличии в организме инсулиномы. Если оно сохраняется после прохождения курса лечения, то велика вероятность развития метастазов или рецидивов заболевания. С-пептид позволяет определять уровень инсулина у больных сахарным диабетом, получающих лечение, и соответственно корректировать характер терапевтических мероприятий. Кроме того, он помогает отслеживать состояние плода у женщин, страдающих диабетом беременных
Электрические процессы в мышце в состоянии покоя и при возбуждении. Методы регистрации электрических потенциалов мышц. Электромиограмма.
Нервно-мышечные синапсы. Механизмы проведения возбуждения через синапсы.
Нервно-мышечные синапсы обеспечивают проведение возбуждения с нервного волокна на мышечное благодаря медиатору ацетилхолину, который при возбуждении нервного окончания переходит в синаптическую щель и действует на концевую пластинку мышечного волокна. Следовательно, как и межнейронный синапс, нервно-мышечный синапс имеет пресинаптическую часть, принадлежащую нервному окончанию, синаптическую щель, постсинаптическую часть (концевая пластинка), принадлежащую мышечному волокну.
В пресинаптической терминали образуется и скапливается в виде пузырьков ацетилхолин. При возбуждении электрическим импульсом, идущим по аксону, пресинаптической части синапса ее мембрана становится проницаемой для ацетилхолина.
Эта проницаемость возможна благодаря тому, что в результате деполяризации пресинаптической мембраны открываются ее кальциевые каналы. Ион Са2+ входит в пресинаптическую часть синапса из синаптической щели. Ацетилхолин высвобождается и проникает в синаптическую щель. Здесь он взаимодействует со своими рецепторами постсинаптической мембраны, принадлежащей мышечному волокну. Рецепторы, возбуждаясь, открывают белковый канал, встроенный в липидный слой мембраны. Через открытый канал внутрь мышечной клетки проникают ионы Na+, что приводит к деполяризации мембраны мышечной клетки, в результате развивается так называемый потенциал концевой пластинки (ПКП). Он вызывает генерацию потенциала действия мышечного волокна.
Нервно-мышечный синапс передает возбуждение в одном направлении: от нервного окончания к постсинаптической мембране мышечного волокна, что обусловлено наличием химического звена в механизме нервно-мышечной передачи.
Скорость проведения возбуждения через синапс намного меньше, чем по нервному волокну, так как здесь тратится время на активацию пресинаптической мембраны, переход через нее кальция, выделение ацетилхолина в синаптическую щель, деполяризацию постсинаптической мембраны, развитие ПКП.
Синаптическая передача возбуждения имеет рад свойств:
1) наличие медиатора в пресинаптической части синапса;
2) относительная медиаторная специфичность синапса, т. е. каждый синапс имеет свой доминирующий медиатор;
3) переход постсинаптической мембраны под влиянием медиаторов в состояние де- или гиперполяризации;
4) возможность действия специфических блокирующих агентов на рецептирующие структуры постсинаптической мембраны;
5) увеличение длительности постсинаптического потенциала мембраны при подавлении действия ферментов, разрушающих синаптической медиатор;
6) развитие в постсинаптической мембране ПСП из миниатюрных потенциалов, обусловленных квантами медиатора;
7) зависимость длительности активной фазы действия медиатора в синапсе от свойств медиатора;
8) односторонность проведения возбуждения;
9) наличие хемочувствительных рецепторуправляемых каналов постсинаптической мембраны;
10) увеличение выделения квантов медиатора в синаптическую щель пропорционально частоте приходящих по аксону импульсов;
11) зависимость увеличения эффективности синаптической передачи от частоты использования синапса («эффект тренировки»);
12) утомляемость синапса, развивающаяся в результате длительного высокочастотного его стимулирования. В этом случае утомление может быть обусловлено истощением и несвоевременным синтезом медиатора в пресинаптической части синапса или глубокой, стойкой деполяризацией постсинаптической мембраны (пессимальное торможение).
Механизмы мышечного сокращения. Одиночное и тетапическое сокращение мышечных волокон. Сокращение целой мышцы.
Одиночное сокращение можно вызвать только искусственно в лаборатории на нервно-мышечном препарате. Оно возникает в ответ на одно кратковременное раздражение (один импульс). На миограмме одиночного мышечного сокращения (рис. 51, А) различают три периода. Мышца начинает сокращаться всегда через некоторое время после раздражения. Первый период - между приложением раздражителя и началом сокращения мышцы - называют периодом скрытого возбуждения, или латентным периодом. Для мышц человека он измеряется тысячными долями секунды. Затем следует второй период - период сокращения, или укорочения мышцы, и за ним третий - период расслабления мышцы.
будима (рефрактерная фаза), в периоде сокращения возбудимость мышцы постепенно возрастает и достигает уровня более высокого, чем в состоянии покоя (фаза экзальтации), вслед за этим, в период расслабления, возбудимость мышцы падает. К периоду покоя возбудимость мышцы возвращается к исходному уровню.
В целом организме имеют место не одиночные, а длительные, или тетанические, сокращения скелетных мышц (тетанус). Тетанические сокращения являются результатом того, что в организме раздражения к мышцам из центральной нервной системы по нервам поступают не в виде однократных импульсов, а одно за другим. Форма длительного (тетанического) сокращения зависит от частоты импульсов. Если частота импульсов меньше продолжительности одиночного сокращения (0,1 секунды), то возникает серия одиночных мышечных сокращений (рис. 51, Б, I). Если частота будет больше и следующий импульс будет поступать в момент расслабления мышцы, сокращение приобретет форму зубчатого тетануса (рис. 51, II и III). При дальнейшем возрастании частоты импульсов они будут поступать в мышцу в фазу экзальтации. При этом возникает гладкий тетанус, характеризующийся непрерывными сокращениями (рис. 51, Б, IV). Частота импульсов столь велика, что новое возбуждение в мышце возникает раньше, чем закончилось предыдущее сокращение.
Работа мышцы, значение темпа движений и величины поднимаемого груза. Закон средних нагрузок. Коэффициент полезного действия мышц.
|
Закон средних нагрузок: работа мышц будет наибольшей при
средних нагрузках.
Закон средних скоростей: максимальная работа мышцы будет
наибольшей при среднем ритме (скорости) сокращения.
Формула для расчета коэффициента полезного действия
мышечной деятельности. Коэффициент полезного действия
мышцы (КПД) – отношение количества работы, совершенной
мышцей при одиночном сокращении, к общему количеству
выделенной при этом энергии:
58
K =Q
H
где К – коэффициент полезного действия мышцы, %,
Q – количество энергии, выделенной при работе, ккал,
Н – общий расход энергии при выполнении работы, ккал.
Нормативный показатель:
КПД человека = 20-25 %.
Изотонический, изометрический и ауксотонический режимы мышечной активности.
Основные режимы сокращения мышцы
1. Изометрический режим - режим сокращения мышцы, при которой длина мышцы остается постоянной в течение всего цикла сокращения. Изометрическое мышечное сокращение, сокращение мышцы, выражающееся в усилении её напряжения при неизменной длине (например, сокращение мышцы конечности, оба конца которой закреплены неподвижно). В организме к Изометрическому мышечному сокращению приближается напряжение, развиваемое мышцей при попытке поднять непосильный груз.
На Рис. 1 показана траектория развития напряжения мышцы в изометрическом режиме сокращения.
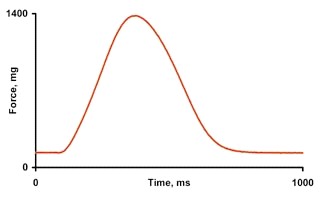
Рис. 1. Траектория развития силы мышцы в изометрическом режиме сокращения.
2. Режим ненагруженного укорочения - режим сокращения мышцы под нулевой (субнулевой) внешней нагрузкой. В этом случае активное напряжение мышцы равно 0 в течение всего цикла сокращения. Соответственно, в этом режиме мышца укорачивается до минимально возможной длины.
3. Изотонический режим - режим сокращения мышцы под постоянной ненулевой внешней нагрузкой. На Рис. 2. показаны траектории развития напряжения и укорочения мышцы в изотоническом режиме сокращения. В этом режиме можно выделить 4 фазы: фазу изометрического развития напряжения (А), фазу изотонического укорочения (Б), фазу изотонического расслабления (В) и фазу изометрического расслабления (Г).
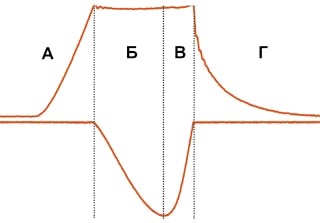
Рис. 2. Траектории развития силы и укорочения мышцы в изотоническом режиме сокращения.
4. Физиологический режим - режим сокращения мышцы под постоянной внешней нагрузкой, как и в случае изотонического режима. Отличие от предыдущего режима состоит в том, что как только мышца достигает конечно-систолической длины, ее длина искусственно фиксируется, и расслабление мышцы происходит уже при новой длине .
5.Ауксотонический режим - режим сокращения мышцы под переменной внешней нагрузкой. Типичный пример траектории развития силы мышцы в ауксотоническом режиме показан на Рис. 4. Забегая вперед скажем, что при сокращении мышцы в дуплете (см. ниже), она функционирует именно под переменной внешней нагрузкой, т.е. сокращается ауксотонически.
Реально ни изометрических, ни изотонических условий сокращения мышцы в чистом виде не существует. В естественных условиях сокращение осуществляется в ауксотонических условиях, когда в полной мере не фиксированы ни длина мышцы, ни сила ее сокращения.
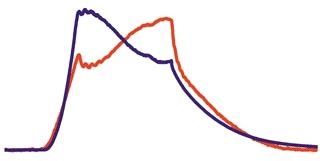
Рис. 4. Траектории развития силы реальной и виртуальной мышц в дуплете (ауксотонический режим сокращения).
Нервная клетка и ее функции, разновидности нервных клеток (афферентные, эфферентные, вставочные). Рефлекс, рефлекторная дуга, обратные связи.
Чувствительные, или афферентные, нервные приводящие волокна несут возбуждение в Ц. н. с. от периферических рецепторов; по отводящим эфферентным (двигательным и вегетативным) нервным волокнам возбуждение из Ц. н. с. направляется к клеткам исполнительных рабочих аппаратов (мышцы, железы, сосуды и т.д.). Во всех отделах Ц. н. с. имеются афферентные нейроны, воспринимающие приходящие с периферии раздражения, и эфферентные нейроны, посылающие нервные импульсы на периферию к различным исполнительным эффекторным органам. Афферентные и эфферентные клетки своими отростками могут контактировать между собой и составлять двухнейронную рефлекторную дугу (См. Рефлекторная дуга), осуществляющую элементарные рефлексы (например, сухожильные рефлексы спинного мозга). Но, как правило, в рефлекторной дуге между афферентными и эфферентными нейронами расположены вставочные нервные клетки, или интернейроны (рис. 1). Связь между различными отделами Ц. н. с. осуществляется также с помощью множества отростков афферентных, эфферентных и вставочных нейронов этих отделов, образующих внутрицентральные короткие и длинные проводящие пути. В состав Ц. н. с. входят также клетки нейроглии (См. Нейроглия), которые выполняют в ней опорную функцию, а также участвуют в метаболизме нервных клеток.
Рефлекторный принцип работы Ц. н. с., как основной принцип её деятельности, до 19 в. был экспериментально установлен и изучен только в отношении деятельности отделов, расположенных ниже уровня больших полушарий головного мозга. Были выявлены общие закономерности и приспособительный характер рефлекторной деятельности Ц. н. с., а также специфические, частные особенности функций её различных отделов. В 19 в. И. М.Сеченовым и некоторыми др. прогрессивными учёными была высказана смелая идея о рефлекторной природе деятельности также и высших отделов Ц. н. с., в том числе и психической деятельности. Эта передовая, материалистическая идея послужила основой для классических экспериментальных и теоретических исследований И. П. Павлова, приведших к созданию им учения о высшей нервной деятельности (См. Высшая нервная деятельность). Павлов установил, что рефлексы, осуществляемые у высокоразвитых организмов корой больших полушарий головного мозга, в отличие от рефлексов всех нижележащих отделов Ц. н. с., не врождённые, а формируются в течение индивидуальной жизни организма в процессе его взаимодействия с окружающей средой и обеспечивают его наиболее совершенное приспособление к условиям существования. Этот новый класс рефлексов, в отличие от врождённых, или безусловных рефлексов (См. Безусловные рефлексы), Павлов назвал условными рефлексами (См. Условные рефлексы).
Pефлекс (от лат. "рефлексус" - отражение) - реакция организма на изменения внешней или внутренней среды, осуществляемая при посредстве центральной нервной системы в ответ на раздражение рецепторов.
Рефлексы проявляются в возникновении или прекращении какой-либо деятельности организма: в сокращении или расслаблении мышц, в секреции или прекращении секреции желез, в сужении или расширении сосудов и т. п.
Благодаря рефлекторной деятельности организм способен быстро реагировать на различные изменения внешней среды или своего внутреннего состояния и приспособляться к этим изменениям. У позвоночных животных значение рефлекторной функции центральной нервной системы настолько велико, что даже частичное выпадение ее (при оперативном удалении отдельных участков нервной системы или при заболеваниях ее) часто ведет к глубокой инвалидности и невозможности осуществлять необходимые жизненные функции без постоянного тщательного ухода.
Значение рефлекторной деятельности центральной нервной системы в полной мере было раскрыто классическими трудами И. М. Сеченова и И. П. Павлова. И. М. Сеченов еще в 1862 г. в своем составившем эпоху труде "Рефлексы головного мозга" утверждал: "Все акты сознательной и бессознательной жизни по способу происхождения суть рефлексы".
Виды рефлексов
Все рефлекторные акты целостного организма разделяют на безусловные и условные рефлексы.
Безусловные рефлексы передаются по наследству, они присущи каждому биологическому виду; их дуги формируются к моменту рождения и в норме сохраняются в течение всей жизни. Однако они могут изменяться под влиянием болезни.
Условные рефлексы возникают при индивидуальном развитии и накоплении новых навыков. Выработка новых временных связей зависит от изменяющихся условий среды. Условные рефлексы формируются на основе безусловных и с участием высших отделов головного мозга.
Безусловные и условные рефлексы можно классифицировать на различные группы по ряду признаков.
