
- •Классификация аминокислот.
- •4. Простые и сложные белки, их классификация. Характер связей простетических групп с белком. Биологические функции белков. Способность к специфическим взаимодействиям с лигандом.
- •5. Углеводсодержащие белки: гликопротеины, протеогликаны. Основные углеводы организма человека: моносахариды, дисахариды, гликоген, гетерополисахариды, их структура и функции.
- •8. Хромопротеины, их классификация. Флавопротеины, их структура и функции. Гемопротеины, структура, представители: гемоглобин, миоглобин, каталаза, пероксидаза, цитохромы. Функции гемопротеинов.
- •13. Энзимопатия у детей и важность их биохимической диагностики (на примере нарушения азотистого и углеводного обмена).
- •14. Витамины, классификация витаминов (по растворимость и функциональная). История открытия и изучения витаминов.
- •15. Витамин а, структура, участие в обменных процессах. Гипо- гипер- и авитаминоз а, их причины и особенности проявления. Пищевые источники, суточная потребность.
- •17. Витамин рр, структура коферментов, участие в обменных процессах. Гипо - и авитаминоз рр. Пищевые источники, суточная потребность.
- •18. Витамин в2, структура коферментов, участие в обменных процессах. Гиповитаминоз и авитаминоз в2. Суточная потребность, пищевые источники.
- •19. Витамин с, структура, участие в обменных процессах. Гипо- и авитаминоз с. Пищевые источники, суточная потребность.
- •20. Витамин в1, структура кофермента, участие в обменных процессах. Гиповитаминоз и авитаминоз в1. Пищевые источники, суточная потребность.
- •21. Витамин в6, структура кофермента, участие в обменных процессах. Гиповитаминоз и авитаминоз в6. Пищевые источники, суточная потребность.
- •22. Пантотеновая кислота и биотин, их участие в обменных процессах. Гиповитаминозы и авитаминозы в3 и н. Суточная потребность, источник этих витаминов.
- •23. Фолиевая кислота и кобаламин, их участие в обменных процессах, авитаминозы. Пищевые источники, суточная потребность.
- •24. Витамин е и к, участие их в обменных процессах. Гиповитаминозы и авитаминозы этих витаминов. Пищевые источники, суточная потребность.
- •25. Возрастные потребности в отдельных витаминах у ребенка. Особенности проявления гипо- и авитаминозов в раннем детском возрасте.
- •27. Гормоны гипоталамуса – либерины и статины. Химическая природа. Механизм их действия на молекулярном уровне, биологический эффект.
- •29. Гормоны задней доли гипофиза: вазопрессин, окситоцин. Химическая природа. Механизм их действия, биологический эффект. Нарушения функций организма, связанные с недостатком выработки этих гормонов.
- •32. Паратгормон и кальцитонин. Химическая природа. Механизм действия на молекулярном уровне. Влияние на обмен кальция, гиперкальциемия и гипокальциемия.
- •35. Половые гормоны: андрогены, эстрогены. Химическая природа. Механизм действия на молекулярном уровне, влияние на обмен веществ. Нарушения обмена при недостатке и избытке этих гормонов в организме.
- •45. Свободно-радикальное окисление. Токсичность кислорода: образование активных форм кислорода, их действие на липиды и другие вещества клетки. Механизм защиты: антиоксидантные системы
- •Регуляция глюконеогенеза происходит с участием гормонов и с участием метаболитов.
- •60. Лабильность уровня глюкозы в крови у детей раннего возраста. Наклонность к гипогликемии. Своеобразие учета результатов нагрузной пробой сахара у детей.
- •62. Особенности переваривания и всасывания жиров в организме ребенка.
- •72. Повышенная активность биосинтеза и распада нейтральных жиров в тканях ребенка. Бурый жир, его значение.
- •73. Неустойчивость липидного обмена, связанная с недостаточно сформированной нейроэндокринной регуляцией. Кетонемия и ацетонемия у детей. Факторы, способствующие их развитию.
- •Гормональная регуляция синтеза и мобилизации жиров.
- •75. Патология обмена холестерина у детей. Наследственные нарушения липидного обмена: семейная гиперхолестеринемия и семейная триглицеридемия.
- •76. Обмен аминокислот и белков в питании ребенка. Понятие об азотистом балансе. Физиологическая азотемия новорожденных.
- •79. Замедленное переваривание белков в желудке у детей. Особенности исследования функции желудка в детском возрасте.
- •84. Обмен фенилаланина и тирозина. Образование катехоламинов, гормонов щитовидной железы, меланина. Нарушения процессов распада тирозина: фенилкетонурия, алкаптонурия, альбинизм.
- •85. Лабильность дезаминирования в гепатоцитах ребенка. Повышенная концентрация аминокислот в крови и моче ребенка раннего возраста. Своеобразие обмена некоторых аминокислот. Фенилаланин, тирозин.
- •88. Пути обезвреживания аммиака в организме ребенка. Преобладание у детей раннего возраста урикотелического пути обмена аммиака. Причины нарастания аммиака крови.
- •89. Биосинтез пиримидиновых нуклеотидов, этапы этого процесса. Оротацидурия. Распад пиримидиновых нуклеотидов. Биосинтез дезоксирибонуклеотидов. Участие утф и цтф в обменных процессах.
- •91. Обмен нуклеиновых кислот и нуклеотидов у ребенка. Генетические нарушения, связанные с наследственными заболеваниями.
- •92. Биосинтез днк (репликация): стехиометрия реакций, днк-полимераза, матрица. Повреждение и распад днк.
- •Этапы биосинтеза днк.
- •93. Биосинтез рнк (транскрипция): рнк-полимераза, стехиометрия реакции, днк как матрица. Регуляция транскрипции. Посттранскрипционная достройка рнк. Молекулярные мутации. Наследственные болезни.
- •96. Распад гема. Билирубин как продукт распада гема. Метаболизм билирубина. Нарушение его обмена. Желтухи и их биологическая диагностика.
- •97. Физиологическая желтуха новорожденных, ее причины.
- •98. Обмен гемоглобина у детей. Типы и виды гемоглобина. Его возрастная эволюция. Возрастные особенности 2,3-дфг эритроцита. Гемоглобинопатии.
- •101.Возрастные колебания общего белка крови и его фракции. Наличие фетальных белков в крови. Иммуноглобулины. Неспецифические факторы защиты.
- •103.Возрастные особенности содержание и распределения воды в организме ребенка. Лябильность водного обмена. Физиологическая потеря жидкости новорожденными.
- •106.Важность минеральных солей для обменных процессов у детей (пластическая и регуляторная роль). Значение прикорма ребенка для уменьшения дефицита минеральных солей.
- •110. Мукополисахаридоз у детей – наследственная лизосомальная болезнь накопления.
- •113.Роль креатинфосфата в мышечном сокращении у ребенка. Физиологическая креатинурия. Врожденные энзимопатии (фосфорилаза и фосфоглюкомутаза), приводящие к патологии мышечной системы.
- •114.Биохимия мышечной ткани у детей.
- •118.Своеобразие химического состава и метаболических процессов мозга плода и у ребенка раннего возраста.
- •120.Важность определения функционального состояния печени в детском возрасте.
- •121.Возрастные особенности процессов гниения в желудочно-кишечном тракте ребенка.
- •123.Характеристика периода новорожденности и его биохимические аспекты. Биохимические сдвиги новорожденного впервые часы постнатального периода.
- •124.Своеобразие метаболизма ребенка и его регуляция в различные возрастные периоды. Биохимические критерии, характеризующие отдельные возрастные этапы.
- •126.Особенности обмена веществ у ребенка раннего возраста. Несовершенство высших форм регуляции. Своеобразие гормональной регуляции.
- •127.Изменения ферментативных систем в ходе индивидуального развития организма как проявление биохимической адаптации. Срочная и замедленная адаптация.
45. Свободно-радикальное окисление. Токсичность кислорода: образование активных форм кислорода, их действие на липиды и другие вещества клетки. Механизм защиты: антиоксидантные системы
Свободнорадикальное окисление – важный и многогранный биохимический процесс превращений кислорода, липидов, нуклеиновых кислот, белков и других соединений под действием свободных радикалов, а перекисное окисление липидов (ПОЛ) – одно из его последствий. Свободные радикалами (СР) представляют собой соединения, имеющие неспаренный электрон на наружной орбите и обладающие высокой реакционной способностью. К числу первичных СР относятся супероксидный анион-радикал, окись азота, а вторичными СР являются гидроксильный радикал, синклетный кислород, перекись водорода, пероксинитрит. Образование СР тесно связано, с одной стороны, с появлением свободных электронов при нарушениях процессов окисления в дыхательной цепи, превращении ксантина, синтезе лейкотриенов и простогландинов. Эти реакции зависят от активности ксантиноксидазы, дегидроротатдегидрогеназы, льдегидоксидазы, холестериноксидазы, ферментов цитохрома Р-450. Синтез супероксид — аниона инициируется ангиотензином II, который образуется из ангиотензина I под действием ангиотензинпревращающего фермента. Его активность в сосудах больных с выраженным атеросклерозом особенно высока. Причина этого явления пока неясна. Оксид азота образуется при окисленииL-аргинина под действием NO-синтетазы при участии кальмодулина. В литературе представлены данные о том, что синтез NO при атеросклерозе не нарушен, но его дефицит может возникать при увеличении его соединения с супероксид – анионом. Оно завершается синтезом пероксинитрита с большими патогенными потенциями, в том числе и образованием окисленных форм ЛПНП. С другой стороны, для синтеза вторичных СР используется водород НАДФ-Н, НАД-Н — его донаторов. Супероксид — анион может восстанавливать Fe3+ в Fe2+, при взаимодействии которого с перекисью водорода, перекисями липидов и гипохлоритом образуются высокотоксичные вторичные радикалы. Из всех СР наибольшей активностью обладают гидроксильный радикал и пероксинитрит. Активность СР ограничивается антиоксидантами, которые разрывают цепи молекул при реакциях СРО, разрушают молекулы перекисей. К числу ферментных антиоксидантов относятся супероксиддисмутаза (СОД), глютатионпероксидаза, каталаза, находящиеся в клеточных структурах. Неферментные антиоксиданты – витамины Е, К, С, убихиноны, триптофан, фенилаланин, церулоплазмин, трансферрин, гаптоглобин, глюкоза, каротиноиды – блокируют активность СР в крови.
46. Микросомальное окисление. Структурные компоненты и функции оксидаз, монооксигеназ и диоксигеназ. Значение микросомального окисления для организма: обезвреживание природных и искусственных экотоксикантов.
Свободное окисление. Одна из задач свободного (несопряженного) окисления – превращения природных или неприродных субстратов, называемых в этом случае ксенобиотиками (ксено – несовместимый, биос – жизнь). Они осуществляются ферментами диоксигеназами и монооксигеназами. Окисление протекает при участии специализированных цитохромов, локализованных чаще всего в эндоплазматическом ретикулуме, поэтому иногда этот процесс называют микросомальным окислением. В реакциях свободного окисления участвуют также кислород и восстановленные дыхательные переносчики (чаще всего НАДФН). Акцептором электронов является цитохром Р-450 (иногда цитохром b5). Окисление субстрата протекает по следующей схеме:
SH + O2 –> SOH.
Механизм действия оксигеназ включает изменение валентности входящих в их состав ионов двухвалентных металлов (железа или меди). Диоксигеназы присоединяют к субстрату молекулярный кислород, активируя его за счет электрона атома железа в активном центре (железо при этом становится трехвалентным). Оксигенация протекает как атака субстрата образующимся супероксид-анионом кислорода. Одной из биологически важных реакций такого типа является превращение β-каротина в витамин А. Монооксигеназы требуют участия в реакции НАДФН, атомы водорода которого взаимодействуют с одним из атомов кислорода, поскольку только один электрон связывается с субстратом. К широко распространенным монооксигеназам относятся разнообразные гидроксилазы. Они принимают участие в окислении аминокислот, оксикислот, полиизопреноидов. В процессе свободного окисления вследствие особенностей используемых цепей передачи электронов не происходит образования АТФ; биологическая роль этих процессов заключается в метаболизме ряда природных и ксенобиотических субстратов. В последнем случае свободное окисление выполняет важную функцию модификации чужеродных соединений.
47. Основные углеводы пищи. Переваривание углеводов в ротовой полости и желудочно-кишечном тракте, амилолитические ферменты слюны, поджелудочной железы, гидролиз дисахаридов. Всасывание моносахаридов (механизм всасывания).
По количеству углеводных остатков УВ разделяются на 3 основных класса: 1. моносахариды (глюкоза, фруктоза, галактоза, манноза и др.); 2. дисахариды (мальтоза, сахароза, лактоза); 3. полисахариды (гомополисахариды крахмал, гликоген, клетчатка). Крахмал – резервный гомополисахарид растений, построенный из остатков α-глюкозы. Крахмал представляет собой смесь двух гомополисахаридов: амилозы и амилопектина. В амилозе остатки глюкозы связаны α-1,4-гликозидными связями, в точках ветвления амилопектина - α-1,6-гликозидными связями. Молекулярная масса крахмала – 106-107. Гликоген – резервный гомополисахарид высших животных и человека, построенный из остатков α–Д-глюкозы. Гликоген содержится практически во всех органах и тканях человека и животных; наибольшее его количество находится в печени и мышцах. Молекулярная масса гликогена 107 – 109 и выше. Гликоген по своему строению близок к амилопектину. Остатки глюкозы связаны α-1,4-гликозидными и α-1,6-гликозидными связями (в точках ветвления). В молекуле гликогена имеется большее число α-1,6-гликозидных связей по сравнению с крахмалом. Клетчатка – это единственный гомополисахарид, который не переваривается в ЖКТ человека, т.к. пищеварительные железы человека не вырабатывают β–глюкозидазу. Однако клетчатка выполняет ряд важных функций: 1. способствует формированию кала; 2. усиливает перистальтику кишечника; 3. является адсорбентом, с которым из кишечника выводятся излишки холестерина, соли тяжелых металлов. Роль углеводов: 1. Энергетическая (глюкоза – основной источник энергии для организма. При сгорании 1 г УВ выделяется 4 ккал энергии). 2. Структурно-функциональная (УВ – обязательный компонент гликопротеинов и протеогликанов, которые выполняют разнообразные функции: гормональную, рецепторную, защитную, ферментативную и др.). 3. Метаболическая (пентозы участвуют в синтезе нуклеиновых кислот и нуклеотидных коферментов). Суточная потребность в углеводах составляет 400-500 г. Переваривание углеводов - это совокупность процессов поэтапного ферментативного гидролиза полисахаридов до моносахаридов, которые всасываются в кишечнике, разносятся током крови к печени и другим тканям организма, где подвергаются различным метаболическим превращениям. Переваривание УВ начинается в ротовой полости под действием фермента амилазы слюны (оптимум рН=6,8-7,2), которая гидролизует в крахмале α -1,4-гликозидные связи с образованием декстринов. Всасывание УВ из просвета кишечника в энтероцит и из энтероцита в кровь происходит: 1) облегченной диффузией с участием переносчиков; 2) вторично активным транспортом (симпортом с ионами натрия) с использованием энергии K, Na-АТФ-азы. Быстрее всех всасываются глюкоза и галактоза. От кишечника всосавшиеся моносахариды транспортируются в печень, где происходит до 90% превращений моносахаров. Поступление глюкозы в клетки сердечной, скелетных мышц и жировой ткани регулируется инсулином.
48. Потребность ребенка в углеводах. Своеобразие переваривания и всасывания углеводов в желудочно-кишечном тракте у ребенка.
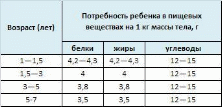
49. Обмен галактозы, фруктозы, маннозы. Взаимопревращение моносахаров в организме. Наследственные нарушения обмена моносахаридов: галактоземия, непереносимость фруктозы.
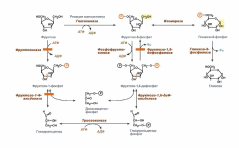
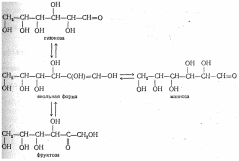
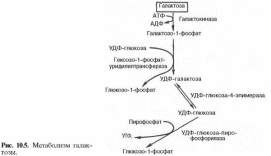
Нарушения, связанные с недостаточностью ферментов, которые принимают участие в переваривании и всасывании УВ.
1. Непереносимость лактозы: а) врожденная. Дефект по лактазе в просвете тонкого кишечника. Большой осмотический эффект невсосавшейся лактозы вызывает приток жидкости в тонкий кишечник, поэтому клиническими симптомами являются вздутие живота, тошнота, судороги, боль и водная диарея. Наследуется по аутосомно-рецессивному типу. б) приобретенная (временная). Может быть, и у взрослых вследствие инфекционных заболеваний или интенсивного лечения антибактериальными препаратами.
2. Нарушения обмена фруктозы: а) Фруктоземия (наследственная непереносимость фруктозы). Недостаточность фермента кетозо-1- фосфат-альдолазы приводит к резкому увеличению концентрации фруктозо-1-фосфата в клетках печени, вследствие чего развиваются хроническая недостаточность функций печени и почек, гипогликемия, диарея, рвота, боли в животе. б) Эссенциальная фруктозурия. Причина: недостаток фруктокиназы. Следствие: нарушение фосфорилирования фруктозы приводит к повышению содержания фруктозы в крови и аномальному выведению фруктозы с мочой. Это нарушение не вызывает патологических симптомов.
3. Нарушения обмена галактозы: а) Галактоземия. Причина: недостаток фермента гексозо-1-фосфатуридилтрансфераза печени. Больные дети плохо растут, прием молока вызывает рвоту и понос. Происходит увеличение печени и желтуха. При этом заболевании увеличивается концентрация галактозы и галактозо-1-фосфата. Галактоземия сопровождается галактозурией. У детей галактоземия приводит к умственной отсталости и катаракте хрусталика. Определяющим диагностическим критерием служит отсутствие в эритроцитах гексозо-1-фосфатуридилтрансферазы. б) Недостаток галактокиназы. Происходит накопление галактозы и ее превращение в галактитол. Следствие: раннее развитие катаракты.
5 0.
Анаэробный распад глюкозы. Этапы этого
процесса. Гликолитическая оксиредукция,
субстратное фосфорилирование.
Энергетическая ценность анаэробного
распада глюкозы. Регуляторные механизмы,
участвующие в этом процессе.
0.
Анаэробный распад глюкозы. Этапы этого
процесса. Гликолитическая оксиредукция,
субстратное фосфорилирование.
Энергетическая ценность анаэробного
распада глюкозы. Регуляторные механизмы,
участвующие в этом процессе.
Гликолиз – синоним молочнокислого брожения – сложный ферментативный процесс превращения глюкозы до двух молекул молочной кислоты, протекающий в тканях человека и животных без потребления кислорода. Гликолиз включает 11 ферментативных реакций, протекающих в цитоплазме клетки. Реакции гликолиза проходят в 2 стадии. В ходе первой стадии – энергопотребляющей – используются 2 АТФ в 1-ой и 3-ей реакциях. В процессе 7-ой и 10-ой реакций второй стадии – энергодающей – образуются 4 АТФ. Из 11 реакций - 3 необратимые (1-ая, 3-я и 10-ая).
51. Анаэробный гликолиз, повышенная активность анаэробного распада глюкозы у ребенка раннего возраста. Биохимические критерии гликолиза. Связь с возникновением ацидоза.
Значение анаэробного гликолиза: 1. каждая молекула глюкозы в анаэробных условиях снабжает клетку 2-мя молекулами АТФ; 2. промежуточные метаболиты гликолиза (фосфоглицериновый альдегид, фосфодиоксиацетон, фосфоглицерат, пируват) могут использоваться клеткой в обмене липидов и белков; 3. пируват и НАДН используются в реакциях аэробного окисления глюкозы; 4. восемь реакций гликолиза из 11 обратимые, поэтому возможен синтез глюкозы из лактата (глюконеогенез). Эффект Пастера. Подавление анаэробного гликолиза аэробным окислением глюкозы. Факультативные анаэробы потребляют больше глюкозы, т.к. энергоотдача гликолиза – всего 2 АТФ. При добавлении О2 в среду потребление глюкозы резко уменьшается, т.к. возрастает количество АТФ, которое блокирует активность гексокиназы и фосфофруктокиназы.
Спиртовое брожение. В процессе спиртового брожения молекула глюкозы в анаэробных условиях превращается в пируват, который затем декарбоксилируется и восстанавливается при участии НАДН с образование этанола.
Особенности гликолиза и его нарушения у детей. У новорожденного аэробные процессы преобладают над аэробными. Это продолжается в течение первого месяца, пока фетальный Hb F не заменится на взрослый HbА. У детей высокая скорость аэробных процессов, в ходе которых вырабатывается АТФ, необходимая для синтетических процессов и роста. Детям требуется больше УВ в пище в качестве источника энергии. В детском организме анаэробные механизмы распада глюкозы и получения энергии подключаются при стрессах быстрее, чем у взрослых. Это свидетельствует о лучшей адаптации организма к экстремальным ситуациям. В подростковом возрасте еще не совершенны процессы гормональной регуляции (действие инсулина, глюкагона, адреналина). Распад гликогена может идти быстро, расход глюкозы большой. Но если не восполняется количество глюкозы в крови, легко наступает гипогликемия.
52. Аэробный распад глюкозы: этапы этого процесса и его энергетика. Физиологическое значение аэробного распада глюкозы.
Аэробный путь окисления глюкозы и его энергетика. Аэробный путь окисления глюкозы происходит в 3 этапа: 1. окисление молекулы глюкозы до 2 молекул пирувата; 2. окислительное декарбоксилирование пирувата (с образованием 2 молекул ацетил-КоА); 3. реакции цикла Кребса, где каждая молекула ацетил-КоА сгорает с образованием 12 АТФ.
1-ый этап. Окисление молекулы глюкозы до 2 молекул пирувата - это первые 10 реакций гликолиза. Суммарная реакция 1 этапа:
Глюкоза + 2 НАД++ 2 АДФ → 2 пирувата + 2 НАДН + Н+ + 2 АТФ
2-ой этап. Окислительное декарбоксилирование пирувата (с образованием 2 молекул ацетилКоА) происходит в матриксе митохондрий и осуществляется мультиферментным комплексом пируватдегидрогеназой. В его состав входят 3 фермента и 5 коферментов: 1. Пируватдекарбоксилаза – кофермент тиаминпирофосфат (активная форма витамина В1). 2. Дегидролипоилацетилтрансфераза – кофермента: в активном центре – липоевая кислота (витаминоподобное вещество), из матрикса митохондрий используется Коэнзим А (КоА~SH). 3. Дигидролипоилдегидрогеназа – коферменты: в активном центре – ФАД, из матрикса митохондрий используется – НАД. Суммарная реакция:
2 Пируват + 2 НАД+ + КоА → 2 ацетил-КоА + 2 НАДН + Н+
Каждый восстановленный НАД в митохондриях отдает протоны и электроны в полную ц.п.э., где образуется 2 х 3 АТФ = 6 АТФ. Таким образом, ценность второго этапа – 6 АТФ. Эти реакции происходят только в аэробных условиях!
3-ий этап. Реакции цикла Кребса, где каждая молекула ацетил-КоА сгорает с образованием 12 АТФ. Следовательно, энергетический выход третьего этапа (в расчете на молекулу глюкозы) – 2 х 12 АТФ = 24 АТФ . Энергетическая ценность аэробного окисления глюкозы: 1 этап – 8 (6) АТФ 2 этап – 6 АТФ 3 этап – 24 АТФ Итого: 38 (36) АТФ (разница в 2 АТФ зависит от челнока, который переносит протоны и электроны из цитозоля от НАДН, образованного в 6-ой реакции гликолиза в митохондрии в ц.п.э.). Аэробное окисление глюкозы является главным источником энергии для большинства клеток организма.
53. Интенсификация процесса прямого окисления глюкозы у детей раннего возраста. Причины этого явления.
54. Пентозофосфатный путь превращения глюкозы. Этапы и стадии этого процесса. Окислительная стадия пентозного цикла. Значение пентозофосфатного пути превращения глюкозы для организма.

55. Биосинтез глюкозы (глюконеогенез) из неуглеводных продуктов. Основные этапы, три обходных реакции гликолиза. Значение процесса. Гормональная регуляция глюконеогенеза. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
Биосинтез глюкозы (глюконеогенез) из молочной кислоты. Глюконеогенез – обращение реакций гликолиза. Из 11 реакций гликолиза 3 необратимы (1-ая, 3-я и 10-я):
1. глюкоза → глюкозо-6 фосфат
2. фруктозо-6-фосфат → фруктозо-1,6-дифосфат
3. фосфоенолпируват → пируват
Для этих реакций существуют обходные пути.
Первый обходной путь начинается в матриксе митохондрий. Пируват проникает сквозь мембрану митохондрий в матрикс митохондрии, затем пируват подвергается карбоксилированию под действием фермента пируваткарбоксилаза (с использованием биотина и энергии АТФ). В результате этой реакции образуется оксалоацетат. Затем оксалоацетат превращается в малат, чтобы выйти из митохондрий в цитозоль клетки для дальнейшего превращения. В цитозоле малат обратимо превращается в оксалоацетат (под действием цитозольной малатдегидрогеназы). Образовавшийся оксалоацетат под действием фермента фосфоенолпируваткарбоксикиназы (при участии биотина и энергии ГТФ) превращается в фосфоенолпируват. В дальнейшем реакции глюконеогенеза идут до образования фруктозо-1,6-дифосфата (обратимые реакции гликолиза).
Второй обходной путь: Фруктозо-1,6-дифосфат + Н2О → фруктозо-6-фосфат + Фн (реакцию катализирует фруктозо-1,6-бифосфатаза)
Третий обходной путь: Глюкозо-6-фосфат + Н2О → глюкоза + Фн (реакцию катализирует глюкозо-6-фосфатаза) В процессе глюконеогенеза 7-я реакция гликолиза (1,3-дифосфоглицерат + АДФ ↔ 3- фосфоглицерат + АТФ) расходуется 2 АТФ. В ходе синтеза глюкозы используются макроэргические соединения: 4 АТФ и 2 ГТФ.
