
- •3.Закон Стефана-Больцмана для теплового излучения. Закон смещения Вина. § 199. Законы Стефана — Больцмана и смещения Вина
- •5.Определение и основные закономерности фотоэффекта. Объяснение с точки зрения квантовой теории. Формула Эйнштейна для фотоэффекта. § 202. Виды фотоэлектрического эффекта. Законы внешнего фотоэффекта
- •§ 203. Уравнение Эйнштейна для внешнего фотоэффекта. Экспериментальное подтверждение квантовых свойств света
- •§ 204. Применение фотоэффекта
- •6.Энергия, масса и импульс фотона. Давление света и его экспериментальное подтверждение. § 205. Масса и импульс фотона. Давление света
- •8)Атом как сложная система электически заряженных частиц и спектр его излучения. Сериальные формулы.
- •9) Модель атома резерфорда.. Постулаты бора Модель атома Резерфорда (Ядерная или Планетарная модель атома)
- •Квантовые постулаты Бора
- •10.Элементарная боровская теория атома водорода. Уровни энергии атома водорода. Вывод обобщенной формулы Бальмера. Недостатки теории Бора. § 208. Модели атома Томсона и Резерфорда
- •§ 209. Линейчатый спектр атома водорода
- •§ 210. Постулаты Бора
- •§ 214. Некоторые свойства волн да Бройля
- •§ 215. Соотношение неопределенностей
- •§ 213. Корпускулярно-волновой дуализм свойств вещества
- •§ 215. Соотношение неопределенностей
- •§ 217. Общее уравнение Шредингера. Уравнение Шредингера для стационарных состояний
- •15)Квантоваяя теория атома вводорода
- •§ 227. Принцип Паули. Распределение электронов в атоме по состояниям
- •§ 240. Понятие о зонной теории твердых тел
- •§ 241. Металлы, диэлектрики и полупроводники по зонной теории
15)Квантоваяя теория атома вводорода
18.Распределение электронов в атоме по энергетическим уровням. Принцип Паули. Понятие электронных оболочек и подоболочек.
§ 227. Принцип Паули. Распределение электронов в атоме по состояниям
Если тождественные частицы имеют одинаковые квантовые числа, то их волновая функция симметрична относительно перестановки частиц. Отсюда следует, что два одинаковых фермиона, входящих в одну систему, не могут находиться в одинаковых состояниях, так как для фермионов волновая функция должна быть антисимметричной. Обобщая опытные данные, В. Паули сформулировал принцип, согласно которому системы фермионов встречаются в природе только в состояниях, описываемых антисимметричными волновыми функциями (квантово-механическая формулировка принципа Паули).
Из этого положения вытекает более простая формулировка принципа Паули, которая и была введена им в квантовую теорию (1925) еще до построения квантовой механики: в системе одинаковых фермионов любые два из них не могут одновременно находиться в одном и том же состоянии. Отметим, что число однотипных бозонов, находящихся в одном и том же состоянии, не лимитируется.
Напомним, что состояние электрона в атоме однозначно определяется набором четырех квантовых чисел:
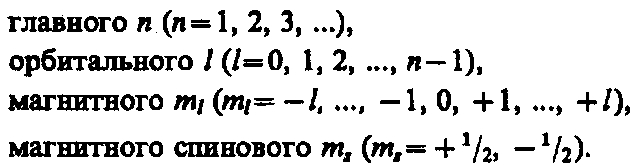
Распределение электронов в атоме подчиняется принципу Паули, который может быть использован в его простейшей формулировке: в одном и том же атоме не может быть более одного электрона с одинаковым набором четырех квантовых чисел п, l, ml и тs т. е.
![]()
где Z(п, l, ml, тs) — число электронов, находящихся в квантовом состоянии, описываемом набором четырех квантовых чисел: п, l, ml, тs. Таким образом, принцип Паули утверждает, что два электрона, связанные в одном и том же атоме, различаются значениями по крайней мере одного квантового числа.
Согласно формуле (223.8), данному n соответствует n2 различных состояний, отличающихся значениями l и ml. Квантовое число тs может принимать лишь два значения (± ½). Поэтому максимальное число электронов, находящихся в состояниях, определяемых данным главным квантовым числом, равно
![]()
Совокупность электронов в многоэлектронном атоме, имеющих одно и то же главное квантовое число n, называют электронной оболочкой. В каждой из оболочек электроны распределяются по подоболочкам, соответствующим данному l. Поскольку орбитальное квантовое число принимает значения от 0 до n–1, число подоболочек равно порядковому номеру n оболочки. Количество электронов в подоболочке определяется магнитным и магнитным спиновым квантовыми числами: максимальное число электронов в подоболочке с данным l равно 2(2l+1). Обозначения оболочек, а также распределение электронов по оболочкам и подоболочкам представлены в табл. 6.
Таблица 6

22.Общие положения зонной теории твердых тел: расщепление энергетических уровней отдельных атомов, энергетические зоны, возможности внутризонных и межзонных переходов электронов.
§ 240. Понятие о зонной теории твердых тел
Используя уравнение Шредингера — основное уравнение динамики в нерелятивистской квантовой механике, — в принципе можно рассмотреть задачу о кристалле, например найти возможные значения его энергии, а также соответствующие энергетические состояния. Однако как в классической, так и в квантовой механике отсутствуют методы точного решения динамической задачи для системы многих частиц. Поэтому эта задача решается приближенно сведением задачи многих частиц к одноэлектронной задаче об одном электроне, движущемся в заданном внешнем поле. Подобный путь приводит к зонной теории твердого тела.
В основе зонной теории лежит так называемое адиабатическое приближение. Квантово-механическая система разделяется на тяжелые и легкие частицы — ядра и электроны. Поскольку массы и скорости этих частиц значительно различаются, можно считать, что движение электронов происходит в поле неподвижных ядер, а медленно движущиеся ядра находятся в усредненном поле всех электронов. Принимая, что ядра в узлах кристаллической решетки неподвижны, движение электрона рассматривается в постоянном периодическом поле ядер.
Далее используется приближение самосогласованного поля. Взаимодействие данного электрона со всеми другими электронами заменяется действием на него стационарного электрического поля, обладающего периодичностью кристаллической решетки. Это поле создается усредненным в пространстве зарядом всех других электронов и всех ядер. Таким образом, в рамках зонной теории многоэлектронная задача сводится к задаче о движении одного электрона во внешнем периодическом поле — усредненном и согласованном поле всех ядер и электронов.
Рассмотрим мысленно «процесс образования» твердого тела из изолированных атомов. Пока атомы изолированы, т. е. находятся друг от друга на макроскопических расстояниях, они имеют совпадающие схемы энергетических уровней (рис. 313). По мере «сжатия» нашей модели до кристаллической решетки, т. е. когда расстояния между атомами станут равными межатомным расстояниям в твердых телах, взаимодействие между атомами приводит к тому, что энергетические уровни атомов смещаются, расщепляются и расширяются в зоны, образуется зонный энергетический спектр.
Из рис. 313, на котором показано расщепление энергетических уровней в зависимости от расстояния r между атомами, видно, что заметно расщепляются и расширяются лишь уровни внешних, валентных электронов, наиболее слабо связанных с ядром и имеющих наибольшую энергию, а также более высокие уровни, которые в основном состоянии атома вообще электронами не заняты. Уровни же внутренних электронов либо совсем не расщепляются, либо расщепляются слабо. Таким образом, в твердых телах внутренние электроны ведут себя так же, как в изолированных атомах, валентные же электроны «коллективизированы» — принадлежат всему твердому телу.
Образование зонного энергетического спектра в кристалле является квантово-механическим эффектом в вытекает из соотношения неопределенностей. В кристалле валентные электроны атомов, связанные слабее с ядрами, чем внутренние электроны, могут переходить от атома к атому сквозь потенциальные барьеры, разделяющие атомы, т. е. перемещаться без изменений полной энергии (туннельный эффект, см. § 221). Это приводит к тому, что среднее время жизни валентного электрона в данном атоме по сравнению с изолированным атомом существенно уменьшается и составляет примерно 10–15 с (для изолированного атома оно примерно 10–8 с). Время же жизни электрона в каком-либо состоянии связано с неопределенностью его энергии (шириной уровня) соотношением неопределенностей E~h/ (см. (215.5)). Следовательно, если естественная ширина спектральных линий составляет примерно 10–7 эВ, то в кристаллах E110 эВ, т. е. энергетические уровни валентных электронов расширяются в зону дозволенных значений энергии.
Энергия внешних электронов может принимать значения в пределах закрашенных на рис. 313 областей, называемых разрешенными энергетическими зонами. Каждая разрешенная зона «вмещает» в себя столько близлежащих дискретных уровней, сколько атомов содержит кристалл: чем больше в кристалле атомов, тем теснее расположены уровни в зоне. Расстояние между соседними энергетическими уровнями в зоне составляет приблизительно 10–22 эВ. Так как оно столь ничтожно, то зоны можно считать практически непрерывными, однако факт конечного числа уровней в зоне играет важную роль для распределения электронов по состояниям.
Разрешенные энергетические зоны разделены зонами запрещенных значений энергии, называемыми запрещенными энергетическими зонами. В них электроны находиться не могут. Ширина зон (разрешенных и запрещенных) не зависит от размера кристалла. Разрешенные зоны тем шире, чем слабее связь валентных электронов с ядрами.

23. Металлы, диэлектрики и полупроводники с точки зрения зонной теории твердого тела.
