
Билет №28: 1) Формула тонкой линзы
Расстояния от точки предмета до центра линзы и от точки изображения до центра линзы называются сопряжёнными фокусными расстояниями.
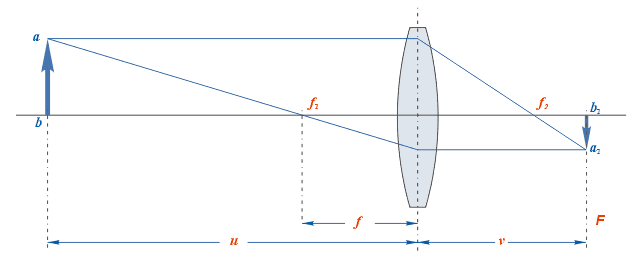
Эти величины находятся в зависимости между собой и определяются формулой, называемой формулой тонкой линзы (открытой Исааком Барроу):
![]()
где ![]() —
расстояние от линзы до предмета;
—
расстояние от линзы до предмета; ![]() —
расстояние от линзы до изображения;
—
расстояние от линзы до изображения; ![]() —
главное фокусное расстояние линзы. В
случае толстой линзы формула остаётся
без изменения с той лишь разницей, что
расстояния отсчитываются не от центра
линзы, а от главных
плоскостей.
—
главное фокусное расстояние линзы. В
случае толстой линзы формула остаётся
без изменения с той лишь разницей, что
расстояния отсчитываются не от центра
линзы, а от главных
плоскостей.
Для нахождения той или иной неизвестной величины при двух известных пользуются следующими уравнениями:
![]()
![]()
![]()
Увеличение линзы - это отношение размера изображения к размеру предмета, но еще это и отношение расстояния от изображения к линзе к расстоянию от предмета к линзе. Г=Н/h=f/d
2) Под энергией связи атомного ядра понимают энергию, которую нужно затратить, чтобы расщепить ядро на отдельные нуклоны. Такая же энергия выделяется при образовании ядра из свободных нуклонов. Ее можно рассчитать, пользуясь формулой Л. Эйнштейна, связывающей массу частицы и энергию:
W=mc2
Изото́пы (от др.-греч. ισος — «равный», «одинаковый», и τόπος — «место») — разновидности атомов (и ядер) какого-либохимического элемента, которые имеют одинаковый атомный номер, но при этом разные массовые числа. Название связано с тем, что все изотопы одного атома помещаются в одно и то же место (в одну клетку) таблицы Менделеева. Химические свойства атома зависят от строения электронной оболочки, которая, в свою очередь, определяется в основном зарядом ядра Z (то есть количеством протонов в нём), и почти не зависят от его массового числа A (то есть суммарного числа протонов Z и нейтронов N). Все изотопы одного элемента имеют одинаковый заряд ядра, отличаясь лишь числом нейтронов. Обычно изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, означающего массовое число (например,12C, 222Rn). Можно также написать название элемента с добавлением через дефис массового числа (например, углерод-12, радон-222). Некоторые изотопы имеют традиционные собственные названия (например, дейтерий, актинон).
Пример изотопов: 168O, 178O, 188O — три стабильных изотопа кислорода.
Билет №29: 1) Планетарная модель атома, или модель Резерфорда, - историческая модель строения атома, которую предложил Эрнест Резерфорд в результате эксперимента с рассеиванием альфа-частиц. По этой модели атом состоит из небольшого положительно заряженного ядра, в котором сосредоточена почти вся масса атома, вокруг которого движутся электроны, - подобно тому, как планеты движутся вокруг Солнца. Планетарная модель атома соответствует современным представлениям о строении атома с учётом того, что движение электронов имеет квантовый характер и не описывается законами классической механики. Исторически планетарная модель Резерфорда пришла на смену «модели сливового пудинга» Джозефа Джона Томсона, которая постулирует, что отрицательно заряженные электроны помещены внутрь положительно заряженного атома.
Новую модель строения атома Резерфорд предложил в 1911 году как вывод из эксперимента по рассеиванию альфа-частиц на золотой фольге, проведённого под его руководством. При этом рассеянии неожиданно большое количество альфа-частиц рассеивалось на большие углы, что свидетельствовало о том, что центр рассеяния имеет небольшие размеры и в нём сосредоточен значительный электрический заряд. Расчёты Резерфорда показали, что рассеивающий центр, заряженный положительно или отрицательно, должен быть по крайней мере в 3000 раз меньше размера атома, который в то время уже был известен и оценивался как примерно 10-10 м. Поскольку в то время электроны уже были известны, а их масса и заряд определены, то рассеивающий центр, который позже назвали ядром, должен был иметь противоположный электронам заряд. Резерфорд не связал величину заряда с атомным номером. Этот вывод был сделан позже. А сам Резерфорд предположил, что заряд пропорционален атомной массе.
Недостатком планетарной модели была её несовместимость с законами классической физики. Если электроны движутся вокруг ядра как планеты вокруг Солнца, то их движение ускоренное, и, следовательно, по законам классической электродинамики они должны были бы излучать электромагнитные волны, терять энергию и падать на ядро. Следующим шагом в развитии планетарной модели стала модель Бора, постулирующая другие, отличные от классических, законы движения электронов. Полностью противоречия электродинамики смогла решить квантовая механика.
Постулаты Бора — основные допущения, сформулированные Нильсом Бором в 1913 году для объяснения закономерности линейчатого спектра атома водорода и водородоподобных ионов (формула Бальмера-Ридберга) и квантового характера испускания и поглощения света. Бор исходил из планетарной модели атомаРезерфорда.
Атом может находиться только в особенных стационарных или квантовых состояниях, каждому из которых отвечает определенная энергия. В стационарном состоянии атом не излучает электромагнитных волн.
Электрон в атоме, не теряя энергии, двигается по определённым дискретным круговым орбитам, для которых момент импульсаквантуется:
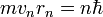 ,
где
,
где 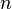 — натуральные
числа,
а
— натуральные
числа,
а 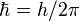 — постоянная
Планка.
Пребывание электрона на орбите определяет
энергию этих стационарных
состояний.
— постоянная
Планка.
Пребывание электрона на орбите определяет
энергию этих стационарных
состояний.При переходе электрона с орбиты (энергетический уровень) на орбиту излучается или поглощается квант энергии
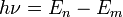 ,
где
,
где 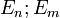 — энергетические
уровни,
между которыми осуществляется переход.
При переходе с верхнего уровня на нижний
энергия излучается, при переходе с
нижнего на верхний — поглощается.
— энергетические
уровни,
между которыми осуществляется переход.
При переходе с верхнего уровня на нижний
энергия излучается, при переходе с
нижнего на верхний — поглощается.
Используя данные постулаты и законы классической механики, Бор предложил модель атома, ныне именуемую Боровской моделью атома[1]. В дальнейшем Зоммерфельд расширил теорию Бора на случай эллиптических орбит. Её называют моделью Бора-Зоммерфельда.
2) Механическая работа — это физическая величина, являющаяся скалярной количественной мерой действия силы или сил на тело или систему, зависящая от численной величины, направления силы (сил) и от перемещения точки (точек) тела или системы
Мо́щность — физическая величина, равная отношению работы ко времени, за которое она была совершена. В более узком смысле мощность равна отношению работы, выполняемой за некоторый промежуток времени, к этому промежутку времени
Билет №30:
1)Радиоактивность (от лат. radio — излучаю, radius — луч и activus — действенный), самопроизвольное (спонтанное) превращение неустойчивого изотопа химического элемента в другой изотоп (обычно — изотоп другого элемента). Сущность явления Р. состоит в самопроизвольном изменении состава атомного ядра, находящегося в основном состоянии либо в возбуждённом долгоживущем (метастабильном) состоянии. Такие превращения сопровождаются испусканием ядрами элементарных частиц либо других ядер, например ядер 2He (a-частиц). Все известные типы радиоактивных превращений являются следствием фундаментальных взаимодействий микромира: сильных взаимодействий (ядерные силы) или слабых взаимодействий. Первые ответственны за превращения, сопровождающиеся испусканием ядерных частиц, например a-частиц, протонов или осколков деления ядер: вторые проявляются в b-распаде ядер.Электромагнитные взаимодействия ответственны за квантовые переходы между различными состояниями одного и того же ядра, которые сопровождаются испусканием гамма-излучения. Эти переходы не связаны с изменениями состава ядер и поэтому, согласно современной классификации, не принадлежат к числу радиоактивных превращений. Понятие "Р." распространяют также на b-распад нейтронов.
СОСТАВ АТОМНОГО ЯДРА
Ядро атома состоит из нуклонов, которые подразделяются на протоны и нейтроны.
Символическое обозначение ядра атома:
![]()
А- число нуклонов, т.е. протонов + нейтронов ( или атомная масса ) Z- число протонов ( равно числу электронов ) N- число нейтронов ( или атомный номер )
N = A - Z
Ядерные силы, силы, удерживающие нуклоны (протоны и нейтроны) в ядре. Обусловливают самые интенсивные из всех известных в физике взаимодействий. Ядерн. силы являются короткодействующими (радиус их действия ~ 10-13см)
Деление тяжёлых ядер — экзотермический процесс, в результате которого высвобождается большое количество энергии в виде кинетической энергии продуктов реакции, а также излучения. Деление ядер служит источником энергии вядерных реакторах и ядерном оружии.
2) Зако́н сохране́ния эне́ргии — фундаментальный закон природы, установленный эмпирически и заключающийся в том, что для изолированной физической системы может быть введена скалярная физическая величина, являющаяся функцией параметров системы и называемая энергией, которая сохраняется с течением времени. Поскольку закон сохранения энергии относится не к конкретным величинам и явлениям, а отражает общую, применимую везде и всегда, закономерность, то его можно именовать не законом, а принципом сохранения энергии.
