
- •1. Макро- и микроструктура металлов. Методы исследования металлов.
- •2. Атомно-кристаллическая структура металлов. Виды кристаллических решеток.
- •3. Дефекты кристаллической решетки металлов.
- •Формирование структуры металлов при кристаллизации.
- •4. Гомогенная (самопроизвольная) кристаллизация.
- •5. Число центров кристаллизации. Величина зерна.
- •6. Гетерогенное образование зародышей. Модифицирование.
- •7. Строение металлического слитка.
- •8. Полиморфные превращения.
- •Фазы и микроструктура в металлических сплавах.
- •2. Химические соединения.
- •3. Механические смеси.
- •Формирование структуры сплавов при кристаллизации.
- •1. Процесс кристаллизации и фазовые превращения в сплавах.
- •2. Диаграммы фазового равновесия.
- •3. Диаграммы состояния сплавов, образующих неограниченные твердые растворы.
- •4. Неравновесная кристаллизация.
- •5. Дендритная (внутрикристаллитная) ликвация.
- •6. Диаграммы состояния сплавов, образующих ограниченные твердые растворы.
- •7. Ликвация по плотности.
- •8. Диаграммы состояния сплавов, компоненты которых имеют полиморфные превращения.
- •1. Компоненты и фазы в системе железо-углерод.
- •2. Диаграмма состояния железо-цементит (метастабильное равновесие).
- •3. Влияние углерода, постоянных примесей и легирующих элементов на свойства стали.
- •1. Теория термической обработки стали. Превращение ферритно-карбидной структуры в аустенит при нагреве.
- •2. Теория термической обработки стали. Рост зерна аустенита при нагреве.
- •2. Теория термической обработки стали. Влияние величины зерна на свойства сталей. Определение и выявление величины зерна.
- •3. Теория термической обработки стали. Перлитное превращение переохлажденного аустенита.
- •4. Теория термической обработки стали. Мартенситное превращение в сталях.
- •5. Влияние легирующих элементов на устойчивость переохлажденного аустенита. Превращение аустенита при непрерывном охлаждении.
- •6. Превращение мартенсита и остаточного аустенита при нагреве.
- •7. Влияние отпуска на механические свойства.
- •8. Виды отпускной хрупкости в легированных сталях.
- •9. Термическое и деформационное старение углеродистых сталей.
- •1. Технология термической обработки стали. Отжиг I рода.
- •2. Технология термической обработки стали. Отжиг II рода.
- •3. Технология термической обработки стали. Закалка, выбор температуры закалки.
- •4. Технология термической обработки стали. Продолжительность нагрева деталей для закалки, охлаждающие среды.
- •5. Технология термической обработки стали. Закаливаемость и прокаливаемость стали.
- •6. Технология термической обработки стали. Внутренние напряжения в закаленной стали.
- •7. Технология термической обработки стали. Способы закалки.
- •8. Технология термической обработки стали. Отпуск стали.
- •9. Краткая характеристика видов термомеханической обработки.
- •10. Технология термической обработки стали. Дефекты, возникающие при термической обработке.
- •1. Теория химико-термической обработки сталей. Понятие эффективной толщины диффузионного слоя.
- •2. Цементация. Образование цементованного слоя. Цементация в твердом и газовом карбюризаторе.
- •3. Азотирование. Технология процесса азотирования.
- •4. Нитроцементация и цианирование. Особенности процессов.
- •5. Борирование, силицирование. Виды диффузионного насыщения металлами.
- •Порошковые антифрикционные материалы на основе железа. Структура. Область применения. Технология получения деталей.
- •Полимеры и пластмассы. Их классификация и способы получения.
- •Неорганические стекла. Классификация и область применения.
Формирование структуры металлов при кристаллизации.
4. Гомогенная (самопроизвольная) кристаллизация.
Кристаллизация—переход металла из жидкого состояния в твердое. Процесс кристаллизации возможен в тех условиях, когда система переходит к термодинамически более устойчивому состоянию с меньшей свободной энергией (энергией Гиббса), G, то есть энергия кристалла меньше энергии Гиббса жидкой фазы. Изменение энергии Гиббса металла в жидком и твердом состоянии зависит от температуры.
К
Рис. 5. Изменение энергии Гиббса.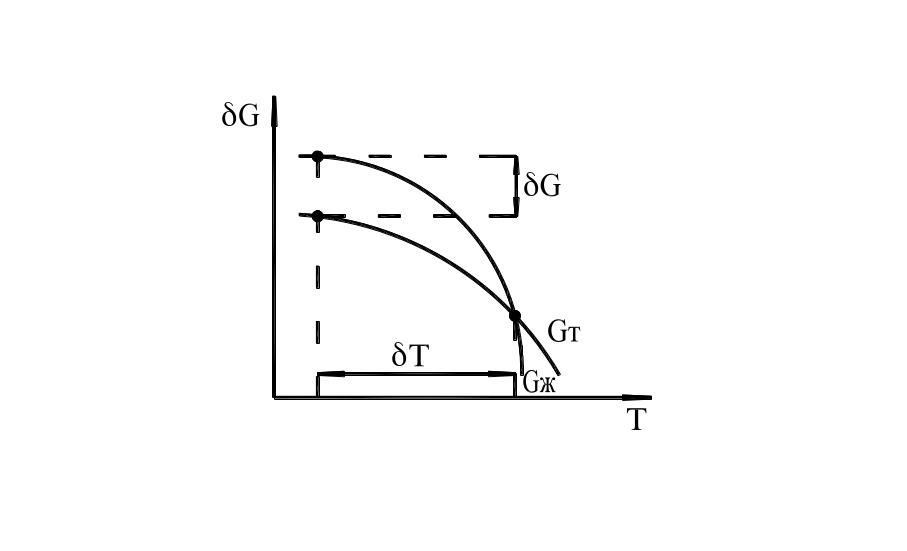
Таким образом, процесс кристаллизации может протекать только при переохлаждении металла ниже равновесной температуры Тп, то есть когда существует разность энергий Гиббса жидкой и твердой фаз.
δТ=Тп-Тк—степень переохлаждения.
При
очень медленном охлаждении металла
степень переохлаждения невелика и
процесс кристаллизации протекает при
темпратуре близкой к равновесной.
[Горизонтальный
участок на графике указывает на выделение
скрытой теплоты кристаллизации, не
смотря на отвод тепла, при котором
п
Рис.6. Влияние скорости охлаждения
на
температуру кристаллизации.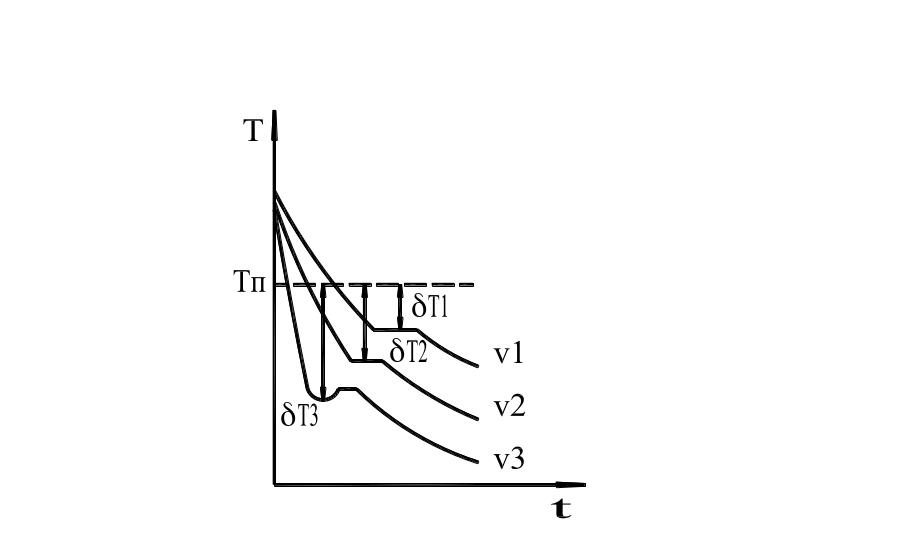
С увеличением скорости охлаждения процесс кристаллизации протекает при температурах значительно ниже равновесной. Чем чище жидкий металл, тем выше его степень переохлаждения.
При охлаждении металла ниже равновесной температуры в расплаве появляются устойчивые, способные к росту кристаллические зародыши.
Первые кристаллы растут свободно, но по мере увеличения их количества, правильная форма их нарушается, так как на некоторых участках рост граней кристаллов прекращается. В результате кристаллы растут только в тех направлениях, где возможен свободный доступ жидкости. Такие зародыши называются кристаллитами. Рост зародышей возможен только при условии, если они достигли определенной величины, с которой начинается уменьшение энергии Гиббса.
В
Рис. 7. Энергия Гиббса.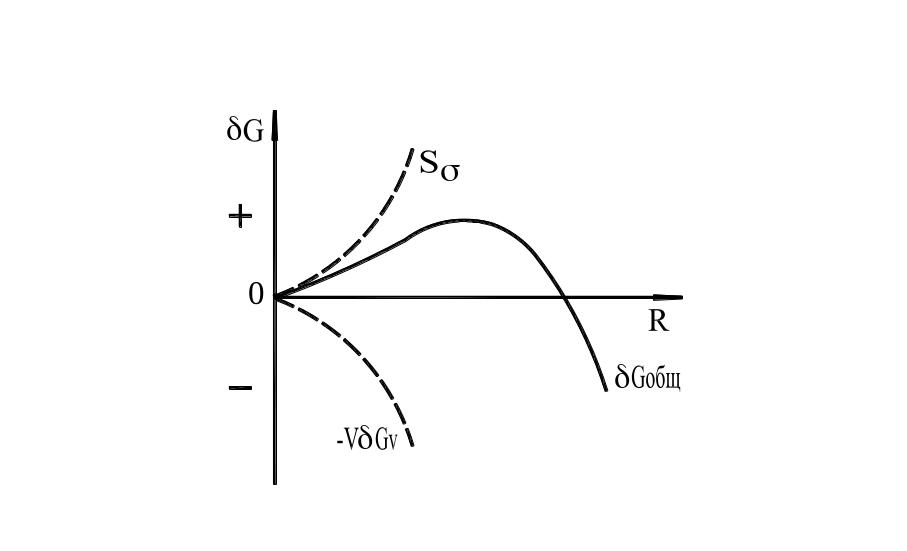
Общее изменение энергии Гиббса будет иметь вид: δGобщ=Sσ-VδGv,
где S—суммарная площадь поверхности кристаллов;
σ—удельное поверхностное натяжение на границе разделяя между зернами;
VδGv—разность энергий Гиббса жидкой и твердой фаз.
Рис. 8. Критический размер зародыша.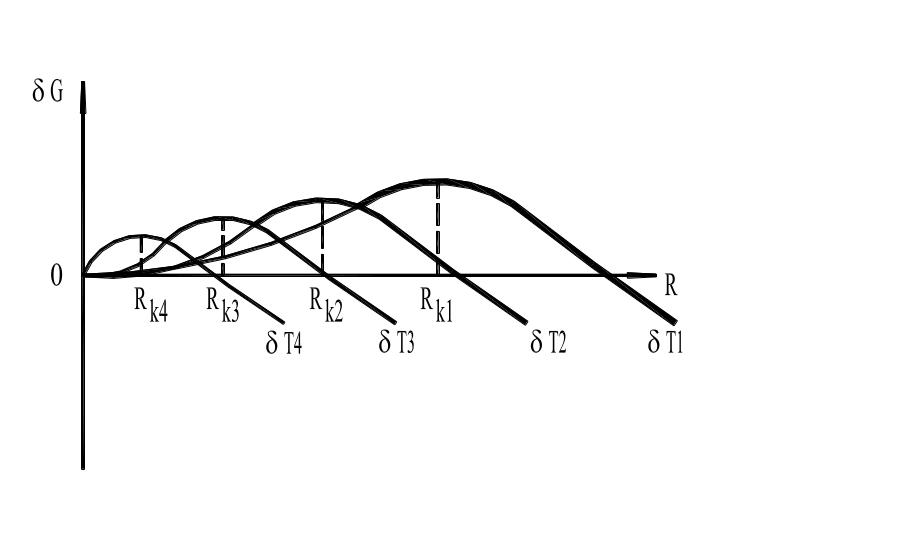
При образовании зародыша размером меньше, чем Rк свободная энергия системы возрастает, так как возрастание энергии Гиббса вследствие образования новой поверхности перекрывает ее уменьшение. Зародыши размером меньше Rк расти не может и растворится в жидком металле.
Минимальный размер зародыша, Rк, способного к росту при данных температурных условиях, называется критическим размером зародыша, а сам зародыш равновесным. Тогда выражение для определения критического размера зародыша примет вид:
![]()
При уменьшении степени переохлаждения разность энергий Гиббса жидкой и твердой фаз увеличивается, следовательно, увеличивается число центров кристаллизации (зародышей) и скорость их роста. При температуре близкой к равновесной возможность образования зародышей очень мала.
