
- •1. Макро- и микроструктура металлов. Методы исследования металлов.
- •2. Атомно-кристаллическая структура металлов. Виды кристаллических решеток.
- •3. Дефекты кристаллической решетки металлов.
- •Формирование структуры металлов при кристаллизации.
- •4. Гомогенная (самопроизвольная) кристаллизация.
- •5. Число центров кристаллизации. Величина зерна.
- •6. Гетерогенное образование зародышей. Модифицирование.
- •7. Строение металлического слитка.
- •8. Полиморфные превращения.
- •Фазы и микроструктура в металлических сплавах.
- •2. Химические соединения.
- •3. Механические смеси.
- •Формирование структуры сплавов при кристаллизации.
- •1. Процесс кристаллизации и фазовые превращения в сплавах.
- •2. Диаграммы фазового равновесия.
- •3. Диаграммы состояния сплавов, образующих неограниченные твердые растворы.
- •4. Неравновесная кристаллизация.
- •5. Дендритная (внутрикристаллитная) ликвация.
- •6. Диаграммы состояния сплавов, образующих ограниченные твердые растворы.
- •7. Ликвация по плотности.
- •8. Диаграммы состояния сплавов, компоненты которых имеют полиморфные превращения.
- •1. Компоненты и фазы в системе железо-углерод.
- •2. Диаграмма состояния железо-цементит (метастабильное равновесие).
- •3. Влияние углерода, постоянных примесей и легирующих элементов на свойства стали.
- •1. Теория термической обработки стали. Превращение ферритно-карбидной структуры в аустенит при нагреве.
- •2. Теория термической обработки стали. Рост зерна аустенита при нагреве.
- •2. Теория термической обработки стали. Влияние величины зерна на свойства сталей. Определение и выявление величины зерна.
- •3. Теория термической обработки стали. Перлитное превращение переохлажденного аустенита.
- •4. Теория термической обработки стали. Мартенситное превращение в сталях.
- •5. Влияние легирующих элементов на устойчивость переохлажденного аустенита. Превращение аустенита при непрерывном охлаждении.
- •6. Превращение мартенсита и остаточного аустенита при нагреве.
- •7. Влияние отпуска на механические свойства.
- •8. Виды отпускной хрупкости в легированных сталях.
- •9. Термическое и деформационное старение углеродистых сталей.
- •1. Технология термической обработки стали. Отжиг I рода.
- •2. Технология термической обработки стали. Отжиг II рода.
- •3. Технология термической обработки стали. Закалка, выбор температуры закалки.
- •4. Технология термической обработки стали. Продолжительность нагрева деталей для закалки, охлаждающие среды.
- •5. Технология термической обработки стали. Закаливаемость и прокаливаемость стали.
- •6. Технология термической обработки стали. Внутренние напряжения в закаленной стали.
- •7. Технология термической обработки стали. Способы закалки.
- •8. Технология термической обработки стали. Отпуск стали.
- •9. Краткая характеристика видов термомеханической обработки.
- •10. Технология термической обработки стали. Дефекты, возникающие при термической обработке.
- •1. Теория химико-термической обработки сталей. Понятие эффективной толщины диффузионного слоя.
- •2. Цементация. Образование цементованного слоя. Цементация в твердом и газовом карбюризаторе.
- •3. Азотирование. Технология процесса азотирования.
- •4. Нитроцементация и цианирование. Особенности процессов.
- •5. Борирование, силицирование. Виды диффузионного насыщения металлами.
- •Порошковые антифрикционные материалы на основе железа. Структура. Область применения. Технология получения деталей.
- •Полимеры и пластмассы. Их классификация и способы получения.
- •Неорганические стекла. Классификация и область применения.
4. Неравновесная кристаллизация.
В реальных условиях охлаждения состав в пределах каждого кристалла и разных кристаллов не успевает выравниваться.
Рассмотрим сплав, содержащий 50% компонента В, начинающий затвердевать при температуре t1, при которой кристаллы α; состав их соответствует точке k1 (Рис. 15.).
При температуре
t2
состав жидкой фазы будет соответствовать
точке m,
а α-фазы – точке n.
Но отдельные части кристаллов α-фазы,
которые образовались при температурах,
превышающих температуру t2,
не изменили своего начального состава,
средний состав кристаллов будет
соответствовать точке k2.
При понижении температуры средний
состав кристаллов α-твердого раствора
все более отклоняется от равновесного.
При температуре t3
он будет соответствовать не точке n1,
а точке k3.
Если через точки k1—k5
провести кривую, о
Рис. 15. Диаграмма состояния для
случая
неограниченной растворимости компонентов
А и В.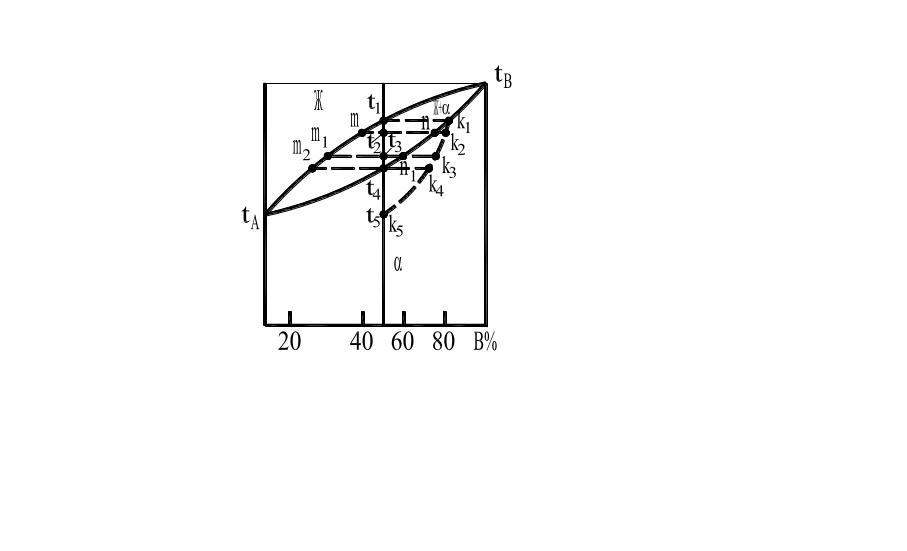
Следовательно, в неравновесных условиях сплав затвердевает ниже равновесной температуры затвердевания. Линию k1—k5 называют неравновесный солидус. каждый сплав при соей скорости охлаждения характеризуется своим неравновесным солидусом.
5. Дендритная (внутрикристаллитная) ликвация.
В результате неравновесной кристаллизации химический состав образующихся кристаллов твердого раствора по сечению оказывается переменным.
В процессе кристаллизации обычно образуются кристаллы дендритного типа, поэтому оси первого порядка, возникающие в начальный момент, обогащены более тугоплавким компонентом В. Слои кристалла и межосные пространства, кристаллизующиеся в последнюю очередь, будут обогащены компонентом А, понижающим температуру плавления сплава.
Такую неоднородность состава сплава внутри отдельных кристаллов называют внутрикристаллитной или дендритной ликвацией. Чем больше разность температур между солидусом и ликвидусом, тем больше разница по составу между жидкой и твердой фазами и тем сильнее проявляется этот вид ликвации.
Такому виду ликвации способствует быстрое охлаждение сплава. Дендритная ликвация ухудшает механические свойства сплава.
Дендритная ликвация может быть ослаблена продолжительным нагревом затвердевающего сплава при температурах, обеспечивающих высокую скорость диффузии (нагрев несколько ниже линии солидуса). Такой нагрев называется диффузионным отжигом или гомогенизацией и после него структура сплава состоит из однородных кристаллов.
6. Диаграммы состояния сплавов, образующих ограниченные твердые растворы.
В
Рис. 16. Диаграмма состояния сплавов
с эвтектическим превращением.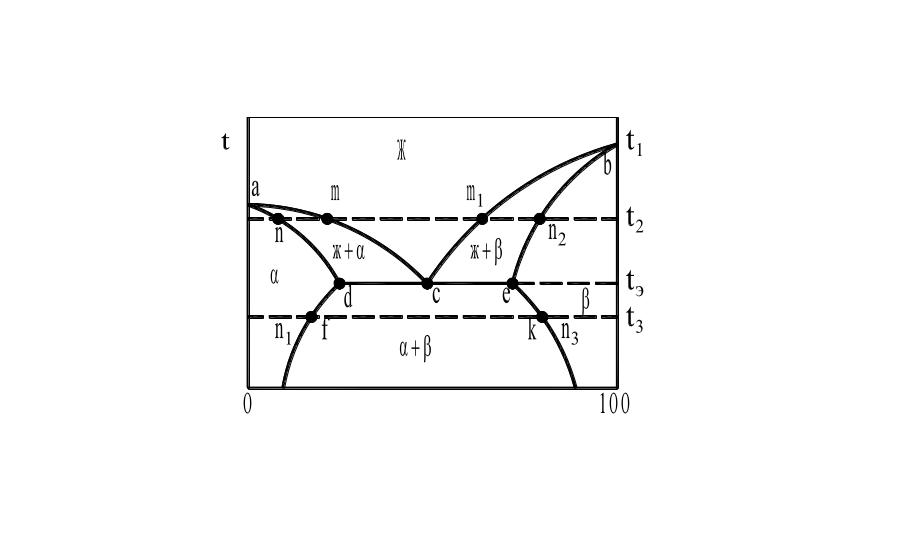
Как видно из рис. 16, при температуре t1 энергия Гиббса жидкой фазы ниже, чем энергия Гиббса α- и β-фаз, поэтому выше линии ликвидус acb устойчива лишь жидкая фаза.
Линия adceb—солидус. При температурах ниже линии солидус сплавы обладают меньшей энергией Гиббса в кристаллическом состоянии: в интервале концентраций of устойчив раствор α (твердый раствор компонента В в компоненте А), в интервале концентраций fk—смесь двух фаз α- и β-растворов и в интервале концентраций k100 одна фаза—β-раствор (твердый раствор компонента А в В).
М
Рис. 17. Кривые охлаждения и диаграмма
состояния сплавов, образующих
ограниченные твердые растворы и
эвтектику:
а-кривые охлаждения;
б-диаграмма состояния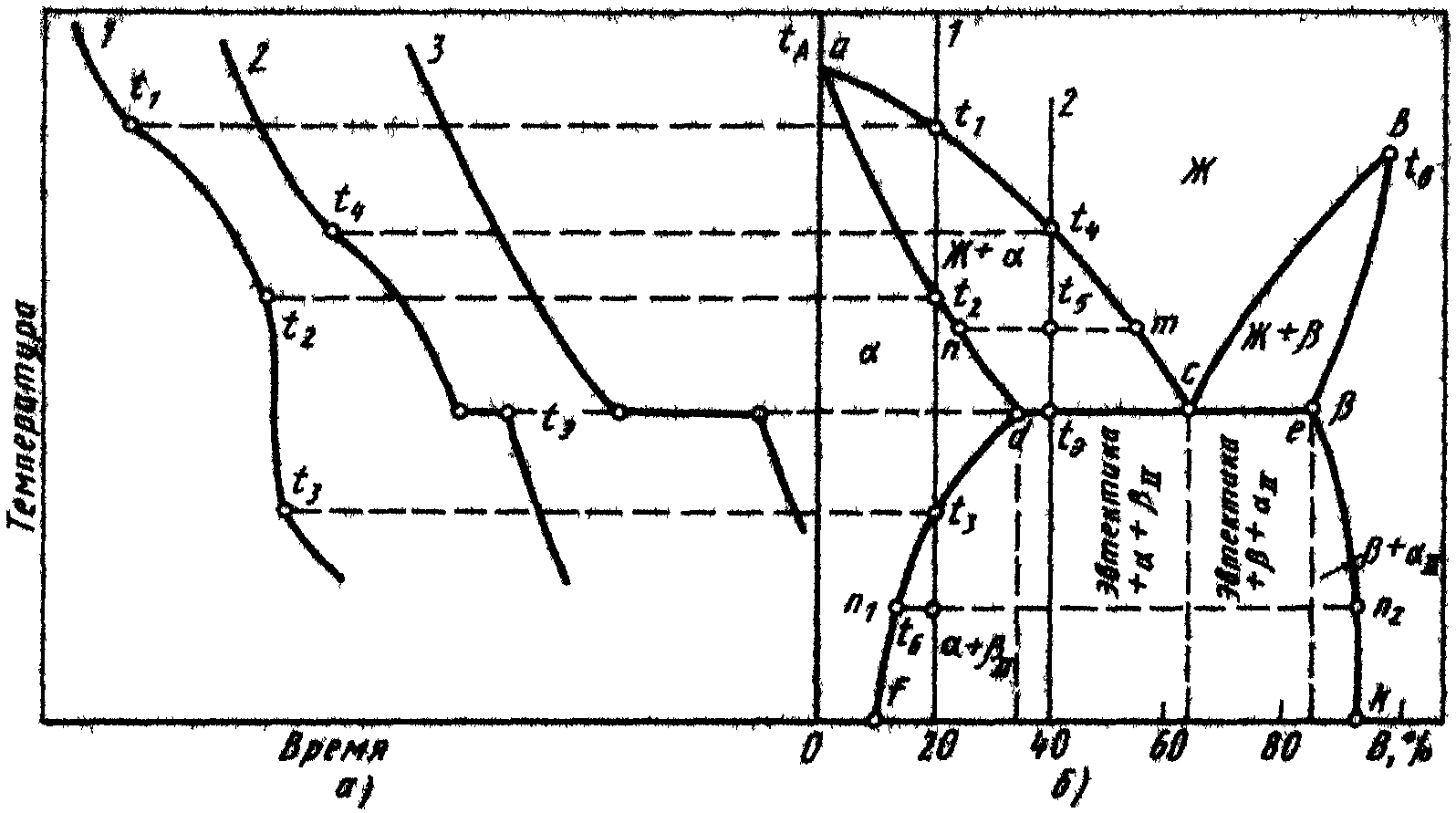
При температурах, соответствующих линии ac, из жидкого сплава выделяются кристаллы α-твердого раствора; а линии cb—кристаллы β-твердого раствора (Рис. 17.). Таким образом, линии ac и cb соответствуют температурам кристаллизации сплавов различного состава и показывают степень насыщенности жидкой фазы компонентами А и В, то есть являются линиями растворимости.
Точка d характеризует предельную растворимость компонента В в А, точка e – компонента А в В при температуре tэ, а точки f и k характеризуют предельную растворимость соответственно компонент В в А и А в В при нормальной температуре.
Таким образом, линия df характеризует изменение растворимости компонента В в А, а линия ek – изменение растворимости компонента А в В с изменением температуры. Эти линии называются линиями предельной растворимости.
Сплав, соответствующий точке с (55% В), затвердевает при постоянной температуре tэ.
При температуре несколько ниже tэ сплав насыщен α- и β-твердыми растворами, так как точка с принадлежит сразу двум ветвям ликвидуса (Рис. 17. б.). Поэтому при температуре tэ одновременно с жидким раствором сосуществуют предельно насыщенные кристаллы твердых растворов αd и βе, образующих гетерогенную структуру.
Сплавы, в которых происходит одновременная кристаллизация α- и β-фаз при постоянной и самой низкой для данной системы сплавов температуре, называют эвтектическими.
Структуру, состоящую из определенного сочетания двух или более твердых фаз, одновременно кристаллизовавшихся из жидкого сплава, называют эвтектикой.
Рассмотрим процесс кристаллизации некоторых сплавов. Сплавы, расположенные левее точки d (Рис. 17. б.) и правее точки е, кристаллизуются так же, как и сплавы с неограниченной растворимостью.
После затвердевания сплавы, лежащие левее точки d, состоят только из кристаллов α-твердого раствора, а сплавы, лежащие правее точки k, – из кристаллов β-твердого раствора.
Рассмотрим кристаллизацию доэвтектического сплава 2. При достижении температуры несколько ниже t4 в жидкости образуются кристаллы твердого раствора α. Процесс кристаллизации α-твердого раствора будет проходить в интервале температур, так как система имеет одну степень свободы (С=2+1-2=1).
Процесс выделения кристаллов α-твердого раствора будет продолжаться до температуры tэ. Количество жидкой и твердой фаз определяется по правилу отрезков. При достижении эвтектической температуры tэ кристаллы α достигают предельной концентрации (точка d) В в А, а жидкая фаза получает эвтектический состав (точка с). В этих условиях при температуре tэ из жидкой фазы одновременно кристаллизуются предельно насыщенные растворы αd и βе с образованием эвтектики: Жс→(αd+βе)/эвтектика.
Процесс кристаллизации эвтектики протекает при постоянной температуре tэ, так как согласно правилу фаз при одновременном существовании трех фаз постоянного состава (Жс, αd, βе) система нонвариантна (С=0). Следовательно, после затвердевания сплав состоит из первичных кристаллов α и эвтектики (α+β).
Кристаллизация заэвтектических сплавов, лежащих правее точки с, протекает так же, как и доэвтектических. Однако вместо кристаллов α-твердого раствора из жидкой фазы будут выделяться кристаллы твердого раствора β. Структура заэвтектических сплавов состоит из первичных кристаллов β-фазы и эвтектики (α+β).
Область диаграммы, расположенная между кривыми растворимости df и ek, принадлежит двухфазному состоянию—α+β-твердые растворы. В до- и заэвтектических сплавах фазы с понижением температуры меняют свой состав. Это связано с распадом кристаллов α и β-твердых растворов. При понижении температуры из α-фазы выделяются кристаллы βII-фазы (такое обозначение объясняется тем, что кристаллы выделяются не из жидкости, а из твердого раствора), а из β-фазы выделяется αII-фаза.
Состав α-фазы изменяется по линии df, а β-фазы – по линии ek. Если концентрация выбранного сплава находится между точками f и d, то в таком сплаве при температурах ниже линии df из α-твердого раствора выделяется βII-фаза. При распаде β-фазы в процессе охлаждения, то есть ниже линии ek, выделяется αII-фаза.
Разберем на примере сплава 1 превращения, связанные с распадом твердого раствора, вследствие уменьшения растворимости компонента В в компоненте А с понижением температуры.
Сплав 1 ниже температуры t2 состоит только из кристаллов α-твердого раствора. При дальнейшем охлаждении по достижении температуры t3 твердый раствор α оказывается насыщенным компонентом В; при более низких температурах растворимость второго компонента уменьшается, поэтому из α-твердого раствора начинает выделяется избыточный компонент в виде кристаллов βII.
При температурах ниже t3 сплав состоит из двух фаз: кристаллов α-твердого раствора и вторичных кристаллов β-твердого раствора. Состав кристаллов α-твердого раствора с понижением температуры изменяется по линии df, а кристаллов твердого раствора β – по линии ek (например, при температуре t6 состав α-фазы определяется точкой n1, а состав β-фазы – точкой n2, рис. 17, б.).
После окончательного охлаждения сплав состоит из кристаллов α-твердого раствора состава, отвечающего точке f, и вторичных кристаллов β-твердого раствора состава точки k.
Быстрым охлаждением можно подавить распад твердого раствора и переохладить его до низких температур (закалкой). Пересыщенный твердый раствор α неустойчив и при нагреве, а в некоторых случаях и при нормальной температуре начинает распадаться с выделением дисперсных частиц избыточной фазы.
Нередко при распаде твердого раствора вместо стабильной β-фазы образуется метастабильная βI-фаза, которая по структуре или составу является промежуточной между α- и β-фазами. Далее метастабильная фаза переходит в стабильную β-фазу. Распад пересыщенного твердого раствора, полученного путем закалки, связанный с упрочнением сплава, называется дисперсионным старением (твердением). Образовавшиеся при старении дисперсные частицы избыточных фаз имеют пластинчатое строение.
