
- •1. Макро- и микроструктура металлов. Методы исследования металлов.
- •2. Атомно-кристаллическая структура металлов. Виды кристаллических решеток.
- •3. Дефекты кристаллической решетки металлов.
- •Формирование структуры металлов при кристаллизации.
- •4. Гомогенная (самопроизвольная) кристаллизация.
- •5. Число центров кристаллизации. Величина зерна.
- •6. Гетерогенное образование зародышей. Модифицирование.
- •7. Строение металлического слитка.
- •8. Полиморфные превращения.
- •Фазы и микроструктура в металлических сплавах.
- •2. Химические соединения.
- •3. Механические смеси.
- •Формирование структуры сплавов при кристаллизации.
- •1. Процесс кристаллизации и фазовые превращения в сплавах.
- •2. Диаграммы фазового равновесия.
- •3. Диаграммы состояния сплавов, образующих неограниченные твердые растворы.
- •4. Неравновесная кристаллизация.
- •5. Дендритная (внутрикристаллитная) ликвация.
- •6. Диаграммы состояния сплавов, образующих ограниченные твердые растворы.
- •7. Ликвация по плотности.
- •8. Диаграммы состояния сплавов, компоненты которых имеют полиморфные превращения.
- •1. Компоненты и фазы в системе железо-углерод.
- •2. Диаграмма состояния железо-цементит (метастабильное равновесие).
- •3. Влияние углерода, постоянных примесей и легирующих элементов на свойства стали.
- •1. Теория термической обработки стали. Превращение ферритно-карбидной структуры в аустенит при нагреве.
- •2. Теория термической обработки стали. Рост зерна аустенита при нагреве.
- •2. Теория термической обработки стали. Влияние величины зерна на свойства сталей. Определение и выявление величины зерна.
- •3. Теория термической обработки стали. Перлитное превращение переохлажденного аустенита.
- •4. Теория термической обработки стали. Мартенситное превращение в сталях.
- •5. Влияние легирующих элементов на устойчивость переохлажденного аустенита. Превращение аустенита при непрерывном охлаждении.
- •6. Превращение мартенсита и остаточного аустенита при нагреве.
- •7. Влияние отпуска на механические свойства.
- •8. Виды отпускной хрупкости в легированных сталях.
- •9. Термическое и деформационное старение углеродистых сталей.
- •1. Технология термической обработки стали. Отжиг I рода.
- •2. Технология термической обработки стали. Отжиг II рода.
- •3. Технология термической обработки стали. Закалка, выбор температуры закалки.
- •4. Технология термической обработки стали. Продолжительность нагрева деталей для закалки, охлаждающие среды.
- •5. Технология термической обработки стали. Закаливаемость и прокаливаемость стали.
- •6. Технология термической обработки стали. Внутренние напряжения в закаленной стали.
- •7. Технология термической обработки стали. Способы закалки.
- •8. Технология термической обработки стали. Отпуск стали.
- •9. Краткая характеристика видов термомеханической обработки.
- •10. Технология термической обработки стали. Дефекты, возникающие при термической обработке.
- •1. Теория химико-термической обработки сталей. Понятие эффективной толщины диффузионного слоя.
- •2. Цементация. Образование цементованного слоя. Цементация в твердом и газовом карбюризаторе.
- •3. Азотирование. Технология процесса азотирования.
- •4. Нитроцементация и цианирование. Особенности процессов.
- •5. Борирование, силицирование. Виды диффузионного насыщения металлами.
- •Порошковые антифрикционные материалы на основе железа. Структура. Область применения. Технология получения деталей.
- •Полимеры и пластмассы. Их классификация и способы получения.
- •Неорганические стекла. Классификация и область применения.
3. Диаграммы состояния сплавов, образующих неограниченные твердые растворы.
Диаграмма состояния для случая полной взаимной растворимости компонентов A и B в жидком и твердом состояниях и изменение энергии Гиббса в зависимости от концентрации и температуры даны на рис. 13.
П
Рис. 13. Диаграмма состояния системы,
состоящей из двух компонентов,
неограниченно растворяющихся в жидком
и твердом состояниях, и энергия Гиббса
растворов при разных температурах.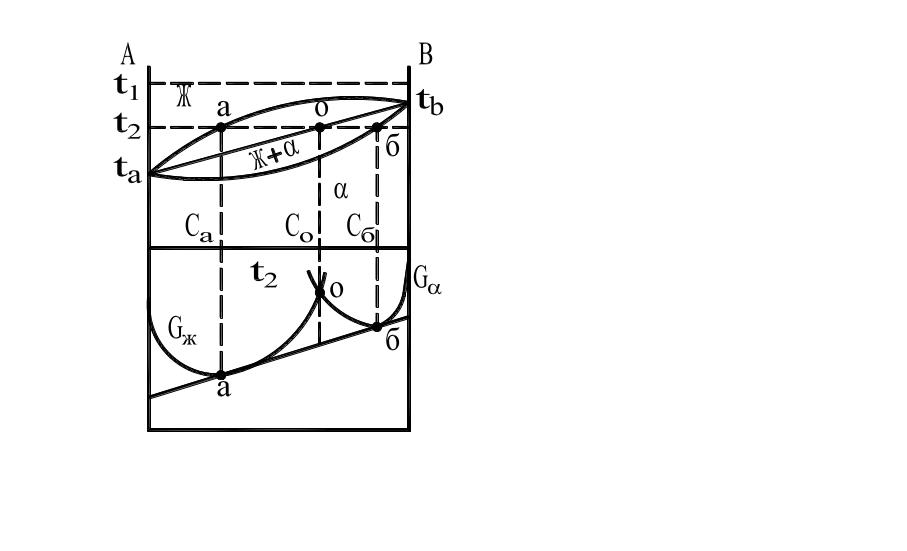
В области ниже линии tAбtB, называемой линией солидус, устойчив α-твердый раствор, так как его энергия Гиббса меньше энергии Гиббса жидкой фазы.
Между линиями ликвидус и солидус в равновесии находятся жидкая фаза и α-твердый раствор. При температуре t2 энергия Гиббса меняется с изменением состава по линии GжабGα. В интервале tACа устойчив жидкий раствор, а в интервале CбtB— α-твердый раствор.
В интервале CаCб равновесным является двухфазное состояние: жидкость состава точки а (Cа) и кристаллы α состава точки б (Cб). Энергия Гиббса этих сплавов определяется прямой аб, являющейся отрезком общей касательной к кривым изменения свободной энергии жидкого Gж и твердого Gα растворов.
П
Рис. 14. Построение диаграммы состояния
для случая неограниченной растворимости
компонентов А и В в твердом и
жидком состояниях:
а – кривые охлаждения; б – диаграмма
состояния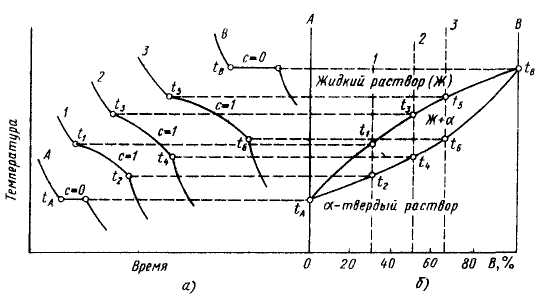
Температура охлаждаемого чистого компонента А равномерно понижается до tA (кривая А), при которой компонент А затвердевает. На кривой отмечается остановка (прямой участок), так как согласно правилу фаз только в этом случае при постоянной температуре могут существовать две фазы—твердая и жидкая (С=1+1-2=0). После затвердевания компонента А, когда Ф=1, температура снова равномерно понижается. Аналогично может быть рассмотрена кристаллизация и компонента B.
При охлаждении сплава 1 температура понижается до t1. При температуре t1 начинается процесс кристаллизации и на кривой охлаждения отмечается перегиб (критическая точка), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты кристаллизации.
Начиная от температуры t1, из жидкого сплава кристаллизуется α-твердый раствор. Процесс кристаллизации протекает при понижающейся температуре, так как согласно правилу фаз в двухкомпонентной системе при наличии двух фаз число степеней свободы будет равно единице (С=2+1-2=1).
При достижении температуры t2 сплав затвердевает, и при более низких температурах существует только α-твердый раствор. Аналогично затвердевают и другие сплавы.
Если найденные критические точки перенести на диаграмму, где по оси абсцисс нанесен состав сплава, а по оси ординат – температура, и одноименные критические точки соединить плавными кривыми, то получится диаграмма состояния системы сплавов А и В, образующих непрерывный ряд твердых растворов (Рис. 14. б.). Начало затвердевания сплавов происходит при температурах, соответствующих линии ликвидус tАt1t3t5tВ. Температура окончания кристаллизации соответствует линии солидус tАt2t4t6tВ. В интервале температур между линиями ликвидус и солидус существуют две фазы—жидкий сплав и α-твердый раствор.
