
- •3.Особенности генома эукариот.
- •3. Репрессия синтеза белков. Триптофановый и гистидиновый опероны
- •Багульник болотный - Ledum palustre.
- •Вороний глаз - Paris guadrifolia l., Ландыш майский - Convallaria majalis l.
- •Багульник болотный - Ledum palustre.
- •Вороний глаз - Paris guadrifolia l., Ландыш майский - Convallaria majalis l.
- •3. Репрессия синтеза белков. Триптофановый и гистидиновый опероны
- •79.Роль регуляторных белков в регуляции генной активности (репрессоры, активаторы).
- •Багульник болотный - Ledum palustre.
- •Вороний глаз - Paris guadrifolia l., Ландыш майский - Convallaria majalis l.
- •82.Изменение структурной организации хромосом. Хромосомные мутации.
- •Багульник болотный - Ledum palustre.
- •Вороний глаз - Paris guadrifolia l., Ландыш майский - Convallaria majalis l.
Билет 1
1. Морфологические и функциональные особенности зрелых гамет млекопитающих и человека.
Гамета (gamete): зародышевая клетка (спермий или яйцеклетка), содержащая гаплоидный набор хромосом , то есть имеющая по одному экземпляру каждой из хромосом.
При половом способе размножения потомство, как правило, имеет двух родителей. Каждый из родителей производит половые клетки. Половые клетки, или гаметы, обладают половинным или гаплоидным набором хромосом и возникают в результате мейоза . Таким образом, гамета (от греч. gamete - жена, gametes - муж) - зрелая репродуктивная клетка, содержащая гаплоидный набор хромосом и способная при слиянии с аналогичной клеткой противоположного пола образовать зиготу , при этом число хромосом становится диплоидным. В диплоидном наборе каждая хромосома имеет себе парную (гомологичную) хромосому. Одна из гомологичных хромосом происходит от отца, другая - от матери.. Женская гамета называется яйцеклеткой , мужская - сперматозоидом. Процесс образования гамет носит общее название - гаметогенез.
Всем животным свойственна оогамия - наличие крупных неподвижных яйцеклеток и мелких, обычно обладающих подвижностью сперматозоидов. Многие животные раздельнополы, остальные являются обоеполыми, или гермафродитами . У гермафродитных видов одни и те же особи образуют и яйцеклетки, и сперматозоиды. У раздельнополых животных самки производят яйцеклетки, самцы - сперматозоиды. Гермафродитами являются большинство плоских червей , малощетинковые кольчатые черви , большинство брюхоногих моллюсков. Раздельнополость характерна для большинства членистоногих и позвоночных. У раздельнополых животных и человека гермафродитизм иногда встречается как результат нарушений развития особи.
Половые клетки у таких многоклеточных, как губки или турбеллярии, могут возникать в любом участке тела. У большинства же организмов они образуются в специальных органах: у животных это гонады (греч. gone - семя), или половые железы, у растений - спорангии , у грибов - гаметангии . У некоторых организмов будущие половые клетки закладываются на самых ранних этапах дробления. Например, у аскариды уже на стадии 16 бластомеров выделяется половой зачаток, из которого впоследствии возникнут половые клетки. Ряд клеточных поколений от первичных половых клеток до гамет получил название зародышевого пути.
У эмбрионов всех позвоночных на ранней стадии развития определенные клетки обособляются как предшественники будущих гамет. Такие первичные половые клетки мигрируют в развивающиеся гонады ( яичники у самок, семенник и у самцов), где после периода митотического размножения претерпевают мейоз и дифференцируются в зрелые гаметы. В половых клетках перед мейозом активируются дополнительные гены, которые регулируют спаривание гомологичных хромосом, рекомбинацию и разделение рекомбинированных гомологичных хромосом в анафазе первого деления.
Яйцеклетки развиваются из первичных половых клеток , которые на ранней стадии развития организма мигрируют в яичник и превращаются там в оогонии . После периода митотического размножения оогонии становятся ооцитами первого порядка , которые, вступив в первое деление мейоза , задерживаются в профазе I на время, измеряемое сутками или годами в зависимости от вида организма. В период этой задержки ооцит растет и накапливает рибосомы, мРНК и белки, зачастую используя при этом другие клетки, включая окружающие вспомогательные клетки. Дальнейшее развитие (созревание яйцеклетки) зависит от полипептидных гормонов ( гонадотропинов ), которые, воздействуя на окружающие каждый ооцит вспомогательные клетки, побуждают их индуцировать созревание небольшой части ооцитов. Эти ооциты завершают первое деление мейоза, образуя маленькое полярное тельце и крупный ооцит второго порядка , который позже переходит в метафазу второго деления мейоза . У многих видов ооцит задерживается на этой стадии до тех пор, пока оплодотворение не инициирует завершение мейоза и начало развития эмбриона.
Спермий обычно представляет собой маленькую и компактную клетку, которая в высокой степени специализирована для функции внесения своей ДНК в яйцеклетку. В то время как у многих организмов весь пул ооцитов образуется еще на ранней стадии развития самки, у самцов после наступления половой зрелости в мейоз вступают все новые и новые половые клетки, причем каждый сперматоцит первого порядка дает начало четырем зрелым спермиям. Дифференцировка спермиев осуществляется после мейоза, когда ядра гаплоидны. Однако, поскольку при митотическом делении зрелых сперматогониев и сперматоцитов цитокинез не доводится до конца, потомки одного сперматогония развиваются в виде синцития . В связи с этим дифференцировка спермия может контролироваться продуктами хромосом от обоих родителей.
2.Генетическая гетерогенность популяций в человеческом обществе. Популяционно-статистический метод.
С помощью популяционно-статистического метода изучают наследственные признаки в больших группах населения, в одном или нескольких поколениях. Существенным моментом при использовании этого метода является статистическая обработка получаемых данных. Этим методом можно рассчитать частоту встречаемости в популяции различных аллелей гена и разных генотипов по этим аллелям, выяснить распространение в ней различных наследственных признаков, в том числе заболеваний. Он позволяет изучать мутационный процесс, роль наследственности и среды в формировании фенотипического полиморфизма человека по нормальным признакам, а также в возникновении болезней, особенно с наследственной предрасположенностью. Этот метод используют и для выяснения значения генетических факторов в антропогенезе, в частности в расообразовании.
При статистической обработке материала, получаемого при обследовании группы населения по интересующему исследователя признаку, основой для выяснения генетической структуры популяции является закон генетического равновесия Харди — Вайнберга. Он отражает закономерность, в соответствии с которой при определенных условиях соотношение аллелей генов и генотипов в генофонде популяции сохраняется неизменным в ряду поколений этой популяции (см. разд. 10.2.3, т.2). На основании этого закона, имея данные о частоте встречаемости в популяции рецессивного фенотипа, обладающего гомозиготным генотипом (аа), можно рассчитать частоту встречаемости указанного аллеля (а) в генофонде данного поколения. Распространив эти сведения на ближайшие поколения, можно предсказать частоту появления в них людей с рецессивным признаком, а также гетерозиготных носителей рецессивного аллеля.
Математическим выражением закона Харди — Вайнберга служит формула (рА. + qa)2, где р и q — частоты встречаемости аллелей А и а соответствующего гена. Раскрытие этой формулы дает возможность рассчитать частоту встречаемости людей с разным генотипом и в первую очередь гетерозигот — носителей скрытого рецессивного аллеля: p2AA + 2pqAa + q2аа. Например, альбинизм обусловлен отсутствием фермента, участвующего в образовании пигмента меланина и является наследственным рецессивным признаком. Частота встречаемости в популяции альбиносов (аа) равна 1:20 000. Следовательно, q2 = 1/20 000, тогда q = 1/141, up = 140/141. В соответствии с формулой закона Харди — Вайнберга частота встречаемости гетерозигот = 2pq, т.е. соответствует 2 х (1/141) х (140/141) = 280/20000 = 1/70. Это означает, что в данной популяции гетерозиготные носители аллеля альбинизма встречаются с частотой один на 70 человек.
Анализ частот встречаемости разных признаков в популяции в случае их соответствия закону Харди — Вайнберга позволяет утверждать, что признаки обусловлены разными аллелями одного гена. Так, например, установлено, что в США 29,16% белого населения имеют группу крови М, 49,58%—группу MN, 21,26%—группу N. Эти частоты разных фенотипов соответствуют формуле p2М + 2pqMN + q2N. Следовательно, эти три варианта признака обусловлены сочетанием двух аллелей одного гена, взаимодействующих по типу кодоминирования: группа М — LmLm, группа N — LnLn, группа MN—LmLn.
3.Паразитизм, как биологический феномен. Специфика среды обитания паразитов.
Всякий организм живет в определенной среде, в которой кроме него обитают и другие существа. Любое живое существо находится в тесной зависимости от окружающей среды, к обитанию в которой оно приспособилось в процессе эволюционного формирования соответствующего вида.
В отношении факторов питания всех животных можно разделить на три группы: - плотоядных, или животных, которые пожирают другие организмы или даже себе подобных (хищные); - животных, питающихся падалью, разлагающимися органическими веществами (личинки трупной мухи, комнатной мухи, некоторые млекопитающие и птицы); - животных-паразитов, которые питаются за счет соков тканей тела или переваренной пищей живых хозяев.
Хищники, нападая на добычу, убивают и пожирают ее. Паразиты же пользуются своими хозяевами многократно в течение всей жизни или жизни своих хозяев. Поэтому паразиты или вовсе не губят своего хозяина, или же не приводят к его смерти в течение продолжительного срока вследствие вызываемого ими заболевания.
Паразитизм - это форма сожительства, при которой один организм - паразит живет за счет организма другого вида - хозяина.
Паразитизм - это форма сожительства двух генетически разнородных организмов разных видов, при которой один организм (паразит) использует другого (хозяина) как источник питания и среду существования, причиняя ему вред, но, как правило, не уничтожая его.
Формы паразитизма чрезвычайно разнообразны. Различают облигатный (постоянно встречающийся, обязательный) и факультативный (возможный, необязательный), временный и постоянный, истинный и ложный, экто- и эндопаразитизм.
Паразитизм широко распространен в природе. Он встречается почти во всех типах животного царства. Особенно много паразитов имеется в типах простейших, плоских и круглых червей, членистоногих. Согласно данным В. А. Догеля (1947 г.) в природе около 60-65 тыс. видов являются животными-паразитами. Широкое распространение и разнообразие видов паразитизма позволяет считать, что эта форма сожительства возникла в природе в различных систематических группах животных независимо одна от другой.
Билет 2
В1.Оплодотворение, его формы и биологическая функция. Моно- и полиспермия.
Половой процесс, или оплодотворение, или амфимиксис (др.-греч. ἀμφι- — приставка со значением обоюдности, двойственности и μῖξις — смешение) — процесс слияния гаплоидных половых клеток, или гамет, приводящий к образованию диплоидной клетки зиготы. Не следует смешивать это понятие с половым актом (встречей половых партнёров у многоклеточных животных).
Половой процесс закономерно встречается в жизненном цикле всех организмов, у которых отмечен мейоз. Мейоз приводит к уменьшению числа хромосом в два раза (переход от диплоидного состояния к гаплоидному), половой процесс — к восстановлению числа хромосом (переход от гаплоидного состояния к диплоидному).
Различают несколько форм полового процесса:
изогамия — гаметы не отличаются друг от друга по размерам, подвижны, жгутиковые или амебоидные;
анизогамия (Гетерогамия) — гаметы отличаются друг от друга по размерам, но оба типа гамет (макрогаметы и микрогаметы) подвижны и имеют жгутики;
оогамия — одна из гамет (яйцеклетка) значительно крупнее другой, неподвижна, деления мейоза, приводящие к её образованию, резко асимметричны (вместо четырёх клеток формируется одна яйцеклетка и два абортивных «полярных тельца»); другая (спермий, или сперматозоид) подвижна, обычно жгутиковая или амебоидная.
Биологическое значение амфимиксиса непосредственно связано с биологической сущностью определенных сторон процесса оплодотворения. Дарвин, открывший «великий закон природы», говорил о прогрессивном значении появления полового процесса в истории органического мира, рассматривая при этом перекрёстное опыление как источник обогащения наследственности. Благодаря бипариентальному наследованию (материнское — от яйцеклетки и отцовское — от спермия) в результате амфимиксиса получаются более жизнеспособные организмы, обладающие более широким спектром изменчивости по сравнению с апомиктичными растениями.
В2 Методы в генетике человека. Молекулярно-генетические методы (исследование ДНК). Генетическое тестирование. Генетическое прогнозирование.
Молекулярно-генетические методы - большая и разнообразная группа методов, предназначенная для выявления вариаций (повреждений) в структуре участка ДНК (аллеля, гена, региона хромосомы) вплоть до расшифровки первичной последовательности оснований. В основе этих методов лежат генно-инженерные манипуляции с ДНК и РНК. Исходным этапом всех молекулярно-генетических методов является получение образцов ДНК. Источником геномной ДНК могут быть любые ядросодержащие клетки. На практике чаще используют лейкоциты, хорион, амниотические клетки, культуры фибробластов. Возможность проведения молекулярно-генетического анализа с небольшим количеством легкодоступного биологического материала является методическим преимуществом методов данной группы. Выделенная ДНК одинаково пригодна для проведения различных исследований и может долго сохраняться в замороженном виде. Во многих случаях для успешной диагностики болезни достаточно исследовать небольшой фрагмент генома. Выделение таких фрагментов стало возможным благодаря открытию ферментов - рестриктаз, которые разрезают молекулу ДНК на фрагменты в строго определенных местах.
Применение этих ферментов в эксперименте дает возможность получить относительно короткие фрагменты ДНК, в которых легко можно определить последовательность нуклеотидов. Получение достаточного количества таких фрагментов осуществляется путем амплификации (умножения) ДНК при помощи полимеразной цепной реакции. Различают прямую и косвенную ДНК-диагностику моногенных наследственных болезней. При прямой диагностике предметом анализа являются мутации гена. В ДНК-диагностике в настоящее время используются разнообразные прямые методы. Наиболее просто обнаруживаются мутации, изменяющие длину амплифицированных фрагментов ДНК, которые выявляются при электрофоретическом анализе. Для выявления точковых мутаций, небольших делеций и инверсий в исследуемых генах используют методы, при помощи которых можно проанализировать уникальную последовательность ДНК. Примером может служить метод секвенирования - определение нуклеотидной последовательности ДНК. Любые типы мутаций могут быть обнаружены путем прямого секвенирования мутантной ДНК. Для некоторых генов, имеющих небольшие размеры, этот метод с успехом применяется как основной метод сканирования мутаций. Главное преимущество прямых методов диагностики - почти 100 % эффективность.
Косвенное выявление мутаций применяется в тех случаях, когда нуклеотидная последовательность гена еще не известна, но имеется представление о положении гена на генетической карте. Косвенная ДНК-диагностика сводится к анализу полиморфных генетических маркеров у больных и здоровых членов семьи. Маркеры должны быть расположены в том хромосомном регионе, где и ген болезни. Такими маркерами могут быть участки ДНК, существующие в популяции в нескольких аллельных вариантах. Отличия могут быть по составу нуклеотидов, по числу динуклеотидных повторов. На основе вариабельности маркерных участков ДНК можно дифференцировать материнское или отцовское происхождение конкретного варианта маркера, сцепленного с геном болезни. Благодаря анализу полиморфных генетических маркеров можно определить и проследить в поколениях хромосому, несущую патологический ген. Технические приемы в косвенной диагностике те же, что и в прямой диагностике (получение ДНК, электрофорез и другие). Главный недостаток косвенных методов диагностики - обязательное предварительное изучение генотипа как минимум одного пораженного родственника.
В3.Экологические основы выделения групп паразитов. Классификация паразитических форм животных.
ПАРАЗИТЫ И ИХ ХАРАКТЕРИСТИКА
"Паразиты - это такие организмы, которые используют другие живые организмы в качестве источника пищи и среды обитания, возлагая при этом частично или полностью на своих хозяев задачу регуляции своих взаимоотношений с окружающей внешней средой" (Догель В. А., 1947). Паразитов в зависимости от среды обитания делят на две большие группы: экто- и эндопаразиты.
К эктопаразитам относят животных, обитающих на теле человека. К ним относятся, в основном, членистоногие. Эктопаразиты могут быть постоянными (например, вши), если весь жизненный цикл проводят на покровах тела животного, и временными (клещи, комары, мухи и др.), которые находятся на теле человека только в момент питания (сосания крови).
Эндопаразитов в зависимости от локализации в организме человека классифицируют на: - внутриклеточных (лейшмании, плазмодии, токсоплазма); - тканевых (дизентерийная амеба, трипаносомы, балантидий, шистосомы, филярии, ришта, личинки трихинеллы, чесоточный зудень и др.); - внутриорганных (описторхис, клонорхис, фасциола, парагонимус и др.); - полостных (свиной и бычий цепни, широкий лентец, аскарида, острица, анкилостома, власоглав и др).
Все эндопаразиты являются постоянными паразитами человека. Вообще ни один орган и ни одна ткань не застрахованы от возможности поселения в них паразита. Один и тот же паразит может жить в различных органах своего хозяина (эхинококк, финки свиного цепня). Некоторые паразиты могут мигрировать по телу хозяина, пока не достигнут окончательного места обитания (аскарида, некатор, анкилостома).
Когда речь идет о паразитизме, то всегда подразумевается два или несколько организмов разных видов, один из которых является паразитом, а другой - его хозяином. Паразитов, которые инвазируют и развиваются в теле одного хозяина, называют моноксенными или однохозяинными. Например, карликовый цепень, острица паразитируют только у человека. Большинство моноксенных гельминтов (аскарида, власоглав, анкилостома и др.) для завершения цикла развития обязательно нуждаются в выходе оплодотворенного яйца из хозяина во внешнюю среду.
Эндопаразиты, которые для завершения своего жизненного цикла нуждаются в двух и более разных хозяевах, называются 2 0гетероксенными или многохозяинными (малярийный плазмодий, свиной и бычий цепни, сосальщики и др.)
Явление паразитизма носит всеобщий характер в природе. Известно свыше 50 тыс. видов паразитов, 500 из которых могут паразитировать у человека.
Паразиты имеются среди представителей типа Простейших. Так, в классе Саркодовых имеются паразитические амебы; в классе Жгутиковых - лейшмании, трипаносомы, лямблии, трихомонады; в классе Споровиков - возбудители малярии, токсоплазма; в классе Инфузорий - балантидий. В типе Плоских червей паразитами человека являются сосальщики и ленточные черви. В типе Круглых червей имеется также много паразитов животных и растений. Наконец, в типе Членистоногих имеются паразиты в классах Паукообразных и Насекомых. Биологические особенности жизненных циклов гельминтов, относящихся к эндопаразитам, положены К. И. Скрябиным и Р. С. Шульцем (1931) в основу их эпидемиологической классификации.
В настоящее время всех гельминтов делят на геогельминтов, биогельминтов и контактных гельминтов.
Геогельминты - это черви-паразиты, у которых развитие инвазионной личинки из оплодотворенного яйца происходит через немытые овощи, фрукты, на которых находятся инвазионные яйца (например, аскариды, власоглава), либо личинками при непосредственном контакте с почвой (например, анкилостомы, некатора).
Биогельминты - это черви паразиты, у которых жизненные циклы осуществляются обязательно со сменой хозяев (все трематоды, цестоды, филярии, трихинелла и др.)
Контактные гельминты - это такие черви-паразиты, цикл развития которых может полностью проходить в организме человека без выхода во внешнюю среду (карликовый цепень, острица).
Билет3
В1.Закономерности овогенеза у млекопитающих и человека.
Первая фаза раневого процесса — фаза воспаления — характеризуется травматическим отеком тканей, повышением сосудистой проницаемости, ацидозом, миграцией лейкоцитов, тучных клеток и макрофагов. Происходит очищение раны путем фагоцитоза и лизиса некротизированных тканей.
Во второй фазе раневого процесса — фазе регенерации — происходит развитие грануляционной ткани, постепенно заполняющей раневой дефект. Основными структурами этой ткани являются фибробласты, межклеточное вещество и капилляры. Клетки фиброблас-тического дифферона грануляционной ткани отличаются от фибробластов нормальной соединительной ткани высокой функциональной активностью. Они синтезируют белки и гликозаминоглнканы, образуя коллагеновые волокна. В развитии и созревании грануляционной ткани важную роль играют также макрофаги, тучные и плазматические клетки. Грануляционная ткань впоследствии преобразуется в рубцовую соединительную ткань.
Третья фаза раневого процесса — фаза реорганизации рубца — характеризуется прогрессирующим уменьшением числа кровеносных сосудов и клеточных элементов (фибробластов, макрофагов, тучных клеток) при явлениях нарастания общей массы коллагеновых волокон. Параллельно с созреванием грануляционной ткани и ее превращением в рубцовую ткань происходит эпителизация раны. Эпителизация раны и созревание грануляционной ткани строго соответствуют во времени.
В зависимости от характера и величины ранения, особенностей реактивности организма и других условий раневой процесс протекает по-разному. При небольшом объеме поражения имеет место заживление раны первичным натяжением. Воспаление и замещение дефекта в тканях следуют непосредственно за их травматическим отеком и не сопровождаются нагноением. К концу первой недели раневой процесс в основном завершается. Если же объем поражения велик и края раны оказываются на более или менее значительном расстоянии друг от друга, то заживление раны осуществляется через нагноение с образованием хорошо развитой грануляционной ткани с последующим ее рубцеванием. Заживление раны происходит вторичным натяжением со значительной продолжительностью фаз раневого процесса.
Заживление раны первичным и вторичным натяжением имеет количественные, но не качественные различия. Механизмы регенерации при этом принципиально сходны и включают воспаление, разрастание соединительной ткани, эпителизацию. Знание ключевых звеньев регенерацbонного процесса позволяет целенаправленно вести поиск средств регуляции заживления ран и разработке способов тканевой терапии.
Развитие половых клеток.
Развитие половых клеток называется прогенезом, или гаметогенезом, и происходит в половых железах. Суть гаметогенеза состоит в образовании из диплоидных стволовых предшественников половых клеток высокодифференцированных клеток (сперматозоидов и яйцеклеток) с гаплоидным набором хромосом.
Развитие мужских половых клеток — сперматогенез, включает четыре фазы: размножения, роста, созревания, формирования. В результате сперматогенеза возникают клетки сперматозоиды (спермин), содержащие Х- или Y-половую хромосому.
Развитие женских половых клеток — овогенез, состоит из трех фаз: размножения, роста, созревания. В результате овогенеза образуются яйцеклетки (овоциты), содержащие Х-половую хромосому.
В основном мужской и женский гаметогенезы протекают однотипно. В фазе размножения исходные половые клетки (сперматогонии — в сперматогенезе и овогонии — в овогенезе) в ходе клеточного цикла синтезируют ДНК и митотически делятся; их размножение протекает на основе общих закономерностей, характерных и для соматических клеток. В процессе сперматогенеза делится только часть сперматогонии, так называемые светлые сперматогонии типа А, которые являются полустволовыми клетками, дающими начало сперматогониям типа В. Сперматогонии типа В проходят несколько митотических циклов, при этом не происходит полной цитотомии сперматогонии и они остаются связанными цитоплазматическими мостиками. Фаза размножения сперматогонии контролируется естественными митогенами — гормоном аденогипофиза фоллитропином и интерлейкином-1, вырабатываемым клетками Сертоли и клетками Лейдига (интерстициальными эндокриноцитами) яичек.
В2.Методы в генетике человека. Биохимический метод. Дерматоглифика.
В отличие от цитогенетического метода, который позволяет изучать структуру хромосом и кариотипа в норме и диагностировать наследственные болезни, связанные с изменением их числа и нарушением организации, наследственные заболевания, обусловленные генными мутациями, а также полиморфизм по нормальным первичным продуктам генов изучают с помощью биохимических методов.
Впервые эти методы стали применять для диагностики генных болезней еще в начале XX в. В последние 30 лет их широко используют в поиске новых форм мутантных аллелей. С их помощью описано более 1000 врожденных болезней обмена веществ. Для многих из них выявлен дефект первичного генного продукта. Наиболее распространенными среди таких заболеваний являются болезни, связанные с дефектностью ферментов, структурных, транспортных или иных белков.
Дефекты структурных и циркулирующих белков выявляются при изучении их строения. Так, в 60-х гг. XX в. был завершен анализ (3-глобино-вой цепи гемоглобина, состоящей из 146 аминокислотных остатков. Установлено большое разнообразие гемоглобинов у человека, связанное с изменением структуры его пептидных цепей, что нередко является причиной развития заболеваний (см. § 4.1).
Дефекты ферментов устанавливают путем определения содержания в крови и моче продуктов метаболизма, являющихся результатом функционирования данного белка. Дефицит конечного продукта, сопровождающийся накоплением промежуточных и побочных продуктов нарушенного метаболизма, свидетельствует о дефекте фермента или его дефиците в организме (см. § 4.1).
Биохимическую диагностику наследственных нарушений обмена проводят в два этапа. На первом этапе отбирают предположительные случаи заболеваний, на втором —более точными и сложными методами уточняют диагноз заболевания. Применение биохимических исследований для диагностики заболеваний в пренатальном периоде или непосредственно после рождения позволяет своевременно выявить патологию и начать специфические медицинские мероприятия, как, например, в случае фенилкетонурии.
Для определения содержания в крови, моче или амниотической жидкости промежуточных, побочных и конечных продуктов обмена кроме качественных реакций со специфическими реактивами на определенные вещества используют хроматографические методы исследования аминокислот и других соединений.
В3.Популяционный уровень взаимодействия паразитов и хозяев. Типы регуляции и механизмы устойчивости системы «паразит-хозяин».
С представлением о паразите неразрывно связано понятие о его хозяине.
Хозяин паразита - это организм животного или человека, в теле которого обитает паразит временно или постоянно и размножается половым или бесполым путем.
Смена хозяина обусловлена стадийностью жизненного цикла паразита. Личиночные стадии, как правило, развиваются в организме одного вида, а половозрелые - другого вида. Перемена хозяев паразитами, в основном, обусловлена чередованием поколений, размножающихся половым или бесполым способами.
Хозяин, в теле которого паразит достигает половозрелой стадии и размножается половым путем, называется 2 0окончательным или дефинитивным 2 0хозяином. Так, человек является окончательным хозяином для большинства видов цестод, трематод, нематод.
Хозяин, в теле которого обитает личиночная стадия паразита, получил название 2 0промежуточного. Человек является промежуточным хозяином для малярийных плазмодиев, эхинококка, альвеококка и др. Для некоторых паразитов (описторхис, парагонимус, широкий лентец и др.) для завершения цикла развития требуется не один, а два (или несколько) промежуточных хозяев. Второго промежуточного хозяина называют дополнительным. Так, у описторхиса два промежуточных хозяина: первый - моллюск Bithynia leachi, дополнительный многие виды карповых рыб (плотва, линь, язь, карп, лещ, вобла, сазан и др.).
У многих паразитов перемена хозяев не связана с чередованием поколений, но осуществляется по ходу развития одной и той же особи паразита. Например, степной клещ - переносчик клещевого сыпного тифа в Сибири (в состоянии личинки и нимфы нападает на различных мелких грызунов, а во взрослом состоянии - на крупных млекопитающих или человека).
Практически один и тот же хозяин может иметь большое количество паразитов одного вида (малярийные плазмодии) или разных видов. У человека могут одновременно паразитировать острицы, власоглав, кишечные амебы, плазмодии и т.д.
Хозяева, у которых паразиту обеспечивается наилучшая выживаемость, быстрый рост и наибольшая плодовитость, получили название облигатных, или 2 0обязательных. Человек является облигатным хозяином для дизентерийной амебы, аскариды, анкилостомы и других паразитов.
Хозяин, в теле которого паразит может обитать, но не полностью адаптироваться, называется факультативным. Например, человек является облигатным хозяином для лентеца широкого. Однако эта цистода может паразитировать и в организме лисицы, но ее размеры при этом не достигают большой длины и срок жизни не превышает двух месяцев.
Организм, в котором не происходит развитие паразита, а наблюдается лишь его накопление в инвазионной стадии, называется 2 0резервуарным хозяином. Последний кумулирует возбудителя и сохраняет инвазию, что способствует большей зараженности окончательного хозяина. Например, щука, поедая дополнительного хозяина широкого лентеца (карповых рыб), накапливает в своих тканях личиночные стадии (плероцеркоиды) паразита и таким образом выполняет функцию резервуарного хозяина.
Билет 4
В1.Закономерности сперматогенеза у млекопитающих и человека.
Семенник состоит из нескольких тысяч цилиндрических семенных канальцев, в каждом из которых развиваются миллионы сперматозоидов. Стенки этих канальцев выстланы первичными, неспециализированными половыми клетками — сперматогониями. В течение эмбрионального развития и в детском возрасте сперматогонии делятся митотически, давая начало дополнительным сперматогониям, что ведет к росту семенника. После наступления половой зрелости некоторые из сперматогониев вступают в сперматогенез, состоящий из серии превращений, ведущих к образованию зрелых сперматозоидов. Другие сперматогонии продолжают делиться митотически и производят новые сперматогонии для последующих сперматогенезов. У большинства диких животных имеется определенный период, приходящийся на весну или на осень, когда семенники увеличиваются в размерах и в них происходит сперматогенез. В промежутке же между этими периодами семенник имеет небольшие размеры и содержит только сперматогонии. У человека и у большинства домашних животных сперматогенез после достижения половой зрелости протекает круглый год. Сперматогенез начинается с того, что сперматогонии вырастают и превращаются в более крупные клетки, известные под названием сперматоцитов первого порядка. Последние приступают к первому мейотическому делению, дающему начало двум одинаковым по величине клеткам — сперматоцитам второго порядка. В них происходит второе мейотическое деление, в результате которого образуются четыре одинаковые сперматиды. Сперматида — сферическая клетка, содержащая значительное количество цитоплазмы, — представляет собой зрелую гамету, так как она имеет гаплоидное число хромосом, но для того, чтобы превратиться в функционирующий сперматозоид, она должна приобрести обтекаемую форму, которая дает ей возможность плавать и встретиться с яйцом. Это связано со сложными процессами роста и видоизменения (не сопровождающимися, однако, клеточным делением). Ядро уменьшается в размерах и превращается в головку сперматозоида, который сбрасывает большую часть своей цитоплазмы. Некоторые из телец Гольджи собираются у переднего конца сперматозоида, образуя так называемую акросому, которая, возможно, помогает сперматозоиду прокалывать оболочку яйцеклетки. Обе имеющиеся в сперматиде центриоли перемещаются и располагаются непосредственно позади ядра. В ядре появляется небольшое углубление, и одна из центриолей — проксимальная — располагается в нем под прямым углом к оси сперматозоида. Вторая — дистальная — центриоль, лежащая позади проксимальной, дает начало осевой нити хвоста. Подобно осевым нитям жгутиков, эта нить состоит из двух продольных волокон, расположенных в середине, и окружающего их кольца из 9 пар продольных волокон. Митохондрии передвигаются к месту соединения головки и хвоста и образуют небольшой промежуточный участок (шейку), доставляющий энергию для биения хвостика. Большая часть цитоплазмы сперматиды отбрасывается; остается лишь тонкий слой, окружающий митохондрии в средней части и осевую нить хвостика. Сперматозоиды разных видов животных сильно различаются между собой. Почти все они имеют хвостик, но его величина и форма, так же как и особенности строения головки и шейки, могут быть весьма разнообразны. У некоторых животных, например у паразитического круглого червя аскариды, сперматозоиды не имеют хвостов и перемещаются при помощи амебоидных движений. У крабов и раков сперматозоиды необычные — у них нет хвоста, но на головке имеется три остроконечных выроста, которые прикрепляются к поверхности яйца и прочно удерживают сперматозоид. Шейка такого сперматозоида раскручивается подобно пружине и проталкивает его ядро в цитоплазму яйца, осуществляя таким образом оплодотворение.
В2.Методы в генетике человека. Близнецовый метод.
Исследование генетических закономерностей на близнецах. Монозиготными близнецами называют индивидов, выросших из одной зиготы, т. е. обладающих идентичными генотипами. Дизиготные близнецы развиваются вследствие оплодотворения двух яйцеклеток, имеющих с генетической точки зрения, 50 % общих генов, т. е. сходные как братья и сестры. При близнецовом методе исследования проводят сопоставление монозиготных близнецов с дизиготными, а также монозиготных близнецов. При диагностике близнецовости используют метод сходства (сопоставление по внешним морфологическим признакам - пигментация кожи, волос, форма носа, губ, ушных раковин и т. д.), а также анализируют некоторые моногенные признаки - эритро- и лейкоцитарные антигены, группа белков крови, группы крови и т. д. Какой-либо качественный признак (заболевание) может встречаться у обоих близнецов (конкордантность) или у одного из них (дискордантность). Сопоставление степени парной конкордантности у моно- и дизиготных близнецов дает приблизительный ответ на вопрос о соотношении роли наследственности и среды в развитии заболевания. Если доминирующую роль в возникновении заболевания играет наследственность, то конкордантность у монозиготных близнецов выше, чем у дизиготных. Если в развитии болезни определенную роль играют негененетические факторы, то один из монозиготных близнецов может быть больным, другой здоровым. Следует все же учитывать, что определение роли среды и наследственности с помощью близнецового метода в формировании того или иного заболевания является сложным вопросом и требует более детального рассмотрения. Поэтому здесь следует упомянуть о недостатках близнецового метода, имеющих много биологических и социальных причин.
Классический близнецовый метод: в этом случае используется такая схема эксперимента, при которой выраженность исследуемого признака сопоставляется в парах и близнецов и оценивается уровень внутрипарного сходства партнеров.
Метод контрольного близнеца: этот метод используется на выборках МЗ близнецов. Так как МЗ близнецы весьма сходны по многим признакам, то из партнеров МЗ пар можно составить две выборки, уравненные по большому числу параметров. Такие выборки используют для исследования влияния конкретных средовых воздействий на изменчивость признака. При этом отобранная часть близнецов (по одному из каждой пары) подвергается специфическому воздействию, другая же часть является контрольной группой. Поскольку в эксперименте участвуют генетически идентичные люди, то этот способ можно считать моделью для изучения воздействия различных средовых факторов на одного и того же человека.
Лонгитюдное близнецовое исследование: в этом случае проводится длительное наблюдение одних и тех же близнецовых пар. Фактически это сочетание классического близнецового метода с лонгитюдным. Широко используется для изучения влияния средовых и генетических факторов в развитии.
Метод близнецовых семей: является сочетанием семейного и близнецового метода. При этом исследуются члены семей взрослых близнецовых пар. Дети МЗ близнецов по генетической конституции являются как бы детьми одного человека. Метод широко используется при изучении наследственных причин ряда заболеваний.
Исследование близнецов как пары: предполагает исследование специфических близнецовых эффектов и особенностей внутрипарных отношений. Используется как вспомогательный метод для проверки справедливости гипотезы о равенстве средовых условий для партнеров МЗ и ДЗ пар.
Сопоставление близнецов с неблизнецвми.
Также вспомогательный метод, позволяющий оценить существенность разницы между близнецами и неблизнецами. Если разница между близнецами и остальными людьми не является значимой, то близнецы и остальные люди относятся к одной генеральной выборке и, следовательно, результаты бллизнецовых исследований можно распространять на всю популяцию. Так, было отмечено некоторое отставание членов близнецовых пар в развитии от одиночнорожденных. Особенно эта разница заметна в раннем возрасте. Но сопоставление результатов исследования членов близнецовых пар, чей партнер умер в раннем детстве и одиночнорожденных не выявил существенной разницы в уровне развития. То есть особенности развития близнецов обусловлены не столько трудностями эмбрионального развития, сколько с особенностями воспитания близнецов как пары (семейные трудности при рождении близнецов, замкнутость близнецов в паре и т.п.). Таким образом, близнецы несколько отличаются от всей популяции, но с возрастом эта разница заметно сглаживается и близнецы по большей части становятся сопоставимы с остальной популяцией.
Метод разлученных близнецов: Из-за особенностей развития ДЗ и МЗ пар близнецов классический близнецовый метод и его разновидности принято считать “нежесткими” экспериментами: в них невозможно однозначно разделить влияние генетических и средовых факторов, так как в силу ряда причин условия развития близнецов по целому ряду причин оказываются несопоставимыми.
Метод частично разлученных близнецов: Этот метод состоит в сравнении внутрипарного сходства МЗ и ДЗ близнецов, живущих какое-то время врозь.
В этих исследованиях также можно определить в какой степени справедлив постулат о равенстве сред МЗ и ДЗ близнецов. Так, если МЗ близнецы живущие отдельно становятся все менее схожи друг с другом по некой психологической характеристике, а ДЗ близнецы, живущие врозь, не отличаются по внутрипарному сходству от вместе живущих ДЗ близнецов, то можно сделать вывод, что средовые условия МЗ и ДЗ неравноценны, а выводы о наследуемости изучаемой характеристики завышают показатель наследуемости этой характеристики.
В3.Пути происхождения групп паразитов.
Условия жизни паразита внутри тела своего хозяина резко отличаются от свободного существования во внешней среде. Эндопаразиту не приходится отыскивать себе пищу, у него нет необходимости в таких органах чувств, как глаза.
Приспособление паразита к таким специальным условиям жизни неизбежно отражается на его организации и сводится к двум процесса: 1) к исчезновению тех органов, которые не требуются в новых условиях существования; 2) к возникновению, развитию или преобразованию органов, работа которых связана с особенностями жизни или питания на поверхности тела или внутри организма.
Вся совокупность изменений организации паразитов сводится к упрощению строения и нередко к изменению внешнего вида.
Паразитизм как явление живой природы возник у свободноживущих организмов в результате различных форм симбиоза и хищничества.
Различают несколько категорий симбиоза:
1) мутуализм - такая форма сожительства, при которой оба партнера приносят друг другу какую либо пользу (лишайники - сожительство водорослей и грибов);
2) синойкия - сожительство, при котором один партнер использует другого в качестве временного убежища (рыба-горнак и двустворчатый моллюск беззубка);
3) коменсализм - такая категория сожительства, при которой один вид животного использует другого для питания остатками пищи другого вида (рыба-прилипала и акула);
4) паразитизм.
Допускается, что паразитизм появился вскоре после возникновения жизни.
В процессе эволюции пары сожителей могут видоизменяться так, что один партнер начинает как-либо вредить другому. В итоге симбиоз переходит в паразитизм (один из симбиоза становится паразитом, другой - хозяином паразита).
Другой путь возникновения паразитизма может быть связан с приспособлением мелких организмов к повторному питанию за счет живого организма хозяина, которому при этом наносится ущерб.
Наконец, часть паразитов развилась благодаря способности их предков некоторое время жить в каких-либо хозяевах на положении ложных паразитов. Возникновение паразитизма шло по-разному у экто- и эндопаразитов.
Эктопаразитизм формировался прежде всего у свободноживущих хищных клещей, насекомых и других животных за счет удлинения сроков питания и времени пребывания на хозяине. Большую роль в эволюции эктопаразитов сыграли переход от полифагии к монофагии и специализации питания, в частности, питание кровью (клещи, комары, москиты, вши, кровососущие мухи).
Эндопаразитизм, в частности, кишечный как наиболее распространенный, формировался в результате случайного заноса цист простейших и яиц гельминтов в желудчно-кишечный тракт животного или человека. В результате случайных контактов у паразитов вырабатывались такие особенности, которые способствовали установлению паразитических отношений.
Эндопаразитизм мог возникнуть также в результате изменения инстинкта откладки яиц не на гниющий органический материал, а на раневую поверхность или в полости тела человека, сообщающиеся с внешней средой (вольфартова муха).
Кровепаразитизм рассматривается как вторичное явление, явившееся следствием первичного кишечного паразитизма. При этом считают, что современные кровепаразиты позвоночных (например, плазмодии) были кишечными паразитами беспозвоночных, а с переходом хозяев к гематофагии приспособились к жизни в кровяном русле позвоночных, сохранив при этом связь и с беспозвоночными.
У одноклеточных в процессе эволюции сформировались органоиды передвижения (у трипаносом); для проникновения в цитоплазму клетки хозяина - коноид. Многоклеточные организмы в процессе адаптации к паразитизму потеряли ряд морфологических структур. Например, у цестод нет кишечника, слабо выражен мышечный слой. Наряду с этим возникли и адаптации прогрессивного характера: мощные органы фиксации (присоски, ботрии, крючья), большая плодовитость, быстрый темп роста, роль кутикулы как защитного барьера от пищеварительных ферментов хозяина и т.д.
Билет 5
В1.Гаметогенез. Строение половых клеток.
Гаметогенез подразделяется на сперматогенез (процесс образования сперматозоидов у самцов) и оогенез (процесс образования яйцеклетки). По тому, что происходит с ДНК, эти процессы практически не отличаются: одна исходная диплоидная клетка дает четыре гаплоидные. Однако, по тому, что происходит с цитоплазмой, эти процессы кардинально различаются.
В яйцеклетке накапливаются питательные вещества, необходимые в дальнейшем для развития зародыша, поэтому яйцеклетка – это очень крупная клетка, и когда она делится, цель – сохранить питательные вещества для будущего зародыша, поэтому деление цитоплазмы несимметрично. Для того чтобы сохранить все запасы цитоплазмы и при этом избавиться от ненужного генетического материала, от цитоплазмы отделяются полярные тельца, которые содержат очень мало цитоплазмы, но позволяют поделить хромосомный набор. Полярные тельца отделяются при первом и втором делении мейоза

В2.Кариотип человека. Денверская и Парижская Классификация хромосом.
Кариоти́п — совокупность признаков (число, размеры, форма и т. д.) полного набора хромосом, присущая клеткам данного биологического вида (видовой кариотип), данного организма (индивидуальный кариотип) или линии (клона) клеток. Кариотипом иногда также называют и визуальное представление полного хромосомного набора (кариограммы).
Диверге́нция (от средневекового лат. divergo — отклоняюсь) (в биологии) — расхождение признаков и свойств у первоначально близких групп организмов в ходе эволюции, результат обитания в разных условиях и неодинаково направленного естественного или искусственного отбора
В3.Пути морфо-физиологической адаптации к паразитическому образу жизни.
Переход к паразитическому образу жизни сопровождается появлением у паразитов ряда адаптации, облегчающих их существование, развитие и размножение в специфических условиях организма хозяина Разнообразие форм паразитизма, различное систематическое положение паразитов (их принадлежность к разным отрядам, классам и типам), а также обитание их в разных органах и системах хозяина обусловливают многообразие этих адаптации. Однако некоторые приспособления являются абсолютно универсальными. К ним в первую очередь относятся высокая плодовитость и особенности половой системы. Действительно, возможность оставления потомства и попадания его в благоприятную среду — организм хозяина — у паразитов часто ничтожна. В связи с этим интенсивность размножения паразитов по сравнению со свободноживущими формами гораздо более велика. Достигается это разными способами. У многоклеточных это сильная степень развития половой системы и образование огромного количества половых продуктов. Этому способствуют первичный гермафродитизм плоских червей, изначально высокая плодовитость круглых червей и основной массы членистоногих. Нередко высокая интенсивность полового размножения дополняется размножением личиночных стадий жизненного цикла. Особенно это характерно для сосальщиков, личинки которых размножаются партеногенетически, а у некоторых ленточных червей — внутренним или наружным почкованием. Присасывательные диски у инфузории и лямблии, сложная присоска и кутикулярные шипики на коже у сосальщиков, крючья и сложные присоски на головках ленточных червей, конечности, служащие для прикрепления, у ракообразного и насекомого Некоторые паразиты из типа простейших приобретают способность к множественному делению — шизогонии, когда из одного паразита может образоваться более 1000 дочерних особей, или к спорогонии, в результате которой из одной особи могут образоваться десятки тысяч организмов следующего поколения. Практически у всех эктопаразитов и паразитов, обитающих в полостных органах, имеются адаптации для прикрепления к телу хозяина. Они встречаются у простейших (присасывательные диски лямблии), у гельминтов (присоски, шипики, крючья плоских червей, хитинизированный ротовой аппарат ряда круглых червей) и паразитических членистоногих (своеобразные конечности).Эндопаразиты, обитающие в полостных органах, имеют покровы, обладающие антиферментными свойствами, быстро регенерирующие либо вообще непроницаемые для ферментов хозяина. Паразиты, живущие в тканях, часто там инкапсулируются.Паразиты, питающиеся кровью (представлены в основном членистоногими), имеют колюще-сосущий ротовой аппарат, а также сильно растяжимый хитиновый покров, часто разветвленную пищеварительную трубку, антикоагулянтные свойства слюны и консервантные свойства ферментов пищеварительной системы.Эндопаразиты, активно отыскивающие хозяина, обладают органами ориентации в среде, используемыми для поисков хозяина (светочувствительные глазки, термо- и хеморецепторы), и органами передвижения.Передний конец тела паразитов, внедряющихся в организм хозяина, снабжен органами проникновения — специализированными железами, колющими стилетами и т.д. Это касается даже некоторых простейших, способных проникать в ткани хозяина через неповрежденные покровы.Все паразиты, развивающиеся со сменой хозяев, используют в качестве таковых виды, связанные между собой непосредственными пищевыми взаимоотношениями или обитающие с ними в одной среде. Большинство промежуточных хозяев являются источником питания для основных. Другой распространенный путь попадания паразита в организм хозяина — это использование многочисленных переносчиков, которые обеспечивают не только постоянную циркуляцию паразитов в экологических системах, но и их широкое расселение.Высшей степенью адаптации паразитов к хозяевам является наблюдаемая часто полная зависимость паразита от жизнедеятельности хозяев. При этом паразит нередко вызывает такие реакции хозяина, которые обеспечивают максимальную вероятность заражения последнего. Так, самки остриц, откладывая яйца в области анального отверстия, вызывают зуд. Расчесывание зудящих мест способствует распространению яиц этого паразита руками по окружающим предметам. Таким же образом обеспечивается расселение чесоточного клеща. Зуд в пораженной конечности, прекращающийся от соприкосновения с водой, способствует циркуляции в природе такого паразита, как ришта. Высокая температура больных паразитарными заболеваниями, распространяющимися с помощью кровососущих членистоногих, привлекает переносчиков нередко с больших расстояний и также оказывается полезной для паразитов.Нередко особенности жизнедеятельности паразитов оказываются синхронизированными с образом жизни хозяев. Так, откладка яиц шистосомами происходит обычно в самое жаркое время суток, когда наиболее вероятным оказывается контакт хозяев с водой, куда для развития должны попасть яйца этих паразитов. В это же время в поверхностных слоях воды скапливаются в поисках хозяев церкарии этих шистосом. Таким образом облегчается циркуляция паразита сразу на двух стадиях его жизненного цикла. Если в циркуляцию паразита включены несколько хозяев, то наблюдаются их взаимные адаптации, оказывающиеся выгодными паразитам и обеспечивающие его эффективное развитие. Так, выход микрофилярий в кровеносные сосуды человека происходит в часы суток, соответствующие периоду максимальной активности кровососущих насекомых, являющихся их переносчиками.Нередко паразиты даже модифицируют поведение одних хозяев таким образом, что в результате облегчается их попадание к другим. Так, рыбы, пораженные личинками ленточных червей, плавают в основном у поверхности воды и чаще вылавливаются рыбаками и хищными животными. Ленточные черви, использующие в качестве промежуточных хозяев копытных животных, снижают их жизнеспособность, и, таким образом, хищники поедают их в первую очередь. Сосальщики, заражающие травоядных животных и человека через случайное проглатывание насекомых, вызывают обездвиживание последних и плотное прикрепление к растениям, облегчающее им попадание в пищеварительный тракт хозяина.Одновременно с перечисленными признаками свойства паразитов переживать неблагоприятные условия внешней среды являются также несомненными адаптациями к паразитизму. Большинство простейших, заражение которыми происходит без участия переносчиков, во внешней среде способны инцистироваться. Яйца большинства гельминтов обладают феноменальной устойчивостью к неблагоприятным воздействиям. Капсулы с личинками трихинелл переносят не только промораживание, кипячение, но и многократное прохождение через пищеварительную систему рыб, земноводных, птиц, насекомых и ракообразных, не теряя жизнеспособности.Для большинства паразитов, переживших нахождение во внешней среде или в промежуточном хозяине в покоящихся стадиях и попавших в организм окончательного хозяина, существует комплекс условий, являющийся сигналом к началу активной жизнедеятельности. У млекопитающих он часто неспецифичен: это температура тела около 37°С, водная среда и высокая ее кислотность, а также наличие ферментов желудочного сока. Такие условия характерны для желудка любого млекопитающего, поэтому цисты, яйца и другие инвазионные стадии паразитов, обитающие у разных млекопитающих могут, попадая в желудок человека, начинать развитие. Некоторые из них проходят лишь часть цикла и, не находя специфических условий, гибнут успевая, однако, привести к тяжелым последствиям.Указанные особенности паразитов, общие для многих из них, не состоящих в родстве, возникли в разных их группах независимо друг от друга, иллюстрируя конвергентный характер эволюции организмов разных видов, классов и типов, адаптирующихся к сходным условиям.
Билет 6
В1.Цитологические основы полового размножения. Мейоз, как специфический процесс при формировании половых клеток.
Мейоз (от греч. meiosis — уменьшение) или редукционное деление клетки — деление ядра эукариотической клетки с уменьшением числа хромосом в два раза. Происходит в два этапа (редукционный и эквационный этапы мейоза). Мейоз не следует смешивать с гаметогенезом — образованием специализированных половых клеток, или гамет, из недифференцированных стволовых.
С уменьшением числа хромосом в результате мейоза в жизненном цикле происходит переход от диплоидной фазы к гаплоидной. Восстановление плоидности (переход от гаплоидной фазы к диплоидной) происходит в результате полового процесса.
В связи с тем, что в профазе первого, редукционного, этапа происходит попарное слияние (конъюгация) гомологичных хромосом, правильное протекание мейоза возможно только в диплоидных клетках или в чётных полиплоидах (тетра-, гексаплоидных и т. п. клетках). Мейоз может происходить и в нечётных полиплоидах (три-, пентаплоидных и т. п. клетках), но в них, из-за невозможности обеспечить попарное слияние хромосом в профазе I, расхождение хромосом происходит с нарушениями, которые ставят под угрозу жизнеспособность клетки или развивающегося из неё многоклеточного гаплоидного организма.
Этот же механизм лежит в основе стерильности межвидовых гибридов. Поскольку у межвидовых гибридов в ядре клеток сочетаются хромосомы родителей, относящихся к различным видам, хромосомы обычно не могут вступить в конъюгацию. Это приводит к нарушениям в расхождении хромосом при мейозе и, в конечном счете, к нежизнеспособности половых клеток, или гамет. Определенные ограничения на конъюгацию хромосом накладывают и хромосомные мутации (масштабные делеции, дупликации, инверсии или транслокации).
Мейоз состоит из 2 последовательных делений с короткой интерфазой между ними.
Профаза I — профаза первого деления очень сложная и состоит из 5 стадий:
Лептотена или лептонема — упаковка хромосом.
Зиготена или зигонема — конъюгация (соединение) гомологичных хромосом с образованием структур, состоящих из двух соединённых хромосом, называемых тетрадами или бивалентами.
Пахитена или пахинема — кроссинговер (перекрест), обмен участками между гомологичными хромосомами; гомологичные хромосомы остаются соединенными между собой.
Диплотена или диплонема — происходит частичная деконденсация хромосом, при этом часть генома может работать, происходят процессы транскрипции (образование РНК), трансляции (синтез белка); гомологичные хромосомы остаются соединёнными между собой. У некоторых животных в ооцитах хромосомы на этой стадии профазы мейоза приобретают характерную форму хромосом типа ламповых щёток.
Диакинез — ДНК снова максимально конденсируется, синтетические процессы прекращаются, растворяется ядерная оболочка; центриоли расходятся к полюсам; гомологичные хромосомы остаются соединёнными между собой.
Метафаза I — бивалентные хромосомы выстраиваются вдоль экватора клетки.
Анафаза I — микротрубочки сокращаются, биваленты делятся и хромосомы расходятся к полюсам. Важно отметить, что, из-за конъюгации хромосом в зиготене, к полюсам расходятся целые хромосомы, состоящие из двух хроматид каждая, а не отдельные хроматиды, как в митозе.
Телофаза I — хромосомы деспирализуются и появляется ядерная оболочка.
Второе деление мейоза следует непосредственно за первым, без выраженной интерфазы: S-период отсутствует, поскольку перед вторым делением не происходит репликации ДНК.
Профаза II — происходит конденсация хромосом, клеточный центр делится и продукты его деления расходятся к полюсам ядра, разрушается ядерная оболочка, образуется веретено деления.
Метафаза II — унивалентные хромосомы (состоящие из двух хроматид каждая) располагаются на «экваторе» (на равном расстоянии от «полюсов» ядра) в одной плоскости, образуя так называемую метафазную пластинку.
Анафаза II — униваленты делятся и хроматиды расходятся к полюсам.
Телофаза II — хромосомы деспирализуются и появляется ядерная оболочка.
В результате из одной диплоидной клетки образуется четыре гаплоидных клетки. В тех случаях, когда мейоз сопряжён с гаметогенезом (например, у многоклеточных животных), при развитии яйцеклеток первое и второе деления мейоза резко неравномерны. В результате формируется одна гаплоидная яйцеклетка и два так называемых редукционных тельца (абортивные дериваты первого и второго делений).
В2.Методы в генетике человека. Цитогенетические методы. Кариотип человека.
Генеалогический метод, Популяционный метод., Близнецовый метод. Цитологический метод, Биохимический метод.
Цитогенетические методы исследования применяют для диагностики хромосомных болезней. Они включают:
исследования полового хроматина - определение Х- и Y-хроматина;
кариотипирование (кариотип - совокупность хромосом клетки) - определение количества и структуры хромосом с целью диагностики хромосомных болезней (геномных мутаций и хромосомных аберраций).
Определение Х- и Y-хроматина
Определение Х- и Y-хроматина часто называют методом экспресс-диагностики пола. Исследуют клетки слизистой оболочки ротовой полости вагинального эпителия или волосяной луковицы. В ядрах клеток женщин в диплоидном наборе присутствуют две хромосомы X, одна из которых полностью инактивирована (спирализована, плотно упакована) уже на ранних этапах эмбрионального развития и видна в виде глыбки гетерохроматина, прикреплённого к оболочке ядра. Инактивированная хромосома X называется половым хроматином или тельцем Барра. Для выявления полового Х-хроматина (тельца Барра) в ядрах клеток мазки окрашивают ацетарсеином и препараты просматривают с помощью обычного светового микроскопа. В норме у женщин обнаруживают одну глыбку Х-хроматина, а у мужчин её нет. Для выявления мужского Y-полового хроматина (F-тельце) мазки окрашивают акрихином и просматривают с помощью люминисцентного микроскопа. Y-хроматин выявляют в виде сильно светящейся точки, по величине и интенсивности свечения отличающейся от остальных хромоцентров. Он обнаруживается в ядрах клеток мужского организма. Отсутствие тельца Барра у женщин свидетельствует о хромосомном заболевании - синдроме Шерешевского-Тернера (кариотип 45, ХО). Присутствие у мужчин тельца Барра свидетельствует о синдроме Кляйнфелтера (кариотип 47, XXY). Определение Х- и Y-хроматина - скрининговый метод, окончательный диагноз хромосомной болезни ставят только после исследования кариотипа.
Кариотипирование
Для изучения хромосом чаще всего используют препараты кратковременной культуры крови, а также клетки костного мозга и культуры фибробластов. Доставленную в лабораторию кровь с антикоагулянтом подвергают центрифугированию для осаждения эритроцитов, а лейкоциты инкубируют в культуральной среде 2-3 дня. К образцу крови добавляют фитогемагглютинин, так как он ускоряет агглютинацию эритроцитов и стимулирует деление лимфоцитов. Наиболее подходящая фаза для исследования хромосом - метафаза митоза, поэтому для остановки деления лимфоцитов на этой стадии используют колхицин. Добавление этого препарата к культуре приводит к увеличению доли клеток, находящихся в метафазе, то есть в той стадии клеточного цикла, когда хромосомы видны лучше всего. Каждая хромосома реплицируется (производит свою копию) и после соответствующей окраски видна в виде двух хроматид, прикреплённых к центромере, или центральной перетяжке. Затем клетки обрабатывают гипотоническим раствором хлорида натрия, фиксируют и окрашивают. Для окраски хромосом чаще используют краситель Романовского-Гимзы, 2% ацеткармин или 2% ацетарсеин. Они окрашивают хромосомы целиком, равномерно (рутинный метод) и могут быть использованы для выявления численных аномалий хромосом человека. Для получения детальной картины структуры хромосом, идентификации (определения) отдельных хромосом или их сегментов используют различные способы дифференциального окрашивания. Наиболее часто применяют методы Гимза, а также G- и Q-бендинга. При микроскопии препарата по длине хромосомы выявляется ряд окрашенных (гетерохроматин) и неокрашенных (эухроматин) полос. Характер поперечной исчерченности, получаемый при этом, позволяет идентифицировать каждую хромосому в наборе, так как чередование полос и их размеры строго индивидуальны и постоянны для каждой пары.Метафазные пластинки отдельных клеток фотографируют. Из фотографий вырезают индивидуальные хромосомы и наклеивают их по порядку на лист бумаги; такая картина хромосом называется кариотипом.Применение дополнительного окрашивания, а также новые методы получения хромосомных препаратов, позволяющих растягивать хромосомы в длину, значительно увеличивают точность цитогенетической диагностики.Для описания кариотипа человека разработана специальная номенклатура. Нормальный кариотип мужчины и женщины обозначают как 46, XY и 46, XX соответственно. При синдроме Дауна, характеризующемся наличием дополнительной хромосомы 21 (трисомия 21), кариотип женщины описывают как 47, XX 21+, а мужчины - 47, XY, 21+. При наличии структурной аномалии хромосомы необходимо указать изменённое длинное или короткое плечо: буквой р обозначают короткое плечо, q - длинное плечо, t - транслокацию. Так, при делеции короткого плеча хромосомы 5 (синдром «кошачьего крика») женский кариотип описывают как 46, XX, 5р-. Мать ребёнка с транслокационным синдромом Дауна - носительница сбалансированной транслокации 14/21 имеет кариотип 45, XX, t(14q; 21q). Транслокационная хромосома образуется при слиянии длинных плеч хромосомы 14 и 21, короткие плечи при этом теряются.
Каждое плечо разделяется на районы, а они в свою очередь - на сегменты, и те и другие обозначают арабскими цифрами. Центромера хромосомы является исходным пунктом для отсчёта районов и сегментов.
Таким образом, для топографии хромосом используют четыре метки: номер хромосомы, символ плеча, номер района и номер сегмента в пределах данного района. Например, запись 6р21.3 означает, что речь идёт о хромосоме 6-й пары, её коротком плече, районе 21, сегменте 3. Существуют ещё дополнительные символы, в частности pter - конец короткого плеча, qter - конец длинного плеча.
Цитогенетический метод исследования позволяет обнаружить делеции и другие изменения в хромосомах только размером приблизительно в 1 млн оснований (нуклеотидов).
В3. Понятие об трансмиссивных болезнях. Экологические основы их выведения.
Трансмиссивные болезни (лат. transmissio — перенесение на других) — заразные болезни человека, возбудители которых передаются кровососущими членистоногими (насекомыми и клещами).
Трансмиссивные болезни включают более 200 нозологических форм, вызываемых вирусами, бактериями, риккетсиями, простейшими и гельминтами. Часть из них передаётся только с помощью кровососущих переносчиков (облигатные трансмиссивные болезни, например сыпной тиф, малярия и др.), часть различными способами, в том числе и трансмиссивно (например, туляремия, заражение которой происходит при укусах комаров и клещей, а также при снятии шкурок с больных животных).
В передаче возбудителей трансмиссивных болезней участвуют специфические и механические переносчики. В специфических переносчиках возбудитель либо размножается и накапливается (например, вирусы в теле клещей), либо созревает до инвазионной стадии (например, личинки филярий в комарах, мошках, слепнях, малярийные плазмодии в теле комаров). Как размножение, так и развитие возбудителей в теле специфических переносчиков может происходить только при достаточно высокой, строго определённой температуре для каждой пары паразит — переносчик. Так, половое размножение, или спорогония, возбудителя трёхдневной малярии продолжается 19 дней при 20 °C и 6½ дней при температуре 30 °C, и только после этого в слюнных железах переносчика появляется инвазионная стадия паразита — спорозоит. Передача возбудителя переносчиком осуществляется различными способами. Наиболее часто возбудитель проникает со слюной, которую переносчик вводит в место укола перед началом кровососания. Так вводятся спорозоиты малярийного паразита. Перенос риккетсий вшами (см. Сыпной тиф эпидемический) и трипаносом триатомовыми клопами происходит во время дефекации переносчика; возбудитель из фекалий проникает затем в ранку на месте укола. Возбудитель вшиного возвратного тифа (Borrelia recurrentis) скапливается в теле вши и может проникнуть в организм человека лишь при раздавливании вши руками и втирании ее гемолифмы в кожу при расчёсах. Многие переносчики передают лишь одного, специфического для них паразита. Так, мухи цеце передают лишь трипаносому — возбудителя сонной болезни человека, мошки — возбудителя онхоцеркоза, триатомовые клопы — возбудителя американского трипаносомоза (болезни Шагаса). Москиты могут переносить возбудителей лейшманиозов и лихорадки паппатачи. Наиболее разнообразные связи с паразитами установились у комаров и клещей. Комары семейства Culicidae передают многие виды вирусов, в том числе возбудителя жёлтой лихорадки, лихорадки денге, вирусных энцефалитов (см. Энцефалиты комариные). Они являются переносчиками также малярии и филяриатозов. Иксодовые клещи передают вирусы, в том числе возбудителей клещевого энцефалита и геморрагических лихорадок, риккетсий — возбудителей пятнистых лихорадок, североазиатского сыпного тифа (см. Североазиатский клещевой риккетсиоз) и др., а также спирохет. В переносе возбудителей болезни у многих групп насекомых участвуют только самки. У мухи цеце, вшей и у всех групп клещей кровососами и переносчиками являются особи обоего пола.
В ряде случаев возбудитель болезни передается переносчиком своему потомству. Такая трансовариальная передача выявлена у комаров, инфицированных вирусами, у клещей, инфицированных вирусами и спирохетами и у москитов, инфицированных флебовирусами.
В организме механических переносчиков возбудители не развиваются и не размножаются. Попавший на хоботок, в кишечник или на поверхность тела механического переносчика возбудитель передается непосредственно (при укусе) либо путем контаминации ран, слизистых оболочек хозяина или пищевых продуктов. Самыми распространенными механическими переносчиками являются мухи семейства Muscidae, которые известны как переносчики вирусов, бактерий, простейших, гельминтов.
Билет 7
В1. Принцип компартмации. Биологическая мембрана.
|
К Высокая упорядоченность внутреннего содержимого эукариотической клетки достигается путем компартментации ее объема — подразделения на «ячейки», отличающиеся деталями химического (ферментного) состава. Компартментация способствует пространственному разделению веществ и процессов в клетке. Отдельный компартмент представлен органеллой (лизосома) или ее частью (пространство, отграниченное внутренней мембраной митохондрии). 1—ядро, 2—шероховатая цитоплазматическая есть, 3—митохондрия, 4 - транспортный цитоплазматический пузырек, 5—лизосома, 6—пластинчатый комплекс, 7 —гранула секрета. Предложено несколько схем взаимоотношения в мембране основных химических компонентов - белков и липидов, а также веществ, размещаемых на мембранной поверхности. В настоящее время принята точка зрения, согласно которой мембрана составлена из бимолекулярного слоя липидов. Гидрофобные участки их молекул повернуты друг к другу, а гидрофильные - находятся на поверхности слоя. Разнообразные белковые молекулы встроены в этот слой или размещены на его поверхностях. Благодаря компартментации клеточного объема в эукариотической клетке наблюдается разделение функций между разными структурами. Одновременно различные структуры закономерно взаимодействуют друг с другом. |
В2.Ген – функциональная единица наследственности. Эволюция представлений о гене.
Ген — структурная и функциональная единица наследственности, контролирующая развитие определенного признака или свойства. Совокупность генов родители передают потомкам во время размножения. В настоящее время, в молекулярной биологии установлено, что гены — это участки ДНК, несущие какую-либо целостную информацию — о строении одной молекулы белка или одной молекулы РНК. Эти и другие функциональные молекулы определяют развитие, рост и функционирование организма.
В то же время, каждый ген характеризуется рядом специфических регуляторных последовательностей ДНК, таких как промоторы, которые принимают непосредственное участие в регулировании проявления гена. Регуляторные последовательности могут находиться как в непосредственной близости от открытой рамки считывания, кодирующей белок, или начала последовательности РНК, как в случае с промоторами (так называемые cis-регуляторные элементы, англ. cis-regulatory elements), так и на расстоянии многих миллионов пар оснований (нуклеотидов), как в случае с энхансерами, инсуляторами и супрессорами (иногда классифицируемые как trans-регуляторные элементы, англ. trans-regulatory elements). Таким образом, понятие гена не ограничено только кодирующим участком ДНК, а представляет собой более широкую концепцию, включающую в себя и регуляторные последовательности.
Изначально термин ген появился как теоретическая единица передачи дискретной наследственной информации. История биологии помнит споры о том, какие молекулы могут являться носителями наследственной информации. Большинство исследователей считали, что такими носителями могут быть только белки, так как их строение (20 аминокислот) позволяет создать больше вариантов, чем строение ДНК, которое составлено всего из четырёх видов нуклеотидов. Позже было экспериментально доказано, что именно ДНК включает в себя наследственную информацию, что было выражено в виде центральной догмы молекулярной биологии.
Гены могут подвергаться мутациям — случайным или целенаправленным изменениям последовательности нуклеотидов в цепи ДНК. Мутации могут приводить к изменению последовательности, а следовательно изменению биологических характеристик белка или РНК, которые, в свою очередь, могут иметь результатом общее или локальное изменённое или анормальное функционирование организма. Такие мутации в ряде случаев являются патогенными, так как их результатом является заболевание, или летальными на эмбриональном уровне. Однако, далеко не все изменения последовательности нуклеотидов приводят к изменению структуры белка (благодаря эффекту вырожденности генетического кода) или к существенному изменению последовательности и не являются патогенными. В частности, геном человека характеризуется однонуклеотидными полиморфизмами и вариациями числа копий (англ. copy number variations), такими как делеции и дупликации, которые составляют около 1 % всей нуклеотидной последовательности человека.[1] Однонуклеотидные полиморфизмы, в частности, определяют различные аллели одного гена.
Мономеры, составляющие каждую из цепей ДНК, представляют собой сложные органические соединения, включающие в себя азотистые основания: аденин(А) или тимин(Т) или цитозин(Ц) или гуанин(Г), пятиатомный сахар-пентозу-дезоксирибозу,по имени которой и получила название сама ДНК, а так же остаток фосфорной кислоты.Эти соединения носят название нуклеотидов.
дискретность — несмешиваемость генов;
стабильность — способность сохранять структуру;
лабильность — способность многократно мутировать;
множественный аллелизм — многие гены существуют в популяции во множестве молекулярных форм;
аллельность — в генотипе диплоидных организмов только две формы гена;
специфичность — каждый ген кодирует свой признак;
плейотропия — множественный эффект гена;
экспрессивность — степень выраженности гена в признаке;
пенетрантность — частота проявления гена в фенотипе;
амплификация — увеличение количества копий гена.
3.Особенности генома эукариот.
Количественные особенности генома эукариот
Главная количественная особенность генетического материала эукариот – наличие избыточной ДНК. Этот факт легко выявляется при анализе отношения числа генов к количеству ДНК в геноме бактерий и млекопитающих. Если средний размер гена бактерий 1500 пар нуклеотидов (п.н.), а длина кольцевой молекулы ДНК хромосомы Е. coli и В. subtilis составляет свыше 1 мм, то в такой хромосоме могут разместиться около 3 тысяч генов. Примерно такое число генов было экспериментально определено у бактерий по числу типов иРНК. Если это число умножить на средний размер гена, то получится, что около 95% генома бактерий состоит из кодирующих (генных) последовательностей. Остальные 5%, по-видимому, заняты регуляторными элементами. Иная картина наблюдается у эукариотических организмов. Например, у человека насчитывают приблизительно 50 тысяч генов (имеется в виду только суммарная длина кодирующих участков ДНК – экзонов). В то же время размер генома человека 3×109 (три миллиарда) п.н. Это означает, что кодирующая часть его генома составляет всего 15…20 % от тотальной ДНК. Существует значительное число видов, геном которых в десятки раз больше генома человека, например некоторые рыбы, хвостатые амфибии, лилейные. Избыточная ДНК характерна для всех эукариот. В этой связи необходимо подчеркнуть неоднозначность терминов генотип и геном. Под генотипом следует понимать совокупность генов, имеющих фенотипическое проявление, тогда как понятие генома обозначает количество ДНК, находящееся в гаплоидном наборе хромосом данного вида
В3.Виды экологии: аутэкология, демэкология, синэкология. Понятие об экосистеме.
Аутэколо́гия — раздел экологии, изучающий взаимоотношения организма с окружающей средой. В отличие от демэкологии и синэкологии, сосредоточенных на изучении взаимоотношений со средой популяций и экосистем, состоящих из множества организмов, исследует индивидуальные организмы на стыке с физиологией. Данный термин ныне считается устаревшим , а предмет раздела полагают неотличимым от такового демэкологии. Это связано с тем, что уровнем организации живого, на котором возможно изучение взаимодействия с косной средой, считают популяцию организмов определенного вида. раздел экологии, изучающий влияние факторов окружающей среды на отдельные организмы, популяции и виды (растений, животных, грибов, бактерий). Задача А. — выявление физиологических, морфологических и прочих приспособлений (адаптаций) видов к различным экологическим условиям: режиму увлажнения, высоким и низким температурам, засолению почвы (для растений). В последние годы у А. появилась новая задача — изучение механизмов реагирования организмов на различные варианты химического и физического загрязнения (включая радиоактивное загрязнение) среды. Теоретическая основа А. — ее законы. Первый закон А. — закон оптимума: по любому экологическому фактору любой организм имеет определенные пределы распространения (пределы толерантности). Как правило, в центре ряда значений фактора, ограниченного пределами толерантности, лежит область наиболее благоприятных условий жизни организма, при которых формируется самая большая биомасса и высокая плотность популяции. Напротив, у границ толерантности расположены зоны угнетения организмов, когда падает плотность их популяций и виды становятся наиболее уязвимыми к действию неблагоприятных экологических факторов, включая и влияние человека (рис. 3). Второй закон А. — индивидуальность экологии видов: каждый вид по каждому экологическому фактору распределен по-своему, кривые распределений разных видов перекрываются, но их оптимумы различаются (рис. 4). По этой причине при изменении условий среды в пространстве (например, от сухой вершины холма к влажному логу) или во времени (при пересыхании озера, при усилении выпаса, при зарастании скал, см. Экологическая сукцессия) состав экосистем изменяется постепенно. Известный российский эколог Л. Г. Раменский сформулировал этот закон образно: «Виды — это не рота солдат, марширующих в ногу». Третий закон А. — закон лимитирующих (ограничивающих) факторов: наиболее важным для распределения вида является тот фактор, значения которого находятся в минимуме или максимуме. Например, в степной зоне лимитирующим фактором развития растений является увлажнение (значение находится в минимуме) или засоление почвы (значение находится в максимуме), а в лесной — ее обеспеченность питательными элементами (значения находятся в минимуме). Законы А. широко используются в сельскохозяйственной практике, например, при выборе сортов растений и пород животных, которые наиболее целесообразно выращивать или разводить в конкретном районе (см. Адаптивный подход).
Синэколо́гия — раздел экологии, изучающий взаимоотношения организмов различных видов внутри сообщества организмов. Часто синэкологию рассматривают как науку о жизни биоценозов, то есть многовидовых сообществ животных, растений и микроорганизмов.
В настоящее время является одним из 3 главных разделов общей экологии (наряду с аутэкологией и демэкологией).
Экосисте́ма, или экологи́ческая систе́ма (от др.-греч. οἶκος — жилище, местопребывание и σύστημα — система) — биологическая система, состоящая из сообщества живых организмов (биоценоз), среды их обитания (биотоп), системы связей, осуществляющей обмен веществом и энергией между ними. Одно из основных понятий экологии.
Пример экосистемы — пруд с обитающими в нём растениями, рыбами, беспозвоночными животными, микроорганизмами, составляющими живую компоненту системы, биоценоз. Для пруда как экосистемы характерны донные отложения определенного состава, химический состав (ионный состав, концентрация растворенных газов) и физические параметры (прозрачность воды, тренд годичных изменений температуры), а также определённые показатели биологической продуктивности, трофический статус водоёма и специфические условия данного водоёма. Другой пример экологической системы — лиственный лес в средней полосе России с определённым составом лесной подстилки, характерной для этого типа лесов почвой и устойчивым растительным сообществом, и, как следствие, со строго определёнными показателями микроклимата (температуры, влажности, освещённости) и соответствующим таким условиям среды комплексом животных организмов. Немаловажным аспектом, позволяющим определять типы и границы экосистем, является трофическая структура сообщества и соотношение производителей биомассы, её потребителей и разрушающих биомассу организмов, а также показатели продуктивности и обмена вещества и энергии.
Билет 8
В1. Принцип клеточной компартментации. Организация и свойства биологической мембраны. История изучения.
|
К омпартментация объема клетки с помощью мембран. Высокая упорядоченность внутреннего содержимого эукариотической клетки достигается путем компартментации ее объема — подразделения на «ячейки», отличающиеся деталями химического (ферментного) состава. Компартментация способствует пространственному разделению веществ и процессов в клетке. Отдельный компартмент представлен органеллой (лизосома) или ее частью (пространство, отграниченное внутренней мембраной митохондрии). 1—ядро, 2—шероховатая цитоплазматическая есть, 3—митохондрия, 4—транспортный цитоплазматический пузырек, 5—лизосома, 6—пластинчатый комплекс, 7 —гранула секрета. Предложено несколько схем взаимоотношения в мембране основных химических компонентов - белков и липидов, а также веществ, размещаемых на мембранной поверхности. В настоящее время принята точка зрения, согласно которой мембрана составлена из бимолекулярного слоя липидов. Гидрофобные участки их молекул повернуты друг к другу, а гидрофильные - находятся на поверхности слоя. Разнообразные белковые молекулы встроены в этот слой или размещены на его поверхностях. Благодаря компартментации клеточного объема в эукариотической клетке наблюдается разделение функций между разными структурами. Одновременно различные структуры закономерно взаимодействуют друг с другом. |
Биологические мембраны образуют наружную оболочку всех животных клеток и формируют многочисленные внутриклеточные органеллы. Наиболее характерным структурным признаком является то, что мембраны всегда образуют замкнутые пространства, и такая микроструктурная организация мембран позволяет им выполнять важнейшие функции: Барьерная функция выражается в том, что мембрана при помощи соответствующих механизмов участвует в создании концентрационных градиентов, препятствуя свободной диффузии. При этом мембрана принимает участие в механизмах электрогенеза. К ним относятся механизмы создания потенциала покоя, генерация потенциала действия, механизмы распространения биоэлектрических импульсов по однородной и неоднородной возбудимым структурам.
Регуляторная функция заключается в тонкой регуляции внутриклеточного содержимого и внутриклеточных реакций за счет рецепции внеклеточных биологически активных веществ, что приводит к изменению активности ферментных систем мембраны и запуску механизмов вторичных "мессенджеров" ("посредники").
Контактная функция клеточной мембраны заключается в организации зон специфического или неспецифического контакта между клетками с образованием тканевой структуры. При этом в области контакта возможен обмен ионами, медиаторами, макромолекулами между клетками, или передача электрических сигналов.
Преобразование внешних стимулов неэлектрической природы в электрические сигналы (в рецепторах).
Высвобождение нейромедиаторов в синаптических окончаниях.
В2.Организация генома эукариот.
У эукариотических организмов механизм регуляции транскрипции гораздо более сложен. В результате клонирования и секвенирования генов эукариот обнаружены специфические последовательности, принимающие участие в транскрипции и трансляции. Для эукариотической клетки характерно: 1. Наличие интронов и экзонов в молекуле ДНК. 2. Созревание и-РНК - вырезание интронов и сшивка экзонов. 3. Наличие регуляторных элементов, регулирующих транскрипцию, таких как: а) промоторы - 3 вида, на каждый из которых садится специфическая полимераза. Pol I реплицирует рибосомные гены, Pol II - структурные гены белков, Pol III - гены, кодирующие небольшие РНК. Промотор Pol I и Pol II находятся перед участком инициации транскрипции, промотор Pol III - в рамках структурного гена; б) модуляторы - последовательности ДНК, усиливающие уровень транскрипции; в) усилители - последовательности, усиливающие уровень транскрипции и действующие независимо от своего положения относительно кодирующей части гена и состояния начальной точки синтеза РНК; г) терминаторы - специфические последовательности, прекращающие и трансляцию, и транскрипцию. Эти последовательности по своей первичной структуре и расположению относительно инициирующего кодона отличаются от прокариотических, и бактериальная РНК-полимераза их не "узнает". Таким образом, для экспрессии эукариотических генов в клетках прокариот нужно, чтобы гены находились под контролем прокариотических регуляторных элементов. Это обстоятельство необходимо учитывать при конструировании векторов для экспрессии.
В3.Природноочаговые протозоонозы. Структура природного очага, основные эелементы (на примере лейшманиоза).
Это заболевания, вызываемые простейшими паразитами, которые, находясь в окружающей среде, существуют в форме цист. Они могут сохраняться длительное время. Попадая в организм, паразит меняет свою форму. Заражение обычно происходит при употреблении зараженной цистами воды и продуктов, при контакте с фекалиями больного животного или человека.
Лейшмании — род паразитических простейших, вызывающих лейшманиозы[4]. Переносчиками лейшманий являются москиты из рода Phlebotomus в Старом Свете, и из рода Lutzomyia в Новом Свете. Естественным резервуаром разных видов служат позвоночные животные, относящиеся к шести отрядам млекопитающих и ящерицам[5]; впрочем, на основании изоферментного анализа паразитов ящериц было предложено выделить в отдельный род отряда трипаносоматид — Sauroleishmania[6]. Лейшмании в основном поражают грызунов, собак и людей, но также отмечены случаи поражения у даманов, кошек и лошадей. В Новом Свете инфекция встречается у опоссумов, ленивцев и броненосцев[7]; зарегистрированы случаи лейшманиоза у кенгуру в Австралии[8]. По оценкам ВОЗ от начала 1990-х, лейшманиозами больны около 12 миллионов человек в 88 странах.
Жизненный цикл: лейшмании, как и все трипаносоматиды, являются облигатными паразитами. Жизненный цикл лейшманий включает двух хозяев: млекопитающее и насекомое (москит).
Москиты заражаются лейшманиями, когда пьют кровь заражённого млекопитающего. Кровью питаются только самки москитов. Лейшмании вместе с проглатываемой кровью проникают в пищеварительный канал москита. В задней части средней кишки вокруг проглоченной крови у москита (как и у некоторых других кровососущих насекомых, например, комаров) образуется так называемая перитрофическая матрица.
Промастиготы лейшманий размножаются в пищеварительном канале самок москитов. Приблизительно через неделю инфекция распространяется до верхних отделов пищеварительного канала и паразиты блокируют просвет канала своими телами и секретируемым им гелем. Когда самка кусает потенциального хозяина, она выделяет в кожу свою слюну. Самка с блокированным пищеварительным каналом не может глотать, и у неё возникают спастические движения, в результате которых она отрыгивает промастиготы в ранку на коже хозяина.
В среднем во время укуса инфицированным москитом в кожу попадает 102 — 103 промастигот.
Первыми на место повреждения прибывают полиморфоядерные нейтрофилы, которые фагоциритуют паразитов. Внутри нейтрофилов лейшмании не размножаются и не превращаются в амастиготы. Затем, когда нейтрофилы переходят в фазу апоптоза, они уничтожаются макрофагами, и лейшмании проникают в макрофаги, не вызывая иммунного ответа.[15] Макрофаги являются основными клетками-хозяевами лейшманий в организме млекопитающих. Внутри макрофагов лейшмании трансформируются во внутриклеточную морфологическую форму — амастиготы.
Внутри макрофага лейшмании заключены в так называемые "паразитифорные вакуоли", которые образуются от слияния первичной фагосомы c лизосомами и эндосомами. В них промастиготы транформируются в амастиготы. При этом происходят изменения в морфологии — продолговатые промастиготы с длинным жгутиком превращаются в овальные амастиготы с коротким жгутиком, в метаболизме, чтобы приспособиться к кислой среде, и в биохимическом составе мембраны. Трансформация занимает от двух до пяти дней. Амастиготы способны выживать в кислой среде этих вакуолей и питаться их содержимым. Внутри вакуоли амастиготы медленно размножаются, и каждый цикл размножения занимает около 24 часов.
При кожном лейшманиозе инфильтрат образуется в коже и содержит преимущественно макрофаги, а также лимфоидные клетки и немного плазматических клеток. При висцеральном лейшманиозе очаги инфекции образуются в органах ретикуло-эндотелиальной системы.
В4. Болезнь Дауна. Трисомия по 21 хромосоме, продолжительность жизни сокращена, уголки глаз несколько приподняты, лицо выглядит несколько плоским, полость рта – маленькая, а язык – большой, ладони широкие с короткими пальцами, и слегка загнутыми внутрь мизинцами, длина и вес новорожденного меньше обычного.
Билет 9
В1. Структурная организация и свойства биологической мембраны.
К омпартментация объема клетки с помощью мембран. Высокая упорядоченность внутреннего содержимого эукариотической клетки достигается путем компартментации ее объема — подразделения на «ячейки», отличающиеся деталями химического (ферментного) состава. Компартментация способствует пространственному разделению веществ и процессов в клетке. Отдельный компартмент представлен органеллой (лизосома) или ее частью (пространство, отграниченное внутренней мембраной митохондрии). 1—ядро, 2—шероховатая цитоплазматическая есть, 3—митохондрия, 4—транспортный цитоплазматический пузырек, 5—лизосома, 6—пластинчатый комплекс, 7 —гранула секрета. Предложено несколько схем взаимоотношения в мембране основных химических компонентов - белков и липидов, а также веществ, размещаемых на мембранной поверхности. В настоящее время принята точка зрения, согласно которой мембрана составлена из бимолекулярного слоя липидов. Гидрофобные участки их молекул повернуты друг к другу, а гидрофильные - находятся на поверхности слоя. Разнообразные белковые молекулы встроены в этот слой или размещены на его поверхностях. Благодаря компартментации клеточного объема в эукариотической клетке наблюдается разделение функций между разными структурами. Одновременно различные структуры закономерно взаимодействуют друг с другом. |
Биологические мембраны образуют наружную оболочку всех животных клеток и формируют многочисленные внутриклеточные органеллы. Наиболее характерным структурным признаком является то, что мембраны всегда образуют замкнутые пространства, и такая микроструктурная организация мембран позволяет им выполнять важнейшие функции: Барьерная функция выражается в том, что мембрана при помощи соответствующих механизмов участвует в создании концентрационных градиентов, препятствуя свободной диффузии. При этом мембрана принимает участие в механизмах электрогенеза. К ним относятся механизмы создания потенциала покоя, генерация потенциала действия, механизмы распространения биоэлектрических импульсов по однородной и неоднородной возбудимым структурам.
Регуляторная функция заключается в тонкой регуляции внутриклеточного содержимого и внутриклеточных реакций за счет рецепции внеклеточных биологически активных веществ, что приводит к изменению активности ферментных систем мембраны и запуску механизмов вторичных "мессенджеров" ("посредники").
Контактная функция клеточной мембраны заключается в организации зон специфического или неспецифического контакта между клетками с образованием тканевой структуры. При этом в области контакта возможен обмен ионами, медиаторами, макромолекулами между клетками, или передача электрических сигналов.
Преобразование внешних стимулов неэлектрической природы в электрические сигналы (в рецепторах).
Высвобождение нейромедиаторов в синаптических окончаниях.
В2.Химическая организация гена. Классификация генов по структуре и функциям.
Структура
генов
Ген
представляет собой последовательность
нуклеотидов ДНК размером от нескольких
сотен до миллиона пар нуклеотидов, в
которых закодирована генетическая
информация о первичной структуре белка
(число и последовательность аминокислот).
Для регулярного правильного считывания
информации в гене должны присутствовать:
кодон инициации, множество смысловых
кодонов и кодон терминации. Три подряд
расположенных нуклеотида представляют
собой кодон, который и определяет, какая
аминокислота будет располагаться в
данной позиции в белке. Например, в
молекуле ДНК последовательность
оснований ТАС является кодоном для
аминокислоты метионина, а последовательность
ТТТ кодирует фенилаланин. В молекуле
иРНК вместо тимина (Т) присутствует
основание урацил (У). Таблица генетического
кода во всех руководствах представлена
именно символами иРНК. Из 64 возможных
кодонов смысловыми являются 61, а три
триплета — УАА, УАГ, УГА — не кодируют
аминокислоты и поэтому были названы
бессмысленными, однако на самом деле
они представляют собой знаки терминации
трансляции.
Для прокариот характерна
относительно простая структура генов.
Так, структурный ген бактерии, фага или
вируса, как правило, контролирует одну
ферментативную реакцию. Специфичным
для прокариот является оперонная система
организации нескольких генов. Гены
одного оперона (участка генетического
материала, состоящего из 1, 2 и более
сцепленных структурных генов, которые
кодируют белки (ферменты), осуществляющие
последовательные этапы биосинтеза
какого-либо метаболита; в оперон эукариот
входит, как правило, 1 структурный ген;
оперон содержит регуляторные элементы)
расположены в кольцевой хромосоме
бактерии рядом и контролируют ферменты,
осуществляющие последовательные или
близкие реакции синтеза (лактозный,
гистидиновый и др. опероны).
Структура
генов у бактеориофагов и вирусов в
основном схожа с бактериями, но более
усложнена и сопряжена с геномом хозяев.
Например, у фагов и вирусов обнаружено
перекрывание генов, а полная зависимость
вирусов эукариот от метаболизма
клетки-хозяина привела к появлению
экзон-интронной структуры генов.
Эукариотические гены, в отличие от
бактериальных, имеют прерывистое
мозаичное строение. Кодирующие
последовательности (экзоны) перемежаются
с некодирующими (интронами). Экзон [от
англ. ex(divssi)on — выражение, выразительность]
- участок гена, несущий информацию о
первичной структуре белка. В гене экзоны
разделены некодирующими участками —
интронами. Интрон (от лат. inter — между)
- участок гена, не несущий информацию о
первичной структуре белка и расположенный
между кодирующими участками — экзонами.
В результате структурные гены эукариот
имеют более длинную нуклеотидную
последовательность, чем соответствующая
зрелая иРНК, последовательность
нуклеотидов в которой соответствует
экзонам. В процессе транскрипции
информация о гене списывается с ДНК на
промежуточную иРНК, состоящую из экзонов
и интронов. Затем специфические ферменты
— рестриктазы — разрезают эту про-иРНК
по границам экзон-интрон, после чего
экзонные участки ферментативно
соединяются вместе, образуя зрелую иРНК
(так называемый сплайсинг). Количество
интронов может варьировать в разных
генах от нуля до многих десятков, а длина
— от нескольких пар оснований до
нескольких тысяч.
Ген может кодировать
различные РНК-продукты путем изменения
инициирующих и терминирующих кодонов,
а также альтернативного сплайсинга.
Альтернативная экспрессия гена
осуществляется и путем использования
различных сочетаний экзонов в зрелой
иРНК, причем полипептиды, синтезированные
на таких иРНК, будут различаться как по
количеству аминокислотных остатков,
так и по их составу.
Наряду со
структурными и регуляторными генами
обнаружены участки повторяющихся
нуклеотидных последовательностей,
функции которых изучены недостаточно,
а также мигрирующие элементы (мобильные
гены), способные перемещаться по геному.
Найдены также так называемые псевдогены
у эукариот, которые представляют собой
копии известных генов, расположенные
в других частях генома и лишенные
интронов или инактивированные мутациями.
3.
Классификация генов
Накопленные
знания о структуре, функциях, характере
взаимодействия, экспрессии, мутабильности
и других свойствах генов породили
несколько вариантов классификации
генов.
По месту локализации генов в
структурах клетки различают расположенные
в хромосомах ядра ядерные гены и
цитоплазматические гены, локализация
которых связана с хлоропластами и
митохондриями.
По функциональному
значению различают структурные гены,
характеризующиеся уникальными
последовательностями нуклеотидов,
кодирующих свои белковые продукты,
которые можно идентифицировать с помощью
мутаций, нарушающих функцию белка, и
регуляторные гены — последовательности
нуклеотидов, не кодирующие специфические
белки, а осуществляющие регуляцию
действия гена (ингибирование, повышение
активности и др.).
По влиянию на
физиологические процессы в клетке
различают летальные, условно летальные,
супервитальные гены, гены-мутаторы,
гены-антимутаторы и др.
Следует
отметить, что любые биохимические и
биологические процессы в организме
находятся под генным контролем. Так,
деление клеток (митоз, мейоз) контролируется
несколькими десятками генов; группы
генов осуществляют контроль восстановления
генетических повреждений ДНК (репарация).
Онкогены и гены — супрессоры опухолей
участвуют в процессах нормального
деления клеток. Индивидуальное развитие
организма (онтогенез) контролируется
многими сотнями генов. Мутации в генах
приводят к измененному синтезу белковых
продуктов и нарушению биохимических
или физиологических процессов.
Гомеозисные мутации у дрозофилы
позволили открыть существование генов,
нормальной функцией которых является
выбор или поддержание определенного
пути эмбрионального развития, по которому
следуют клетки. Каждый путь развития
характеризуется экспрессией определенного
набора генов, действие которых приводит
к появлению конечного результата: глаза,
голова грудь, брюшко, крыло, ноги и т. д.
Исследования генов комплекса bithorax
дрозофилы американским генетиком
Льюисом показали, что это гигантский
кластер тесно сцепленных генов, функция
которых необходима для нормальной
сегментации груди (thorax) и брюшка (abdomen).
Подобные гены получили название
гомеобоксных. Гомеобоксные гены
расположены в ДНК группами и проявляют
свое действие строго последовательно.
Такие гены обнаружены и у млекопитающих,
и они имеют высокую гомологию (сходство).
4.
Функции генов
В
процессе реализации наследственной
информации, заключенной в гене, проявляется
целый ряд его свойств. Определяя
возможность развития отдельного
качества, присущего данной клетке или
организму, ген характеризуется
дискретностью действия (от лат. discretus —
разделенный, прерывистый), прерывностью
(интроны и экзоны). Дискретность
наследственного материала, предположение
о которой высказал еще Г. Мендель,
подразумевает делимость его на части,
являющиеся элементарными единицами, -
гены. В настоящее время ген рассматривают
как единицу генетической функции. Он
представляет собой минимальное количество
наследственного материала, которое
необходимо для синтеза тРНК, рРНК или
полипептида с определенными свойствами.
Ген несет ответственность за формирование
и передачу по наследству отдельного
признака или свойства клеток, организмов
данного вида. Кроме того, изменение
структуры гена, возникающее в разных
его участках, в конечном итоге приводит
к изменению соответствующего элементарного
признака.
Ввиду того что в гене
заключается информация об аминокислотной
последовательности определенного
полипептида, его действие является
специфичным. Однако в некоторых случаях
одна и та же нуклеотидная последовательность
может детерминировать синтез не одного,
а нескольких полипептидов. Это наблюдается
в случае альтернативного сплайсинга у
эукариот и при перекрывании генов у
фагов и прокариот. Очевидно, такую
способность следует оценить как
множественное, или плейотропное, действие
гена (хотя традиционно под плейотропным
действием гена принято понимать участие
его продукта – полипептида – в разных
биохимических процессах, имеющих
отношение к формированию различных
сложных признаков). Например, участие
фермента в ускорении определенной
реакции (см. рис.), которая является
звеном нескольких биохимических
процессов, делает зависимыми результаты
этих процессов от нормального
функционирования гена, кодирующего
этот белок. Нарушение реакции A→B,
катализируемой белком α, в результате
мутации гена ведет к выключению
последующих этапов формирования
признаков D и E.
![]()
![]() α
D
α
D
![]()
![]() A
B
A
B
![]() C
Определяя возможность транскрибирования
мРНК для синтеза конкретной полипептидной
цепи, ген характеризуется дозированностью
действия, т.е. количественной зависимостью
результата его экспрессии от дозы
соответствующего аллеля этого гена.
Примером может служить зависимость
степени нарушения транспортных свойств
гемоглобина у человека при
серповидно-клеточной анемии от дозы
аллеля НЬS. Наличие в генотипе человека
двойной дозы этого аллеля, приводящего
к изменению структуры β-глобиновых
цепей гемоглобина, сопровождается
грубым нарушением формы эритроцитов и
развитием клинически выраженной картины
анемии вплоть до гибели. У носителей
только одного аллеля НЬS при нормальном
втором аллеле лишь незначительно
изменяется форма эритроцитов и анемия
не развивается, а организм характеризуется
практически нормальной жизнеспособностью.
C
Определяя возможность транскрибирования
мРНК для синтеза конкретной полипептидной
цепи, ген характеризуется дозированностью
действия, т.е. количественной зависимостью
результата его экспрессии от дозы
соответствующего аллеля этого гена.
Примером может служить зависимость
степени нарушения транспортных свойств
гемоглобина у человека при
серповидно-клеточной анемии от дозы
аллеля НЬS. Наличие в генотипе человека
двойной дозы этого аллеля, приводящего
к изменению структуры β-глобиновых
цепей гемоглобина, сопровождается
грубым нарушением формы эритроцитов и
развитием клинически выраженной картины
анемии вплоть до гибели. У носителей
только одного аллеля НЬS при нормальном
втором аллеле лишь незначительно
изменяется форма эритроцитов и анемия
не развивается, а организм характеризуется
практически нормальной жизнеспособностью.
В3. Фитотоксиканты
химические и природные вещества в рецептурной форме для поражения различных видов растительности. Подразделяются на альгициды (поражение водной растительности), арборициды (древесно-кустарниковой), гербициды, десиканты (вегетирующей), дефолианты и др.
Фитотоксиканты — это загрязняющие атмосферу вещества, вредные для растений. Они поглощаются листьями, оттуда поступают в побега и другие органы растений. Атмосферные осадки способствуют поступлению растворенных фитотокси-кантов в растения.
Фитотоксиканты - химические вещества, вызывающие поражение растительности. Растения, обработанные фитотоксикантами, теряют листву, засыхают и погибают.
Билет 10
В1. Опишите путь секреторного белка от места синтеза белка до выхода из клетки.
В клетках, в которых секреция происходит в ответ на внеклеточный сигнал , секретируемые белки концентрируются и хранятся в секреторных пузырьках (их часто называют секреторными гранулами из-за темной сердцевины). При получении соответствующего сигнала они высвобождаются путем экзоцитоза . Секреторные пузырьки отпочковываются от транс-сети Гольджи . Полагают, что для их образования нужен клатрин и связанные с ним белки, создающие "кайму", потому что часть поверхности формирующихся пузырьков обычно покрыта клатрином. Эта кайма удаляется вскоре после того, как пузырек полностью сформируется ( рис.8-76 ).
Подобно лизосомным гидролазам белки, предназначенные для секреторных пузырьков (их часто называют секреторными белками ) должны быть отобраны и упакованы в соответствующие пузырьки в транс-сети Гольджи . По-видимому, в этом случае происходит избирательная агрегация секреторных белков. Образовавшиеся агрегаты в электронном микроскопе выглядят как электроноплотный материал в транс-сети Гольджи. "Сигнал сортировки" , направляющий белок к таким агрегатам, неизвестен, но видимо, это сигнальный участок, общий для многих секреторных белков. Такой вывод подтверждается следующими данными: если ген, кодирующий секреторный белок, перенести в секреторную клетку другого типа, в норме не синтезирующую данный белок, то чужой белок будет также упаковываться в секреторные пузырьки.
Неизвестно, каким образом при образовании секреторных пузырьков отбираются агрегаты, содержащие секреторные белки. Секреторные пузырьки имеют уникальные мембранные белки , часть из которых может служить рецепторами (в транс-сети Гольджи ) для связывания агрегированного материала, подлежащего упаковке. Секреторные пузырьки больше транспортных пузырьков, переносящих лизосомные гидролазы , и агрегаты, которые в них содержатся, слишком велики для того, чтобы каждая молекула секретируемого белка могла связаться с рецептором в мембране пузырька , как это происходит при транспорте лизосомных ферментов . Захват этих агрегатов секреторными гранулами скорее напоминает поглощение частиц при фагоцитозе на клеточной поверхности, которое также происходит с участием покрытых клатрином мембран .
После того, как незрелые секреторные пузырьки отпочкуются от транс- сети Гольджи, они утрачивают кайму, и их содержимое сильно концентрируется. Такая конденсация происходит резко и, возможно, вызывается закислением среды в полости пузырька за счет работы ATP- зависимой протонной помпы в его мембране. Агрегация секретируемых белков (или других компонентов) и последующая их конденсация в секреторных пузырьках обусловливает увеличение концентрации этих белков в 200 раз по сравнению с аппаратом Гольджи . Благодаря этому секреторные пузырьки имеют возможность высвобождать по "команде" большие количества материала.
В2.История изучения структуры гена.
Современное представление о структуре гена, его функционировании, регуляции его активности складывалось во второй половине XX века. Важными вехами на этом пути стали; • открытие двухспиральной структуры ДНК; • выделение РНК и выяснение ее роли в передаче наследственной информации от ДНК к РНК и белку; • расшифровка генетического кода.
В 1961 г. М. Ниренберг и Дж. Матеи открыли кодирующие свойства синтетических полирибонуклеотидов в бесклеточных системах трансляции. Было показано, что UUU кодирует фенилаланин, AAA —лизин, ССС - пролин. В 1964 г. генетический код был расшифрован полностью. Стало очевидно, что ген представляет собой определенную последовательность нуклеотидов в молекуле ДНК.
При этом каждые три основания в цепи ДНК кодируют одну аминокислоту в соответствующих полипептидных цепях,
В отличие от генов, кодирующих белки, процесс считывания информации с генов рибосомной РНК (рРНК) и транспортной РНК (тРНК) заканчивается на их транскрипции. С 1966 г. методом гибридизации ДНК с радиоактивно меченной РНК изучалась локализация генов рРНК у ряда объектов. Оказалось, что локусы рибосомных генов 18S и 28S чаще расположены в гетерохроматиновых прицентромерной и теломерной областях хромосом, У человека рибосомные гены картируются в коротких плечах акроцентрических хромосом. Гены JS-pPHK, как правило, выявляются в различных хромосомах и вне ядрышкового организатора.
Во второй половине 70-х гг. появились данные о локализации генов тРН К у Е. coli, дрожжей, Xenopus laevis, Drosophita melanogaster. Гены, кодирующие рибосомную и транспортную РНК были отнесены к генам «домашнего хозяйства», поскольку работают в каждой клетке и необходимы для поддержания ее жизнеспособности. Однако в отличие от генов рРНК, гены тРН К диспергированы по геному.
Бурное развитие молекулярной биологии, появление новых методов и приборов, в частности секвенаторов, сделало возможным изучение структуры генов у эукаритов.
Первыми в конце 70-х гг. были расшифрованы нуклеотидные последовательности глобиновых генов человека. Оказалось, что эукариотические гены устроены сложнее, чем гены прокариотов. Они имеют мозаичную структуру и состоят из кодирующих участков - экзонов и расположенных между ними некодируюших областей - нитронов. При транскрипции ДНК считывается целиком, а затем образовавшаяся пре-мРНК подвергается созреванию (процессингу); участки РНК транскрибированные с интронов, вырезаются, а участки РНК, ситезированные на экзонах, сшиваются (сплайсинг), Наряду с последовательным вырезанием интронов, существует eute и альтернативный сплайсинг, в результате которого экзоны одного гена соединяются в разных комбинациях с образованием различных зрелых мРНК.
Это явление в корне изменило представление о гене, как единице наследственности, кодирующей только одггу полипептид>гую цепь. Вот почему в современной генетической литературе нет единого общепринятого определения термина «ген». Так, в основу одних определений положена структурная организация гена, других — функция в организме, в третьих определениях - ген рассматривается как единица в процессе транскрипции, а четвертых — к перечисленным функциям добавляется возможность транскрипции с одного гена нескольких вариантов мРН К. Мы предлагаем расширенное определение термина «ген» с учетом его структурных и функциональных особенностей.
Структурный ген — это участок ДИК или РНК (у некоторых вирусов), определяющий линейную последовательность полипептидной цепи или одной молекулы тРНК или рРНК. За счет разных рамок считывания, альтернативного сплайсинга и различных промоторов с одного гена могут быть транскрибированы несколько мРНК, выполняющих сходные иди различные функции.
В3.Дизентерийная амёба. Особенности строения, цикла развития, пути распространения, патогенное действие. Методы лабораторной диагностики.
Дизентерийная амёба (лат. Entamoeba histolytica) — вид паразитических протозоа класса саркодовые. Вызывает тяжёлое заболевание — амебиаз (амёбную дизентерию, амёбный колит). Вид впервые описан в 1875 году русским ученым Ф. А. Лешем[1].
Размером дизентерийная амёба мельче обыкновенной амёбы (Amoeba proteus), подвижна. Эктоплазма чётко отграничена от эндоплазмы, псевдоподии короткие и широкие.

Заражение
Заражение наступает при попадании цист в верхний отдел толстого кишечника (слепая и восходящая ободочная кишка). Здесь цисты превращаются в просветные формы и внедряются в ткань кишки (тканевая форма), что сопровождается воспалением и формированием язв.
Просветная форма
Просветная форма дизентерийной амёбы (лат. forma minuta) имеет размер около 20 мкм. Находится в верхнем отделе толстого кишечника. Движется с помощью псевдоподий. Ядро сферическое, 3-5 мкм в поперечнике, хроматин расположен под ядерной оболочкой в виде небольших глыбок; в центре ядра небольшая кариосома.
Тканевая форма
При внедрении просветной формы амёбы в ткани образуется тканевая форма (лат. forma magna) размером 20-60 мкм. В отличие от просветной формы не содержит в цитоплазме никаких включений. В этой стадии амёба размножается в стенке толстой кишки, образуя язвы. Язвенное поражение толстого кишечника сопровождается выделением слизи, гноя и крови.
Большая вегетативная форма
Просветные и тканевые формы амёбы, попавшие в просвет кишки из язв, увеличиваются в размере до 30 мкм и больше и приобретают способность фагоцитировать эритроциты. Эта форма называется большой вегетативной, или эритрофагом.
Иногда амёбы из кишечника по кровеносным сосудам проникают в другие органы (прежде всего печень), формируя там вторичные очаги — абсцессы (внекишечный амёбиаз).
При затихании острой фазы болезни большая вегетативная форма уменьшается в размерах, переходит в просветную форму, которая инцистируется в кишечнике. Выброшенная при дефекации во внешнюю среду, она погибает в течение 15-20 минут.
Цисты образуются при сгущении фекалий в толстой кишке. Просветная форма окружается оболочкой и превращается в шаровидную цисту (размер около 12 мкм) с 4 ядрами, не отличающимися по строению от ядра вегетативной формы. Незрелые цисты содержат 1-2 или 3 ядра. Имеют вакуоль с гликогеном. Часть цист хроматоидные тела.
С фекалиями цисты выбрасываются во внешнюю среду и при попадании в желудочно-кишечный тракт человека после метацистной стадии развития (деления на 8 дочерних амёб) образуют просветные формы.
Цисты могут сохранять жизнеспособность в воде и влажной почве более месяца[1].
Билет 11
В1.----
В2.Генетический полиформизм и разнообразие геномов человека.
Генетически полифомизм- это сосуществование в пределах популяции (См. Популяция) двух или нескольких различных наследственных форм, находящихся в динамическом равновесии в течение нескольких и даже многих поколений. Чаще всего Г. п. обусловливается либо варьирующими давлениями и векторами (направленностью) отбора в различных условиях (например, в разные сезоны), либо повышенной относительной жизнеспособностью гетерозигот. Один из видов Г. п. — сбалансированный Г. п. — характеризуется постоянным оптимальным соотношением полиморфных форм, отклонение от которого оказывается неблагоприятным для вида, и автоматически регулируется (устанавливается оптимальное соотношение форм). В состоянии сбалансированного Г. п. у человека и животных находится большинство генов. Различают несколько форм Г. п., анализ которых позволяет определять действие отбора в природных популяциях.
В3. Схема клинической классификации ядовитых растений представляется в следующем виде.
Растения, вызывающие преимущественно симптомы поражения центральной нервной системы:
растения, вызывающие возбуждение центральной нервной системы;
растения, вызывающие возбуждение центральной нервной системы и одновременно действующие на пищеварительный тракт, сердце и почки;
растения, вызывающие угнетение и паралич центральной нервной системы;
растения, вызывающие угнетение и паралич центральной нервной системы и одновременно действующие на желудочно-кишечный тракт и сердечно-сосудистую систему.
Растения, вызывающие преимущественно симптомы поражения желудочно-кишечного тракта и одновременно действующие на центральную нервную систему и почки.
Растения, вызывающие преимущественно симптомы поражения органов дыхания и пищеварительного тракта (растения, образующие горчичные масла).
Растения, вызывающие преимущественно симптомы поражения сердца.
Растения, вызывающие преимущественно симптомы поражения печени.
Растения, вызывающие аноксемические явления (явления задушения):
растения, образующие (при определенных условиях) синильную кислоту;
растения, образующие (при определенных условиях) низшие окислы азота.
Растения, сенсибилизирующие (повышающие чувствительность) животных к действию солнечного света.
Растения, вызывающие признаки геморрагического диатеза (множественных кровоизлияний).
Растения, вызывающие нарушения половой деятельности животных.
Растения, вызывающие заболевания с характером витаминной недостаточности.
Растения, вызывающие симптомы нарушения солевого обмена.
Растения, причиняющие механические повреждения.
Отравления водорослями. Планктонные отравления.
Растения, вызывающие порчу молока.
Растения, вызывающие гибель пчел и порчу меда.
Растения, менее изученные в токсикологическом отношении.
Растения с атропиновым действием: Беладонна, Красавка, Дурман обыкновенный, Белена черная, отравления растениями, содержащими атропин наблюдается преимущественно вавгусте – сентябре, в период созревания их плодов.
Билет 12
В1. Пероксисомы. Образование строение ф-ции.
Пероксисома (лат. peroxysoma) — обязательная органелла эукариотической клетки, ограниченная мембраной, содержащая большое количество ферментов, катализирующих окислительно-восстановительные реакции (оксидазы D-аминокислот, уратоксидазы и каталазы). Имеет размер от 0,2 до 1,5 мкм, отделена от цитоплазмы одной мембраной.
Набор функций пероксисом различается в клетках разных типов. Среди них: окисление жирных кислот, фотодыхание, разрушение токсичных соединений, синтез желчных кислот, холестерина, а также эфиросодержащих липидов, построение миелиновой оболочки нервных волокон, метаболизме фетановой кислоты и т. д. Наряду с митохондриями пероксисомы являются главными потребителями O2 в клетке.
В пероксисоме обычно присутствуют ферменты, использующие молекулярный кислород для отщепления атомов водорода от некоторых органических субстратов (R) с образованием перекиси водорода (H2O2):
RH2 + O2 → R + H2O2
Каталаза использует образующуюся H2O2 для окисления множества субстратов — например, фенолов, муравьиной кислоты, формальдегида и этанола:
H2O2 + R`H2 --> R`+ 2H2O
Этот тип окислительных реакций особенно важен в клетках печени и почек, пероксисомы которых обезвреживают множество ядовитых веществ, попадающих в кровоток. Почти половина поступающего в организм человека этанола окисляется до ацетальдегида этим способом. Кроме того, реакция имеет значения для детоксикации клетки от самой перекиси водорода.
Новые пероксисомы образуются чаще всего в результате деления предшествующих, как митохондрии и хлоропласты. Они, однако, могут формироваться и de novo из эндоплазматического ретикулума, не содержат ДНК и рибосом, поэтому высказанные ранее предположения об их эндосимбиотическом происхожденим необоснованны[1].
Все ферменты, находящиеся в пероксисоме, должны быть синтезированы на рибосомах вне её. Для их переноса из цитозоля внутрь органеллы мембраны пероксисом имеют систему избирательного транспорта.
В2.Регуляция экспрессии генов у эукариот (на уровне транскрипции, процессинга и посттранскрипционном уровне).
Переключение генов лучше всего изучено у прокариот (бактерий). Рассмотрим механизмы регуляции активности генов на примере лактозного оперона кишечной палочки (Escherichia coli) – классического объекта генетики микроорганизмов. Единицей регуляции экспрессии генов у прокариот является оперон.
Оперон – это участок бактериальной хромосомы, включающий следующие участки ДНК: Р – промотор, О – оператор, Z, Y, А – структурные гены, Т – терминатор. (В состав других оперонов может входить до 10 структурных генов и более.)
Промотор – это регуляторный участок ДНК, который служит для присоединения РНК-полимеразы к молекуле ДНК. В лактозном опероне присоединение РНК-полимеразы происходит с помощью комплекса CAP-цАМФ (CAP – это специфический белок; в свободной форме является неактивным активатором, цАМФ – циклоаденозинмонофосфат – циклическая форма аденозинмонофосфорной кислоты).
Оператор – это регуляторный участок ДНК, который способен присоединять белок-репрессор, который кодируется соответствующим геном lac. Если репрессор присоединен к оператору, то РНК-полимераза не может двигаться вдоль молекулы ДНК и синтезировать мРНК.
Структурные гены кодируют три фермента, необходимые для расщепления лактозы (молочного сахара) на глюкозу и галактозу. Молочный сахар лактоза – менее ценный продукт питания, чем глюкоза, поэтому в присутствии глюкозы сбраживание лактозы является невыгодным для бактерии процессом. Однако при отсутствии глюкозы бактерия вынуждена переходить на питание лактозой, для чего синтезирует соответствующие ферменты Z (β-галактозидазу), Y (галактозидпермеазу), А (тиогалактозидтрансацетилазу).
Терминатор – это регуляторный участок ДНК, который служит для отсоединения РНК-полимеразы после окончания синтеза мРНК, соответствующей ферментам Z, Y, А, необходимым для усвоения лактозы.
Для регуляции работы оперона необходим ген cya, кодирующий белок CYA, который катализирует образование цАМФ из АТФ, Если в клетке имеется глюкоза, то белок CYA вступает с ней в реакцию и переходит в неактивную форму. Таким образом, глюкоза блокирует синтез цАМФ и делает невозможным присоединение РНК-полимеразы к промотору. Следовательно, глюкоза является репрессором лактозного оперона.
Если же в клетке имеется лактоза, то она взаимодействует с белком-репрессором и превращает его в неактивную форму. Белок-репрессор, связанный с лактозой, не может присоединиться к оператору и не преграждает путь РНК-полимеразе. Таким образом, лактоза является индуктором лактозного оперона.
Предположим, что первоначально в клетке имеется только глюкоза. Тогда белок-репрессор присоединен к оператору, а РНК-полимераза не может присоединиться к промотору. Оперон не работает, структурные гены выключены.
При появлении в клетке лактозы и при наличии глюкозы белок-репрессор отщепляется от оператора и открывает путь РНК-полимеразе. Однако РНК-полимераза не может присоединиться к промотору, поскольку глюкоза блокирует синтез цАМФ. Оперон по-прежнему не работает, структурные гены выключены.
Если же в клетке имеется только лактоза, то белок-репрессор связывается с лактозой, отщепляется и открывает путь РНК-полимеразе. В отсутствии глюкозы белок CYA катализирует синтез цАМФ, и РНК-полимераза присоединяется к промотору. Структурные гены включаются, РНК-полимераза синтезирует мРНК, с которой транслируются ферменты, обеспечивающие сбраживание лактозы.
Таким образом, лактозный оперон находится под двойным контролем индуктора (лактозы) и репрессора (глюкозы).
Общие принципы регуляции активности генов
Кроме лактозного оперона, у кишечной палочки хорошо изучены и другие опероны: триптофановый (trp), гистидиновый (his) и другие.
Общие принципы регуляции активности генов в оперонах разработали Франсуа Жакоб и Жак Моно (1961; Нобелевская премия 1965). Согласно концепции Жакоба–Моно, единицей регуляции активности генов у прокариот является оперон. Транскрипция группы структурных генов, регулируется двумя элементами – геном-регулятором и оператором. Оператор часто локализуется между промотором и структурными генами; ген-регулятор может локализоваться рядом с опероном или на некотором расстоянии от него.
Если продуктом гена-регулятора является белок-репрессор, его присоединение к оператору блокирует транскрипцию структурных генов, препятствуя присоединению РНК-полимеразы к специфичному участку – промотору, необходимому для инициации транскрипции. Напротив, если белком-регулятором служит активный апоиндуктор, его присоединение к оператору создает условия для инициации транскрипции. В регуляции работы оперонов участвуют также низкомолекулярные вещества – эффекторы, выступающие как индукторы либо корепрессоры структурных генов, входящих в состав оперонов.
Различают индуцируемые (включаемые) и репрессируемые (выключаемые) опероны в зависимости от типа влияния на их работу молекул-эффекторов.
У индуцируемых оперонов эффектор присоединяется к белку-репрессору и блокирует его связывание с оператором, препятствуя транскрипции структурных генов. Такой тип регуляции работы оперона называют негативным. При негативном контроле эффектор, являющийся корепрессором, присоединяется к неактивному репрессору и активирует его. В результате репрессор приобретает способность присоединяться к оператору и тем самым блокировать транскрипцию оперона. Таким образом, при негативном контроле эффектор связывается с репрессором, что приводит к его инактивации либо активации и соответственно индуцирует либо репрессирует транскрипцию оперона.
Наряду с этим, индуцируемые опероны могут находиться под позитивным контролем регуляции, при котором эффектор связывается с регуляторным белком и активирует его. Активный апоиндуктор присоединяется к оператору, что обеспечивает возможность транскрипции оперона. Оба типа контроля регуляции действуют и в отношении репрессируемых оперонов. При позитивном контроле функционирования репрессируемого оперона корепрессор связывается с активным апоиндуктором. Такой комплекс не может присоединяться к оператору, и структурные гены не транскрибируются. При позитивном контроле эффектор присоединяется не к репрессору, а к апоиндуктору, что разрешает, или, напротив, блокирует транскрипцию в зависимости от того, какую форму (активную или неактивную) приобретает апоиндуктор в результате связывания с эффектором. Поскольку при транскрипции оперона, состоящего из нескольких структурных генов, образуется один общий транскрипт в виде молекулы полицистронной мРНК, все эти гены экспрессируются координировано.
В3.Понятие о гельминтах. Гео- и биогельминты.
Геогельминты (от гео... и гельминты), группа паразитических червей человека и животных, развивающихся (в отличие от биогельминтов) без промежуточных хозяев. Яйца Геогельминты с фекалиями попадают в почву, где развиваются в тёплое время года до стадии личинок. Заражение человека происходит либо через немытые овощи, фрукты, руки, на которых находятся инвазионные яйца (например, аскариды, власоглава человеческого, острицы), либо при непосредственном контакте с землёй, где живут личинки (например, анкилостомид).
Биогельминты (от био... и гельминты), группа паразитических червей, которые во взрослом состоянии паразитируют в т. н. дефинитивном (окончательном) хозяине (человек, животное), а на стадии личинки — в промежуточном хозяине (разные животные), в отличие от геогельминтов, развивающихся без промежуточного хозяина. Например, взрослый бычий цепень (см. Цепни) паразитирует в кишечнике человека, а его личинки — финки — развиваются в мышцах крупного рогатого скота. Заражение человека происходит при употреблении в пищу полусырого финнозного мяса. К Биогельминты относятся также лентец широкий, печеночная двуустка, трихина, эхинококк и многие другие гельминты. Термин предложен советским гельминтологом К. И. Скрябиным.
В4. В3 Схема клинической классификации ядовитых растений представляется в следующем виде.
Растения, вызывающие преимущественно симптомы поражения центральной нервной системы:
растения, вызывающие возбуждение центральной нервной системы;
растения, вызывающие возбуждение центральной нервной системы и одновременно действующие на пищеварительный тракт, сердце и почки;
растения, вызывающие угнетение и паралич центральной нервной системы;
растения, вызывающие угнетение и паралич центральной нервной системы и одновременно действующие на желудочно-кишечный тракт и сердечно-сосудистую систему.
Растения, вызывающие преимущественно симптомы поражения желудочно-кишечного тракта и одновременно действующие на центральную нервную систему и почки.
Растения, вызывающие преимущественно симптомы поражения органов дыхания и пищеварительного тракта (растения, образующие горчичные масла).
Растения, вызывающие преимущественно симптомы поражения сердца.
Растения, вызывающие преимущественно симптомы поражения печени.
Растения, вызывающие аноксемические явления (явления задушения):
растения, образующие (при определенных условиях) синильную кислоту;
растения, образующие (при определенных условиях) низшие окислы азота.
Растения, сенсибилизирующие (повышающие чувствительность) животных к действию солнечного света.
Растения, вызывающие признаки геморрагического диатеза (множественных кровоизлияний).
Растения, вызывающие нарушения половой деятельности животных.
Растения, вызывающие заболевания с характером витаминной недостаточности.
Растения, вызывающие симптомы нарушения солевого обмена.
Растения, причиняющие механические повреждения.
Отравления водорослями. Планктонные отравления.
Растения, вызывающие порчу молока.
Растения, вызывающие гибель пчел и порчу меда.
Растения, менее изученные в токсикологическом отношении.
Билет 13
В1. К мембранным белкам относятся белки, которые встроены в клеточную мембрану или мембрану клеточной органеллы или ассоциированы с таковой. Около 25 % всех белков являются мембранными.
Липи́ды (от греч. λίπος, lípos — жир) — широкая группа органических соединений, включающая жирные кислоты, а также их производные, как по радикалу, так и по карбоксильной группе.
Билет 7: Мембранные белки, липиды
1.Простые.
2.Сложные.
3.жироводобные.
Простые: простые + жирные кислоты
Шпора №2.
Сложные: спирт + жирная к-та + доп.стр.
Жироподобные в-ва: спирты (халестерин, сфингазин)
жирные к-ты (насыщенные) СН3-(СН)2-СООН.
производные липидов, стероиды, тестестерон.
Фосфолипид:
Шпора 3
Ф-ции липидов:
1.Источник энергии.
2.Запасные питательные в-ва. Запасы жиров расходуются животными и растениями в периоде зимней спячки.
3. «строительный материал». Фосфолипиды и стероиды формируют биологическую мембрану.
4. источник метаболической воды
5.выполняют защитную ф-цию
6.являются гормонами.
7.являются витаминами.
8. Жир - играет роль теплоизоляцилирующей прослойки
В2. Стволовы́е кле́тки — недифференцированные (незрелые) клетки, имеющиеся во всех многоклеточных организмах. Стволовые клетки способны самообновляться, образуя новые стволовые клетки, делиться посредством митоза и дифференцироваться в специализированные клетки, то есть превращаться в клетки различных органов и тканей.
Развитие многоклеточных организмов начинается с одной стволовой клетки — зиготы. В результате многочисленных циклов деления и процесса дифференцировки образуются все виды клеток, характерные для данного биологического вида. В человеческом организме их более 220. Стволовые клетки сохраняются и функционируют и во взрослом организме, благодаря им может осуществляться обновление и восстановление тканей и органов. Тем не менее, в процессе старения организма их количество уменьшается.
В современной медицине стволовые клетки человека трансплантируют, то есть пересаживают в лечебных целях. Например, трансплантация гемопоэтических стволовых клеток производится для восстановления процесса кроветворения при лечении лейкозов и лимфом.
1 июля 2010 года Федеральная службой по надзору в сфере здравоохранения и социального развития выдала первое разрешение на применение новой медицинской технологии ФС № 2010/255 (лечение собственными стволовыми клетками).
3 февраля 2011 года Федеральная службой по надзору в сфере здравоохранения и социального развития выдала разрешение на применение новой медицинской технологии ФС № 2011/002 (лечение донорскими стволовыми клетками следующих патологий: возрастные изменения кожи лица второй или третьей степени, наличие раневого дефекта кожи, трофической язвы, лечение аллопеции, атрофическое поражение кожи, в том числе атрофические полосы (striae), ожоги, диабетической стопы)
В3.Виды малярийных плазмоидов, патогенное действие для человека. Лабораторная диагностика.
Виды (формы) малярии
Симптоматика, течение и прогноз заболевания отчасти зависят от вида плазмодия, который является возбудителем данной формы болезни.
Возбудитель тропической малярии — P. falciparum. Вызывает наиболее опасную форму, часто протекающую с осложнениями и имеющую высокую смертность. Эта же форма наиболее широко распространена (91 % всех случаев малярии в 2006 г).
Возбудитель четырехдневной малярии — Plasmodium malariae. Приступы происходят обычно через 72 часа.
Возбудители трехдневной малярии и похожей на неё овале-малярии — соответственно, Plasmodium vivax и Plasmodium ovale. Приступы происходят через каждые 40-48 часов.
Эти формы малярии различаются также по длительности инкубационного периода, продолжительности разных стадий жизненного цикла плазмодиев, симптоматике и течению
Симптомы малярии обычно следующие: лихорадка, ознобы, артралгия (боль в суставах), рвота, анемия, вызванная гемолизом, гемоглобинурия (выделение гемоглобина в моче) и конвульсии. Возможно также ощущение покалывания в коже, особенно в случае малярии, вызванной P. falciparum. Также могут наблюдаться спленомегалия (увеличенная селезенка), нестерпимая головная боль, ишемия головного мозга. Малярийная инфекция смертельно опасна. Особенно уязвимы дети и беременные женщины.
Диагноз ставится на основе выявления паразитов в мазках крови. Традиционно используют два типа мазков — тонкий и толстый (или так называемую «толстую каплю»). Тонкий мазок позволяет с большей надёжностью определить разновидность малярийного плазмодия, поскольку внешний вид паразита (форма его клеток) при данном типе исследования лучше сохраняется. Толстый мазок позволяет микроскописту просмотреть больший объём крови, поэтому этот метод чувствительнее, но внешний вид плазмодия при этом изменяется, что не позволяет легко различать разновидности плазмодия. Поставить диагноз на основе микроскопического исследования зачастую бывает затруднительно, так как незрелые трофозоиты разных видов малярийного плазмодия плохо различимы, и обычно необходимо несколько плазмодиев, находящихся на разных стадиях созревания, для надёжной дифференциальной диагностики.
В настоящее время используются также быстрые диагностические тесты (RDT, Rapid Diagnostic Tests) с использованием иммунохимических наборов (более дорогие, но дающие результат через 5-15 минут и не требующие использования микроскопа) и тесты с помощью ПЦР (наиболее дорогие, но наиболее надежные)[23]
Билет 15
В1. Синтез белка в клетке. Генетический код. Функции и-,т-,р-РНК.
Одним из важнейших процессов, протекающих в клетке, является синтез белков. Клетка содержит тысячи белков, клетка должна непрерывно синтезировать белки для восстановления своих мембран, органоидов и т. п. Синтез белка требует больших затрат энергии. Источником этой энергии, как и для всех клеточных процессов, является АТФ. Многообразие функций белков определяется их первичной структурой, т. е. последовательностью аминокислот в их молекуле. В свою очередь наследственная информация о первичной структуре белка заключена в последовательности нуклео- тидов в молекуле ДНК. Участок ДНК, в котором содержится информация о первичной структуре одного белка, называется геном. Каждой аминокислоте белка в ДНК соответствует последовательность из трех расположенных друг за другом нуклеотидов — триплет. К настоящему времени составлена карта генетического кода, т. е. известно, какие триплетные сочетания нуклеотидов ДНК соответствуют той или иной из 20 аминокислот, входящих в состав белков. 64 различные аминокислоты, тогда как кодируется только 20 аминокислот. Оказалось, что многим аминокислотам соответствует не один, а несколько различных триплетов — кодонов. Очень важное свойство генетического кода — специфичность, один триплет всегда обозначает только одну-единственную аминокислоту. Генетический код универсален. Носителем всей генетической информации является ДНК, расположенная в ядре. Сам синтез белка происходит в цитоплазме клетки, на рибосомах. Из ядра в цитоплазму информация о структуре белка поступает в виде и-РНК. Для того чтобы синтезировать и-РНК, участок ДНК «разматывается», деспирализуется, а затем по принципу комплементарности на одной из цепочек ДНК с помощью ферментов синтезируются молекулы РНК. Т.о, информация о последовательности нуклеотидов какого-либо гена ДНК «переписывается» в последовательность нуклеотидов и-РНК. Это называется транскрипции. Строение всех т-РНК сходно. Виды т-РНК обязательно различаются по триплету нуклеотидов, расположенному на «верхушке». Этот триплет, получивший название антикодон, по генетическому коду соответствует той аминокислоте, которую предстоит переносить этой т-РНК. В цитоплазме происходит последний этап синтеза белка — трансляция. На тот конец и-РНК, с которого нужно начать синтез белка, нанизывается рибосома (рис. 1.15). Рибосома перемещается по молекуле и-РНК прерывисто, «скачками», задерживаясь на каждом триплете приблизительно 0,2 с. За это мгновение одна т-РНК из многих способна «опознать» своим антикодоном триплет, на котором находится рибосома. И если антикодон комплементарен этому триплету и-РНК, аминокислота отсоединяется от «черешка листа» и присоединяется пептидной связью к растущей белковой цепочке. В этот момент ибосома сдвигается по и-РНК на следующий триплет, кодирующий очередную аминокислоту синтезируемого белка, а очередная т-РНК «подносит» необходимую аминокислоту, наращивающую цепочку белка. Эта операция повторяется столько раз, сколько аминокислот должен содержать «строящийся» белок. Когда в рибосоме оказывается один из трипле тов, являющийся «стоп-сигналом» между генами, то ни одна и-РНК к такому триплету присоединиться не может, так как антикодонов к ним у т-РНК не бывает. В этот момент синтез белка заканчивается. Все описываемые реакции происходят за очень короткие промежутки времени. Подсчитано, что на синтез довольно крупной молекулы белка уходит всего около двух минут. Таким образом, трансляция — это перевод последовательности нуклеотидов молекулы и-РНК в последовательность аминокислот синтезируемого белка. И для каждой отдельной реакции белкового синтеза требуются специализированные ферменты. Генети́ческий код — свойственный всем живым организмам способ кодирования аминокислотной последовательности белков при помощи последовательности нуклеотидов.
В ДНК используется четыре нуклеотида — аденин (А), гуанин (G), цитозин (С), тимин (T), которые в русскоязычной литературе обозначаются буквами А, Г, Ц и Т. Эти буквы составляют алфавит генетического кода. В РНК используются те же нуклеотиды, за исключением тимина, который заменён похожим нуклеотидом — урацилом, который обозначается буквой U (У в русскоязычной литературе). В молекулах ДНК и РНК нуклеотиды выстраиваются в цепочки и, таким образом, получаются последовательности генетических букв. Для построения белков в природе используется 20 различных аминокислот. Каждый белок представляет собой цепочку или несколько цепочек аминокислот в строго определённой последовательности. Эта последовательность определяет строение белка, а следовательно все его биологические свойства. Набор аминокислот также универсален почти для всех живых организмов.
Реализация генетической информации в живых клетках (то есть синтез белка, кодируемого геном) осуществляется при помощи двух матричных процессов: транскрипции (то есть синтеза и-РНК на матрице ДНК) и трансляции генетического кода в аминокислотную последовательность (синтез полипептидной цепи на р-РНК). Для кодирования 20 аминокислот, а также сигнала «стоп», означающего конец белковой последовательности, достаточно трёх последовательных нуклеотидов. Набор из трёх нуклеотидов называется триплетом. Принятые сокращения, соответствующие аминокислотам и кодонам.
иРНК - информационная - несёт закокодированную информацию о ДНК в рибосомы. в трансляции несет инфо о последовательности аминокислот белка. тРНК - транспортная - переносит аминокислоты в место синтеза белков рРНК - рибосомная - производит синтез белка
В2.Периоды онтогенеза человека (пренатальное развитие). Понятие о критических периодах.
Исследования преимуществ внутриутробной стимуляции проводились по всему миру. Их результаты показали, что ребенок может обучаться до рождения. Поэтому, хотя традиционно считалось, что самое главное - это стимуляция детей с рождения до 7 лет, не менее важно помнить о преимуществах внутриутробного обучения. Исследования показали, что дети, которых стимулировали до рождения, быстрее смогли овладеть многими зрительными, языковыми и двигательными навыками. Кроме того, были получены данные, свидетельствующие о том, что мозг таких детей лучше развит, и их интеллектуальный уровень очень высок. Один из видов пренатальной стимуляции - проигрывание ребенку классической музыки. Многие специалисты считают, что классическая музыка - один из лучших источников информации. Кроме того, можно говорить со своим ребенком, петь ему и гладить свой живот - все это будет способствовать внутриутробному обучению малыша. И все-таки лучший способ внутриутробной стимуляции ребенка и развития его мозга - это звук. Считается, что если ребенок, находясь в утробе, слышал голоса своих родителей, он узнает их и сразу после рождения. Разговор с ребенком будет полезен не только как стимуляция, но и как еще одна возможность для отца ребенка установить с ним более тесную связь. Когда вы говорите со своим ребенком не забывайте о том, что первый шаг в овладении языковыми навыками - это усвоение интонаций. Очень важно, чтобы с ребенком говорили оба родителя. Голос матери более высок и мелодичен, к тому же ребенок слышит его постоянно. Голос отца более низкий и сильный, поэтому он легче проникает через плаценту.
В3.Описать ядовитые растения, преимущественно оказывающие действие на ЦНС.
Ядовитые растения - это растения, вырабатывающие и накапливающие в процессе жизнедеятельности яды, вызывающие отравления животных и человека. В мировой флоре известно более 10 тыс. видов таких растений. Многие растительные яды в небольших дозах являются ценными лечебными средствами.
1. Растения с преимущественным действием на центральную нервную систему, которое проявляется в виде повышенного возбуждения, усиления кровообращения и дыхания, появления судорог или, наоборот, затрудненности произвольных движений, понижения общей чувствительности и т.д. (отравления дурманом, беленой, полынью, вехом, плевелом опьяняющим, пикульником).
Билет 16
В1. Поверхностный аппарат клетки. Пассивный транспорт.
1.Поверхностный аппарат клетки (гликокаликс).
2. плазматическая мембрана (жидкостно-мазаичная), плазмолема – жидкостно-мазаичная модель.
3. субмемранный комплекс (гипопротеиды – белки меняющие, алигосахариды –белки которые от 2-16 углиродов).
+шпора 7 и 6
Пассивный транспорт – перенос веществ по градиенту концентрации из области высокой концентрации в область низкой, без затрат энергии (напр. Диффузия, осмос) Диффузия – пассивное перемещение вещества из участка большей концентрации к участку меньшей концентрации. Осмос – пассивное перемещение некоторых веществ через полупроницаемую мембрану (обычно мелкие молекулы проходят, крупные нет). Существует 3 типа проникновения веществ в клетку через мембраны: простая диффузия, облегченная диффузия, активный транспорт.
В2.Организация генома человека.
Международная организация по изучению генома человека (англ. The Human Genome Organisation, HUGO) — организация, созданная в рамках проекта проекта «Геном человека». HUGO была создана в 1989 году в качестве международной организации, прежде всего для стимулирования сотрудничества между генетиками во всем мире. С момента образования в HUGO вошли 220 учёных из разных стран, в том числе пять советских биологов.
С самого начала работ по геномному проекту была выработана договорённость об открытости и доступности всей получаемой информации для его участников независимо от их вклада и государственной принадлежности. Все 23 хромосомы человека были поделены между странами-участницами. Советские учёные должны были исследовать структуру 3-й и 19-й хромосом. Однако, в связи с политической обстановкой в СССР и последующем его распадом финансирование этих работ было урезано, и реального участия в секвенировании отечественные учёные не принимали[1]. Программа геномных исследований в России была полностью перестроена и сконцентрирована на новой области — биоинформатике, занимающейся анализом и осмыслением уже полученных результатов.
На сегодняшний день целями исследований HUGO являются[2]:
Исследование природы, структуры, функций и взаимодействий генов, геномных элементов и генома человека, а также установление взаимосвязи между генами и соответствующими заболеваниями;
Изучение природы, распределения и эволюцию генетических вариаций в организме человека и в других организмах;
Установление взаимосвязи между генетическими изменениями и окружающей средой, изучение генетических особенностей различных народов и разработка методов диагностики, лечения и профилактики генетических заболеваний;
Развитие сотрудничества, распространение информации и координация деятельности в областях протеомики, биоинформатики, моделирования биологических систем, а также в области медицинских
В3. Трансмиссивные болезни (лат. transmissio — перенесение на других) — заразные болезни человека, возбудители которых передаются кровососущими членистоногими (насекомыми и клещами).
Трансмиссивные болезни включают более 200 нозологических форм, вызываемых вирусами, бактериями, риккетсиями, простейшими и гельминтами. Часть из них передаётся только с помощью кровососущих переносчиков (облигатные трансмиссивные болезни, например сыпной тиф, малярия и др.), часть различными способами, в том числе и трансмиссивно (например, туляремия, заражение которой происходит при укусах комаров и клещей, а также при снятии шкурок с больных животных).
Билет 17
В1. Поверхностный аппарат клетки. Активный транспорт.
1.Поверхностный аппарат клетки (гликокаликс).
2. плазматическая мембрана (жидкостно-мазаичная), плазмолема – жидкостно-мазаичная модель.
3. субмемранный комплекс (гипопротеиды – белки меняющие, алигосахариды –белки которые от 2-16 углиродов).
(трансмембранный А.т.) или через слой клеток (трансцеллюлярный А.т.), протекающий против градиента концентрации из области низкой концентрации в область высокой, т. е. с затратой свободной энергии организма. В большинстве случаев, но не всегда, источником энергии служит энергия макроэргических связей АТФ.
Различные транспортные АТФазы, локализованные в клеточных мембранах и участвующие в механизмах переноса веществ, являются основным элементом молекулярных устройств — насосов, обеспечивающих избирательное поглощение и откачивание определенных веществ (например, электролитов) клеткой. Активный специфический транспорт неэлектролитов (молекулярный транспорт) реализуется с помощью нескольких типов молекулярных машин — насосов и переносчиков. Транспорт неэлектролитов (моносахаридов, аминокислот и других мономеров) может сопрягаться с симпортом — транспортом другого вещества, движение которого по градиенту концентрации является источником энергии для первого процесса. Симпорт может обеспечиваться ионными градиентами (например, натрия) без непосредственного участия АТФ.
Шпора 6 и 7
В2.Понятие о геномике и новый взгляд на эволюцию.
Геномика, наука о структуре и функционировании генома. Cформировалась в конце 80-х гг. 20 в. Стремительное её развитие ( работы по физич. и генетич. картированию генома, секвенированию ДНК, анализу последовательностей нуклеотидов с помощью компъютерных технологий) было обусловлено исследованиями, проводимыми по международной программе “ Геном человека”.
Геномика подразделяют на структурную, функциональную и сравнительную. Задачами структурной Г. являются изучение содержания и организации геномной информации – последовательности нуклеотидов всех молекул ДНК клетки (ядерной, митохондриальной, хлоропластной). Функциональная геномика. анализирует пути реализации информации от гена к признаку, начиная с этапа модификации нуклеотидов в молекуле ДНК (эпигеномика). Функциональную геномику часто отождествляют с транскриптомикой, исследующей структуры и количества всех матричных РНК (первичных продуктов функционирования генов) в данной клетке в данных условиях. Иногда в круг её интересов входит и познание последующих уровней реализации генетич. информации, названных (про аналогии с геномикой) протеомикой, метаболомикой (изучающей метаболиты) и целомикой (исследующей работу клеток). На уровне выше клеточного структурными и функциональными единицами являются организм, затем генетически целостная совокупность организмов, поддерживаемая в поколениях ( популяция), и, наконец, совокупность популяций разных видов, взаимодействующих в данном поколении и в их череде (биоценоз).
Сравнительная геномика изучает варианты последовательностей нуклеотидов или их блоков в участках молекулы ДНК, общих по происхождению у разных организмов одного вида или у разных видов, в т. ч. отдалённых. Все эти направления Геномика вносят вклад в фундаментальную биологию, а также здравоохранение, с. х-во и биотехнологию. В медицине это ДНК-диагностика большинства инфекционных болезней человека, определение предрасположенности к наследственным болезням, генная терапия. Данные геномики используют в судебно-медицинской экспертизе при установлении отцовства, идентификации личности преступника и жертв катастроф, в т. ч. по останкам. На стыке геномики с этнографией, историей, археологией и лингвистикой возникла этногеномика, исследующая происхождение народов и их миграции по земному шару. В с. х-ве и биотехнологии понимание закономерностей функционирования геномов позволяет в короткие сроки получать растения, животных и микроорганизмы с заданными свойствами (напр., устойчивость к вредным воздействиям или эффективная продукция необходимых веществ, в т.ч. лекарственных).
В3. проблемы питания
Недостаточное питание. около 115 млн. детей всего мира имеют недостаточную массу тела; недостаточное питание способствует примерно трети всех случаев смерти детей; задержка развития (показатель хронического недоедания) препятствует развитию 186 миллионов детей в возрасте до 5 лет; 13 миллионов детей рождаются с низкой массой тела или преждевременно из-за недоедания матерей или в силу иных факторов; скрытое голодание выражается в недостатке основных витаминов и минералов в рационе, что влияет на иммунитет и здоровое развитие. Более трети детей дошкольного возраста всего мира испытывают нехватку витамина А; недостаточное питание матерей, широко распространенное во многих развивающихся странах, влечет неблагоприятное развитие плода и более высокий риск осложнений беременности; в совокупности на недостаточное питание матерей и детей приходятся более 10 процентов глобального бремени болезней.
Избыточный вес и ожирение: около 1,7 млрд. человек во всем мире имеют избыточный вес, из которых 500 млн. страдают ожирением; избыточным весом страдают 43 млн. детей в мире; рост показателей избыточного веса матерей усиливает риски осложнений беременности и влечет повышение массы тела при рождении и ожирение среди детей; во всем мире, по крайней мере, 2,6 млн. людей ежегодно умирают по причине избыточного веса или ожирения.
Сегодня экологически чистые (органические) продукты питания широко востребованы на мировом рынке.В развитых странах существуют четкие критерии, позволяющие отнести продукт к категории экологически чистые (органические) продукты. Экологически чистые продукты (органические) не содержат генетически модифицированные ингредиенты. Экологически чистые продукты (органические) не содержат ингредиенты выращенные при использовании пестицидов, гербицидов, ядохимикатов и искусственных удобрений. Экологически чистые продукты (органические) не содержат искусственные консерванты, красители и вкусовые добавки. Экологически чистые (органические) продукты обязаны иметь на упаковке специальные лицензионные символы «Органика».
Генетически модифицированные организмы (ГМО, genetically modified organism, GMO) создаются методами генной инженерии (genetic engineering) - науки, которая позволяет вводить в геном растения, животного или микроорганизма фрагмент ДНК из любого другого организма с целью придания ему определенных свойств
Билет 18
В1. Поверхностный аппарат клетки. Транспорт макромолекул.
Пузырьки осуществляют транспорт различных веществ путем быстрого и непрерывного челночного перемещения между различными окруженными мембраной органеллами эукариотической клетки. Экзоцитоз и эндоцитоз через плазматическую мембрану - лишь наиболее известные примеры этого сложного процесса. Несмотря на важность везикулярного транспорта , довольно мало известно о молекулярных механизмах, приводящих в действие, направляющих и регулирующих его. Очевидно, что для подобных процессов требуется энергия, возможно, в виде гидролиза АТР. Известно, что движение пузырьков в цитоплазме направляется микротрубочками и осуществляется белками-транслокаторами.
На цитоплазматических поверхностях пузырьков имеются, очевидно, специальные молекулы- маркеры , направляющие пузырьки к соответствующей мембране, однако о природе и разнообразии этих молекул ничего не известно.
Можно предположить, что непрерывное слияние мембран , имеющее место при опосредуемом пузырьками транспорте, приводит к значительному перемешиванию мембранных компонентов, однако различные мембраны в клетке сохраняют свой характерный состав. Подобное постоянство означает, что в клетке должны существовать специальные механизмы, восстанавливающие мембраны после их перемешивания .
В2.Экспериментальные доказательства генетической роли нуклеиновых кислот.
Известно, что бактерия Pneutnococcus pneumoniae имеет несколько форм. Вирулентность бактерии определяется наличием мукополисахаридной капсулы, расположенной па поверхности клетки. Эта капсула защищает бактерию от воздействий со стороны организма-хозяина. В результате, размножившиеся бактерии убивают зараженное животное. Бактерии этого штамма (S-штамм) образуют гладкие колонии. Авирулентные формы бактерий не имеют защитной капсулы и образуют шероховатые колонии (R-штамм). Микробиолог Фредерик Гриффитс в 1928 году инъецировал мышам живого пневмококка R-штамма вместе с S-штаммом, убитым высокой температурой (65°С). Спустя некоторое время ему удалось выделить из заражённых мышей живых пневмококков, обладающих капсулой. Таким образом, оказалось, что свойство убитого пневмококка - способность образовывать капсулу - перешло к живой бактерии, т.е. произошла трансформация. Поскольку признак наличия капсулы является наследственным, то следовало предположить, что какая-то часть наследственного вещества от бактерий штамма S перешла к клеткам штамма R.
В 1944 году О.Т. Эвери, К.М. Маклеод и М. Маккарти показали, что такое же превращение типов пневмококков может происходить в пробирке, т.е. in vitro. Эти исследователи установили существование особой субстанции -"трансформирующего принципа", -экстракта из клеток штамма S, обогащенного ДНK. Как далее выяснилось, ДНK, выделенная из клеток S-штамма добавленная в культуру R-штамма, трансформировала часть клеток в S-форму, Клетки стойко передавали это свойство при дальнейшем размножении. Обработка "трансформирующего фактора" ДНК-азой, ферментом разрушающим ДНK, блокирована трансформацию. Эти данные впервые показали, что именно ДНК, а не белок, как полагали до тех пор, является наследственным материалом.
2. 1952г. Эксперимент Альфреда Херши и Марты Чейз.
К ак
известно, фаг Т2 является вирусом,
инфицирующим бактерию E. coli. фаговые
частицы абсорбируются на наружной
поверхности клетки, их материал проникает
внутрь и примерно через 20 минут бактерия
лизируется, освобождая большое количество
фаговых частиц - потомков. В 1952 году
Альфред Херши и Марта Чейз инфицировали
бактерии фагами Т2, которые были мечены
радиоактивными соединениями: ДНК - с
помощью 32P. Белковая часть фага - 35S. После
инфекции бактерии фагами, с помощью
центрифугирования удалось выделить
две фракции: пустые белковые оболочки
фага и бактерии, инфицированных фаговой
ДНК. Оказалось, что 80% метки 35S осталась
в пустых фаговых оболочках, а 70% метки
32P - в инфицированных бактериях.
Фаги-потомки получили только около 1%
исходного белка, меченного 35S, однако
они же обнаружили около 30% метки 32P.
ак
известно, фаг Т2 является вирусом,
инфицирующим бактерию E. coli. фаговые
частицы абсорбируются на наружной
поверхности клетки, их материал проникает
внутрь и примерно через 20 минут бактерия
лизируется, освобождая большое количество
фаговых частиц - потомков. В 1952 году
Альфред Херши и Марта Чейз инфицировали
бактерии фагами Т2, которые были мечены
радиоактивными соединениями: ДНК - с
помощью 32P. Белковая часть фага - 35S. После
инфекции бактерии фагами, с помощью
центрифугирования удалось выделить
две фракции: пустые белковые оболочки
фага и бактерии, инфицированных фаговой
ДНК. Оказалось, что 80% метки 35S осталась
в пустых фаговых оболочках, а 70% метки
32P - в инфицированных бактериях.
Фаги-потомки получили только около 1%
исходного белка, меченного 35S, однако
они же обнаружили около 30% метки 32P.
Результаты этого эксперимента прямо показали, что ДНК родительских фагов проникает в бактерии и затем становиться составляющей развившихся новых фагов частиц.
3. 1957г. Опыты Френкеля - Конрата
Френкель-Конрат работал с вирусом табачной мозаики (ВТМ). В этом вирусе содержится РНК, а не ДНК. Было известно, что разные штаммы вируса вызывают разную картину поражения листьев табака. После смены белковой оболочки "переодетые" вирусы вызывали картину поражения, характерную для того штамма, чья РНК была покрыта чужим белком.
Следовательно, не только ДНК, но и РНК может служить носителем генетической информации.
На сегодняшний день существуют сотни тысяч доказательств генетической роли нуклеиновых кислот. Приведенные три являются классическими.
В3. Фитотоксиканты
химические и природные вещества в рецептурной форме для поражения различных видов растительности. Подразделяются на альгициды (поражение водной растительности), арборициды (древесно-кустарниковой), гербициды, десиканты (вегетирующей), дефолианты и др.
Фитотоксиканты — это загрязняющие атмосферу вещества, вредные для растений. Они поглощаются листьями, оттуда поступают в побега и другие органы растений. Атмосферные осадки способствуют поступлению растворенных фитотокси-кантов в растения.
Фитотоксиканты - химические вещества, вызывающие поражение растительности. Растения, обработанные фитотоксикантами, теряют листву, засыхают и погибают.
Билет 19
В1.Клетка –элиментарная единица живого. Отличительные признаки про- и эукоритических клеток.
Клетка представляет собой обособленную, наименьшую по размерам структуру, которой присуща вся совокупность свойств жизни и которая может в подходящих условиях окружающей среды поддерживать эти свойства в самой себе, а также передавать их в ряду поколений. Клетка, таким образом, несет полную характеристику жизни. Вне клетки не существует настоящей жизнедеятельности. Поэтому в природе планеты ей принадлежит роль элементарной структурной, функциональной и генетической единицы.
Это означает, что клетка составляет основу строения, жизнедеятельности и развития всех живых форм — одноклеточных, многоклеточных и даже неклеточных. Благодаря заложенным в ней механизмам клетка обеспечивает обмен веществ, использование биологической информации, размножение, свойства наследственности и изменчивости, обусловливая тем самым присущие органическому миру качества единства и разнообразия.
Занимая в мире живых существ положение элементарной единицы, клетка отличается сложным строением. При этом определенные черты обнаруживаются во всех без исключения клетках, характеризуя наиболее важные стороны клеточной организации как таковой.
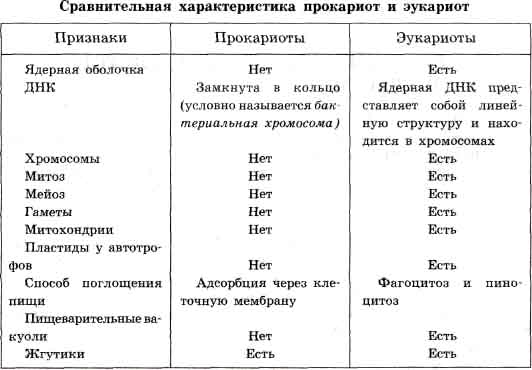
В2.Дифференциация пола эмбриона. Развитие вторичных половых признаков.
Определение пола плода в пренатальном периоде нетолько интересует будущих родителей, но и имеет большое значение для дифференциальной диагностики ряда врожденных и наследственных заболеваний. Тем не менее оценка пола плода не включена к настоящему моменту в обязательную часть скрининговыхультразвуковых исследований в акушерстве в первую очередь по этическим соображениям.
Определение пола плода при ультразвуковом исследовании во второй половине беременности обычно не вызывает затруднений. Мужской пол плода устанавливается при визуализации полового члена и мошонки, а женский - при визуализации половых губ. Для этого изучается область промежности в различных сечениях при двухмерной эхографии или используется режим поверхностной реконструкции при трехмерной эхографии.
Следует отметить, что в ряде случаев изображение петель пуповины, пальцев или отечных половых губ может имитировать изображение мужских половых признаков. Кроме этого, неудобное положение плода может препятствовать получению отчетливого изображения наружных половых органов. На сегодняшний день врач имеет право выбора: сообщать или не сообщать пациентке пол будущего ребенка.
Если пол сообщается, то должна сообщаться и вероятность возможной ошибки.
В последние годы особое внимание исследователей было направлено на разработку диагностических критериев, позволяющих определять пол плода в ранние сроки беременности. Начало формирования гениталий происходит на 5-6 нед гестации. При разрастании мезенхимы формируются половой бугорок, содержащий зачатки пениса или клитора, и половые складки, позже формирующие мошонку или половые губы. Между бугорком и складками образуется первичное половое отверстие. На ранних этапах гестации гениталии не дифференцированы. Их дифференцировка происходит под влиянием гормонов и видимые различия в строении наружных гениталий начинают проявляться в конце I триместра беременности.
Поэтому с внедрением трансвагинальной эхографии в клиническую практику появилась реальная возможность определения пола плода уже при скрининговом ультразвуковом исследовании в ранние сроки беременности. Согласно результатам проведенных исследований, точность определения пола плода в 11 нед беременности составляет 46-91,7%, в 12 нед-53,8-100%, в 13 нед-57,8-100% и в 14 нед - 80-94%. Наиболее часто среди причин невозможности установления пола плода указывается его неудобное для исследования положение, а среди причин ошибочного определения пола - схожее изображение наружных половых органов у плодов мужского и женского пола в ранние сроки. По данным В. Benoit, ошибки при определении пола плода из-за схожести изображения возможны не только в 11-12 нед, но и в 12-13 нед беременности.
Схожесть изображения наружных половых органов у плодов мужского и женского пола в ранние сроки беременности обусловлена эмбриологическими особенностями развития, которые объяснены в статье М.А. Эсетова. Именно поэтому определение пола плода на основании визуальных признаков, используемых во второй половине беременности не столь эффективно в ранние сроки. В связи с этим Z. Efrat и соавт. для определения пола плода в 11-14 нед беременности предложили проводить оценку угла между половым бугорком и горизонтальной линией, проходящей через поверхность кожи пояснично-крестцового отдела позвоночника. При величине угла более 30° пол плода расценивался как мужской, а при величине угла менее 30° или при расположении полового бугорка параллельно горизонтальной линии - как женский. Существенным преимуществом этого метода является отсутствие значительного влияния субъективного фактора. Согласно результатам авторов, точность определения пола плода составила 98,7% в 12 нед и 100% - в 13 нед беременности.
Высокая информативность этой методики послужила поводом для ее широкого применения, однако следует помнить и о морально-этических аспектах определения пола плода в ранние сроки беременности. В специальной книге, посвященной этике в акушерстве и гинекологии, справедливо отмечено: «Принятие решения определять или не определять пол плода при скрининговом ультразвуковом исследовании является только прерогативой исследователя». Именно специалист принимает решение отвечать или не отвечать на вопрос: «Доктор, а кто у меня будет - мальчик или девочка?!». При ответе на этот казалось бы, простой вопрос необходимо помнить следующие аспекты.
Во-первых, исследование проводится в ранние сроки, когда ваш ответ может повлиять на принятие решения о прерывании беременности. В настоящее время основным методом определения пола плода в ранние сроки является аспирация ворсин хориона. Хотя он и обладает наиболее высокой точностью, но существует риск прерывания беременности. С появлением неинвазивного метода определения пола плода в ранние сроки большее количество семей захотят регулировать рождение ребенка конкретного пола. Это в первую очередь оказывает влияние на увеличение рождения мальчиков и соответственно приводит к дискриминации плодов женского пола. Согласно данным одного из регионов Индии, на протяжении 10-летнего применения ультразвукового обследования во время беременности соотношение рождения мальчиков и девочек возросло с 107:100 до 132:100 за счет прерываний беременностей в случаях обнаружения плодов женского пола.
Во-вторых, процент ошибок при определении пола плода при ультразвуковом исследовании в ранние сроки беременности достаточно велик. Поэтому задающие вопрос пациентки должны быть информированы о реальных цифрахточности эхографии в руках конкретного специалиста, проводящего исследование. Это требует проведения специального детального анализа своей работы каждым врачом, который занимается оценкой пола плода в ранние сроки. Хочется надеяться, что отечественные специалисты будут взвешивать все «за» и «против» при определении пола плода при скрининговом ультразвуковом исследовании в ранние сроки беременности, руководствуясь главным принципом - «не навреди».
Одним из важных медицинских показаний для ультразвуковой оценки половых органов плода является установление гермафродитизма. Выделяют истинный гермафродитизм, мужской и женский псевдогермафродитизм.
Пренатальная диагностика этих состояний основана на сопоставлении данных кариотипа плода и визуальной картины половых органов. Т.С. Грищенкои Т.В. Комова приводят описание случая пренатальнои диагностики гермафродитизма в 33-34 нед беременности. При ультразвуковом исследовании у плода в области клитора визуализировалось образование размером 12x9 мм, по форме напоминающее половой член. Провести дифференциацию между гипертрофией клитора и гермафродитизмом не удалось. Окончательный диагноз был сформулирован после рождения ребенка, при осмотре которого выявлены гипоспадия, недоразвитие мошонки, напоминающей половые губы, отсутствие яичек. По этим данным был установлен мужской пол, а по результатам кариотипирования -женский пол.
О случае наиболее ранней диагностики женского псевдогермафродитизма сообщили V. Mazza и соавт.. Им удалось четко визуализировать мужские гениталии у плода в 13 нед беременности, а при кариотипировании был зарегистрирован женский кариотип.
В3.Токсоплазма. Морфофункциональная характеристика: цикл развития, пути заражения, патогенное действие, методы лабораторной диагностики.
Токсоплазма (лат. Toxoplasma) — монотипный род паразитических протозоев, включающий, видимо, один вид — Toxoplasma gondii. Основные хозяева токсоплазм — представители семейства кошачьих. В качестве промежуточных хозяев выступают различные виды теплокровных животных, в том числе и люди. Токсоплазмоз, болезнь, вызываемая токсоплазмой, обычно протекает у человека легко. Однако для плода, в случае если мать заразилась токсоплазмозом во время беременности, а также для человека или кошки с пониженным иммунитетом эта болезнь может иметь серьёзные последствия, вплоть до летального исхода. Toxoplasma gondii принадлежит к типу Apicomplexa и является единственным описанным видом рода Toxoplasma. Тем не менее, высказывалась гипотеза, что на самом деле может существовать несколько видов токсоплазм[
Жизненный цикл Toxoplasma gondii состоит из двух фаз. Половая часть жизненного цикла проходит только в особях некоторых видов семейства кошачьих (дикие и домашние кошки), которые становятся первичным хозяином паразитов. Бесполая часть жизненного цикла может проходить в любом теплокровном животном, например, в млекопитающих (и в кошках тоже) и в птицах.
В этих промежуточных хозяевах паразит вторгается в клетки, формируя так называемые межклеточные паразитофорные вакуоли, содержащие брадизоиты, медленно воспроизводящиеся формы паразита[2]. Вакуоли формируют тканевые цисты, в основном, в мышцах и в мозге. Так как паразит находится внутри клеток, то иммунная система хозяина не может обнаружить эти цисты. Сопротивляемость к антибиотикам различна, но цисты очень трудно вывести из организма полностью. Внутри этих вакуолей T. gondii размножается последовательностью делений на две части до тех пор, как инфицированная клетка в конце концов не лопается и тахизоиты не выходят наружу. Тахизоиты подвижны и бесполым способом размножаются, производя новых паразитов. В отличие от брадизоитов, свободные тахизоиты легко устраняются иммунной системой хозяина, но при этом могут заразить клетки и сформировать брадизоиты, тем самым поддерживая инфекцию.
Тканевые цисты проглатываются кошкой (например, когда она съедает заражённую мышь). Цисты выживают в желудке кошки, и паразиты заражают эпителиальные клетки тонкой кишки, где они приступают к половому размножению и формированию ооцист. Ооцисты выходят наружу с фекалиями. Животные (в том числе, люди) проглатывают ооцисты (например, поедая немытые овощи и т. д.) или тканевые цисты (в плохо приготовленном мясе) и заражаются. Паразиты внедряются в макрофаги в кишечном тракте и через кровь распространяются по телу.

Заражение токсоплазмой в острой стадии может быть бессимптомным, но часто вызывает симптомы гриппа на раннеострых стадиях, и, как и грипп, может в редких случаях привести к смерти. Острая стадия спадает за период от нескольких дней до месяцев, переходя в хроническую стадию. Хроническая инфекция обычно бессимптомна, но в случае иммунноослабленных пациентов (а также пациентов, заражённых ВИЧ, или пациентов, проходящих иммунноподавляющую терапию после пересадки органов) токсоплазмоз может развиваться. Наиболее частым проявлением токсоплазмоза у иммунноослабленных пациентов является токсоплазмозный энцефалит, который может привести к смерти. Если заражение T. gondii возникает впервые во время беременности, то паразит может проникнуть через плаценту, заразить плод, что может привести к гидроцефалии, внутричерепному обызвествлению или к хориоретиниту, а также к самопроизвольному аборту или внутриутробной смерти.
Было доказано, что паразит может влиять на поведение хозяина: заражённые крысы и мыши меньше боятся кошек; замечены факты того, что заражённые крысы сами ищут места, где мочилась кошка. Этот эффект благоприятен для паразита, который сможет размножаться половым способом, если его хозяин будет съеден кошкой[3]. Механизм этого изменения ещё до конца не изучен, но существуют доказательства того, что токсоплазмоз повышает уровень дофамина у заражённых мышей.
Существует несколько независимых наблюдений, подтверждающих роль заражения токсоплазмой в случаях проявления шизофрении и паранойи[5]:
Острая инфекция токсоплазмы иногда ведёт к психотическим симптомам, не отличающимся от шизофрении.
Некоторые антипсихотические медицинские препараты, используемые для лечения шизофрении (например, галоперидол), также останавливают развитие токсоплазмы в клеточных культурах.
Несколько исследований нашли значительно повышенные уровни антител к токсоплазме у пациентов, больных шизофренией, по сравнению со всем остальным населением.[6]
Заражение токсоплазмой ведёт к повреждению астроцитов в головном мозге, точно такие же повреждения астроцитов наблюдаются при шизофрении.
Активным исследователем роли токсоплазмы и других инфекций при шизофрении является американский психиатр Фуллер Тори.
Билет 20
В1.Опишите путь гидролаз от места их синтеза до места назначения.
ГИДРОЛАЗЫ, класс ферментов, катализирующих гидролиз. Могут действовать на сложноэфирные и гликозидные связи, на связи С—О в простых эфирах. С—S в сульфидах, С—N в пет идах, и др.
Гидролазы, катализирующие гидролиз сложноэфирных связей (эстеразы), действуют на сложные эфиры карбоновых и тио-карбоновых кислот, моноэфиры фосфорной кислоты и др. К этому подклассу относятся, в частности, ферменты, играющие важную роль в метаболизме липидов. нуклеиновых кислот и нуклеозидов. например арилсульфатазы, ацетилхолинэстераза, дезоксирибонуклеазы. липазы, фосфатазы, фосфолипазы и эндодезоксирибонуклеазы
Ферменты, катализирующие гидролиз связи С—N в пептидах и белках (пептидгидролазы),- самая многочисленная группа гидролазы К ним относятся ферменты, отщепляющие одну или две аминокислоты с N- или С-конца полипептидной цепи (напр., аминопептидазы, карбоксипептидазы), а также эндопептидазы, или протеиназы, расщепляющие цепь вдали от концевых остатков. Пептидгидролазы играют важную роль не только в катаболизме белков и пептидов, но и в биол. регуляции (гормональной регуляции, активации проферментов, регуляции кровяного давления и солевого обмена и т.д.).
В2.Классификация генов человека по структуре и функциям.
Ген представляет собой последовательность нуклеотидов ДНК размером от нескольких сотен до миллиона пар нуклеотидов, в которых закодирована генетическая информация о первичной структуре белка (число и последовательность аминокислот). Для регулярного правильного считывания информации в гене должны присутствовать: кодон инициации, множество смысловых кодонов и кодон терминации. Три подряд расположенных нуклеотида представляют собой кодон, который и определяет, какая аминокислота будет располагаться в данной позиции в белке. Например, в молекуле ДНК последовательность оснований ТАС является кодоном для аминокислоты метионина, а последовательность ТТТ кодирует фенилаланин. В молекуле иРНК вместо тимина (Т) присутствует основание урацил (У). Таблица генетического кода во всех руководствах представлена именно символами иРНК. Из 64 возможных кодонов смысловыми являются 61, а три триплета — УАА, УАГ, УГА — не кодируют аминокислоты и поэтому были названы бессмысленными, однако на самом деле они представляют собой знаки терминации трансляции. Для прокариот характерна относительно простая структура генов. Так, структурный ген бактерии, фага или вируса, как правило, контролирует одну ферментативную реакцию. Специфичным для прокариот является оперонная система организации нескольких генов. Гены одного оперона (участка генетического материала, состоящего из 1, 2 и более сцепленных структурных генов, которые кодируют белки (ферменты), осуществляющие последовательные этапы биосинтеза какого-либо метаболита; в оперон эукариот входит, как правило, 1 структурный ген; оперон содержит регуляторные элементы) расположены в кольцевой хромосоме бактерии рядом и контролируют ферменты, осуществляющие последовательные или близкие реакции синтеза (лактозный, гистидиновый и др. опероны). Структура генов у бактеориофагов и вирусов в основном схожа с бактериями, но более усложнена и сопряжена с геномом хозяев. Например, у фагов и вирусов обнаружено перекрывание генов, а полная зависимость вирусов эукариот от метаболизма клетки-хозяина привела к появлению экзон-интронной структуры генов. Эукариотические гены, в отличие от бактериальных, имеют прерывистое мозаичное строение. Кодирующие последовательности (экзоны) перемежаются с некодирующими (интронами). Экзон [от англ. ex(divssi)on — выражение, выразительность] - участок гена, несущий информацию о первичной структуре белка. В гене экзоны разделены некодирующими участками — интронами. Интрон (от лат. inter — между) - участок гена, не несущий информацию о первичной структуре белка и расположенный между кодирующими участками — экзонами. В результате структурные гены эукариот имеют более длинную нуклеотидную последовательность, чем соответствующая зрелая иРНК, последовательность нуклеотидов в которой соответствует экзонам. В процессе транскрипции информация о гене списывается с ДНК на промежуточную иРНК, состоящую из экзонов и интронов. Затем специфические ферменты — рестриктазы — разрезают эту про-иРНК по границам экзон-интрон, после чего экзонные участки ферментативно соединяются вместе, образуя зрелую иРНК (так называемый сплайсинг). Количество интронов может варьировать в разных генах от нуля до многих десятков, а длина — от нескольких пар оснований до нескольких тысяч. Ген может кодировать различные РНК-продукты путем изменения инициирующих и терминирующих кодонов, а также альтернативного сплайсинга. Альтернативная экспрессия гена осуществляется и путем использования различных сочетаний экзонов в зрелой иРНК, причем полипептиды, синтезированные на таких иРНК, будут различаться как по количеству аминокислотных остатков, так и по их составу. Наряду со структурными и регуляторными генами обнаружены участки повторяющихся нуклеотидных последовательностей, функции которых изучены недостаточно, а также мигрирующие элементы (мобильные гены), способные перемещаться по геному. Найдены также так называемые псевдогены у эукариот, которые представляют собой копии известных генов, расположенные в других частях генома и лишенные интронов или инактивированные мутациями. 3. Классификация генов Накопленные знания о структуре, функциях, характере взаимодействия, экспрессии, мутабильности и других свойствах генов породили несколько вариантов классификации генов. По месту локализации генов в структурах клетки различают расположенные в хромосомах ядра ядерные гены и цитоплазматические гены, локализация которых связана с хлоропластами и митохондриями. По функциональному значению различают структурные гены, характеризующиеся уникальными последовательностями нуклеотидов, кодирующих свои белковые продукты, которые можно идентифицировать с помощью мутаций, нарушающих функцию белка, и регуляторные гены — последовательности нуклеотидов, не кодирующие специфические белки, а осуществляющие регуляцию действия гена (ингибирование, повышение активности и др.). По влиянию на физиологические процессы в клетке различают летальные, условно летальные, супервитальные гены, гены-мутаторы, гены-антимутаторы и др. Следует отметить, что любые биохимические и биологические процессы в организме находятся под генным контролем. Так, деление клеток (митоз, мейоз) контролируется несколькими десятками генов; группы генов осуществляют контроль восстановления генетических повреждений ДНК (репарация). Онкогены и гены — супрессоры опухолей участвуют в процессах нормального деления клеток. Индивидуальное развитие организма (онтогенез) контролируется многими сотнями генов. Мутации в генах приводят к измененному синтезу белковых продуктов и нарушению биохимических или физиологических процессов. Гомеозисные мутации у дрозофилы позволили открыть существование генов, нормальной функцией которых является выбор или поддержание определенного пути эмбрионального развития, по которому следуют клетки. Каждый путь развития характеризуется экспрессией определенного набора генов, действие которых приводит к появлению конечного результата: глаза, голова грудь, брюшко, крыло, ноги и т. д. Исследования генов комплекса bithorax дрозофилы американским генетиком Льюисом показали, что это гигантский кластер тесно сцепленных генов, функция которых необходима для нормальной сегментации груди (thorax) и брюшка (abdomen). Подобные гены получили название гомеобоксных. Гомеобоксные гены расположены в ДНК группами и проявляют свое действие строго последовательно. Такие гены обнаружены и у млекопитающих, и они имеют высокую гомологию (сходство). 4. Функции генов В процессе реализации наследственной информации, заключенной в гене, проявляется целый ряд его свойств. Определяя возможность развития отдельного качества, присущего данной клетке или организму, ген характеризуется дискретностью действия (от лат. discretus — разделенный, прерывистый), прерывностью (интроны и экзоны). Дискретность наследственного материала, предположение о которой высказал еще Г. Мендель, подразумевает делимость его на части, являющиеся элементарными единицами, - гены. В настоящее время ген рассматривают как единицу генетической функции. Он представляет собой минимальное количество наследственного материала, которое необходимо для синтеза тРНК, рРНК или полипептида с определенными свойствами. Ген несет ответственность за формирование и передачу по наследству отдельного признака или свойства клеток, организмов данного вида. Кроме того, изменение структуры гена, возникающее в разных его участках, в конечном итоге приводит к изменению соответствующего элементарного признака. Ввиду того что в гене заключается информация об аминокислотной последовательности определенного полипептида, его действие является специфичным. Однако в некоторых случаях одна и та же нуклеотидная последовательность может детерминировать синтез не одного, а нескольких полипептидов. Это наблюдается в случае альтернативного сплайсинга у эукариот и при перекрывании генов у фагов и прокариот. Очевидно, такую способность следует оценить как множественное, или плейотропное, действие гена (хотя традиционно под плейотропным действием гена принято понимать участие его продукта – полипептида – в разных биохимических процессах, имеющих отношение к формированию различных сложных признаков). Например, участие фермента в ускорении определенной реакции (см. рис.), которая является звеном нескольких биохимических процессов, делает зависимыми результаты этих процессов от нормального функционирования гена, кодирующего этот белок. Нарушение реакции A→B, катализируемой белком α, в результате мутации гена ведет к выключению последующих этапов формирования признаков D и E. α D A B C E Определяя возможность транскрибирования мРНК для синтеза конкретной полипептидной цепи, ген характеризуется дозированностью действия, т.е. количественной зависимостью результата его экспрессии от дозы соответствующего аллеля этого гена. Примером может служить зависимость степени нарушения транспортных свойств гемоглобина у человека при серповидно-клеточной анемии от дозы аллеля НЬS. Наличие в генотипе человека двойной дозы этого аллеля, приводящего к изменению структуры β-глобиновых цепей гемоглобина, сопровождается грубым нарушением формы эритроцитов и развитием клинически выраженной картины анемии вплоть до гибели. У носителей только одного аллеля НЬS при нормальном втором аллеле лишь незначительно изменяется форма эритроцитов и анемия не развивается, а организм характеризуется практически нормальной жизнеспособностью.
В3 Схема клинической классификации ядовитых растений представляется в следующем виде.
Растения, вызывающие преимущественно симптомы поражения центральной нервной системы:
растения, вызывающие возбуждение центральной нервной системы;
растения, вызывающие возбуждение центральной нервной системы и одновременно действующие на пищеварительный тракт, сердце и почки;
растения, вызывающие угнетение и паралич центральной нервной системы;
растения, вызывающие угнетение и паралич центральной нервной системы и одновременно действующие на желудочно-кишечный тракт и сердечно-сосудистую систему.
Растения, вызывающие преимущественно симптомы поражения желудочно-кишечного тракта и одновременно действующие на центральную нервную систему и почки.
Растения, вызывающие преимущественно симптомы поражения органов дыхания и пищеварительного тракта (растения, образующие горчичные масла).
Растения, вызывающие преимущественно симптомы поражения сердца.
Растения, вызывающие преимущественно симптомы поражения печени.
Растения, вызывающие аноксемические явления (явления задушения):
растения, образующие (при определенных условиях) синильную кислоту;
растения, образующие (при определенных условиях) низшие окислы азота.
Растения, сенсибилизирующие (повышающие чувствительность) животных к действию солнечного света.
Растения, вызывающие признаки геморрагического диатеза (множественных кровоизлияний).
Растения, вызывающие нарушения половой деятельности животных.
Растения, вызывающие заболевания с характером витаминной недостаточности.
Растения, вызывающие симптомы нарушения солевого обмена.
Растения, причиняющие механические повреждения.
Отравления водорослями. Планктонные отравления.
Растения, вызывающие порчу молока.
Растения, вызывающие гибель пчел и порчу меда.
Растения, менее изученные в токсикологическом отношении.
Растения с преимущественным действием на сердце. В результате отравления ими учащаются сердечные сокращения, изменяется ритм, появляются симптомы слабости, иногда полностью останавливается сердечная деятельность (отравление растениями из рода наперстянка).
Растения, поражающие преимущественно сердечно-сосудистые, нервные центры и сердце. Клинически это выражается сначала замедлением, затем учащением сердечных сокращений. При отравлениях (наперстянкой, ландышем, вороньим глазом, будрой плющевидной) у животных могут появиться понос и другие заболевания.
В4. С - широкий лентец
В – сколекс широкого лентеца
Билет 21
В1. Особенности строения ростительной клетки. Осмос ростительной и животной клетки.
В растительной клетке есть все органоиды, свойственные в животной клетке. Вместе с тем она отличается от животной клетки следующими особенностями строения: 1) прочной клеточной стенкой значительной толщины; 2) особыми органоидами — пластидами, в которых происходит первичный синтез органических веществ из минеральных за счет энергии света — фотосинтез; 3) paзвитой системой вакуолей, в значительной мере обусловливающих осмотические свойства клеток. Растительная клетка, как и животная, окружена цитоплазматической мембраной, но, кроме нее, ограничена толстой состоящей из целлюлозы клеточной стенкой. Наличие клеточной стенки — специфическая Особенность растений. Она определила малую подвижность растений. Вследствие этого питание и дыхание организма стали зависеть от поверхности тела, контактирующей с окружающей средой, что привело в процессе эволюции к большей расчлененности тела, гораздо более выраженной, чем у животных. Клеточная стенка имеет поры, через которые каналы эндоплаэматической сети соседних клеток сообщаются друг с другом. Преобладание синтетических процессов над процессами освобождения энергии — одна из наиболее характерных особенностей обмена веществ растительных организмов. Первичный синтез углеводов из неорганических веществ осуществляется в пластидах. Различают три вида пластид: 1) лейкопласты — бесцветные пластиды, в которых из моносахаридов и дисахаридов синтезируется крахмал (есть лейкопласты, запасающие белки или жиры); 2) хлоропласты — зеленые пластиды, содержащие пигмент хлорофилл, где осуществляется фотосинтез — процесс образования органических молекул из неорганических за счет энергии света, 8) хромопласты, включающие различные пигменты из группы каротиноидов, обусловливающих яркую окраску цветков и плодов. Пластиды могут превращаться друг в друга. Они содержат ДНК и РНК, и увеличение их количества осуществляется делением надвое. Вакуоли окружены мембраной и рецэвиваются из эндоплазматичеокой сети. Вакуоли содержат в растворенном виде белки, углеводы, низкомолекулярные продукты синтеза, витамины, различные соли. Осмотическое давление, создаваемое растворенными в вакуолярном соке веществами, приводит к тому, что в клетку поступает вода, которая обусловливает тургор — напряженное состояние клеточной стенки. Толстые упругие стенки обеспечивают прочность растений к статическим и динамическим нагрузкам.
В2.Международная программа (геном человека).
Проект по расшифровке генома человека (англ. The Human Genome Project, HGP) — международный научно-исследовательский проект, главной целью которого было определить последовательность нуклеотидов, которые составляют ДНК и идентифицировать 20–25 тыс. генов в человеческом геноме.
Проект начался в 1990 году, под руководством Джеймса Уотсона под эгидой Национальной организации здравоохранения США (англ.). В 2000 году был выпущен рабочий черновик структуры генома, полный геном — в 2003 году, однако и сегодня дополнительный анализ некоторых участков ещё не закончен. Частной компанией «Celera Genomics (англ.)» был запущен аналогичный параллельный проект, завершённый несколько ранее международного. Основной объём секвенирования был выполнен в университетах и исследовательских центрах США, Канады и Великобритании. Кроме очевидной фундаментальной значимости, определение структуры человеческих генов является важным шагом для разработки новых медикаментов и развития других аспектов здравоохранения.
Хотя целью проекта по расшифровке генома человека является понимание строения генома человеческого вида, проект также фокусировался и на нескольких других организмах, среди которых бактерии, в частности, Escherichia coli, насекомые, такие как мушка дрозофила, и млекопитающие, например, мышь.
Изначально планировалось определение последовательности более трёх миллиардов нуклеотидов, содержащихся в гаплоидном человеческом геноме. Затем несколько групп объявили о попытке расширить задачу до секвенирования диплоидного генома человека, среди них международный проект HapMap (англ.), «Applied Biosystems», «Perlegen», «Illumina», «JCVI», «Personal Genome Project» и «Roche-454».
Геном любого отдельно взятого организма (исключая однояйцевых близнецов и клонированных животных) уникален, поэтому определение последовательности человеческого генома в принципе должно включать в себя и секвенирование многочисленных вариаций каждого гена. Однако, в задачи проекта «Геном человека» не входило определение последовательности всей ДНК, находящейся в человеческих клетках; а некоторые гетерохроматиновые области (в общей сложности около 8 %) остаются несеквенированными до сих пор.
Предпосылки
Проект стал кульминацией нескольких лет работы поддержанной министерством энергетики США, в частности семинаров проводившихся в 1984-м[1] и 1986-м годах, и последовавшими действиями министерства энергетики[2]. Отчёт 1987 года чётко указывает: «Окончательной целью данного начинания является понимание человеческого генома» и «знание человеческого генома так же необходимо для прогресса медицины и других наук о здоровье, как знание анатомии было необходимо для достижения её нынешнего состояния». Поиски[3] технологий, подходящих для решения предложенной задачи, начинались ещё во второй половине 80-х годов.
Начиная с 1988 года, главой Национального Центра Исследований Человеческого Генома в Национальной Организации Здравоохранения США (NIH) был Джеймс Уотсон. В 1992 его вынудили уйти в отставку, в основном из-за несогласия с позицией его руководителя, Бернадины Хили (англ.) по вопросам патентования генов (англ.). В апреле 1993 его заменил Френсис Коллинз (англ.), а в 1997 году название центра было изменено на Национальный Институт Исследований Человеческого Генома (англ.) (NHGRI).
Трёхмиллиардный проект был формально запущен в 1990 году министерством энергетики США и национальным институтом здравоохранения, и ожидалось, что он продлится 15 лет. Помимо США, в международный консорциум вошли генетики Китая, Франции, Германии, Японии и Великобритании.
В силу широкой международной кооперации и новых достижений в области геномики (особенно в секвенировании), а также значительных достижений в вычислительной технике, «черновик» генома был закончен в 2000 году (о чём было объявлено совместно тогдашним президентом США Биллом Клинтоном и британским премьер-министром Тони Блэром 26 июня 2000 года[4]). Продолжение секвенирования привело к объявлению в апреле 2003 года о почти полном завершении работы, на 2 года раньше, чем планировалось[5]. В мае 2006 года, была пройдена другая веха на пути к завершению проекта, когда в журнале «Nature» была опубликована последовательность последней хромосомы — Хромосомы 1[6].
В3.Понятие об антропонозах, энтропозоонозах. Зоонозах.
Антропонозы (антропонозные инфекции) — (от др.-греч. ἄνθρωπος — человек, νόσος — болезнь), группа инфекционных и паразитарных заболеваний, возбудители которых способны паразитировать в естественных условиях только в организме человека.
Источником возбудителей инфекции при антропонозах являются только люди — больные или носители возбудителей инфекции (или инвазии); при некоторых антропонозах (например, при кори, ветряной оспе) источником возбудителей инфекции является только больной человек.
Инфекционные и инвазионные болезни, общие для человека и животных, носят название антропозоонозов, или зоонозов, как их называют в медицине. Человек заражается ими при контакте с больными животными, трупами, во время снятия шкур, при разделке туш, обработке животного сырья. Заражение может произойти в результате потребления мяса и других животных продуктов или зараженной воды, а также через переносчиков - многочисленных кровососущих насекомых и клещей.
Зоонозы (зоонозные инфекции) — (от др.-греч. ζῷον — «животное, живое существо» и νόσος — «болезнь»), группа инфекционных и паразитарных заболеваний, возбудители которых паразитируют в организме определенных видов животных, и для которых животные являются естественным резервуаром. Источником возбудителей инфекции (или инвазии) для человека является больное животное или животное — носитель возбудителей. При определенных санитарно-экономических условиях, благоприятствующих тому или иному механизму передачи возбудителя, возможно передача зоонозов людям. Но циркулировать в коллективах людей возбудители зоонозов не могут, так как человек для них является биологическим тупиком, не включается в течение эпизоотического процесса и не участвует в эволюции возбудителя как паразитического вида. Лишь при некоторых зоонозах, например при чуме, жёлтой лихорадке, в определенных условиях источником возбудителей инфекции может быть больной человек.
Профилактика зоонозов проводится с учетом эпидемической роли животных — источников инфекции, а также особенности путей передачи возбудителей. Например, при зоонозах, связанных с домашними животными, необходим ветеринарно-санитарный надзор и защита людей от заражения при уходе за животными. При зоонозах связанных с дикими животными, необходимо наблюдение за их численностью (например, численностью грызунов), в некоторых случаях (при борьбе с чумой, туляремией) уничтожение грызунов (дератизация). Кроме того, проводится защита людей от нападения кровососущих насекомых и клещей (например, применение репеллентов, защитных сеток, защитной одежды), а также иммунизация отдельных групп людей по эпидемическим показаниям.
Зооантропонозы , или антропозоонозы, — заболевания, передающиеся от животного человеку или наоборот при естественном контакте. Главным образом данные болезни обнаруживаются у животных, однако могут развиваться и у человека (например, лептоспироз, сибирская язва и бешенство).
Билет 22
В1. Поверхностный аппарат эукариотической клетки. Строение функции.
Состоит из гликокаликса, плазмалеммы и расположенного под ней кортикального слоя цитоплазмы. Плазматическая мембрана называется также плазмалеммой, наружной клеточной мембраной. Это биологическая мембрана, толщиной около 10 нанометров. Обеспечивает в первую очередь разграничительную функцию по отношению к внешней для клетки среде. Кроме этого она выполняет транспортную функцию. На сохранение целостности своей мембраны клетка не тратит энергии: молекулы удерживаются по тому же принципу, по которому удерживаются вместе молекулы жира — гидрофобным частям молекул термодинамически выгоднее располагаться в непосредственной близости друг к другу. Гликокаликс представляет собой «заякоренные» в плазмалемме молекулы олигосахаридов, полисахаридов, гликопротеинов и гликолипидов. Гликокаликс выполняет рецепторную и маркерную функции. Плазматическая мембрана животных клеток в основном состоит из фосфолипидов и липопротеидов со вкрапленными в неё молекулами белков, в частности, поверхностных антигенов и рецепторов. В кортикальном (прилегающем к плазматической мембране) слое цитоплазмы находятся специфические элементы цитоскелета — упорядоченные определённым образом актиновые микрофиламенты. Основной и самой важной функцией кортикального слоя (кортекса) являются псевдоподиальные реакции: выбрасывание, прикрепление и сокращение псевдоподий. При этом микрофиламенты перестраиваются, удлиняются или укорачиваются. От структуры цитоскелета кортикального слоя зависит также форма клетки (например, наличие микроворсинок).
В2.Биохимическая уникальность человека. Гены предрасположенности.
Понятие "гены предрасположенности" в известной мере можно рассматривать как противовес существовавшему ранее представлению о том, что мутации генов, кодирующих синтез определенных белков (так называемых "структурных генов"), неминуемо приводят к тем или иным наследственным болезням.Однако по мере углубления наших знаний о структурно-функциональной организации генома человека появляется все больше данных, не укладывающихся в эту жесткую схему. Прежде всего оказалось,что далеко не всегда и не все мутации структурных генов напрямую связаны с возникновением той или иной наследственной патологии. Обнаружена большая группа наследственных болезней с поздней манифестацией, например нейродегенеративные, вызываемые особым типом так называемых динамических мутаций, эффект которых проявляется уже во взрослом состоянии. Причем в зависимости от характера мутаций их тяжесть и клиника могут меняться в широком диапазоне. Например, очень поздно манифестируют и подвержены значительным функциональным модификациям мутации пресинилиновых генов (PS1, PS2), ответственных за болезнь Альцгеймера (старческое слабоумие).
Существенный вклад в клинический фенотип моногенных болезней вносят и различные трансдействующие мутации, приводящие к количественному и качественному сбою в работе индивидуальных генов. Сюда можно отнести и идентифицированные в последнее время весьма многочисленные и полиморфные по своим функциям гены-регуляторы, в частности гены факторов транскрипции. Сложность взаимоотношения генотип-фенотип нашла свое отражение в молекулярной гетерогенности наследственных болезней, cмысл которой сводится к тому, что фенотипические особенности проявления мутантных генов даже при моногенных болезнях зависят от многих факторов, в том числе от генов, мутации и полиморфизмы которых могут влиять на экспрессию главного гена7. При этом, однако, следует учитывать, что основной причиной болезни остаются мутации структурного гена, тогда как другие гены могут только усиливать и ослаблять патологический эффект его мутации. Следовательно, в случае моногенных болезней "гены предрасположенности" тождественны генам-модификаторам. Их тестирование важно для понимания взаимоотношения генотип-фенотип.
Однако особую практическую ценность представляет непосредственно молекулярное тестирование самих структурных генов. Для некоторых моногенных наследственных заболеваний с поздней манифестацией уже сегодня реальна досимптоматическая диагностика. Помимо нейродегенеративных заболеваний и болезни Альцгеймера к их числу относят и рак молочной железы. По данным ВОЗ, это грозное онкологическое заболевание приводит к смерти до 12% женщин. В последние годы идентифицированы два гена (BRCA1 и BRCA2), мутации которых ответственны примерно за 5% случаев рака молочной железы. К сожалению, большие размеры этих генов и отсутствие мажорных (доминирующих по частоте) мутаций ограничивают их досимптоматическое тестирование. Но недавно в некоторых этнических группах (евреи-ашкенази) удалось выявить отдельные мажорные мутации, что позволило разработать быстрые способы их тестирования.
В3.---
Билет 23
В1. Транспортная роль белков плазмолеммы.
Клеточная мембрана- поверхностная, периферическая структура, окружающая протоплазму растительных и животных клеток. Служит не только механическим барьером, ограничивает свободный двусторонний поток в клетку и из нее низко- и высокомолекулярных веществ. Плазмалемма выступает как структура, «узнающая» различные хим., в-ва и регулирующая избирательный транспорт в-в в клетку. Она возникает и обновляется за счет синтетической активности ЭПС и имеет сходное с ними строении. Барьерно-транспортная роль: Механическая устойчивость плазматической мембраны определяется не только свойствами самой мембраны, но и свойствами прилежащих к ней гликокаликса и кортикального слоя цитоплазмы.
Внешняя поверхность плазматической мембраны покрыта рыхлым волокнистым слоем вещества толщиной 3-4 нм — гликокаликсом. Он состоит из ветвящихся полисахаридных цепей мембранных интегральных белков, между которыми могут располагаться выделенные клеткой гликолипиды и протеогликаны. Тут же обнаруживаются некоторые клеточные гидролитические ферменты, участвующие во внеклеточном расщеплении веществ (внеклеточное пищеварение, например, в эпителии кишечника). Кортикальный слой цитоплазмы, толщиной 0,1-0,5 мкм, не содержит рибосом и мембранных структур, но богат актиновыми микрофиламентами.
Строение плазматической мембраны
Плазматическая мембрана, как и другие липопротеидные мембраны клетки, является полупроницаемой. Максимальной проникающей способностью обладает вода и растворенные в ней газы. Транспорт ионов может проходить по градиенту концентраций, т. е. пассивно, без затрат энергии. В этом случае некоторые мембранные транспортные белки образуют молекулярные комплексы, каналы, через которые ионы проходят сквозь мембрану за счет простой диффузии. В других случаях специальные мембранные белки-переносчики избирательно связываются с тем или иным ионом и переносят его через мембрану. Такой тип переноса называется активным транспортом и осуществляется с помощью белковых ионных насосов. Например, затрачивая 1 молекулу АТФ, система К-Nа насоса откачивает за один цикл из клетки 3 иона Nа и закачивает 2 иона К против градиента концентрации. В сочетании с активным транспортом ионов через плазмалемму проникают различные сахара, нуклеотиды и аминокислоты. Макромолекулы, такие как, например, белки, через мембрану не проходят. Они, а также более крупные частицы вещества транспортируются внутрь клетки посредством эндоцитоза. При эндоцитозе определенный участок плазмалеммы захватывает, обволакивает внеклеточный материал, заключает его в мембранную вакуоль. Эта вакуоль — эндосома — сливается в цитоплазме с первичной лизосомой и происходит переваривание захваченного материала. Эндоцитоз формально разделяют на фагоцитоз (поглощение клеткой крупных частиц) и пиноцитоз (поглощение растворов). Плазматическая мембрана принимает участие и в выведении веществ из клетки с помощью экзоцитоза — процесса, обратного эндоцитозу.
Рецепторная роль плазмалеммы
Белки-переносчики внешней мембраны клетки являются также рецепторами, узнающими определенные ионы и взаимодействующими с ними. В качестве рецепторов на поверхности клетки могут выступать белки мембраны или элементы гликокаликса. Такие чувствительные к отдельным веществам участки разбросаны по поверхности клетки или собраны в небольшие зоны. Роль многих клеточных рецепторов заключается не только в связывании специфических веществ, но и в передаче сигналов с поверхности внутрь клетки. Например, при действии гормона на клетку цепь событий развертывается следующим образом: молекула гормона специфически взаимодействует с рецепторным белком плазмалеммы и, не проникая в клетку, активирует фермент, синтезирующий ЦАМФ. Последний активирует или ингибирует внутриклеточный фермент или группу ферментов.
Разнообразие и специфичность наборов рецепторов на поверхности клеток приводит к созданию очень сложной системы маркеров, позволяющих клеткам отличать «своих» (той же особи или того же вида) от «чужих».
Межклеточные соединения
У многоклеточных организмов за счет межклеточных взаимодействий образуются сложные клеточные ансамбли. При тесном соседстве клеток друг с другом гликокаликс обеспечивает слипание клеток за счет присутствия в нем трансмембранных гликопротеидов кадгеринов. Это простой межклеточный контакт, при котором зазор между клетками составляет 10-20 нм. В эпителиях часто встречается плотное, или запирающее, соединение, при котором внешние слои двух плазматических мембран максимально сближены и в точках их соприкосновения лежат глобулы интегральных белков мембраны. Такой контакт непроницаем для молекул и ионов, он запирает межклеточные полости.
Заякоривающие соединения, или контакты, не только соединяют плазматические мембраны соседних клеток, но и связываются с фибриллярными элементами цитоскелета. Например, для десмосом, имеющих вид бляшек или кнопок, в межклеточном пространстве характерно наличие плотного слоя гликопротеидов десмоглеинов. С цитоплазматической стороны к плазмалемме прилежит слой белка десмоплакина, связанный с промежуточными филаментами цитоскелета.
Щелевые контакты считаются коммуникационными соединениями клеток. В зоне щелевого контакта может быть от 20-30 до нескольких тысяч коннексонов — цилидрических белковых структур с внутренним каналом диаметром 2 нм. Каждый коннексон состоит из 6 субъединиц белка коннектина. Коннексоны играют роль прямых межклеточных каналов, по которым ионы и низкомолекулярные вещества могут диффундировать из клетки в клетку.
В2.Регуляция экспрессии генов у прокариот. Индукция синтеза катаболических ферментов (Lac-оперон).
Многие бактериальные гены устроены таким образом, что они способны функционировать с существенно разной эффективностью. У E. coli, например, относительное содержание различных белков варьирует в очень широких пределах (от менее чем 0.1% до 2%) в зависимости от их функций; при этом каждый белок в хромосоме E. coli кодируется единственным геном. Такие вариации обусловлены действием системы контроля генной экспрессии, которая осуществляется главным образом на уровне транскрипции ДНК. Таким образом, чаще всего уровень активности гена связан с количеством синтезируемой на нем мРНК, то есть с активностью фермента РНК-полимеразы. Последовательности ДНК, расположенные перед началом структурного гена и определяющие степень активности РНК-полимеразы, называются регуляторными последовательностями. Одна из таких последовательностей представляет собой участок ДНК, с которым связывается РНК-полимераза. Этот участок называется промотором. Последовательность оснований промотора определяет частоту инициации синтеза иРНК, причем замена одного основания в этой последовательности может привести к уменьшению частоты инициации в 1000 раз. Промотор может быть сильным и слабым. Сильный промотор инициирует синтез иРНК часто, слабый - гораздо реже. С другой стороны, промотор может быть регулируемым и нерегулируемым. Например, промотор β-лактамазы нерегулируемый, но сильный. Использование таких промоторов не всегда удобно. Дело в том, что большое количество белка может блокировать рост бактерий. Кроме того, интенсивная транскрипция рекомбинантной ДНК может помешать репликации плазмиды, и она будет утрачена. Поэтому удобнее использовать регулируемые сильные промоторы (индуцибельные), включение которых, а значит и синтез чужеродного белка можно осуществить, когда получена большая бактериальная масса. Некоторые плазмидные векторы содержат промотор, работа которого регулируется температурочувствительным белковым продуктом гена-репрессора. Белок-репрессор активен при определенных температурах и блокирует действие промотора. Повысив температуру до 42 оС, можно "включить" промотор и быстро получить большое количество требуемого белка. В качестве индуцибельных промоторов используют также Trp-промотор триптофанового оперона, который регулируется триптофановым голоданием, lac-промотор лактазного оперона, который индуцируется субстратом (лактозой) и другие. Интенсивность транскрипции определенных структурных генов может зависеть от эффективности ее терминации, в частности, от того, как часто РНК-полимераза прекращает синтез РНК, не дойдя до этих генов. Сравнительно недавно обнаружено, что во многих оперонах Е.coli, контролирующих биосинтез аминокислот, между промотором и первым структурным геном имеется терминирующая последовательность. В определенных условиях происходит образование терминирующего сигнала, ослабляющего интенсивность транскрипции. Это явление получило название аттенуации, а участок ДНК - аттенуатор (ослабитель). Как и репрессия, аттенуация зависит от присутствия в среде соответствующих аминокислот. Например, избыток триптофана в клетках триптофанзависимых мутантов, дефектных по репрессору, только 1 из 10 молекул РНК-полимеразы, начавших транскрипцию, преодолевает аттенуатор и считывает структуру генов. Удаление триптофана втрое повышает эффективность транскрипции генов. В отличие от репрессии, антенуация зависит не от самой аминокислоты, а от триптофанил - тРНК (аминокилоты, присоединенной к соответствующей тРНК). На эффективность продуктивности рекомбинантной ДНК в существенной степени влияет количество копий этой ДНК в расчете на клетку. Суммарная активность экспрессируемого гена растет с ростом копийности плазмиды. Таким образом, используя многокопийные плазмиды, можно достичь сверхсинтеза нужных белковых продуктов. Обычно используемые плазмидные векторы (pBR 322 и др.) поддерживаются в клетке в количестве 20-50 копий. Сейчас исследователи имеют в своем распоряжении температурно-чувствительные мутантные плазмиды, способные накопить до одной-двух тысяч копий на клетку, не нарушая ее жизненно-важных функций. Таким образом можно достичь сверхпродукции плазмидных генов бактериальными штаммами-сверхпродуцентами. Регуляция экспрессии у E. coli происходит также и на уровне трансляции. Последовательность оснований длиной 6-8 нуклеотидов, расположенная непосредственно перед инициирующим кодоном АУГ, определяет эффективность трансляции. Эта последовательность представляет собой участок связывания мРНК с рибосомой. Как правило, он отстоит на 8 нуклеотидов от инициирующего кодона, и его сдвиг в ту или иную сторону может резко снижать эффективность трансляции соответствующей мРНК. Описанный участок называется последовательностью Шайна-Дальгарно, по имени исследователей, впервые его идентифицировавших. В состав вектора кроме всего прочего должен входить маркерный ген, позволяющий селектировать измененные клетки. Часто в качестве селективных используют широко распространенные в природе гены ферментов, модифицирующих антибиотики и инактивирующие их действие.
Регуляция экспрессии генов у прокариот. Репрессия синтеза анаболических ферментов (trp-оперон).

 омпартментация
объема клетки с помощью мембран
омпартментация
объема клетки с помощью мембран