
- •1. Лечебный режим.
- •2. Лечебное питание.
- •3. Этиотропное лечение.
- •Патогенетическое лечение.
- •4. Борьба с интоксикацией.
- •5.Симптоматическое лечение.
- •8. Санаторно-курортное лечение и реабилитация.
- •2.Дифференциальный диагноз по воспалительно-инфильтративному синдрому легких.
- •3. Критерии диагностики пневмоний. Неотложная помощь при инфекционно-токсическом шоке.
- •5.Бронхиальная астма. Этиология, схема патогенеза, классификация, клиника, методы исследования, лечение. 5. Бронхиальная астма
- •6. Критерии диагностики бронхиальной астмы. Неотложная помощь при приступе бронхиальной астмы.
- •7.Дифференциальный диагноз по бронхообструктивному синдрому (хобл, бронхиальная астма).
- •9. Диагностические критерии хрон. Легочного сердца
- •10. Ибс. Стенокардия. Определение, этиология, патогенез, клиника, диагностика, лечение.
- •11.Ибс. Инфаркт миокарда. Опеределение, этиология, патогенез, клинические проявления, диагностика, лечение.
- •12.Критерии диагностики острого инфаркта миокарда. Критерии резорбтивно-некротического синдрома.
- •13.Дифференциальный диагноз по ангинозному синдрому (стенокардия напряжения, прогрессирующая стенокардия, инфаркт миокарда). Неотложная помощь при ангинозном приступе.
- •15.Неотложная помощь при кардиогенном шоке.
- •1. При отсутствии выраженного застоя в легких:
- •16.Артериальная гипертензия. Определение, этиология, патогенез, классификация, клиника, диагностика, лечение.
- •17.Гипертонические кризы, клинические особенности, неотложная помощь.
- •18.Аритмии. Определение, этиология, патогенез, клиника, диагностика, лечение, профилактика.
- •19. Экг признаки экстрасистолии. Неотложная помощь.
- •22. Неотложная помощь при фибрилляции предсердей.
- •24.Гэрб. Определение, этиология, патогенез, классификация, клиника, диагностика, лечение, профилактика.
- •25.Критерии диагностики гастро-эзофагеальной рефлюксной болезни.
- •27.Дифференциальный диагноз по абдоминальному синдрому (хронические гастриты, язвенная болезнь желудка и 12- перстной кишки, хронический холецистит, хронический панкреатит.
- •29. Диагностические критерии язвенной болезни ;tkelrf
- •32)Хронический панкреатит.
- •33) Диагностические признаки хронического панкреатита
- •38.Дифференциальный диагноз при асцитах (хроническая сердечная недостаточность, циррозы печени).
- •39.Дифференциальный диагноз по холестатическому синдрому (хронический холецистит, хронический гепатит, цирроз печени).
- •40.Критерии диагностики цирроза печени.
- •41.Лабораторно-инструментальные методы диагностики цирроза печени.
- •42.Критерии диагностики печеночно-клеточной недостаточности.
- •43.Дифференциальный диагноз по асцитическому синдрому.
- •Симптомы асцита
- •44.Дифференциальный диагноз по синдрому портальной гипертензии.
- •45. Критерии диагностики синдрома раздраженной кишки
- •48)Митральный стеноз
- •56 Ревматоидный артрит
- •58 Деформирующий остеоартроз
- •1. Oak без существенных изменений. При реактивном синовите может быть увеличение соэ до 20-25 мм/ч.
- •2. Бак без существенных изменений. В случае развития синовита в крови повышается содержание фибрина, серомукоида, сиаловых кислот, гаптоглобина.
- •3. Анализ мочи: без отклонений от нормы.
- •59 Дифференциальный диагноз заболеваний суставов
- •62 Дермато-полимиозит
- •Вопрос 64:
- •Вопрос 65:
- •Вопрос 66:
- •Вопрос 67
- •Вопрос 68:
- •Вопрос 69:
- •Вопрос 70:
- •Вопрос 71:
- •Вопрос 72:
- •74. В12 дефицитная анемия. Этиология, патогенез, клиника, диагностика, лечение.
- •75.Картина периферической крови при в12-дефицитной анемии.
- •76.Дифференциальный диагноз по анемическому синдрому
- •77.Острые лейкозы. Определение, этиология, патогенез, клиника, диагностика, лечение, профилактика.
- •78.Хронический лимфолейкоз. Определение, этиология, патогенез, клиника, диагностика, лечение, профилактика.
- •79.Лабораторные диагностика хронического миелолейкоза.
- •1.1. Устранение дефицита инсулина и нормализация углеводного обмена
- •1. 1. 1. Постоянная внутривенная инфузия небольших доз инсулина
- •1.1.2. Частые внутримышечные инъекции малых доз инсулина
- •1.2. Усиленная регидратация организма
ощущение неполного опорожнения кишечника)
Выделение слизи
Вздутие живота
Наряду с вышеприведенными диагностическими критериями в диагностике синдрома раздраженного кишечника следует придавать значение следующим характерным обстоятельствам:
• отсутствие болей и диареи в ночное время;
≪ отсутствие так называемых ≪симптомов тревоги≫ (примеси в кале, лихорадка, необъяснимое похудание, анемия, увеличение СОЭ и др.) (А. А. Шептулин, 1997);
≫ длительный анамнез заболевания, изменчивый характер жалоб, несоответствие между обилием и ≪красочностью≫ жалоб и хорошим общим состоянием больного;
отсутствие прогрессировав™ болезни;
• связь ухудшения самочувствия с психоэмоциональными факторами и стрессовыми ситуациями;
• отсутствие патологических изменений со стороны общего и биохимического анализов крови, а также признаков органических изменений при колоноскопии, ректороманоскопии, ирригоскопии, нормальная гистологическая картина биоптатов слизистой оболочки толстой Кишки.
46) Острая ревматическая лихорадка (ОРЛ) — это системное заболевание соединительной ткани с преимущественной локализацией поражений в сердечно-сосудистой системе (кардит, клапанные пороки сердца), развитием суставного (артрит), кожного (ревматические узелки, аннулярная эритема) и неврологического (хорея) синдромов, возникающее у детей 7-15 лет на фоне иммунного ответа организма на антигены бета-гемолитического стрептококка группы А и перекрёстную реактивность со схожими тканями организма человека.
Этиология.ВОЗБУДИТЕЛЬ β-гемолитический стрептококк группы А
Патогенез.Стрептококк вырабатывает вещества, обладающие выраженным кардиотоксическим действием и способные подавлять фагоцитоз, повреждать лизосомальные мембраны. Токсины стрептококка вызывают развитие воспаления в соединительной ткани, сердечно-сосудистой системе; наличие антигенной общности между стрептококком и сердцем приводит к включению аутоиммунного механизма - появлению аутоантител к миокарду, антигенным компонентам соединительной ткани. Гуморальные и клеточные иммунологические сдвиги при ревматизме: повышении титров антистрептолизина-0 (АСЛ-О), антистрептогиалуронидазы (АСГ), антистрептокиназы (АСК), дисиммуноглобулинемии, возрастании процентного и абсолютного количества В-лимфоцитов при снижении процентного и абсолютного количества Т-лимфоцитов.
В патогенезе ОРЛ также можно говорить о ревматической патогенетической триаде:
1. Прямое повреждение миокарда факторами патогенности БГС-А.
2. Аутоиммунный механизм:
а — оголение аутоантигенов миокарда вследствие прямого повреждения;
б — антигенная мимикрия БГС-А и миокарда (сходство антигенов), то есть антитела на БГС-А способны поражать и миокард);
3. Сосудистый механизм (поражение сосудов миокарда по вышеописанным механизмам ведет к дисциркуляторным изменениям в миокарде — ишемии, ацидозу, — способствуя развитию воспаления, с одной стороны, и реактивному фиброзу, с другой)
Классификация
1. Клинический вариант: острая РЛ (ОРЛ), повторная РЛ (ПРЛ).
2. Клинические проявления: кардит, артрит, хорея, кольцевидная эритема, подкожные узелки.
3. Вовлеченность сердца: без поражения сердца, ревматическая болезнь сердца (без порока, с пороком, неактивная фаза).
4. Выраженность хронической сердечной недостаточности: ХСН I, II A, II Б, III ст., ФК I, II, III, IV.
Диагностические критерии
Наличие двух больших или одного большого и двух малых проявлений (критериев) и доказательств предшествующей стрептококковой инфекции подтверждают диагноз ревматизма
Клинико-диагностические критерии ОРЛ Киселя-Джонса:
I. Большие (ревматическая клиническая пентада):
1) ревмокардит (преимущественно эндомиокардит);
2) полиартрит (преимущественно крупных суставов, мигрирующий характер, без остаточных деформаций, рентгенологически негативный);
3) малая хорея (гипотонико-гиперкинетический синдром вследствие поражения полосатого тела подкорки головного мозга);
4) ревматические узелки (периартикулярные подкожные узловатые уплотнения);
5) анулярная эритема (кольцевидные покраснения кожи туловища и проксимальных отделов конечностей).
II. Малые:
1) клинические: лихорадка, артралгии;
2) лабораторно-инструментальные: а) лабораторные (СРБ, СК, ДФА, СМ, АСЛО, АСГН); б) инструментальные (увеличение интервала PQ на ЭКГ)
Лабораторные данные
Общий анализ крови: увеличение СОЭ, лейкоцитоз, сдвиг лейкоцитарной формулы влево.
Биохимический анализ крови: повышение уровня a2 и y-глобулинов, серомукоида, гаптоглобина, фибрина, аспарагиновой трансаминазы.
Общий анализ мочи: нормальный или небольшая протеинурия, микрогематурия.
Иммунологические исследования крови: снижено количество Т-лимфоцитов, снижена функция Т-супрессоров, повышен уровень иммуноглобулинов и титров антистрептококковых антител, появляются ЦИК и СРП.
Инструментальные исследования
ЭКГ: замедление AV-проводимости, снижение амплитуды зубца Т и интервала S-T в прекордиальных отведениях, аритмии.
Эхокардиография: при вальвулите митрального клапана выявляется утолщение и «лохматость» эхо-сигнала от створок и хорд клапана, ограничение подвижности задней створки клапана, уменьшение систолической экскурсии сомкнутых митральных створок, иногда небольшое пролабирование створок в конце систолы. При допплерэхокардиографии ревматический эндокардит митрального клапана проявляется следующими признаками: краевым булавовидным утолщением передней митральной створки; гипокинезией задней митральной створки; митральной регургитацией; куполообразным изгибом передней митральной створки.
При вальвулите аортального клапана эхокардиография выявляет мелкоамплитудное дрожание митральных створок, утолщение эхо-сигнала от створок аортального клапана.
При допплерэхокардиографии ревматический эндокардит аортального клапана характеризуется: ограниченным краевым утолщением аортального клапана; переходящим пролапсом створок; аортальной регургитацией.
ФКГ: При миокардите отмечается снижение амплитуды I тона, его деформация, патологические III и IV тоны, систолический шум, занимающий 1/2-2/3 систолы, убывающий и примыкающий к I тону. При наличии эндокардита регистрируются высокочастотный систолический шум, который усиливается в ходе динамического наблюдения, протодиастолический или пресистолический шум на верхушке при формировании митрального стеноза, протодиастолический шум на аорте при формировании недостаточности клапана аорты, ромбовидный систолический шум на аорте при формировании сужения устья аорты.
Рентгенологическое исследование сердца: увеличение размеров сердца, снижение сократительной способности.
Лечение Острой ревматической лихорадки (ревматизма):
Госпитализация, постельный режим. Диета обогащена витаминамии белком , ограничиваются соли и углеводы.
бензилпенициллин по 100000-150000 ЕД, подросткам по 500000-1000000 ЕД 4 раза в сутки в/м с переходом на пенициллины пролонгированного действия.При непереносимости пенициллина применяют макролиды или линкозамиды.
Подавление активности воспалительного процесса.
- При остром течении заболевания с наличием яркого и умеренно выраженного кардита (панкардита) показан преднизолон в дозе 0,7-0,8 мг/кг/сут (подросткам - 20 мг/сут) в 1 прием утром после еды (обычно 2 недели), далее дозу снижают (на 2,5 мг каждые 5-7 дней) вплоть до полной отмены.
- При слабо выраженном ревмокардите, ревматическом артрите без кардита,показан диклофенак 2-3 мг/кг/сут (подросткам - 75-150 мг/сут) в 3 приема в течение 1,5-2 мес . Симптоматическая терапия.
1. Для уменьшения вероятности развития дистрофических процессов вмиокарде, кардиотрофическая терпия:
- апарагинат калия и магния (панангин, аспаркам), витаминВ6
с магнием поУг-1 таблетки 3 раза в сутки в течение 1 мес,
- антиоксидантный комплекс (витаминыА, Е, С) - 3-4недели ,
- рибоксин: 1) в/в по 5-10 мл на физрастворе – 5-10 дней, 2) внутрь по 2-3 таблеткив день - 2-3 недели,
- милдронат: 1) внутривенно (от 2 до 5 мл), 2) внутрь по 1-3 капсулы. Улушшает трофику миокарда, улучшает микроциркуляциюв миокарде и ЦНС, - неотон (фосфокреатин ) – нормализуетэнергетический обмен в клеткахмиокардаи ЦНС -- внутривенно капельнов течение 4-5 днейпо 1 гвсутки , - актовегин (солкосерил – улучшаетметаболизмвмиокарде и клетках ЦНС-по 1-2 драже в сутки или внутривенно по 2-5 мл на введение - 5-10 дней, - инозин 0,6- 1,2 г/сутв 3 приема в течение 1 мес.
2. При наличии застойной сердечной недостаточности при ОРЛ и ревматических пороках сердца применяют:
- диуретики петлевые, тиазидоподобныеи калийсберегающие,
- блокаторы кальциевых каналов,
- бета-адреноблокаторы,
- сердечные гликозиды.
Митральная недостаточность и митральный порок с преобладанием недостаточности. длительный прием ингибиторов ангиотензинпревращающего фермента (ИАПФ).При декомпенсации, диуретики ,сердечные гликозиды.
При тромбоэмболических осложнениях, выраженном увеличении левого предсердия, мерцательной аритмии,непрямых антикоагулянтов (варфарин) .
Митральный стеноз и митральный порок с преобладанием стеноза. В начале лечения больных митральным стенозом следует выявить и устранить факторы, повышающие давление в левом предсердии (тахикардия, лихорадка, тяжелая физическая нагрузка и др.).
Необходимость в медикаментозном лечении возникает обычно при появлении застоя в легких и симптомов ХСН, для устранения и снижения которых назначаются:
• диуретики
• сердечные гликозиды.
• бета-адреноблокаторы.
• дилтиазем или верапамил.
• антикоагулянты (в частности варфарин )
Хирургическое лечение митрального стеноза показано при уменьшении площади эффективного митрального отверстия менее 1,2 см2 и наличии клинических проявлений заболевания (одышка, застой в легких, выраженная легочная гипертензия).
Аортальная недостаточность
Медикаментозную терапию проводят длительно при хронической стабильной аортальной недостаточности и для улучшения состояния перед проведением хирургического лечения при тяжелой или острой аортальной недостаточности.
При компенсированной тяжелой аортальной недостаточности, помимо ИАПФ, показан систематический прием артериолярных вазодилататоров.
Профилактика
Основным лекарственным средством для вторичной профилактики ОРЛ является бензатинабензилпенициллин ( экстенциллин , ретарпен , пендепон ,
бензатинбензилпенициллин ) . Вводится 1 раз в 3 недели в/м: подросткам - 2,4 млн ЕД, детям с массой тела менее 25 кг - 600000 ЕД, детямс массой тела более 25 кг - 1,2 млн ЕД.
Бициллин-5: до 10 лет - 750 тыс. ЕД недели, старше 10 лет - 1500 тыс. ЕД 1 разв 3-4. 29
47) Диагностические критерии
Наличие двух больших или одного большого и двух малых проявлений (критериев) и доказательств предшествующей стрептококковой инфекции подтверждают диагноз ревматизма
Клинико-диагностические критерии ОРЛ Киселя-Джонса:
I. Большие (ревматическая клиническая пентада):
1) ревмокардит (преимущественно эндомиокардит);
2) полиартрит (преимущественно крупных суставов, мигрирующий характер, без остаточных деформаций, рентгенологически негативный);
3) малая хорея (гипотонико-гиперкинетический синдром вследствие поражения полосатого тела подкорки головного мозга);
4) ревматические узелки (периартикулярные подкожные узловатые уплотнения);
5) анулярная эритема (кольцевидные покраснения кожи туловища и проксимальных отделов конечностей).
II. Малые:
1) клинические: лихорадка, артралгии;
2) лабораторно-инструментальные: а) лабораторные (СРБ, СК, ДФА, СМ, АСЛО, АСГН); б) инструментальные (увеличение интервала PQ на ЭКГ)
Лабораторные данные
Общий анализ крови: увеличение СОЭ, лейкоцитоз, сдвиг лейкоцитарной формулы влево.
Биохимический анализ крови: повышение уровня a2 и y-глобулинов, серомукоида, гаптоглобина, фибрина, аспарагиновой трансаминазы.
Общий анализ мочи: нормальный или небольшая протеинурия, микрогематурия.
Иммунологические исследования крови: снижено количество Т-лимфоцитов, снижена функция Т-супрессоров, повышен уровень иммуноглобулинов и титров антистрептококковых антител, появляются ЦИК и СРП.
Инструментальные исследования
ЭКГ: замедление AV-проводимости, снижение амплитуды зубца Т и интервала S-T в прекордиальных отведениях, аритмии.
Эхокардиография: при вальвулите митрального клапана выявляется утолщение и «лохматость» эхо-сигнала от створок и хорд клапана, ограничение подвижности задней створки клапана, уменьшение систолической экскурсии сомкнутых митральных створок, иногда небольшое пролабирование створок в конце систолы. При допплерэхокардиографии ревматический эндокардит митрального клапана проявляется следующими признаками: краевым булавовидным утолщением передней митральной створки; гипокинезией задней митральной створки; митральной регургитацией; куполообразным изгибом передней митральной створки.
При вальвулите аортального клапана эхокардиография выявляет мелкоамплитудное дрожание митральных створок, утолщение эхо-сигнала от створок аортального клапана.
При допплерэхокардиографии ревматический эндокардит аортального клапана характеризуется: ограниченным краевым утолщением аортального клапана; переходящим пролапсом створок; аортальной регургитацией.
ФКГ: При миокардите отмечается снижение амплитуды I тона, его деформация, патологические III и IV тоны, систолический шум, занимающий 1/2-2/3 систолы, убывающий и примыкающий к I тону. При наличии эндокардита регистрируются высокочастотный систолический шум, который усиливается в ходе динамического наблюдения, протодиастолический или пресистолический шум на верхушке при формировании митрального стеноза, протодиастолический шум на аорте при формировании недостаточности клапана аорты, ромбовидный систолический шум на аорте при формировании сужения устья аорты.
Рентгенологическое исследование сердца: увеличение размеров сердца, снижение сократительной способности.
48)Митральный стеноз
Митральный стеноз - часто встречающийся приобретенный порок сердца. Он может быть изолированным или сочетается с недостаточностью митрального клапана и с поражением других клапанов.
Этиология и патогенез.Причиной стеноза левого атриовентрикулярного отверстия чаще всего служит ревматизм. Стеноз развивается обычно у 40 % всех больных, страдающих ревматизмом сердца; 60 % из них составляют женщины. Поражение створок клапана характеризуется их диффузным утолщением за счет фиброзной ткани и/или отложений кальция. Комиссуры сращены, сухожильные хорды сращены и укорочены, створки клапанов становятся ригидными. Эти изменения в свою очередь приводят к сужению в области верхушки и образованию так называемого воронкообразного клапана. В то время как начальные изменения левого предсердно-желудочкового клапана специфичны для ревматизма, последующие изменения могут быть неспецифичными, являясь следствием травмирования клапана, вызванного нарушением кровотока вследствие его первичной деформации. Кальцификация стенозированного клапана приводит к иммобилизации его створок и к сужению левого атриовентрикулярного отверстия.
Кальцифицированный клапан может сам по себе вызвать образование тромба и артериальную эмболию. Стеноз левого атриовентрикулярного отверстия редко бывает врожденным.
Гемодинамика. Сопротивление кровотоку, создаваемое суженным митральным отверстием, приводит к повышению давления в левом предсердии. Поскольку левое предсердие является довольно слабым отделом сердца, оно сравнительно рано перестает справляться с повышенной нагрузкой, его рабочая гипертрофия постепенно сменяется тоногенной, а затем и миогенной дилатацией. Вследствие перерастяжения стенок предсердия, а также из-за ревматического поражения проводящих путей у больных митральным стенозом достаточно часто возникает мерцательная аритмия. Сокращения предсердий становятся малоэффективными, что приводит к застою крови, и создают благоприятные условия для тромбообразования.
Повышенное вследствие стеноза давление в левом предсердии передается на легочные вены, затем на легочные капилляры и артериолы. При повышении давления в легочных капиллярах до уровня онкотического давления плазмы (около 25 мм рт. ст.) возникает опасность пропотевания плазмы в просвет альвеол и развития отека легкого. В этой ситуации развивается рефлекторный спазм мелких легочных артерий на прекапиллярном уровне (рефлекс Катаева), что предохраняет капиллярную сеть легких от переполнения кровью. Длительно существующий сосудистый спазм способствует органическому перерождению стенок сосудов и приводит к легочной гипертензии.
Таким образом, в начальной стадии развития легочной гипертензии ее причиной является только сужение митрального отверстия, в последующем к этой причине добавляются еще два фактора: спазм и морфологические изменения в системе артериол. Правый желудочек при наличии легочной гипертензии начинает работать с повышенной нагрузкой, гипертрофируется, а в дальнейшем, как и правое предсердие, подвергается также тоногенной и миогенной дилатации. У больных на этом этапе естественного течения митрального стеноза появляются признаки застойной сердечной недостаточности по большому кругу кровообращения: отеки, увеличение печени, асцит, повышение центрального венозного давления.
Субъективно — жалобы на:одышку вначале при физической нагрузке, затем и в покое; при резком подъёме давления в малом круге кровообращения возможно появления сердечной астмы,кашель сухой или с небольшим количеством слизистой мокроты
охриплость голоса (симптом Ортнера),кровохарканье (в мокроте появляются сидерофаги — «клетки сердечных пороков»),боли в области сердца, сердцебиения, перебои; часто развивается мерцательная аритмия,слабость, повышенная утомляемость (так как характерна фиксация минутного объёма — отсутствие адекватного увеличения минутного объёма сердца при физической нагрузке)
Объективно: осмотр: на фоне бледной кожи выявляется резко очерченный лиловый «митральный» румянец щек с цианозом губ и кончика носа (facies mitralis); усиленная эпигастральная пульсация правого желудочка («сердечный толчок»); отсутствие или ослабление верхушечного толчка (так как левый желудочек не увеличен в объёме и смещен гипертрофированным правым желудочком)
пальпация: при пальпации верхушки сердце, особенно после физической нагрузке в положении на левом боку на выдохе — диастолическое дрожание («кошачье мурлыканье» — из-за колебаний крови при прохождении её через суженное митральное отверстие); симптом двух молоточков Нестерова — если положить руку ладонью на верхушку, а пальцами на область II межреберья слева от грудины, то хлопающий I тон ощущается ладонью как первый «молоточек», а акцентированный II тон ощущается пальцами как второй «молоточек»; сердечный горб.
перкуссия: смещение границ относительной тупости сердца вверх (за счёт гипертрофии левого предсердия) и вправо (за счёт расширения правого желудочка), при этом границы абсолютной сердечной тупости увеличиваются больше, чем относительной (так как за счёт расширения правого желудочка сердце, раздвинув края лёгких, прижимается к грудной стенке своей правой увеличенной половиной).
аускультация: усиленный (хлопающий) I тон над верхушкой сердца (в диастолу левый желудочек не наполняется кровью в достаточной мере и быстро сокращается); дополнительный III тон на верхушке (тон открытия митрального клапана; связан с резким движением створок митрального клапана в начале диастолы); I тон + II тон + щелчок открытия митрального клапана — трехчленный ритм на верхушке сердца — ритм «перепела»; диастолический шум на верхушке сердца, возникающий в различные периоды диастолы:
протодиастолический шум — возникает в начале диастолы, связан с движением крови через суженное отверстие из-за разности давления в предсердии и желудочке; убывающий, низкого рокочущего тембра (пальпаторный эквивалент — «кошачье мурлыканье»), выслушивается на ограниченном пространстве, лучше после физической нагрузки, на левом боку, на выдохе, не проводится.
пресистолический шум — возникает в конце диастолы за счёт активной систолы предсердий; имеет нарастающий характер, исчезает при мерцательной аритмии
характеристика пульса и АД: различный пульс (симптом Попова) — пульс на левой лучевой артерии слабее, чем на правой из-за сдавления левой подключичной артерии увеличенным левым предсердием; АД имеет тенденцию к снижению из-за уменьшения сердечного выброса.
Лечение. В стадии компенсации необходимы надлежащий режим, способный предотвратить те осложнения, которые могут ускорить наступление сердечной недостаточности; периодическая оценка активности ревматического процесса и при его рецидивах – комплексная противоревматическая терапия в стационаре. Больной должен избегать всего, что может вызвать одышку, сердцебиение (тяжёлый физический труд, быстрая ходьба, нервное перенапряжение). Следует исключить переохлаждение, воздерживаться от употребления алкоголя и курения. Медикаментозная терапия, помимо профилактики и лечения ревматизма в период обострений, состоит в лечении сердечной недостаточности. Хирургическому лечению (комиссуротомия) подлежат больные с митральным стенозом. При митральной недостаточности применяют операцию протезирования клапана.
Пациенты без симптомов или с минимальными клиническими проявлениями заболевания нуждаются в динамическом наблюдении и неинвазивной оценке размеров и сократительной способности левого желудочка с помощью метода эхокардиографии каждые 6–12 месяцев. Обычно значительное снижение ФВ указывает на тяжелое поражение левого желудочка, при котором протезирование митрального клапана уже не помогает. Оптимальным для проведения хирургического лечения митральной недостаточности считают состояние больных, когда ФВ составляет 50–55%.
Митральный стеноз и митральный порок с преобладанием стеноза. В начале лечения больных митральным стенозом следует выявить и устранить факторы, повышающие давление в левом предсердии (тахикардия, лихорадка, тяжелая физическая нагрузка и др.).
Необходимость в медикаментозном лечении возникает обычно при появлении застоя в легких и симптомов ХСН, для устранения и снижения которых назначаются:
• диуретики
• сердечные гликозиды.
• бета-адреноблокаторы.
• дилтиазем или верапамил.
• антикоагулянты (в частности варфарин )
ИАПФ при выраженном митральном стенозе мало эффективны
Периферические артериолярные (гидралазин, празозин, дигидропиридины) и венозные (нитраты) вазодилататоры противопоказаны.
Хирургическое лечение митрального стеноза показано при уменьшении площади эффективного митрального отверстия менее 1,2 см2 и наличии клинических проявлений заболевания (одышка, застой в легких, выраженная легочная гипертензия).
49) Этиология.Являются результатом инфекционного поражения, воспаления или аутоиммунных реакций, перегрузки и дилатации камер сердца.
Эпидемиология.Митральный порок сердца отмечается наиболее часто. При ревматическом эндокардите чаще всего поражается митральный клапан (до 96% всех случаев), реже – аортальный, ещё реже – трёхстворчатый.
Патогенез.Образующаяся на клапане фиброзная ткань обусловливает неравномерное утолщение створок, которые становятся более плотными и менее подвижными. Рубцовое сморщивание разросшейся ткани нередко укорачивает створки, в связи с чем развивается недостаточность клапана.
При недостаточности митрального клапана часть крови из левого желудочка в момент систолы проникает назад в предсердие (регургитация), что опять-таки вызывает его переполнение.В силу увеличенного кровенаполнения и повышенного давления в полости левого предсердия последнее увеличивается в размерах, а мышца его гипертрофируется. При митральной недостаточности резко увеличивается левое предсердие, так как часть крови, поступающей в левый желудочек, во время систолы возвращается обратно в предсердие. Во время диастолы желудочков вся масса крови поступает из левого предсердия в левый желудочек, который расширяется и гипертрофируется. Увеличенное давление в левом предсердии создаёт повышенное давление в малом круге, что опять-таки вызывает гипертрофию правого желудочка.
При сужении левого предсердно-желудочкового отверстия затрудняется поступление крови из левого предсердия в левый желудочек, часть крови (остаточный объём) остаётся в предсердии, что вызывает его переполнение. Так как давление в легочных венах и капиллярах повышено, то происходит транссудация плазмы крови в межуточную ткань лёгких, а иногда и в просвет альвеол, а это вызывает характерную для декомпенсированного митрального стеноза картину застоя в малом круге с кровохарканием и хроническим интерстициальным отёком лёгких. Иногда на этом фоне отмечается разрастание соединительной ткани вокруг альвеол с последующим развитием фиброза, что ещё больше затрудняет легочную вентиляцию и газообмен. В связи с тем, что мышца правого желудочка гипертрофируется, он обычно несколько расширяется (миогенная дилятация). Следствием этого расширения может быть развитие относительной недостаточности трёхстворчатого клапана. При этом застойные явления из правого желудочка распространяются в правое предсердие, в большой круг кровообращения, что клинически проявляется набуханием шейных вен, застойной печенью, отёками. Так, при декомпенсированном митральном стенозе со временем возникает тотальная (полная сердечная недостаточность.
Клиника
При минимально выраженных клапанных пороках заболевание может клинически не проявляться. При декомпенсации появляется клиника гемодинамических нарушений малом или большом кругах кровообращения. Наиболее характерны одышка при физической нагрузке, цианоз кожных покровов, отёки, серцебиение, боли в области сердца, кашель.
недостаточность митрального клапана.
Субъективно — в стадии компенсации жалобы отсутствуют, при снижении сократительной функции левого желудочка и повышении давления в малом круге кровообращения появляются жалобы на:
одышку вначале при физической нагрузке, а затем и в покое
сердцебиение
боли в области сердца ишемического характера (из-за отставаний развития коронарных коллатералей при гипертрофии миокарда)
сухой кашель
При нарастании симптомов правожелудочковой недостаточности появляются отеки на ногах, боли в правом подреберье (из-за увеличения печени и растяжения её капсулы).
Объективно:
осмотр: акроцианоз, набухание шейных вен
пальпация: усиленный разлитой верхушечный толчок, смещенный влево и нередко вниз в V или в VI межреберье; сердечный горб (при гипертрофии и дилатации правого желудочка)
перкуссия: расширение относительной тупости сердца вначале влево, вверх, а затем и вправо.
аускультация: I тон на верхушке сердца ослаблен или отсутствует (так как нет «периода замкнутых клапанов»); систолический шум на верхушке, распространяющийся вдоль V и VI ребер в подмышечную впадину и в точку Боткина и убывающий в конце систолы (возникает из-за прохождения крови из левого желудочка в левое предсердие через узкую щель между створками клапана); акцент II тона над легочной артерией и его расщепление (из-за быстрого захлопывания клапанов при повышении давления).
характеристики пульса и АД: характерных изменений не имеют.
митральный стеноз
Субъективно — жалобы на:
одышку вначале при физической нагрузке, затем и в покое; при резком подъёме давления в малом круге кровообращения возможно появления сердечной астмы
кашель сухой или с небольшим количеством слизистой мокроты
охриплость голоса (симптом Ортнера)
кровохарканье (в мокроте появляются сидерофаги — «клетки сердечных пороков»)
боли в области сердца, сердцебиения, перебои; часто развивается мерцательная аритмия
слабость, повышенная утомляемость (так как характерна фиксация минутного объёма — отсутствие адекватного увеличения минутного объёма сердца при физической нагрузке)
Объективно:
осмотр: на фоне бледной кожи выявляется резко очерченный лиловый «митральный» румянец щек с цианозом губ и кончика носа (facies mitralis); усиленная эпигастральная пульсация правого желудочка («сердечный толчок»); отсутствие или ослабление верхушечного толчка (так как левый желудочек не увеличен в объёме и смещен гипертрофированным правым желудочком)
пальпация: при пальпации верхушки сердце, особенно после физической нагрузке в положении на левом боку на выдохе — диастолическое дрожание («кошачье мурлыканье» — из-за колебаний крови при прохождении её через суженное митральное отверстие); симптом двух молоточков Нестерова — если положить руку ладонью на верхушку, а пальцами на область II межреберья слева от грудины, то хлопающий I тон ощущается ладонью как первый «молоточек», а акцентированный II тон ощущается пальцами как второй «молоточек»; сердечный горб.
перкуссия: смещение границ относительной тупости сердца вверх (за счёт гипертрофии левого предсердия) и вправо (за счёт расширения правого желудочка), при этом границы абсолютной сердечной тупости увеличиваются больше, чем относительной (так как за счёт расширения правого желудочка сердце, раздвинув края лёгких, прижимается к грудной стенке своей правой увеличенной половиной).
аускультация: усиленный (хлопающий) I тон над верхушкой сердца (в диастолу левый желудочек не наполняется кровью в достаточной мере и быстро сокращается); дополнительный III тон на верхушке (тон открытия митрального клапана; связан с резким движением створок митрального клапана в начале диастолы); I тон + II тон + щелчок открытия митрального клапана — трехчленный ритм на верхушке сердца — ритм «перепела»; диастолический шум на верхушке сердца, возникающий в различные периоды диастолы:
протодиастолический шум — возникает в начале диастолы, связан с движением крови через суженное отверстие из-за разности давления в предсердии и желудочке; убывающий, низкого рокочущего тембра (пальпаторный эквивалент — «кошачье мурлыканье»), выслушивается на ограниченном пространстве, лучше после физической нагрузки, на левом боку, на выдохе, не проводится.
пресистолический шум — возникает в конце диастолы за счёт активной систолы предсердий; имеет нарастающий характер, исчезает при мерцательной аритмии
характеристика пульса и АД: различный пульс (симптом Попова) — пульс на левой лучевой артерии слабее, чем на правой из-за сдавления левой подключичной артерии увеличенным левым предсердием; АД имеет тенденцию к снижению из-за уменьшения сердечного выброса.
Лечение. В стадии компенсации необходимы надлежащий режим, способный предотвратить те осложнения, которые могут ускорить наступление сердечной недостаточности; периодическая оценка активности ревматического процесса и при его рецидивах – комплексная противоревматическая терапия в стационаре. Больной должен избегать всего, что может вызвать одышку, сердцебиение (тяжёлый физический труд, быстрая ходьба, нервное перенапряжение). Следует исключить переохлаждение, воздерживаться от употребления алкоголя и курения. Медикаментозная терапия, помимо профилактики и лечения ревматизма в период обострений, состоит в лечении сердечной недостаточности. Хирургическому лечению (комиссуротомия) подлежат больные с митральным стенозом. При митральной недостаточности применяют операцию протезирования клапана.
Пациенты без симптомов или с минимальными клиническими проявлениями заболевания нуждаются в динамическом наблюдении и неинвазивной оценке размеров и сократительной способности левого желудочка с помощью метода эхокардиографии каждые 6–12 месяцев. Обычно значительное снижение ФВ указывает на тяжелое поражение левого желудочка, при котором протезирование митрального клапана уже не помогает. Оптимальным для проведения хирургического лечения митральной недостаточности считают состояние больных, когда ФВ составляет 50–55%.
Митральный стеноз и митральный порок с преобладанием стеноза. В начале лечения больных митральным стенозом следует выявить и устранить факторы, повышающие давление в левом предсердии (тахикардия, лихорадка, тяжелая физическая нагрузка и др.).
Необходимость в медикаментозном лечении возникает обычно при появлении застоя в легких и симптомов ХСН, для устранения и снижения которых назначаются:
• диуретики
• сердечные гликозиды.
• бета-адреноблокаторы.
• дилтиазем или верапамил.
• антикоагулянты (в частности варфарин )
ИАПФ при выраженном митральном стенозе мало эффективны
Периферические артериолярные (гидралазин, празозин, дигидропиридины) и венозные (нитраты) вазодилататоры противопоказаны.
Хирургическое лечение митрального стеноза показано при уменьшении площади эффективного митрального отверстия менее 1,2 см2 и наличии клинических проявлений заболевания (одышка, застой в легких, выраженная легочная гипертензия).
50. Недостаточность митрального клапана. Диагностические критерии.
1) Аускультативные признаки:
- систолический шум на верхушке, убывающий или нарастающий ко 2 тону;
- ослабление 1 тона на верхушке;
- трехчленная мелодия работы сердца на верхушке (3тон);
2) ФКГ-признаки:
- пансистолический шум или убывающий лентовидный шум на верхушке
начинающийся за 1 тоном;
- уменьшение амплитуды 1 тона на верхушке;
- 3 тон на верхушке;
3) ЭКГ-признаки:
- гипертрофия левого желудочка;
- гипретрофия левого предсердия;
4) Рентгенологические признаки:
- митральная конфигурация сердца;
- увеличение левого желудочка;
- увеличение левого предсердия;
5) ЭхоКГ-признаки: нарушение структуры клапана ( утолщение створок, отрыв хорд, кальциноз, вегетации, пролапс митрального клапана), систолическая сепарация створок, избыточная амплитуда диастолического движения створок, дилатация левых отделов сердца, избыточная экскурсия межжелудочковой перегородки; струя регургитации в полости левого предсердия при доплеровском исследовании.
51.Аортальный стеноз
Стеноз аортального клапана — порок сердца в виде сужения отверстия аорты вследствие патологии аортального клапана и околоклапанных структур. Недостаточность клапана аорты — патологическое состояние, характеризующееся ретроградным током крови из аорты в полость левого желудочка через дефектный аортальный клапан.
Этиология
причиной аортального стеноза выступает ревматизм, в 15% случаев — другие причины (инфекционный эндокардит, болезнь Педжета, гиперхолестеринемия II типа, ревматоидный артрит, СКВ, охроноз, радиационное поражение, ХПН).
Инфекционный эндокардит, расслоение аорты и травматический отрыв створки клапана выступают основными причинами развития острой аортальной недостаточности.
патогенез и изменения гемодинамики. Стеноз устья аорты создает значительное препятствие на пути тока крови из левого желудочка в большой круг кровообращения лишь в случае, если площадь аортального отверстия уменьшается более чем на 50%. Сохранение даже на 10-20% ее нормальной величины совместимо с жизнью.
При наличии препятствия к опорожнению левого желудочка для обеспечения более или менее удовлетворительного снабжения кровью организма включается ряд компенсаторных механизмов. Одним из них является удлинение систолы левого желудочка.
Другой компенсаторный механизм - увеличение давления в полости левого желудочка. Повышение внутрижелудочкового давления обеспечивает увеличение количества крови, протекающей через аортальное отверстие в единицу времени. Степень подъема давления в полости левого желудочка пропорциональна степени сужения аортального отверстия.
Чем больше выражен подъем давления в полости левого желудочка, тем больше величина градиента левый желудочек - аорта. В норме этот градиент отсутствует или весьма назначителен. При данном пороке он достигает 50-100 мм рт. ст. и может превысить 150 мм рт. ст.
Удлинение систолы левого желудочка и рост давления в его полости обусловливает развитие выраженной гипертрофии левого желудочка. Ни при каком другом пороке не развивается такая значительная гипертрофия миокарда левого желудочка, как при стенозе устья аорты.
Так как в компенсации аортального стеноза принимает участие мощный левый желудочек, порок длительное время протекает без расстройства кровообращения. Длительный период компенсации - особенность этого порока.
Минутный объем уменьшается, если площадь аортального отверстия меньше 25% нормальной величины.
При физической нагрузке минутный объем возрастает незначительно или остается без перемен, так как этому препятствует малая пропускная способность аортального отверстия.
При ослаблении сократительной способности левого желудочка полость его увеличивается. Это приводит к уменьшению минутного объема и к росту конечного диастолического давления в левом желудочке, затем и в левом предсердии. Далее повышенное давление из левого предсердия ретроградно передается на легочные вены. Возникает пассивная (венозная) легочная гипертензия, при которой гипертрофии правого желудочка, как правило, нет.
В дальнейшем вследствие прогрессирующей дистрофии миокарда могут возникнуть застойные явления и в большом круге кровообращения.
Клиника
аортальный стеноз
Субъективно — длительно протекает бессимптомно, основные жалобы появляются при сужении аортального отверстия на 2/3 нормы (менее 0,75 см2):
сжимающие боли за грудиной при физической нагрузке (снижение коронарного кровообращения).
головокружение, обмороки (ухудшение мозгового кровообращения);
В дальнейшем при снижении сократительной функции левого желудочка появляются: приступы сердечной астмы; одышка в покое; повышенная утомляемость (обусловлена отсутствием адекватного возрастания минутного объёма сердца при физической нагрузке). При появлении застойных явлений в большом круге кровообращения больные жалуются на: отеки нижних конечностей; боли в правом подреберье (связаны с увеличением печени и растяжением капсулы).
Объективно:
осмотр: бледность кожных покровов (из-за спазма сосудов кожи как реакции на малый сердечный выброс), акроцианоз (при декомпенсации), отеки нижних конечностей, набухание шейных вен, выраженный верхушечный толчок.
пальпация: пальпируется разлитой «высокий» резистентный верхушечный толчок, смещенный вниз (VI межреберье) и влево (до передней подмышечной линии); в точке Боткина и особенно во втором межреберье справа от грудины (над аортой) часто определяется систолическое дрожание («кошачье мурлыканье»), возникающее из-за завихрения крови при прохождении через суженное аортальное отверстие.
перкуссия: расширение левой границы относительной тупости сердца, увеличение размеров поперечника сердца (аортальная конфигурация сердца).
аускультация: первый тон ослаблен (за счёт медленного сокращения левого желудочка и удлинения систолы), второй тон ослаблен над аортой (а при неподвижности сросшихся створок аортального клапана он может совсем исчезать); грубый, нарастающе-убывающий систолический шум с эпицентром над аортой, проводится на сонные артерии, усиливается при выслушивании больного на правом боку с задержкой дыхания во время выдоха.
характеристика пульса и АД: пульс малый, медленный и редкий (кровь в аорту проходит медленно и в меньшем количестве); систолическое АД снижено, диастолическое нормальное или повышено, пульсовое давление уменьшено.
Аортальный стеноз
Показанием к оперативному лечению является появление первых симптомов (одышка, ангинозные боли, синкопальные состояния), грубые изменения аортального клапана с нарастанием систолического градиента свыше 50 мм рт. ст., признаки дилатации левого желудочка. Операцию желательно проводить до возникновения симптомов левожелудочковой недостаточности.
Больным со стенозом устья аорты, значительно ограничивающим физическую активность и снижающим трудоспособность, показана аортальная комиссуротомия или имплантация искусственного клапана.
54. Диагностика аортальной недостаточности.
Прямые признаки:
· Диастолический шум
(прото) - мягкий, дующий над аортой, проводится к верхушке сразу после II
тона и снижается к концу диастолы, лучше выслушивается
в третьем-четвертом межреберьях у левого края грудины
· Ослабление или исчезновение II тона
· I тон ослаблен
· Пресистолический шум Флинта на верхушке
· Систоличнский шум во втором межреберье справа
Косвенные признаки:
“Левожелулочковые:”
· Усиленный и разлитой верхушечный толчок вниз и влево
· Смещение влево левой границы
“Сосудистые:”
· Бледность кожных покровов
· Систолическое артериальное давление повышается, диастолическое
понижается (может до 0)
· Пульс высокий и скорый
· Двойной тон Траубе при аускультации бедренной артерии
· При сдавлении бедренной артерии - двойной шум Виноградова-Дюрозье
· Симптомы легочной гипертензии
· При выраженном дефекте клапанов: пульсация сонных артерий («пляска
каротид»), подключичных артерий, пульсация в яремной ямке, височных и
плечевых артерий
53) Этиология. Этиологическими факторами могут быть ревматическая лихорадка, инфекционный эндокардит, сифилис, атеросклероз, системная красная волчанка, ревматоидный артрит, пролапс, травма.
Патогенез и изменения гемодинамики. Гемодинамические нарушения при данном пороке обусловлены обратным током крови из аорты в левый желудочек в период его диастолы из-за неполного смыкания клапанов аорты. Объем возвращающейся крови зависит в основном от площади незакрытой части аортального отверстия, градиента давления аорта - левый желудочек и длительности диастолы. В левый желудочек может возвращаться от 5 до 50% и более систолического объема крови. Обратный ток крови в левый желудочек вызывает его дилатацию, степень которой пропорциональна объему возвращающейся крови. Такая дилатация левого желудочка является компенсаторной и называется тоногенной, первичной, в отличие от вторичной (миогенной), развивающейся при снижении сократительной способности миокарда.
Вследствие усиленной работы по изгнанию увеличенного количества крови левый желудочек постепенно гипертрофируется. Гипертрофия левого желудочка и развивающаяся тахикардия, препятствующая обратному току крови из аорты в левый желудочек, компенсируют данный порок.
В условиях компенсации порока левое предсердие функционирует нормально; с развитием относительной недостаточности митрального клапана и при снижении сократительной способности левого желудочка давление в левом предсердии повышается, обусловливая его гипертрофию и дилатацию.
Застой крови в левом предсердии передается на сосуды малого круга кровообращения. Повышение давления в легочной артериивызывает изометрическую гиперфункцию правого желудочка и гипертрофию его миокарда. При снижении сократительной способности правого желудочка появляются симптомы правожелудочковой недостаточности.
аортальная недостаточность
Субъективно — в стадии компенсации порока общее самочувствие удовлетворительное, лишь иногда больные ощущают сердцебиение (из-за компенсаторной тахикардии) и пульсацию за грудиной (из-за перемещения увеличенного объёма крови из левого желудочка в аорту и обратно), при декомпенсации жалобы на:
боль в области сердца стенокардитического характера, плохо или некупирующиеся нитроглицерином (обусловлены относительной коронарной недостаточностью за счёт гипертрофии миокарда, ухудшением кровенаполнения коронарных артерий при низком диастолическом давлении в аорте и из-за сдавления субэндокардиальных слоёв избыточным объёмом крови)
головокружение, наклонность к обморокам (связаны с нарушением питания мозга)
одышку вначале при физической нагрузке, а затем и в покое (появляется при снижении сократительной функции левого желудочка)
отеки, тяжесть и боль в правом подреберье (при развитии правожелудочковой недостаточности)
Объективно:
осмотр: бледность кожных покровов (вызвана малым кровенаполнением артериальной системы во время диастолы); пульсация периферических артерий — сонных («пляска каротид»), подключичных, плечевых, височных; ритмичное, синхронное с пульсом покачивание головы (симптом Мюссе); ритмичное изменение цвета ногтевого ложа и губ при легком надавливании прозрачным стеклом на слизистую губ, на конец ногтя, так называемый капиллярный пульс (симптом Квинке).
пальпация: верхушечный толчок определяется в шестом, иногда в седьмом межреберье, кнаружи от среднеключичной линии, разлитой, усиленный, приподнимающий, куполообразный.
перкуссия: граница относительной сердечной тупости смещена вниз и влево, увеличены размеры поперечника сердца и ширина сосудистого пучка (аортальная конфигурация).
аускультация: I тон на верхушке сердца ослаблен (створки митрального клапана захлопываются с меньшей амплитудой вследствие переполнения левого желудочка кровью, давление в полости левого желудочка нарастает медленно при отсутствии периодов замкнутых клапанов); II тон на аорте при ревматическом пороке ослаблен, при сифилитическом и атеросклеротическом — звучный, иногда усилен и даже с металлическим оттенком; шумы:
1,рганический шум — мягкий, дующий протодиастолический шум над аортой, проводящийся к верхушке серд-ца; при ревматическом пороке данный шум не грубый, лучше выслушивается в точке Боткина-Эрба, при сифилитическом пороке — шум более грубый, лучше выслушивается во втором межреберье справа
2,функциональные шумы: систолический шум на верхушке (относительная недостаточность митрального клапана при большом расширении левого желудочка); диастолический, пресистолический шум Флинта (обратный ток крови во время диастолы из аорты в желудочек происходит со значительной силой и оттесняет створку митрального клапана, что создаёт функциональный стеноз митрального отверстия, и во время диастолы создается препятствие току крови из левого предсердия в желудочек).
На бедренной артерии выслушивается двойной тон Траубе (как результат колебаний стенки сосуда во время систолы и во время диастолы) и двойной шум Виноградова-Дюрозье (первый шум стенотический — обусловлен током крови через суженный стетоскопом сосуд; второй — ускорением обратного кровотока по направлению к сердцу во время диастолы).
характеристика пульса и АД: пульс скорый, высокий, большой (из-за большого пульсового давления и увеличенного объёма крови, поступающего в аорту во время систолы); систолическое АД повышается, дистолическое понижается, пулсовое давление повышается.
Лечение
Аортальная недостаточность
Медикаментозную терапию проводят длительно при хронической стабильной аортальной недостаточности и для улучшения состояния перед проведением хирургического лечения при тяжелой или острой аортальной недостаточности.
Легкая аортальная регургитация, как правило, имеет благоприятный прогноз и не требует проведения медикаментозного лечения. Рекомендуется избегать изометрических физических нагрузок, так как они могут увеличить аортальную регургитацию и вызвать повреждение корня аорты.
Пациентам с умеренной аортальной регургитацией рекомендуется раннее, до появления клинических симптомов заболевания, назначение ИАПФ для предупреждения дилатации и дисфункции левого желудочка.
При компенсированной тяжелой аортальной недостаточности, помимо ИАПФ, показан систематический прием артериолярных вазодилататоров.
53. Стеноз устья аорты ( аортальный стеноз ) Диагностические критерии.
1) Аускультативные признаки:
- грубый систолический шум над аортой с иррадиацией на сонные артерии, в межлопаточную область и яремную ямку;
- ослабление или исчезновение 2 тона над аортой;
2) ФКГ-признаки:
- средневысокочастотный ромбовидный систолический шум над аортой;
- снижение амплитуды 2 тона над аортой;
3) ЭКГ-признаки: признаки гипертрофии с ситолической перегрузкой левого
желудочка;
4) Рентгенологические признаки:
- аортальная конфигурация сердца;
- увеличение левого желудочка;
- увеличение дуги аорты;
5) ЭхоКГ-признаки: изменение клапана ( утолщение створок, фиброз, кальциноз, вегетации, двухстворчатый клапан), ограничение раскрытия створок в систолу ( N – 1,5 -2,6 см ) увеличение времени систолического открытия створок, уменьшение площади отверстия ( N – 2,5 – 3,5 см ), гипертрофия стенок левого желудочка на фоне незначительного или умеренного расширения полости левого желудочка. Увеличение скорости систолического потока ( N – 100 – 170 см/сек.) и градиента давления на аортальном клапане.
55 Синдром клапанных поражений (формирование порока сердца, чаще аортального или митрального прежде не измененных клапанов или присоединение новых поражений клапанов к ранее существовавшим).
Пороки митрального клапана
Недостаточность левого предсердно-желудочкового отверстия (митрального) клапана, или митральная недостаточность, — патологическое состояние, при котором створки двустворчатого клапана не закрывают полностью митральное отверстие и во время систолы желудочков происходит обратный ток крови из левого желудочка в левое предсердие (так называемая митральная регургитация).
Дифференциальная диагностика. При дифференциальной диагностике Митральной недостаточности необходимо иметь в виду следующее.
• У здоровых может выслушиваться функциональный систолический шум над верхушкой сердца, но более часто он определяется над основанием. В отличие от больных с пороком сердца у таких лиц не изменены тоны сердца, нет косвенных признаков порока (увеличение левого предсердия ц левого желудочка), шум мягкого тембра изменчив по интенсивности. На ФКГ амплитуда шума невелика, шум начинается позднее, чем при пороке сердца, менее продолжителен, I тон имеет нормальную амплитуду.
• При «митрализации» в течение заболеваний, сопровождающихся резким расширением полости левого желудочка и растяжением фиброзного кольца митрального отверстия (гипертоническая болезнь, постинфарктная аневризма левого желудочка, диффузный миокардит тяжелого течения, ди- латационная кардиомиопатия и пр.), над верхушкой выслушивается систолический шум, обусловленный относительной митральной недостаточностью. Однако в отличие от порока сердца при этих заболеваниях отмечается умеренное увеличение левого предсердия, не соответствующее гораздо большей степени увеличения левого желудочка. Кроме того, дифференциации помогает анализ всей клинической картины.
• Систолический шум над верхушкой сердца может выявляться при синдроме пролапса митрального клапана. Этот синдром заключается в выбухании створок клапана в полость левого предсердия, что обусловливает регургитацию крови. В отличие от митральной недостаточности при пролапсе I тон не изменен, в период систолы определяется добавочный тон (мезосистолический щелчок), систолический шум приходится на вторую половину систолы, что отчетливо выявляется на ФКГ; этот шум регистрируется между мезосистолическим щелчком и II тоном. При переходе больного в вертикальное положение или после приема нитроглицерина шум усиливается, в то время как прием р-адреноблокаторов приводит к ослаб¬лению шума. Эхокардиография окончательно разрешает диагностические трудности, выявляя пролапс митрального клапана.
• Систолический шум над верхушкой сердца может выслушиваться и при других пороках (стеноз устья аорты, трикуспидальная недостаточность).
Стеноз левого атриовентрикулярного отверстия (митральный стеноз) — патологическое состояние, характеризующееся уменьшением площади отверстия митрального клапана в 2—14 раз, что создает препятствие движению крови из левого предсердия в левый желудочек.
Дифференциальный диагноз наиболее затруднен с миксомой левого предсердия. Она периодически закрывает левое атриовентрикулярное отверстие что может формировать клиническую картину, почти неотличимую по симптомам от митрального стеноза. Предположить миксому помогают изменение аускультативной картины при перемене положения тела больного, а также нередко анемия, стойкий субфебрилитет, нарастающее похудание и гиперглобулинемия. Чаще окончательный диагноз устанавливают с помощью эхокардиографии или ангиокардиографии. Эти же методы исследования используют при необходимости дифференцировать митральный стеноз с некоторыми врожденными пороками сердца, анулярным вариантом констриктивного перикардита (так называемый наружный митральный стеноз).
Эхокардиографию следует производить во всех случаях неясной аускультативной картины. Редко митральный стеноз аускультативно проявляется систолическим шумом (так называемый систолический вариант митрального стеноза), что может быть причиной ошибочной диагностики митральной недостаточности. Подобные ошибки могут возникать и при наличии систолического шума, обусловленного относительной трикуспидальной недостаточностью. Правильному диагнозу в этих случаях помогают оценка с помощью эхокардиографии состояния и функции створок митрального клапана, отсутствие на эхокардиограмме признаков гипертрофии левого желудочка сердца и регургитации крови в левое предсердие. Иногда митральный стеноз ошибочно предполагают при усилении I тона сердца, появлении нежного диастолического шума на верхушке и пароксизмов мерцательной аритмии у больных с тиреотоксикозом. В этих случаях кроме результатов эхокардиографии установить диагноз помогают наличие других клинических признаков тиреотоксикоза, исследования функции щитовидной железы и концентрации в крови ее гормонов.
В некоторых случаях при осложнении митрального стеноза рецидивирующим бронхитом дифференциальную диагностику проводят с хроническим легочным сердцем (Лёгочное сердце), что требует тщательного рентгенологического исследования легких и сердца, выполнения эхокардиографии.
Пороки аортального клапана
Стеноз устья аорты — патологическое состояние, при котором имеется препятствие на пути тока крови из левого желудочка в аорту. Различают три формы стеноза устья аорты: клапанный, подклапанный, надклапанный.
Дифференциальный диагноз проводят с пороками и другими заболеваниями сердца, при которых определяются систолический шум и гипертрофия левого желудочка сердца. При неясной этиологии порока, особенно у детей, прежде всего исключают врожденный аортальный стеноз, для которого характерны выявление признаков порока в раннем детском возрасте и нередко сочетание с другими врожденными аномалиями развития сердечно-сосудистой системы (незаращение артериального протока, коарктация аорты). Это же относится и к дефекту межжелудочковой перегородки, для различения которого с аортальным стенозом иногда приходится прибегать к зондированию сердца и вентрикулографии, что необходимо также для определения показаний к оперативному вмешательству. У взрослых дифференциальный диагноз чаще проводят с идиопатическим гипертрофическим субаортальным стенозом, стенозом устья легочного ствола, реже с митральной недостаточностью. Во всех этих случаях существенное значение для правильного диагноза имеет эхокардиографическое исследование.
Недостаточность клапана аорты (аортальная недостаточность) — патологическое состояние, при котором в период диастолы створки клапана не закрывают полностью просвет аорты и вследствие этого происходит об¬ратный ток крови из аорты в левый желудочек (так называемая аортальная регургитация).
Дифференциальный диагноз изолированной аортальной недостаточности с другими патологическими состояниями, как правило, не требуется ввиду четкой клинической очерченности этого порока. Лишь в редких случаях (обычно у детей) возникает необходимость исключить незаращение артериального (боталлова) протока или другие крупные центрально расположенные артериовенозные шунты. Зондирование полостей сердца обычно проводят лишь при определении показаний к оперативному вмешательству.
56 Ревматоидный артрит
Определение ревматоидного артрита.
Ревматоидный артрит (РА) – хроническое аутоиммунное системное заболевание соединительной ткани с преимущественным поражением суставов по типу прогрессирующего полиартрита.
Эпидемиология.
Ревматоидный артрит – это самый распространенный хронический полиартрит. Частота развития ревматоидного артрита колеблется от 0,24 до 1,44% на 100 тысяч населения. Во всем мире ревматоидным артритом страдают около 58 млн. человек. Женщины болеют в 3 раза чаще мужчин. Заболевание чаще начинается в 30 – 50 лет.
Этиология.
Генетические факторы.
Инфекционные антигены.
В последнее годы обсуждается роль микобактерий в развитии РА.
Факторы риска развития РА:
женский пол
возраст 45 лет и старше
наследственная предрасположенность
наличие HLA – антигенов
сопутствующая патология
хронические очаги инфекции
Схема патогенеза ревматоидного артрита [Harte W., 1967 г].
Большинство исследователей относят РА к системным аутоиммунным заболеваниям. Под этим подразумевается ведущая роль в патогенезе РА иммунных нарушений, сопровождающихся появлением антител против антигенов собственного организма (аутоантитела). Антитела могут вырабатываться против самых различных органов и тканей. Отсюда системность поражений в отличие, от так называемых органоспецифических аутоиммунных заболеваний, которые характеризуются реакциями против антигенов какого-либо одного органа.
При РА наиболее изучены нарушения гуморального иммунитета. Прежде всего в сыворотке крови у 70 - 80% больных РА определяется особый макроглобулин – так называемый ревматоидный фактор (РФ). Он является антителом к Fc – фрагменту иммуноглобулинов (Ig M). Fc – фрагмент – это участок иммуноглобулинов, ответственных за связывание комплемента, фиксацию на различных клетках, в частности на тучных и макрофагах. В недалеком прошлом РФ отводили решающую роль в патогенезе РА. В настоящее время четко установлено, что РФ не абсолютно специфичен для РА и скорее является следствием, а не причиной болезни.
РФ нередко обнаруживается в сыворотке при различных инфекциях, опухолях, коллагенозах. Однако наиболее стойко и в наиболее высоких титрах РФ обнаруживается при РА. Важно и то, что РФ образуется именно в синовиальной ткани. Доказано существование различных типов ревматоидного фактора – классического IgM, IgG, IgA, т. е. правильно говорить о ревматоидных факторах. В случае определения с помощью реакции Ваалера – Розе или латекс теста IgM говорит о серопозитивном РА, в противном случае - серонегативном РФ. Иммуноглобулин типа IgG в свободном виде в крови не циркулирует. Именно с этим типом РФ, входящим в состав иммунных комплексов, связывают возникновение васкулитов при РА.
Важнейшим звеном иммунопатологических реакций при РА является формирование иммунных комплексов с участием ревматоидных факторов.
Иммунные комплексы могут длительно сохранятся в суставной ткани, т. к. имеют тропизм к мало васкуляризованным участкам хряща и суставной капсулы. Считается, что именно иммунные комплексы вызывают ряд цепных реакций, индуцирующих и поддерживающих воспаление, определяющих самоподдерживающееся и прогрессирующее течение РА. При наличии в крови циркулирующих иммунных комплексов повышается частота внесуставных проявлений, наблюдается суставно-висцеральная форма РА.
Локальное действие иммунных комплексов многообразно и направленно, прежде всего, на систему комплемента и фагоцитоз. Иммунные комплексы с фиксированным на них комплементом являются мощным стимулом для хемотаксиса лейкоцитов и начало фагоцитарной реакции. Процесс фагоцитоза при РА приводит к повреждению нейтрофилов, высвобождению лизосомных ферментов, повреждению синовиальной ткани. Высвобождающиеся ферменты в свою очередь повреждают и переваривают клеточные структуры с образованием новых аутоантигенов. Они и поддерживают цепную реакцию, столь характерную для РА.
В патогенезе РА огромную роль играют цитокины - низкомолекулярные белковые клеточные регуляторы, являющиеся медиаторами роста и дифференцировки гемопоэтических, лимфоидных и мезенхимальных клеток, иммунных реакций и воспаления. Они вырабатываются преимущественно клетками иммунной системы, костного мозга, фибробластами, тромбоцитами, моноцитами, макрофагами. К цитокинам относятся колониестимулирующие факторы, интерлейкины, интерфероны, факторы роста. В синовиальной жидкости и тканях суставов при РА содержатся в избытке цитокины интерлейкин-1, фактор некроза опухолей, гранулоцитарно-макрофагальный колониестимулирующий фактор, интерлейкин-6. Эти цитокины образуются клетками, выстилающими синовиальную оболочку, а также макрофагами и фибробластами и обладают способностью значительно стимулировать воспалительный процесс.

Классификация РА (принята пленумом Всесоюзного общества ревматологов, 1980 г)
Клинико-анатомическая форма
Иммунологическая характеристика
Течение болезни
Степень
активности
Рентгенологическая
стадия артрита
Функциональная недостаточность
опорно-двигательного
аппарата
РА: полиартрит, олигоартрит, моноартрит
Серопозитивный
Медленно
прогрессирующее
Минимальная
Околосуставной остеопороз
Отсутствует
. РА с системными проявлениями: поражение РЭС, серозных оболочек, легких, сердца, сосудов, глаз, почек,
нервной системы, амилоидоз органов.
Особые синдромы псевдо септический синдром, синдром Фелти
Серонегативный
Быстро прогрессирующее
Средняя
Остеопороз + сужение суставной щели, могут быть единичные узуры
Профессиональная трудоспособность ограничена
РА в сочетании с деформирующим остеоартрозом, ДБСТ, ревматизмом
Без заметного прогрессирования
Высокая ремиссия
Остеопороз + сужение суставной щели, могут быть множественные узуры
Профессиональная трудоспособность утрачена
Ювенильный РА (включая болезнь Стилла)
Остеопороз + сужение суставной щели, могут быть множественные узуры + косные анкилозы
Утрачена способность к самообслуживанию
Примечание: моноартрит - воспаление одного сустава; олигоартрит - воспаление двух-трех суставов; полиартрит - воспаление многих суставов.
Клиника.
Суставной синдром.(рисунок №2)
Повреждение суставов, главное клиническое проявление РА, чаще всего начинается подостро, в виде стойкой полиартралгии, которая у 2/3 больных с самого начала заболевание сопровождается явлениями артрита. Боли наиболее интенсивны во вторую половину ночи и утром, а в течение дня и, особенно к вечеру уменьшается.
Второй важный симптом в начале развития РА – скованность движения по утрам, местная или общая. Утренняя скованность может исчезнуть через 20 – 30 минут после того, как больной поднимется с постели или продолжается в течение всего дня. Все эти явления могут сопровождаться общей слабостью, субфебрильной температурой, увеличением СОЭ.
Реже РА начинается с острого полиартрита, значительной скованности движений по утрам, продолжающейся в течение всего дня, высокой лихорадкой (иногда гектического типа). При подобном типе начала заболевания первыми признаками могут быть внесуставные проявления: лимфаденопатия, увеличение печени и селезенки, поражение серозных оболочек и др. В очень редких случаях при остром начале заболевания основным в клинической картине являются именно внесуставные проявления ревматоидного процесса, а суставной синдром проявляется полиартралгией.
Третий тип начала заболевания встречается реже других. В этих случаях боли, и заметная припухлость суставов нарастают медленно, с преобладанием пролиферативных явлений в тканях сустава и медленным развитием деформаций. Движения в суставах в начале заболевания ограничены, температура тела, и картина крови находится в пределах нормы.
В ранний период заболевания развившийся суставной синдром может исчезнуть на несколько месяцев или даже лет. Значительно чаще артрит приобретает прогрессирующий характер. У 70% больных наблюдается полиартрит, реже моно – или олигоартрит.
Характерной локализацией полиартрита в ранний период является 2-й и 3-й пястно-фаланговые и проксимальные межфаланговые суставы, несколько реже пястнозапястные и плюснефаланговые. На втором месте по частоте стоит поражение коленных и лучезапястных суставов. Остальные суставы в раннюю стадию заболевания поражаются редко, а так называемые «суставы исключения» (дистальные межфаланговые, первый пястно-фаланговый и пятый проксимальный межфаланговый) почти не вовлекаются в процесс. В известной мере поражения «суставов исключения» в начале заболевания имеет дифференциально диагностическое значение.
При РА в 70% случаев полиартрит бывает симметричным, при этом преобладают экссудативные явления, повышение местной температуры и резкая болезненность при пальпации пораженного сустава. При поражении мелких суставов кожа над ними может быть слегка гиперемированна. Боли и периартрикулярная отечность, выпот в полость сустава сопровождаются рефлекторным спазмом близлежащих мышц, что обусловливает ограничение движения в суставах.
Острый и подострый РА часто сопровождается теносиновиитом, главным образом, влагалищ сгибательных мышц.
В период развития заболевания в суставных тканях развиваются пролиферативные и фиброзные изменения, что приводит к изменению конфигурации сустава, а в дальнейшем к развитию деформации за счет утолщения капсулы и изменения суставных поверхностей костей, подвывихов и мышечных контрактур. В этот период РА обычно наблюдается симметричный полиартрит и лишь в редких случаях сохраняется стойкий моноолигоартрит. Характерной локализацией по-прежнему остаются мелкие суставы кистей и стоп. Включение в процесс плечевых и тазобедренных суставов, позвоночника и кресцово-подвздошных сочленений происходит в поздней стадии РА. В этот период развивается атрофия близлежащих мышц (выше пораженного сустава) и трофические изменения ногтей и кожи. При каждом обострении РА в патологический процесс вовлекаются новые суставы. Все эти явления сопровождаются нарастанием общей слабости, уменьшением массы тела, ухудшением сна и аппетита, субфебрильной температурой.
Поражение отдельных суставов при РА имеет некоторые особенности. Наиболее ранним является поражение суставов кистей, в первую очередь 2-й и 3-й пястно-фаланговых и 2 - 4-й проксимальных межфаланговых суставов; в результате местного припухания последних, пальцы приобретают веретенообразную форму. Припухлость пястно-фаланговых суставов, сочетающиеся с припуханием суставов запястья, атрофии межфаланговых мышц, создаёт своеобразный тип «ревматоидной кисти». При прогрессировании РА развивается стойкая деформация кисти, которая может быть нескольких типов
чаще всего вследствие разрушения головок пястных костей и слабость мышц, наблюдается «ульнарная девиация кисти» (отклонение пальцев в сторону локтевой кости), которая придаёт ревматоидной кисти форму «плавника моржа».
характерна деформация кисти в виде «шеи лебедя», образующаяся в следствии сгибательной контрактуры в пястно-фаланговых суставах, переразгибание в межфаланговых и сгибания в дистальных суставах пальцев кисти.
наиболее тяжелой является деформация в виде «бутоньерки» - значительное сгибание в пястно-фаланговых и переразгибание в дистальных межфаланговых суставах. Образование этих деформаций приводит к резкому ограничению функций кисти.
В фазе развернутого заболевания поражаются локтевые и плечевые суставы.
Внесуставные проявления ревматоидного артрита.
Чаще возникают у серопозитивных больных при длительном и тяжелом течении РА.
Поражение мышц – атрофия, снижение мышечного тонуса и силы, развитие очагового миозита.
Поражение кожи - ее истончение, подкожные кровоизлияния (экхимозы), мелкоочаговые некрозы мягких тканей под ногтевыми пластинками или в области ногтевого ложа с развитием гангрены дистальной фаланги, нарушение трофики ногтей.
Ревматоидные узелки - наблюдаются у 20-25% больных и специфичны для РА.
Лимфаденопатия - наблюдается у 18-20% больных, обычно при тяжелом течении РА, при синдроме Фелти, синдроме Стилла у взрослых.
Поражение желудочно-кишечного тракта - проявляется нарушением кислотообразующей функции желудка (на ранних стадиях болезни - повышение, в дальнейшем - снижение желудочной секреции). Возможно развитие хронического энтерита, колита, у 11% больных отмечается амилоидоз слизистой оболочки прямой кишки.
Поражение печени - небольшое увеличение печени наблюдается у 25% больных, изменение функциональных проб печени - у 60-86%. Значительное и постоянное увеличение печени наблюдается при синдроме Фелти, болезни Стилла, амилоидозе печени.
Поражение легких и плевры - проявляется сухим или экссудативным плевритом, диффузным интерстициальным фиброзом или фиброзирующим альвеолитом, пневмонитом, облитерирующим бронхиолитом.
Поражение сердца - перикардит, миокардит, эндокардит, коронарный артериит, гранулематозный аортит. В среднем кардит диагностируется у 20% больных РА.
Поражение почек – проявляется в виде гломерулонефрита или амилоидоза - наиболее тяжелое висцеральное проявление РА.
Полисерозит - сочетанное поражение серозных оболочек (плевры, перикарда).
Ревматоидный васкулит (панартериит) - проявляется кожными симптомами, носовыми и маточными кровотечениями или абдоминальным синдромом (тромбоз, инфаркт кишечника).
Поражение нервной системы - встречается в следующих клинических вариантах: периферическая ишемическая нейропатия проявляется парестезиями, снижением тактильной, болевой, температурной чувствительности, двигательными нарушениями:
Поражение глаз - в виде склерита, эписклерита, поражения сосудов сетчатки.
Особым вариантом РА с внесуставным проявлением является синдром Фелти, описанный в 1924 г. Синдром Фелти характеризуется сочетанием эрозивно-деструктивного РА с множественными системными проявлениями, например подкожными ревматоидным узлами, эписклеритами, хроническими язвами голени, периферической полинейропатии, в сочетании с лейконейтропинией и спленомегалией. Для синдрома Фелти характерна высокая частота развития бактериальной инфекции, почему раннее распознавание и лечение имеют столь большое значение для определения прогноза в целом.
Лабораторные методы исследования:
Клиническое обследование (анамнез, характер боли в суставах, утренняя скованность, исследование формы суставов, объема движения в них, температура тела кожи над суставами).
ОАК: У части больных признаки умеренной анемии, лейкоцитоз с нейтрофильным сдвигом влево, реже - лейкопения, эозинофилия, СОЭ увеличивается соответственно активности патологического процесса.
БАК: повышение содержания α2- и γ-глобулинов, серомукоида, фибрина, фибриногена, сиаловых кислот, миоглобина, гаптоглобина, креатина, активности креатинфосфокиназы (нормальный уровень КФК при тяжелой мышечной атрофии и при наличии в крови ингибитора КФК), трансаминаз, особенно АсАТ, ЛДГ и альдолазы, что отражает остроту и распространенность поражения мышц. Возможно повышение уровня мочевой кислоты.
ИИ: снижение титра комплемента, в небольшом титре РФ, в небольшом количестве и незакономерно - LЕ-клетки, антитела к ДНК, снижение количества Т-лимфоцитов и Т-супрессорной функции, повышение содержания IgМ и IgG и снижение - IgА; НLА В», ВКз, ВК-з, ВК^за. высокие титры миозитспецифических антител.
Исследование биоптатов кожно-мышечного лоскута: тяжелый миозит, потеря поперечной исчерченности, фрагментация и вакуолизация мышц, круглоклеточная инфильтрация, атрофия и фиброз их. В коже - атрофия сосочков, дистрофия волосяных фолликулов и сальных желез, изменения коллагеновых волокон, периваскулярная инфильтрация.
Свойства синовиальной жидкости при РА в норме
Показатель
РА
Норма
Прозрачность
Мутная
Прозрачная
Вязкость
Низкая
Высокая
Количество клеток в 1 мкл
5000-25000
200
нейтрофилы, %
Более 75
Менее 10
мононуклеары, %
Менее 25
Более 90
рагоциты
+
-
Общий белок, г/л
40-вО
10-20
Глюкоза, ммоль/л
0.5-3.5
3.5-5.5
Лактдегидрогеназа, ЕД
Более 300
Менее 200
N-ацетил-р-А-глюкозаминидаза
Более 300
Менее 10
Ревматоидный фактор
+
—
Примечание: рагоциты - нейтрофилы, в цитоплазме которых содержатся включения - РФ (иммунокомплексы IgG, IgМ, СI, по форме рагопиты напоминают тутовую ягоду).
Исследование синовиальной жидкости.
Рагоциты неспецифичны для РА и могут встречаться при ревматизме, псориазе, инфекционных артритах, СКВ, подагре, однако при РА они выявляются чаще и могут составлять до 40% от числа всех клеток.
Биопсия синовиальной оболочки. Для РА характерны: гипертрофия и увеличение количества ворсинок; пролиферация покровных синовиальных клеток (они становятся многоядерными, располагаются многослойно, в виде палисада); пролиферация лимфоидных и плазматических клеток; отложение фибрина на поверхности синовиальной оболочки; возможны очаги некроза.
Диагностические критерии РА (АРА, 1987 г)
Критерии
Определение критерий
Утренняя скованность
Утренняя скованность (суставов и околосуставных тканей), продолжающаяся не менее 1 ч)
Артрит трех или большего числа суставов
Как минимум, три суставные области должны иметь установленные врачом припухание периартикулярных мягких тканей или наличие выпота в полости сустава (но не остеофиты). Учитывают справа и слева по 14 суставным зонам: проксимальные межфаланговые, пястно-фаланговые, лучезапястные, локтевые, коленные, голеностопные и плюснефаланговые
Артрит суставов кисти
Припухание хотя бы одного из следующих суставов: проксимальных межфаланговых, лучезапястных пястно-фаланговых
Симметричный артрит
Одновременное поражение одинаковых суставных зон справа и слева - проксимальных межфаланговых, пястно-фаланговых или плюснефаланговых суставов
Ревматоидные узелки
Подкожные узелки, пальпируемые врачом на разгибательной поверхности предплечья вблизи локтевого сустава или в области других суставов
Ревматоидный фактор в сыворотке крови
Определение повышенных титров ревматоидного фактора любым методом, дающим менее 5% сыворотке крови положительных результатов у здоровых лиц в популяции
Рентгенологические изменения
Типичные для РА рентгенологические изменения на переднезадней рентгенограмме кистей с лучезапястными суставами. которые включают эрозии, или неравномерную декальцификацию (остеопороз кисти), локализованную в пораженных суставах или непосредственно на смежных суставах
Принципы лечения больных РА.
применение комплекса лечебных средств, воздействующих на разные стороны сложного патогенеза заболевания
длительность и этапность лечения
дифференцированная терапия в зависимости от формы, течения и активности заболевания.
Схема патогенетической терапии больных РА.
Лекарственная.
противовоспалительная терапия:
нестероидные противовоспалительные препарата (ГКС).
иммуномодулирующая:
4-аминохинолоновые препараты;
соли золота;
Д-пеницилламин;
левомизол.
иммунносупресивная:
цитостатики
Физическое модулирование:
гемосорбция;
лимфоцитоферез;
плазмоферез;
криоферез;
внутри сосудистое лазерное облучение крови;
гипербарическая оксигенация.
Физическая аналгезия
акупунктура
физиотерапевтические процедуры
Реабилитация больных:
консервативная
хирургическая:
синовэктомия
реконструктивные операции
Прогноз.
Зависит от:
клинического варианта РА
характера висцеральных проявлений
степени активности процесса
возможности настойчивого и комплексного лечения
57 Подагра––П. – метаболическое заболевание с нарушением пуриновоо обмена и накоплением мочевой кислоты, протекающее с повторными приступами острого артрита, кристаллиндуцированными синовиитами и отложением уратов в тканях.
Этиология.
Генетически обусловленный дефект в энзимах, участвующих в метаболизме пуринов, что ведёт к повышению количества мочевой кислоты. С генетическим дефектом связана гипофункция ферментных систем почек, регулирующих экскрецию мочевой кислоты.
Избыточное питание, особенно мясной пищей.
Употребление алкоголя, особенно пиво и сухое вино.
Малоподвижный образ жизни, переохлаждение, травма, ОРВИ, прием препаратов – В12, мочегонные препараты золота и др.
Вторичная подагра связана с болезнью почек, сопровождающихся ХПН или болезни крови с распадом клеток и гиперурикемией (полицитемия, лейкоз).
Патогенез включает 3 фазы.
Гиперурикемия и накопление уратов в организме.
Повышенный биосинтез (или поступление) и/или сниженная экскреция с мочой. В зависимости от уровны МК в моче (урикурия) различают 3 типа подагры: (1) – метаболический – высокая урикурия более 3,6 ммоль/сут с нормальным клиренсом мочевой кислоты, (2) – почечный тип со сниженным клиренсов и уровнем (менее 1,8 мм/сут) и (3) смешанный (нормальная или сниженная уратурия и нормальный клиренс МК).
Отложение уратов в тканях. Вследствие отложения в суставной полости уратов активируется свёртывающая система и комплемент, кинины, что приводит к повышению сосудистой проницаемости и фагоцитозу.
Острое подагрическое воспаление. Фагоцитоз сопровождается высвобождением лизосомальных ферментов и цитокинов, и, как результат, развивается воспалительная реакция.
Клиника.В развитии различают 3 периода:
преморбидный – бессимптомная гиперурикемия.
Интермиттирующий – чередование о.приступов и бессимптомных промежутков.
Хроническая подагра. Характерны Тофусы, хронисекий подагрический артрит, из внесуставных проявлений – поражаются почки.
Приступ развивается среди полного здоровья, внезапно, хотя иногда возможен продром – слабость, повышенная утомляемость, субфебрилитет, артралгия и головная боль.
Появляются резчайшие боли в большом пальце стопы. Он опухает, кожа над ним краснеет, становится синевато-багровой, нарушается ф-я сустава, Т-ра повышается до 38-39 ?С. первый приступ длится 3-10 дней. Следующий приступ может наступить через годы. Со временем светлый промежуток сокращается.
В последующем в патологический процесс вовлекаются плюснефаланговые и предплюсневые суставы, менее типично воспаление лучевых и лучезапястных суставов. Со временем развивается хр. подагрический артрит, при котором чаще поражаются суставы ног с развитием дефигурации , деформации, ограничением подвижности, формированием кнтрактур и подвывихов.
Тофусы – узелки, содержащие ураты в соединительной ткани – располагаются в ушных раковинах, локтях, сумках локтевых суставов, на пальцах кисти, на лбу и хрящевой перегородке носа.
Диагностика. Анамнез, жалобы и данные объективного осмотра. ОАК – при обострении СОЭ и сдвиг влево. Биохимия – повышена МК (№ 0,12-0,24 ммоль/л), также фибрин, сиаловые кислоты.
Лечение.
Купирование острого приступа. НПВС – индометацин 100 мг однократно, затем 2-3 рвд по 100 мг. Диклофенак – // –. Напроксен тоже можно. Если есть колхицин, то это лучше, чем НПВС. При неэффективности терапии и выраженном болевом синдроме можно ввести ГКС внутрисуставно, однократно.
Межприступный период.
Диета с ограничением мяса и др. высокобелковых продуктов – преимущественно молочно-растительная, можно яйца, нежирную рыбу. Ограничить алкоголь. Противопоказаны бобовые, чай, кофе, какао, пряности, потроха, мясные бульоны, мясо солочных животных.
Обильное щелочное питьё и достаточная физическая активность.
Лекарства
урикостатики – аллопуринол, угнетает синтез МК. Доза зависит от тяжести – 233-300-400-600-900/сутки; Поддержка 300-400 постоянно, с 2-месячным перерывом летом.
Урикозурические – угнетают реабсорбцию Мк в канальцах. Показаны при почечном типе. Этамид – 0,7 г*3-4 раза *7-10 дней с недельным перерывом. Антуран 0,4-0,6 г/сут. Длительно не используют и не применяют при уратной нефропатии. Могут вызывать ОПН, поэтому во 2 гкб не применяются!!!
Алломарон – комплекс аллопуринола и бензбромарона – 1 таб/сут.
ФТЛ – тепловые, улечшающие МЦР.
58 Деформирующий остеоартроз
Деформирующий остеоартроз (ДОА) — хроническое дегене¬ративное заболевание суставов, в основе которого лежит дегенера¬ция суставного хряща с последующим изменением костных сус¬тавных поверхностей, развитием краевых остеофитов, деформаци¬ей сустава, а также развитием умеренно выраженного синовита.
Различают первичный и вторичный ДОА. Первичный ДОА развивается в здоровом до этого хряще под влиянием его чрезмер¬ной нагрузки. При вторичном ДОА происходит дегенерация уже предварительно измененного суставного хряща.
Этиология
Причины первичного остеоартроза (ОА) окончательно не из¬вестны. Основными предполагаемыми факторами развития пер¬вичного ОА являются:
• несоответствие между механической нагрузкой на суставный хрящ и его возможностью сопротивляться этому воздействию;
• наследственная предрасположенность, выражающаяся, в част¬ности, в снижении способности хряща противостоять механи¬ческим воздействиям.
В развитии первичного ОА большую роль играет взаимодейст¬вие внешних и внутренних предрасполагающих факторов.
Внешние факторы, способствующие развитию первичного ОА: травмы и микротравматизация сустава; функциональная перегруз - ка сустава (профессиональная, бытовая, спортивная); гипермо¬бильность суставов; несбалансированное питание; интоксикации и профессиональные вредности (нитраты, соли тяжелых металлов, гербициды и др.); злоупотребление и интоксикация алкоголем; перенесенные вирусные инфекции.
Внутренние факторы, предрасполагающие к развитию первич¬ного ОА: дефекты строения опорно-двигательного аппарата и на¬рушения статики, ведущие к изменению конгруэнтности сустав¬ных поверхностей (плоскостопие, дисплазии, genu varum, genu valgum, сколиоз позвоночника); избыточная масса тела; эндокрин¬ные нарушения; нарушения общего и местного кровообращения; сопутствующие хронические заболевания, в том числе предшест¬вующие артриты.
Основными причинами вторичных ОА являются: травмы суста¬ва, эндокринные заболевания (сахарный диабет, акромегалия и др.); метаболические нарушения (гемохроматоз, охроноз, подагра), другие заболевания костей суставов (ревматоидный артрит, ин¬фекционные артриты и другие воспалительные заболевания суста¬вов, асептические некрозы костей.
Патогенез
Под влиянием этиологических факторов происходит более бы¬строе и раннее «постарение» суставного хряща. Метаболизм его нарушается, прежде всего происходит деполимеризация и убыль протеогликанов (в первую очередь хондроитинсульфатов) основ¬ного вещества и гибель части хондроцитов. При OA меняется фе¬нотип хондроцитов и синтезируются не свойственные нормально¬му хрящу протеингликаны и коллаген. Хрящ теряет свою эластич¬ность, раньше всего в центре, становится шероховатым, разволок- няется, в нем появляются трещины, обнажается подлежащая кость, в дальнейшем хрящ может полностью исчезнуть. Отсутствие амортизации при давлении на суставную поверхность костей при¬водит к их уплотнению (субхондральный остеосклероз) с образо¬ванием участков ишемии, склероза, кист. Одновременно по краям суставных поверхностей эпифизов хрящ компенсаторно разраста¬ется, а затем происходит окостенение — образуются краевые ос¬теофиты. Наличие в суставной полости отломков хряща, фагоци-тируемых лейкоцитами с освобождением лизосомальных фермен¬тов цитокинов, приводит к периодическому синовиту, при неод¬нократных рецидивах — к фиброзным изменениям синовии и капсулы. В настоящее время показана роль иммунной системы в патогенезе ДОА (Н. М. Мазина, 1986): повышение функции Т-хе- лперов, способствующее развитию аутоиммунных процессов — по¬явлению специфических аутоантигенов (измененных протеоглика¬нов) хряща, синовии, аутоантител и иммунных комплексов с по¬следующим повреждением хряща. Большую роль играет повыше¬ние катаболической активности различных цитокинов, а также ферментов металлопротеиназ самого хряща.
Клиническая картина
болеет около населения, чаще женщины в возрасте 40-60 лет, после 60 лет заболевание встречается практиче¬ски у 100% людей. Основными и общими признаками для ДОА любой локализации являются следующие:
1. Боли в суставах механического типа, возникают при нагрузке на сустав, больше к вечеру, затихают в покое и ночью. Боли обусловлены трабекулярными микропереломами, костным ве¬нозным стазом и внутримедуллярной гипертензией, раздраже¬нием окружающих тканей остеофитами, спазмом околосустав¬ных мышц. При развитии венозных стазов в субхондральном отделе возможны тупые «сосудистые» боли, возникающие ночью и исчезающие при утренней активности.
2. «Стартовые» боли в суставах, появляющиеся при первых шагах больного, затем исчезающие и вновь возникающие при продолжающейся нагрузке. Могут быть признаком реактивного синовита. Развитие синовита сопровождается усилением боли, припухлостью сустава.
3. Периодическое «заклинивание» сустава («блокадная» боль) — внезапная резкая боль в суставе при малейшем движении, обусловленная суставной «мышью» — ущемлением кусочка некротизированного хряща между суставными поверхностями. Боль исчезает при определенном движении, ведущем к удалению «мыши» с суставной поверхности.
4. Крепитация при движениях в суставе.
5. Стойкая деформация суставов, обусловленная костными изменениями.
6. Сравнительно небольшое ограничение подвижности суставов, за исключением тазобедренного.
7. Наличие в анамнезе механической перегрузки сустава или травмы, воспалительных или метаболических заболеваний суставов.
8. Наличие у больного нарушений статики, нейроэндокринных заболеваний, нарушений местного кровообращения, артроза у родителей.
Коксартроз
Коксартроз — наиболее частая и тяжелая форма ДОА. Обычно приводит к потере функции сустава и инвалидности больного. У 60% больных коксартроз является вторичным и развивается в ре¬зультате перенесенных остеонекроза, пороков развития косгно- суставной системы (протрузия), травм, функциональных перегру¬зок (ожирение, разная длина конечностей и др.). Обычно больной начинает прихрамывать на больную ногу. В дальнейшем появля¬ются и постепенно усиливаются боли в паховой области с ирра¬диацией в колено, наступают хромота, ограничение ротации бедра кнутри и отведения его, позже ограничиваются наружная ротация и приведение бедра, а также его сгибание и разгибание. Иногда возникает «заклинивание» тазобедренного сустава. Довольно быст¬ро развивается атрофия мышц бедра и ягодицы, позже — сгиба- тельная контрактура, укорочение конечности, изменение походки, нарушение осанки, выраженная хромота, а при двустороннем по¬ражении — «утиная походка». Рентгенологически патологический процесс начинается с сужения суставной щели и появления кост¬ных разрастаний, затем головка бедра сплющивается, что ведет к укорочению конечности: в мягких тканях могут наблюдаться обызвествления. Течение коксартроза постоянно прогрессирую¬щее.
Гонартроз
Гонартроз чаще бывает вторичным, связанным с травмой ко¬ленных суставов или нарушением статики; течение его благо-
приятнее, чем течение Основные симптомы — боль с
внутренней или передней стороны сустава при ходьбе, особенно по лестнице, проходящая в покое; боль наблюдается в течение месяца, предшествующего моменту постановки диагноза; неста¬бильность сустава, хруст при активных движениях в коленном суставе, утренняя скованность в пределах 30 минут. На рентгено¬грамме обнаруживают заострение и вытягивание межмьнцелкового возвышения, сужение суставной щели, обильные остеофиты.
Остеоартроз мелких суставов кисти
Характеризуется следующими признаками:
наличие твердых узелков (за счет остеофитов) на боковых по¬верхностях дистальных межфаланговых суставов (узелки Гебер- дена) и на тыльно-боковой поверхности проксимальных меж¬фаланговых суставов (узелки Бушара по одному с каждой сто¬роны); в период формирования узелков ощущается жжение, покалывание, онемение, исчезающие после образования узел¬ков;
• боль и скованность в мелких суставах кисти; ограничение дви¬жения в дистальных межфаланговых суставах, иногда латераль¬ная девиация концевых фаланг;
• признаки синовита (отечность, локальная гиперемия, усиление болей);
• рентгенография кистей выявляет остеофиты, сужение щелей суставов и в редких случаях (при эрозивной форме остеоартро- за) деструкцию суставных поверхностей;
• узелковый остеоартроз межфаланговых суставов характеризует¬ся генетической предрасположенностью, причем эта форма пе¬редается по женской линии (бабушка-мать-дочь);
• наличие узелков Гебердена или Бушара считается прогностиче¬ски неблагоприятным признаком для течения остеоартроза.
Остеоартроз га^гао-здпяствого сустава большого пальца
Наблюдается у женщин обычно в периоде климакса, обычно двусторонний, проявляется болями по внутреннему краю запястья (в месте сочленения I пястной кости и трапециевидной кости за¬пястья) при движениях большого пальца. Одновременно отмечает¬ся ограничение движений большого пальца и хруст. Выраженная стадия заболевания проводит к значительной деформации кисти. Однако обычно боли беспокоят мало, ограничение подвижности выражено незначительно.
Остеоартроз локтевого сустава
Проявляется болями при движении в суставе, возможно неко¬торое ограничение подвижности (преимущественно разгибание
сустава), что обусловлено значительными костными разрастания¬ми вокруг суставной поверхности локтевой кости.
Остеоартроз плечевого сустава
Сопровождается поражением субакромиального сустава, что обусловливает болезненное ограничение отведения плеча в сторо¬ну. При движениях в плечевом суставе отмечается хруст.
Возможна небольшая атрофия прилежащих мышц. Деформа¬ции плечевого сустава не отмечается. Плечевой артроз первичный бывает очень редко, чаще это вторичный остеоартроз.
Остеоартроз грудинно-ключичного сочленения
Часто сочетается с плечелопаточным периартритом. Характер¬ны припухлость и деформация грудинно-юпочичного сочленения, боли при движениях. На рентгенограмме этого сустава обнаружи¬вается сужение суставной щели и остеофиты.
Остеоартроз голеностопного сустава
Обычно посттравматического происхождения, обусловливает нарушение ходьбы, деформацию сустава.
Остеоартроз первого плюснефалангового сустава
Чаще всего бывает двусторонним и частью обусловлен
плоскостопием, иногда травмой, профессиональными факторами. Основными симптомами являются болезненность и ограничение подвижности большого пальца стопы, затруднения при ходьбе, отклонение пальца в наружную сторону (halux valgus), деформация сустава (за счет остеофитов).
Деформированный сустав часто травмируется (в частности, не¬удобной обувью), нередко возникает воспаление околосуставной сумки (бурсит). При рентгенографии определяются сужение сус¬тавной щели, кисты, остеосклероз (субхондральный) и в дальней¬шем подвывих или полный вывих головки первой полюсневой кости.
Полиостеоартроз
Полиостеоартроз (артрозная болезнь, генерализованный остео-артроз, болезнь Келлгрена) — вариант остеоартроза с множествен¬ным поражением периферических и межпозвонковых суставов. В основе полиостеоартроза лежит генетически обусловленная гене¬рализованная хондропатия со снижением резистентности хряща к давлению, физической нагрузке и слабость связочно-мышечного аппарата, обусловленная распадом протеогликанов.
Основными клиническими проявлениями полиостеоартроза являются:
генерализованный артроз (трех и более суставов), поражение суставов обычно двустороннее, при этом в первую очередь
страдают коленные, тазобедренные, дисталыше межфаланго- вые суставы (геберденовские узелки); реже поражаются суставы большого пальца стопы и кисти и голеностопные суставы;
• наличие одновременно остеохондроза межпозвоночных дисков (боли и скованность различных отделов позвоночника; паре¬стезии, снижение рефлексов при сдавлении остеофитами нерв¬ных волокон в межпозвонковых отверстиях; при сдавлении по¬звоночных артерий появляются головные боли, головокруже¬ния, расстройства зрения);
• спондилоз шейного и поясничного отделов;
• различные периартриты: плечелопаточный, стилоидит, эпикон- дилит, трохантерит;
• тендовагиниты.
Полиостеоартроз подразделяется на безузелковую и узелковую формы (узелки Гебердена и Буршара).
По клиническим проявлениям вьщеляют малосимптомные и манифестные формы деформирующего остеоартроза. Манифест¬ные формы, в свою очередь, подразделяют на медленно и быстро прогрессирующие.
Малосимптомные формы отмечаются преимущественно в моло¬дом возрасте. Больных беспокоят редкие, слабой интенсивности кратковременные боли и (или) хруст в 1-3 суставах, появляющиеся после значительной нагрузки; могут наблюдаться судороги икро¬ножных мышц, узелки Гебердена. Функции суставов не нарушены. Рентгенологические изменения I-III стадии определяются в одном или нескольких суставах.
Медленно прогрессирующее течение манифестной формы выявля¬ется в любом возрасте. Суставный болевой синдром умеренно вы¬ражен. Существенные клинико-функциональные проявления во многих суставах развиваются в течение 5 и более лет после начала заболевания. Боли в суставах возникают или усиливаются при ох¬лаждении, изменении погоды, после перенапряжения сустава; по¬являются боли в начале движения (стартовые боли). Боли ною¬щего или грызущего характера, сопровождаются утомляемостью регионарных мышц, тугоподвижносгыо сустава, периодическим «заклиниванием» его. Со временем развиваются деформации сус¬тавов. Рентгенологические изменения преимущественно I-II ста¬дии.
Быстро прогрессирующее течение манифестной формы ДОА обычно возникает у молодых людей, при этом существенные кли- нико-функциональные изменения развиваются в срок до 5 лет от начала заболевания. Отмечаются частые и довольно интенсивные боли одновременно во многих суставах. Они усиливаются при нагрузке, длительном покое; беспокоят судороги конечностей. Определяются узелки Гебердена, часто узелки Бушара, другие де¬формации суставов. Рано появляются периартриты, атрофия
мышц, неврологические осложнения. Рентгенологиче¬
ские изменения варьируют от II до III стадии.
Классификация
Патогенетические варианты
1. Первичный (вдиопатический).
2. Вторичный (обусловлен травмами, нарушениями статики, гипермобильностью суставов, артритами и др.).
П. Клинические формы
узелковый, безузелковый.
2. Олигоостеоартроз.
3. Моноартроз.
4. В сочетании с остеохондрозом позвоночника, зом.
III. Преимущественная локализация
1. Межфаланговые суставы (узелки Гебердена, Бушара).
2. Тазобедренные суставы (коксартроз)
3. Коленные суставы
4. Другие суставы.
IV. Рентгенологическая стадия (по Келлгрену): I, II, III, IV.
V. Синовит:
• имеется;
• отсутствует.
VI. Функциональная способность больного
1. Трудоспособность ограничена временно
2. Трудоспособность утрачена (ФН2).
3. Нуждается в постороннем уходе (ФНз).
Диагностические критерии
(Л. И. Беневоленская и соавт., 1993)
7. Клинические критерии
1.1. Боли в суставах, возникающие в конце дня и/или в первую половину ночи.
1.2. Боли в суставах, возникающие после механической нагрузки и уменьшающиеся в покое.
1.3. Деформация суставов за счет разрастаний (включая узелки Гебердена и Буршара).
2. Рентгенологические критерии
2.1. Сужение суставной щели.
2.2. Остеосклероз.
2.3. Остеофитоз.
Примечание: критерии 1.1 и 1.2. основные, критерий 1.3. дополнительный. Для постанов¬ки диагноза осгеоартроэа ООЯЗатеЛЬНО наличие первых двух клинических И рентгенологических критериев.
Критерии диагноза коксартроза и артроза суставов кистей (Althman, 1995)
A. Критерии диагностики коксартроза Вариант 1
Боль в тазобедренном суставе в течение более, чем половины
прошедшего месяца
+
как минимум два из 3 критериев:
• СОЭ 20 мм/ч
• Остеофиты головки бедренной кости и/или вертлужной впади¬ны (на рентгенограмме)
• Сужение суставной щели на рентгенограмме Вариант 2
Боль в области тазобедренного сустава в течение 2 недель и
более
+
как минимум три из 4 признаков:
• Уменьшение наружной ротации бедра
• Боль при внутренней ротации бедра
• Утренняя скованность < 60 минут
• Возраст > 50 лет
B. Критерии диагностики артроза кистей Вариант 1
Боль в мелких суставах кистей и утренняя скованность в них в
течение более чем половины прошедшего месяца
+
значительное увеличение объема более чем одного из межфаланговых суставов
Вариант 2
Значительное увеличение в объеме двух суставов и более. Отек
двух или одного пястнофалангового сустава
+
деформация более чем одного из 10 суставов
Лабораторные данные
1. Oak без существенных изменений. При реактивном синовите может быть увеличение соэ до 20-25 мм/ч.
2. Бак без существенных изменений. В случае развития синовита в крови повышается содержание фибрина, серомукоида, сиаловых кислот, гаптоглобина.
3. Анализ мочи: без отклонений от нормы.
Инструментальные исследования
Рентгенологическое исследование суставов. Н. С. Косинская вы-деляет три клинико-рентгенологические стадии артроза:
I — незначительное ограничение движений, небольшое, неот¬четливое, неравномерное сужение суставной щели, легкое заост¬рение краев суставных поверхностей (начальные остеофиты);
II — ограничение подвижности в суставе, грубый хруст при движениях, умеренная амиотрофия, выраженное сужение сустав¬ной щели в 2-3 раза по сравнению с нормой, значительные остео¬фиты, субхондральный остеосклероз и кистевидные просветления в эпифизах;
III — деформация сустава, ограничение его подвижности, пол¬ное отсутствие суставной щели, деформация и уплотнение сустав¬ных поверхностей эпифизов, обширные остеофиты, суставные «мыши», субхондральные кисты.
Большинство ревматологов пользуется для определения рент-генологической стадии гонартрита классификацией Kellgren и Lawrence (1957), усовершенствованной Lequesne в 1982 г.
Стадии остеоартроза по Kellgren и Lawrence
0 — отсутствие рентгенологических признаков;
1 — кистовидная перестройка костной структуры, линейный остеосклероз в субХондральных отделах, появление маленьких краевых остеофитов;
II — симптомы I стадии + более выраженный остеосклероз + сужение суставной щели;
III — выраженный субхондральный остеосклероз, большие краевые остеофиты, значительное сужение суставной щели;
IV — грубые массивные остеофиты, суставная щель прослежи¬вается с трудом, эпифизы костей, образующих сустав, деформиро¬ваны, резко уплотнены.
Исследование биоптата синовиальной оболочки: покровные клетки расположены в один ряд, ворсины атрофичны, сосудов мало, значительные поля фиброза, жирового перерождения.
Исследование синовиальной жидкости. Синовиальная жидкость прозрачная или слабомутная, высокой или средней ВЯЗКОСТИ, му- циновый сгусток плотный. Количество клеток в 1 МКЛ синовиаль-
ной жидкости от до составляют менее
могут обнаруживаться фрагменты хрящевой ткани.
Исследование биоптата хрящевой ткани: уменьшение площади перихондроцитарных лакун в поверхностных слоях; снижение плотности клеток в глубоких слоях; уменьшение количества ядер лакунах среднего слоя; увеличение толщины кальфицированного слоя хряща.
Программа обследования
1. ОА крови, мочи.
2. БАК: общий белок, белковые фракции, серомукоид, фибрин, гаптоглобин, сиаловые кислоты, СРП, мочевая кислота.
3. Рентгенография суставов.
4. Биопсия синовии и исследование синовиальной жидкости (в затруднительных для диагностики случаях).
Примеры формулировки диагноза
1. Деформирующий остеоартроз, первичный, медленно про-грессирующий; III стадия рентгенологических изменений; на¬рушение функции суставов I степени.
2. Деформирующий остеоартроз, быстро прогрессирующий с преимущественным поражением тазобедренных суставов; III стадия рентгенологических изменений; с частыми и длительными обострениями; нарушение функции суставов II степени.
Лечение OA продолжает оставаться сложной и нерешенной задачей.
Назначают комплексное лечение, которое преследует следующие цели: замедление прогрессирования патологического процесса, уменьшение вы-раженности боли — основной причины обращения больного к врачу; нор¬мализацию обменных процессов в суставном хряще, улучшение функции пораженных суставов.
Поскольку увеличенная масса тела и снижение тонуса мышц — факторы риска развития и прогрессирования OA, нормализация массы тела и укрепление мышц являются важными направлениями в лечении OA.
• Ликвидация болевого синдрома обеспечивается назначением ненар-котических анальгетиков центрального действия (парацетамол), НПВП и так называемых хондропротекторов.
• При умеренных болях без признаков воспаления (синовит) следует периодически назначать ненаркотический анальгетик центрального действия (парацетамол в дозе до 4 г/сут). Его преимуществом перед НПВП считают меньшую вероятность развития побочных эффектов со стороны ЖКТ.
• У больных с выраженными постоянными болями, часто связанными не только с механическими факторами, но и с воспалением (синовит), препаратами выбора считаются НПВП. Наиболее предпочтительны ибу- профен (в дозе 1200—1400 мг/сут), кетопрофен (100 мг/сут), диклофенак (100 мг/сут). НПВП оказываются эффективными в меньших дозах, чем при лечении РА. Рационально, однако, начинать лечение с полной дозы, а при достижении обезболивающего эффекта дозу снижают до необходимой поддерживающей. При улучшении состояния больного НПВП отменяют, но при обострении их назначают повторно. Применение пироксикама и индометацина не рекомендуется в силу того, что они ослабляют действие других препаратов, которые может принимать пациент пожилого возраста (например, гипотензивные препараты). Кроме того, индометацин оказывает хондродеструктивное действие, и его прием может способствовать про- гессированию дегенерации хряща. У больных пожилого возраста, прини¬мающих НПВП, следует иметь в виду возможность развития эрозивного гастрита, поэтому рекомендуются препараты, оказывающие селективную блокаду фермента циклооксигеназа-2 (ЦОГ-2) — мелоксикам (7,5 мг/сут), целекоксиб (целебрекс) в дозе 100—200 мг/сут.
Обезболивающий эффект оказывают аппликации димексида на пора¬женный сустав (особенно с добавлением раствора НПВП).
• Весьма эффективными препаратами считаются естественные компо ненты суставного хряща (хондропротекторы) — хондроитин сульфат натрия и глюкозамин.
Хондроитин сульфат назначают в дозе 1000—1500 мг/сут в 2—3 приема длительно (возможны повторные курсы), что позволяет снизить дозу НПВП. Сходной эффективностью и переносимостью обладает глюкозамин сульфат, который назначают в дозе 1500 мг/сут однократно в течение не менее 6 мес, повторными курсами.
При гонартрозе используют внутрисуставное введение производных гиалуроновой кислоты.
• Улучшение функции пораженных суставов достигается применени ем физиотерапевтических методов лечения: ЛФК, тепловые процедуры (парафиновые аппликации, озокерит), электропроцедуры (токи УВЧ или ультразвук на область пораженных суставов). Используют также электро форез лидазы и йодида калия, способствующий рассасыванию фиброзной ткани капсулы сустава и прикрепляющихся к суставу сухожилий.
При стихании обострения и уменьшении болей хороший эффект ока¬зывает санаторно-курортное лечение (лечебные грязи, радиоактивные или сульфидные ванны).
• Хирургическое лечение (артроскопические операции для удаления хрящевого детрита) достаточно эффективно. Эндопротезирование тазобед ренного или коленного сустава проводят только при тяжелом инвалидизи- рующем поражении этих суставов.
Прогноз. OA (в особенности первичный) редко приводит к потере тру-доспособности. Однако при локализации процесса в тазобедренном суставе вследствие быстро прогрессирующего ограничения движений больной ста¬новится инвалидом.
Профилактика. Первичная профилактика сводится к борьбе с внешними факторами, которые могут способствовать развитию дегенеративных изменений в суставном хряще (избегать постоянной микротравматизации суставов, длительной функциональной перегрузки; нормализация массы тела и пр.).
Среди многочисленных путей профилактики остеоартроза можно выделить следующие, наиболее значимые:
• профилактика и эффективное лечение травмы сустава
• достаточная двигательная активность на протяжении всей жизни
• снижение избыточного веса тела
• своевременная коррекция приобретённого или врождённого нарушения биомеханики сустава (например, коррекция плоскостопия, исправление травматической деформации оси конечности, лечение врождённого вывыха бедра и т. п.)
59 Дифференциальный диагноз заболеваний суставов
Ревматизм(орл)Ревматизм определяется как системное воспалительное заболевание соединительной ткани с преимущественным поражением сердечно-сосудистой системы, развивающейся в связи с острой А-стрептококковой инфекцией у предрасположенных лиц.Ревматический полиартрит имеет типичную клинику. Поражаются обычно крупные суставы, они припухают, кожа над ними красная, движения резко болезненные и ограниченные. Характерны летучесть поражения суставов и симметричность, т.е. вначале поражается один крупный сустав, далее другой, третий и обязательно противоположный суставы. Диагностическое значение имеет закономерный, положительный быстрый эффект лечения аспирином, другими НПВС и отсутствие суставной инвалидизации после купирования острых явлений полиартрита (деформации, тугоподвижности суставов). Поражение сердца обязательно для ревматизма. При этом поражаются миокард и эндокард Кольцевая эритема на коже внутренней поверхности рук и ног, живота, шеи, грудной клетки - редкий, но патогномоничный признак ревматизма Характерной для ревматизма формой поражения ЦНС является хорея, встречающаяся у детей, реже подростков. Она характеризуется развитием насильственных гиперкинезов мышц лица, туловища, конечностей.Диагностическое значение имеет повышение титра антигиалуронидазы и антистрептокиназы более 1:300, анти-о-стрептолизина более 1:250.
Ревматоидный артрит - системное хроническое заболевание соединительной ткани с преимущественным поражением суставов по типу эрозивных артритов. Отличительной особенностью ревматоидного артрита является прогрессирование суставных изменений с развитием стойкой деформации суставов и нарушением их функции.Течение заболевания отличается большой вариабельностью, у некоторых больных они протекает очень длительно, деформации развиваются медленно; у части больных прогрессирование происходит катастрофически быстро, приводя к стойкой суставной инвалидизации.Существуют факторы риска ревматоидного артрита. К ним относятся пол и возраст - чаще болеют женщины в возрасте старше 40 лет. Отмечается наследственная предрасположенность к заболеванию. Клинико-анатомическая характеристика РАУтренняя скованность движении.Боль при движении или чувствительность по крайней мере, в одном суставе. Припухлость по меньшей мере, в одном суставе. Припухлость хотя бы еще в одном суставе. Симметричное припухание суставов.
Наличие подкожных ревматоидных узелков. Рентгенологические изменения в суставах, характерные для РА. Обнаружение в крови ревматоидного фактора Скудный муциновый преципитат в синовиальной жидкости. Характерные гистологические изменения синовиальной оболочки Характерные гистологические изменения в ревматоидных узелках.
Подагра рассматривается как системное, ферменто-метаболическое заболевание, обусловленное нарушением пуринового обмена, развитием гиперурикемии, гиперурикозурии. Проявляется поражением суставов и внесуставными признаками. В основе повышенного содержания мочевой кислоты в крови - основного метаболического нарушения при подагре, лежит генетически детерминированный дефект ферментных систем, принимающих участие в эндогенном синтезе пуриновых нуклеотидов.У больных подагрой усилен синтез пуринов в организме, способствующими факторами развития заболевания является повышенное поступление пуринов с пищей. Увеличивается образование мочевой кислоты.Наличие в анамнезе или наблюдение не менее двух атак опухания и/или покраснения и сильной боли в суставе (суставах) конечности с ремиссией через 1-2 недели - 2. Моноартикулярный характер артрита. Острый артрит плюснефалангового сустава большого пальца стопы в анамнезе или статусе - 3. Тофусы 4. Мочекаменная болезнь 5. Симптом "пробойника" или крупные кисты на рентгенограмме 6. Гиперурикемия 7.Повышение содержания мочевой кислоты в сыворотке крови более 0,42 ммоль/л у мужчин и 0,36 ммоль/л у женщин.8Кристаллы мочевой кислоты в синовиальной жидкости или в тканях, выявленные химически или морфологически.
Деформирующий остеоартроз - системное дегенеративное заболевание суставных и околосуставных тканей. В основе заболевания лежит дегенерация и деструкция суставного хряща с последующей пролиферацией подлежащей костной ткани. Факторы риска ДОА разные для двух основных форм болезни - по типу моно - и олигоартроза или полиостеоартроза. В первом случае факторами риска являются механическая перегрузка суставов, микротравмы, нарушения статики; во втором - наследственная предрасположенность. заболевание начинается в относительно молодом возрасте - до 40 лет.Характерны вечерние и ночные боли после дневной нагрузки. Иногда возникают очень сильные боли и развивается блокада сустава. Помимо боли, больные жалуются на “хруст” в суставах. Постепенно прогрессирует деформация сустава, однако анкилозы развиваются редко. Естественно, что страдает функция сустава, функциональная недостаточность неуклонно нарастает. Полиостеоартроз характеризуется поражением дистальных межфаланговых суставов кистей. В области суставов появляются плотные симметричные утолщения (узелки Гебердена), нередко развивается реактивный синовит. Постепенно суставы деформируются, фаланги пальцев искривляются. Если узелки образуются в области проксимальных межфаланговых суставов, они носят название узелков Бушара.
60 ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКИ (Американская ревматологическая ассоциация, 1982 г.)
1. Волчаночная бабочка. 2. Дискоидная бабочка. 3. Фотосенсибилизация. 4. Изъязвление слизистой оболочки полости рта и носоглотки. 5. Артрит (неэрозивный артрит, без деформаций). 6. Серозит (плеврит и/или перикардит). 7. Поражение почек (персистирующая протеинурия 0,5 г/сут, и более). 8. Неврологические нарушения (судороги, психоз). 9. Гематологические нарушения (гемолитическая анемия, лейкопения, тромбоцитопения). 10. Иммунные нарушения (наличие LE-клеток или антител к ДНК или Sm-антител или ложноположительная реакция Вассермана). 11. Антинуклеарные антитела (повышение титра антинуклеарных антител). Диагноз достоверен при наличии 4 критериев и более.
61 ДИАГНОСТИЧЕСКИЕ ПРИЗНАКИ СИСТЕМНОЙ СКЛЕРОДЕРМИИ (Н.Г.Гусева, 1993)
Основные признаки: - склеродермическое поражение кожи - синдром Рейно, дигитальные язвочки/рубчики - суставно-мышечный синдром (с контрактурой) - остеолиз - кальциноз - базальный пневмофиброз - крупноочаговый кардиосклероз - склеродермическое поражение пищеварительного тракта - острая склеродермическая нефропатия - наличие специфических антинуклеарных антител (анти-Scl-70 и антицентромерные антитела) - капилляроскопические признаки (по данным широкопольной капилляроскопии) Дополнительные признаки: - гиперпигментация кожи - телеангиэктазии - трофические нарушения - полиартралгии - полимиалгии, полимиозит - полисерозит (чаще адгезивный) - хроническая нефропатия - полиневрит, тригеминит - потеря массы тела (более 10 кг) - увеличение СОЭ (более 20 мм/ч) - гиперпротеинемия (более 85 г/л) - гипергаммаглобулинемия (более 23%) - наличие антител к ДНК или АНФ - наличие ревматоидного фактора Наличие любых трех основных признаков или сочетание одного из основных, если им являются склеродермическое поражение кожи, остеолиз ногтевых фаланг или характерное поражение пищеварительного тракта, с тремя и более вспомогательными признаками достаточно для того, чтобы поставить достоверный диагноз системной склеродермии.
62 Дермато-полимиозит
— диффузное прогрессирующее воспалительное заболевание соединительной ткани с преимущественным поражением поперечно-полосатой и гладкой мускулатуры с нарушением двигательной функции, кожи в виде эритемы и отека, с частым поражением внутренних органов.
Диагностические критерии дерматомиозита и полимиозита (Bohan, Petter, 1975)
1. Дерматологические проявления, включающие гелиотропную окраску кожи век с периорбитальным отеком, чешуйчатый эритематозный дерматит на тыльной поверхности кистей, особенно над пястнофаланговыми и проксимальными межфаланговыми суставами (синдром Гогтрона) и поражение кожи над коленными, локтевыми суставами, кожи лица, шеи, верхней половины грудной клетки.
2. Симметричная слабость мышц плечевого и тазового пояса и передних сгибателей шеи, прогрессирующая в течение нескольких недель или месяцев в сочетании или при отсутствии дисфагии или поражения дыхательной мускулатуры.
3. Повышение сывороточной концентрации мышечных ферментов (КФК, альдолаза, ACT, АЛТ и ЛДГ).
4. Электромиографические изменения: короткие, мелкие полифазные моторные единицы, фибрилляции
5. При гистологическом исследовании мышц признаки некроза мышечных фибрил 1 и 2 типов, фагоцитоз, регенерация с базофилией, крупные ядра и ядрышки в сарколемме, перифасциальная атрофия, вариабельность размера миофибрилл, воспалительный экссудат.
При наличии первого и любых двух из последующих четырех критериев диагностируется дерматомиозит, при наличие четырех критериев (2, 3, 4, 5) диагностируется полимиозит
63 Сахарный диабет – клинический синдром хронической гипергликемии и глюкозурии, обусловленный абсолютной или относительной инсулиновой недостаточностью, приводящий к нарушению обмена веществ, поражению сосудов (различные ангиопатии), нейропатии и патологическим изменениям в различных органах и тканях.
Классификация сахарного диабета (ВОЗ, 1985)
А. Клинические классы
I. Сахарный диабет
1. Инсулинзависимый сахарный диабет (ИЗД)
2. Инсулиннезависимый сахарный диабет (ИНЗД)
а) у лиц с нормальной массой тела
б) у лиц с ожирением
3. Сахарный диабет, связанный с недостаточностью питания
4. Другие типы диабета, связанные с определенными состояниями и синдромами:
а) заболевания поджелудочной железы;
б) эндокринные заболевания;
в) состояния, вызванные приемом лекарственных препаратов или воздействием химических веществ;
г) аномалии инсулинов или его рецептора;
д) определенные генетические синдромы;
е) смешанные состояния.
II. Нарушенная толерантность к глюкозе
а) у лиц с нормальной массой тела
б) у лиц с ожирением
в) связанная с определенными состояниями и синдромами (см. п. 4)
III. Сахарный диабет беременных
Б. Классы статистического риска (лица с нормальной толерантностью к глюкозе, но со значительно повышенным риском развития сахарного диабета)
а) предшествовавшие нарушения толерантности к глюкозе
б) потенциальные нарушения толерантности к глюкозе.
I. Клинические формы диабета
1. Инсулинзависимый диабет (диабет I типа)
вирусиндуцированный или классический (тип IA)
аутоиммунный (тип IB)
медленнопрогрессирующий
2. Инсулиннезависимый диабет (диабет II типа)
у лиц с нормальной массой тела
у лиц с ожирением
у лиц молодого возраста – MODY тип
3. Сахарный диабет, связанный с недостаточностью питания
фиброкалькулезный панкреатический диабет
панкреатический диабет, вызванный белковой
недостаточностью
4. Другие формы сахарного диабета (вторичный, или симптоматический, сахарный диабет):
а) эндокринного генеза (синдром Иценко-Кушинга, акромегалия, диффузный токсический зоб, феохромоцитома и др.)
б) заболевания поджелудочной железы (опухоль, воспаление, резекция, гемохроматоз и др.)
в) заболевания, вызванные более редкими причинами (прием различных лекарственных препаратов, врожденные генетические синдромы, наличие аномальных инсулинов, нарушения функций рецепторов к инсулину и др.)
5. Диабет беременных
А. Степень тяжести диабета
1. Легкая (I)
2. Средняя (II)
3. Тяжелая (III)
Б. Состояние компенсации
1. Компенсация
2. Субкомпенсация
3. Декомпенсация
В. Осложнения лечения
1. Инсулинотерапия – местная аллергическая реакция, анафилактический шок, липоатрофия
2. Пероральные сахароснижающие препараты – аллергические реакции, тошнота, нарушение функции желудочно-кишечного тракта и др.
Г. Острые осложнения диабета (часто как результат неадекватной терапии)
а) кетоацидотическая кома
б) гиперосмолярная кома
в) лактатацидотическая кома
г) гипогликемическая кома
Д. Поздние осложнения диабета
1. Микроангиопатия (ретинопатия, нефропатия)
2. Макроангиопатия (инфаркт миокарда, инсульт, гангрена ног)
3. Нейропатия
Ж. Поражения других органов и систем – энтеропатия, гепатопатия, катаракта, остеоартропатия, дермопатия и др.
II. Нарушенная толерантность к глюкозе – латентный или скрытый диабет
а) у лиц с нормальной массой тела
б) у лиц с ожирением
в) связанная с определенными состояниями и синдромами (см. п. 4)
III. Классы или группы статистического риска, или предиабет (лица с нормальной толерантностью к глюкозе, но с повышенным риском развития сахарного диабета):
а) лица, ранее имевшие нарушения толерантности к глюкозе
б) лица, имеющие потенциальные нарушения толерантности к глюкозе.
В клиническом течении сахарного диабета различают три стадии: 1) потенциальные и предшествовавшие нарушения толерантности к глюкозе, или предиабет, т.е. группы лиц, имеющие статистически достоверные факторы риска; 2) нарушения толерантности к глюкозе, или латентный или скрытый сахарный диабет; 3) явный или манифестный сахарный диабет, ИЗД и ИНЗД, течение которого может быть, легким, средней тяжести и тяжелым.
Инсулинзависимый диабет (ИЗД, I тип) характеризуется острым началом, инсулинопенией, склонностью к частому развитию кетоацидоза. Чаще диабет I типа встречается у детей и подростков, с чем и было связано ранее употреблявшееся название “юношеский диабет”, однако заболеть могут люди любого возраста. Жизнь больных, страдающих этим типом диабета, зависит от экзогенного введения инсулина, в отсутствие которого быстро развивается кетоацидотическая кома. Заболевание сочетается с определенными HLA-типами и в сыворотке крови часто обнаруживаются антитела к антигену островков Лангерганса. Нередко осложняется макро- и микроангиопатией (ретинопатия, нефропатия), нейропатией.
Инсулинзависимый диабет имеет генетическую основу.
Последовательность патогенетических процессов в Копенгагенской модели была представлена следующим образом: а) инициация и деструкция b-клеток зависит от высвобождения под влиянием различных веществ (вирусы, химические вещества, избыток интерлейкина-1) антигена b-клеток; б) триггирование синтеза и высвобождения из макрофагов цитокина интерлейкина -1 (Ил-1); в)стимуляция секреции лимфокинов (g-интерферон и фактор некроза опухолей) Т-хельперами под влиянием Ил-1; г) g-интерферон и фактор некроза опухолей непосредственно принимают участие в разрушении b-клеток; причем g-интерферон индуцирует экспрессию генов HLA-II класса на клетках эндотелия капилляров, а Ил-1 увеличивает проницаемость капилляров и индуцирует экспрессию генов HLA-I и II класса в островке поджелудочной железы, что и замыкает “порочный круг“ деструкции новых b-клеток.
КЛИНИЧЕСКАЯ КАРТИНАДиагностика Больные предъявляют характерные жалобы на сухость во рту, полифагию (повышенный аппетит), чрезмерную жажду (полидипсия), полиурию, похудание (при ИЗД), сонливость, общую слабость, наклонность к инфекции (фурункулез, парадонтоз); у некоторых женщин отмечается зуд кожи в области наружных гениталий, у мужчин - баланит. При обследовании выявляются гипергликемии и глюкозурия, которая служит причиной полиурии.
обменные нарушения: гиперлипемия, гиперлактацидемия, гиперкетонемия, гипергликемия
В диете больного диабетом обычно ограничивают блюда из жирных сортов мяса, рыбы и других продуктов, богатых холестерином (желтки яиц, икра, мозги, печень), особенно в жареном виде. Молоко и молочные продукты должны быть с пониженным содержанием жира.
Инсулинотерапия.
различаются по действию: препараты короткого действия; препараты средней продолжительности и препараты длительного действия. К препаратам инсулина короткого и быстрого действия (начало действия через 30 минут после введения; максимум действия между 2-3 ч после введения и продолжительность – до 6 ч) относятся: Актрапид МС и НМ (Ново-Нордиск), Илетин- II-регуляр и Хумулин-регуляр (Эли-Лилли), Инсуман-нормаль (Хехст), Берлинсулин Н-нормаль (Берлин-Хеми), инсулрап SPP (Плива) и др..
К препаратам средней продолжительности действия относятся: Протофан МС и НМ (Ново-Нордиск), Хумулин-базаль или НПХ, Лента, Иллетин-2 (Эли-Лилли), Инсуман-базаль (Хехст), Берлинсулин Н-базаль (Берлин-Хеми). Начало действия препаратов через 2 ч после введения; максимум действия через 8-10 ч и длительность действия 18-24 ч.
К препаратам длительного действия относятся: Ультратард НМ (Ново-Нордиск), Хумулин ультралента (Эли-Лилли). Начало действия препарата через 4-5 ч после введения; максимум действия через 8-14 ч и продолжительность действия 24-36 ч.
Вопрос 64:
Критерии диагностики несахарного диабета:
выраженной жажде
объеме суточной мочи больше 3 л в сутки
гиперосмоляльности плазмы (больше 290 мосм/кг, зависит от потребления жидкости)
повышенного содержания натрия
гипоосмоляльности мочи (100—200 мосм/кг)
низкой относительной плотности мочи (<1010)
Вопрос 65:
Диференциальный диагноз при инсипидарном синдроме.
ИНСИПИДАРНЫЙ СИНДРОМ характеризуется полидипсией, полиурпей и низким удельным весом мочи (ниже 1010).
Сахарный диабет 1го типа
Сахарный диабет 2 типа
Несахарный диабет
Психогенная жажда
Вопрос 66:
Дифузно-токсический зоб. Определение. Этиология. Патогенез. Классификация. Клиника. Диагностика. Лечение. Профилактика.
аутоиммунное заболевание, обусловленное избыточной секрецией тиреоидных гормонов диффузной тканью щитовидной железы, которое приводит к отравлению этими гормонами — тиреотоксикозу.
Этиология
В основе происхождения заболевания лежит нарушение иммунного контроля со стороны генетически измененных клеток крови, приводящее к образованию "своих" антител к тканям щитовидной железы.
Наследственная предрасположенность выявляется более чем у 30 % больных. К факторам, провоцирующим развитие диффузного токсического зоба, относятся психические травмы, стрессы, острые (грипп, ангина, малярия и др.) и хронические (сифилис, туберкулез, ревматизм и др.) инфекции, органические нарушения центральной нервной системы (травма, энцефалит и др.). Нередко болезнь развивается на фоне другой эндокринной патологии (заболевания половых желез, гипофиза, гипоталамуса и др.).
Патогенез
Клинически наиболее значимым синдромом, развивающимся при диффузном токсическом зобе вследствие гиперстимуляции щитовидной железы антителами к рецептору ТТГ, является тиреотоксикоз. Патогенез изменений со стороны органов и систем, развивающихся при тиреотоксикозе, заключается в значительном повышении уровня основного обмена, которое со временем приводит к дистрофическим изменениям. Самыми чувствительными к тиреотоксикозу структурами, в которых наиболее высока плотность рецепторов к тиреоидным гормонам, являются сердечно-сосудистая (особенно миокард предсердий) и нервная системы.
Классификация.
1. По степени увеличения.
I -- железа незаметна на глаз, прощупывается перешеек.
II -- хорошо прощупываются боковые доли, железа заметна при глотании.
III -- увеличение щитовидной железы заметно при осмотре ("толстая шея").
IV -- зоб ясно виден, изменена конфигурация шеи.
V -- зоб огромных размеров.
2. По степени тяжести тиреотоксикоза.
Легкая степень -- пульс не более 100 уд. в мин., потеря массы тела на 3 -- 5 кг, глазные симптомы отсутствуют или выражены незначительно, повышение поглощения [131]I через 24 часа.
Средняя степень -- усиление тахикардии до 100 -- 120 уд. в мин., потеря массы тела до 8 -- 10 кг, выраженный тремор, повышение систолического и снижение диастолического давления, повышение захвата изотопов щитовидной железой с первых часов, работоспособность частично снижена.
Тяжелая степень -- частота пульса превышает 120 -- 140 уд. в мин., похудание достигает степени кахексии, присоединяются нарушения функции печени, надпочечников, сердечно-сосудистой системы. Полная потеря трудоспособности.
Клиника
Более характерна для молодых пациентов, соотношение мужчин и женщин 1:6, железа увеличена, гладкая, сльшпш шумы. Глазные .симптомы от минимально выраженных до тяжелых: 1) спазм верхнего века с его запаздыванием при движении глазного яблока, 2) наружная офтальмоплегия, 3) экзофтальм с выдвижением глазного яблока вперед, 4) супра- и инфраорбитальная припухлость, 5) застой и отек как показатели тяжести.
Классическая мерзебургская триада (зоб, тахикардия, экзофтальм), описанная еще Карлом Базедовым, встречается примерно у 50% пациентов. Примерно в 2/3 случаев БГ развивается в возрасте после 30 лет, не менее, чем в 5 раз чаще у женщин. В отдельных популяциях (Япония, Швеция) БГ почти в половине случаев манифестирует на протяжении первого года после родов. Как указывалось, клиническая картина БГ определяется синдромом тиреотоксикоза, для которого характерны: похудение (часто на фоне повышенного аппетита), потливость, тахикардия и ощущение сердцебиения, внутреннее беспокойство, нервозность, дрожь рук (а порой, всего тела), общая и мышечная слабость, быстрая утомляемость и ряд других симптомов, подробно описанных в литературе. В отличие от многоузлового токсического зоба, который связан с функциональной автономией ЩЖ, при БГ, как правило, имеет место короткий анамнез: симптомы развиваются и прогрессируют быстро и в большинстве случаев приводят пациента к врачу в пределах 612 месяцев. У пожилых пациентов тиреотоксикоз любого генеза часто протекает олиго или моносимптомно (вечерний субфебрилитет, аритмии) или даже атипично (анорексия, неврологическая симптоматика). При пальпаторном исследовании примерно у 80% пациентов удается выявить увеличение ЩЖ, порой весьма значительное: пальпаторно железа плотноватая, безболезненная. В ряде случаев, при БГ на первое место могут выходить проявления эндокринной офтальмопатии (выраженный экзофтальм, нередко имеющий несимметричный характер, диплопия при взгляде в одну из сторон или вверх, слезотечение, ощущение "песка в глазах", отечность век). Здесь следует оговориться, что наличие у пациента выраженной эндокринной офтальмопатии (ЭОП) позволяет практически безошибочно установить пациенту этиологический диагноз уже по клинической картине, поскольку среди заболеваний, протекающих с тиреотоксикозом, ЭОП сочетается только с БГ.
Диагностика
Диагностика в типичных случаях не вызывает существенных трудностей (табл. 1). При подозрении на наличие у пациента тиреотоксикоза ему показано определение уровня ТТГ высокочувствительным методом (функциональная чувствительность не менее 0,01 мЕд/л). При обнаружении пониженного уровня ТТГ пациенту проводится определение уровня свободных Т4 и Т3: если хотя бы один из них повышен речь идет о манифестном тиреотоксикоза, если они оба в норме о субклиническом. После подтверждения наличия у пациента тиреотоксикоза проводится этиологическая диагностика, направленная на выявление конкретного заболевания, которое его обусловило. При УЗИ примерно в 80% случаев БГ обнаруживается диффузное увеличение ЩЖ; кроме того, этот метод может выявить характерную для большинства аутоиммунных заболевания гипоэхогенность ЩЖ. По данным сцинтиграфии при БГ выявляется диффузное усиление захвата изотопа железой. Как и при всех других аутоиммунных заболеваниях ЩЖ, при БГ могут определяться высокие уровни классических антител к ЩЖ (антитела к тиреоидной пероксидазе - АТ-ТПО и антитела к тиреоглобулину - АТ-ТГ). Это наблюдается не менее чем в 70-80% случаев БГ. Таким образом, обнаружение классических антител не позволяет отличить БГ от хронического аутоиммунного, послеродового и "безболевого" ("молчащего") тиреоидита, но может, в сумме с другими признаками, существенно помочь в дифференциальной диагностике БГ и функциональной автономии ЩЖ. Следует помнить о том, что классические антитела могут обнаруживаться у здоровых людей без каких-либо заболеваний ЩЖ. Большее диагностическое значение имеет определение уровня антител к рецептору ТТГ (АТ-рТТГ), которое, увы, пока не абсолютно из-за несовершенства имеющихся тестсистем. В таблице 2 представлена краткая характеристика других заболеваний, протекающих с тиреотоксикозом, с которыми необходимо дифференцировать БГ.
Диффузный зоб с экзофтальмом и повышением функции щитовидной железы. Поглощение радиоактивного йода 45-90%. Применяется Т3 подавляющий тест, снижение на 50% и меньше является диагностическим.
Лечение
Консервативное фармакологическое лечение
Основным средством консервативного лечения являются препараты мерказолил и метилтиоурацил (либо пропилтиоурацил). Суточная доза мерказолила составляет 30-40 мг, иногда при очень больших размерах зоба и тяжелом течении тиреотоксикоза она может достигать 60-80 мг. Поддерживающая суточная доза мерказолила обычно составляет 10-15 мг. Препарат принимают непрерывно в течение 1/2-2 лет. Снижение дозы мерказолила строго индивидуально, его проводят, ориентируясь на признаки устранения тиреотоксикоза: стабилизацию пульса (70-80 ударов в минуту), увеличение массы тела, исчезновение тремора и потливости, нормализацию пульсового давления. Необходимо каждые 10-14 дней проводить клинический анализ крови (при поддерживающей терапии мерказолилом — 1 раз в месяц). В дополнение к антитиреоидным средствам применяются b-адреноблокаторы, глюкокортикоиды, седативные средства, препараты калия.
Радиойодтерапия
Радиойодтерапия (РЙТ) — это один из современных методов лечения диффузного токсического зоба и других заболеваний щитовидной железы. В ходе лечения радиоактивный йод (изотоп I-131) вводится в организм в виде желатиновых капсул перорально (в редких случаях используется жидкий раствор I-131). Радиоактивный йод, накапливающийся в клетках щитовидной железы, подвергает бета- и гамма- излучению всю железу. При этом уничтожаются клетки железы и опухолевые клетки, распространившиеся за её пределы. Проведение радиойодтерапии подразумевает обязательную госпитализацию в специализированное отделение.
Хирургическое лечение
Абсолютными показаниями для оперативного лечения служат аллергические реакции или стойкое снижение лейкоцитов, отмечаемые при консервативном лечении, большие размеры зоба (увеличение щитовидной железы выше III степени), нарушения ритма сердечных сокращений по типу мерцательной аритмии с симптомами сердечно-сосудистой недостаточности, выраженный зобогенный эффект мерказолила.
Операция проводится только при достижении состояния медикаментозной компенсации, так как в противном случае в раннем послеоперационном периоде может развиться тиреотоксический криз.
Особенности лечения у беременных
Особого внимания заслуживает проблема лечения у беременных из-за возможного влияния антитиреоидных антител на плод в результате их трансплацентарного переноса и аналогичного влияния лекарств. Все это заставляет рекомендовать женщинам предохранение от беременности. Если беременность наступила, то предпочтение отдается препарату пропилтиоурацилу.
Профилактика
Профилактика диффузного токсического зоба включает в себя прежде всего сохранение психического спокойствия, поскольку стрессы – один из самых главных пусковых механизмов возникновения этой болезни. Рекомендуется принимать легкие успокаивающие препараты, особенно на основе трав, пить травяные чаи и принимать ванны с травяными экстрактами. Полезна при стрессах и ароматерапия.
Для защиты организма от инфекций рекомендуется укреплять иммунитет, принимая витамины, особенно относящиеся к группе В, и проводя общеукрепляющие процедуры – теплый душ, обливания теплой водой, прогулки.
Поскольку это заболевание связано с наследственной предрасположенностью, то тем, у кого есть или были страдающие им родственники, необходимо обращаться к врачу даже тогда, когда признаки базедовой болезни еще совсем не явные, – лучше перестраховаться, чем пропустить начальную стадию.
Вопрос 67
Гипотиреоз. . Определение. Этиология. Патогенез. Клиника. Диагностика. Лечение. Профилактика.
Определение
состояние, обусловленное длительным, стойким недостатком гормонов щитовидной железы. Крайняя степень проявления клинической симптоматики гипотиреоза у взрослых — микседема, у детей — кретинизм.
Этиология
Первичный гипотиреоз возникает при непосредственном повреждении щитовидной железы (врожденные аномалии, повреждения: воспалительные — при хронических инфекциях, аутоиммунной природы, после введения радиоактивного йода, операции на щитовидной железе, недостаток йода в окружающей среде).
Вторичный гипотиреоз может быть следствием инфекционных, опухолевых или травматических поражений гипоталамо-гипофизарной системы. Отмечены случаи возникновения функциональной формы первичного гипотиреоза вследствие передозировки мерказолила, действия солей лития и так далее.
Патогенез
Различен, в зависимости от характера поражения:
первичный гипотиреоз — связан с патологией щитовидной железы, ведущей к невозможности вырабатывать достаточное количество тироксина и трийодтиронина — аплазия или агенезия щитовидной железы, аутоиммунный процесс, йоддефицит;
вторичный гипотиреоз — «центральный», связан с выпадением тропной функции гипофиза (снижение продукции тиреотропина), чаще является следствием пангипопитуитаризма.
Клинические проявления
Жалобы часто скудны и неспецифичны, тяжесть состояния больных обычно не соответствует их жалобам: вялость, медлительность, снижение работоспособности и быстрая утомляемость, сонливость, снижение памяти, многие часто жалуются на сухость кожи, одутловатость лица и отечность конечностей, грубый голос, ломкость ногтей, выпадение волос, увеличение массы тела, ощущение зябкости, отмечают парестезии, запоры и др. Выраженность симптомов гипотиреоза во многом зависит от причины заболевания, степени тиреоидной недостаточности и индивидуальных особенностей пациента.
Характерные для гипотиреоза синдромы
Обменно-гипотермический синдром: ожирение, понижение температуры, зябкость, непереносимость холода, гиперкаротинемия, вызывающая желтушность кожных покровов.
Микседематозный отек: периорбитальный отек, одутловатое лицо, большие губы и язык с отпечатками зубов по латеральным краям, отечные конечности, затруднение носового дыхания (связано с набуханием слизистой оболочки носа), нарушение слуха (отек слуховой трубы и органов среднего уха), охрипший голос (отек и утолщение голосовых связок), полисерозит.
Синдром поражения нервной системы: сонливость, заторможенность, снижение памяти, брадифрения, боли в мышцах, парестезии, снижение сухожильных рефлексов, полинейропатия.
Синдром поражения сердечно-сосудистой системы: микседематозное сердце (брадикардия, низкий вольтаж, отрицательный зубец Т при ЭКГ, недостаточность кровообращения), гипотония, полисерозит, возможны нетипичные варианты (с гипертонией, без брадикардии, с постоянной тахикардией при недостаточности кровообращения и с пароксизмальной тахикардией по типу симпатико-адреналовых кризов в дебюте гипотиреоза).
Синдром поражения пищеварительной системы: гепатомегалия, дискинезия желчевыводящих протоков, дискинезия толстой кишки, склонность к запорам, снижение аппетита, атрофия слизистой оболочки желудка, тошнота, иногда рвота.
Анемический синдром: анемия — нормохромная нормоцитарная, гипохромная железодефицитная, макроцитарная, В12-дефицитная.
Синдром гиперпролактинемического гипогонадизма: дисфункция яичников (меноррагия, олигоменорея или аменорея, бесплодие), галакторея.
Синдром эктодермальных нарушений: изменения со стороны волос, ногтей, кожи. Волосы тусклые, ломкие, выпадают на голове, бровях, конечностях, медленно растут. Сухость кожи. Ногти тонкие, с продольной или поперечной исчерченностью, расслаиваются.
Гипотиреоидная (микседематозная) кома.
Диагностика
Дифференциальная диагностика строится на основании клинических исследований пациента, в частности, уровней тиреоидных гормонов в течение некоторого времени. Определяют тироксин (Т4-норма для детей старше 2 мес 50-140 нмоль/л)и трийодтиронин (T3- 1,50-3,85 ммоль/л). При гипотиреозе их уровень снижается пропорционально тяжести заболевания, уровень ТТГ резко повышен. Определённые изменения уровней тиреоидных гормонов возможны под действием неблагоприятных экологических условий, под влиянием факторов профессиональной деятельности (химические вещества, радиация).
Лечение
Лечение основывается на дифференциальной диагностике. В комплексном лечении используется заместительная терапия препаратами щитовидной железы КРС или, что чаще, синтетическими тиреоидными гормонами (тиреоидин, трийодтиронин, тироксин, тиреотом, тиреотом-форте, тиреокомб). Доза определяется индивидуально в каждом конкретном случае.
Основными методами лечения первичного, вторичного и третичного гипотиреоза является заместительная терапия тиреоидными гормонами и содержащими их препаратами.
Применяются следующие тиреоидные препараты.
Тиреоидин (высушенная щитовидная железа животных) – выпускается в таблетках по 0.05 и 0.1 г. Содержание йода в тиреоидине составляет от 0.1 до 0.23%. Содержание Т3 и Т4 в тиреоидине зависит от того, из щитовидной железы какого животного он получен. Ориентировочно0.1 г тиреоидина содержит 8-10 мкг Т3 и 30-40 мкг Т4.
L-тироксин (эутирокс) –натриевая соль левовращающего тироксина, выпускается в таблетках по 50 и 100 мкг. Действие L-тироксин после приема внутрь проявляется через 24-48 часов, период полувыведения составляет 6-7 дней.
Трийодтиронин – выпускается в таблетках по 20 и 50 мкг. Действие трийодтиронина начинается спустя 4-8 ч после приема внутрь, максимум действия приходится на 2-3-й день, полное выведение препарата из организма наступаетчерез 10 дней.
Тиреотом - 1 таблетка препарата содержит 40 мкг Т4 и 10 мкг Т3.
Тиреотом –форте - 1 таблетка препарата содержит 120 мкг Т4 и 30 мкг Т3.
Тиреокомб - 1 таблетка препарата содержит 70 мкг Т4, 10 мкг Т3 и 150 мкг калия йодида.
Профилактика
Для профилактики гипотиреоза очень важно употреблять продукты, богатые йодом
Вопрос 68:
Критерии диагностики гипотиреоза.
Наличие основных симптомов гипотиреоза:
1медлительность, зябкость, сонливость, снижение памяти
2- сухость и оттечность кожи
3-брадикардия
4-запоры
Снижение уровня тироксина и трииодтиронина при:
1-при повышенном содержании тиротропина у больных первичным гипотиреозом
2-низком уровне тиротропина у больных вторичным ( гипофизарном) и третичным ( гипоталамическом) гипотиреозе.
Вопрос 69:
Феохромоцитома. Определение. Этиология. Патогенез. Клиника. Диагностика. Лечение. Профилактика.
Фе́охро́моцито́ма — гормонально активная опухоль хромаффинных клеток симпато-адреналовой системы надпочечниковой или вненадпочечниковой локализации, секретирующая большое количество катехоламинов. Заболевание относится к опухолям (доброкачественным или злокачественным) АПУД-системы и довольно часто является одной из составляющих синдрома множественной эндокринной неоплазии (как правило, в этом случае феохромоцитома бывает двусторонней)
Этиология.
В 80 % случаев феохромоцитомы возникают спорадически, в 10–20 % случаев носят семейный характер. При этом феохромоцитомы могут быть проявлением нескольких наследственных заболеваний, передающихся по аутосомно-доминантному типу.
Патогенез:
В клетках феохромоцитомы происходит синтез и накопление катехоламинов, как и в нормальных клетках мозгового вещества надпочечников. Выброс катехоламинов может провоцироваться изменениями кровотока, некрозом в ткани опухоли и другими причинами. Кроме того, феохромоцитомы накапливают и секретируют большое число пептидов, в том числе эндогенные опиоиды, адреномедуллин, эндотелин, эритропоэтин, нейропептид Y (вазоконстриктор) и др.
Основные патофизиологические изменения, происходящие в организме при феохромоцитоме, связаны с высокой концентрацией катехоламинов в крови.
Клиника.
Главным симптомом феохромоцитомы служит повышение АД (пароксизмальное или постоянное).
К дополнительным симптомам относятся:
— ортостатическая гипотония;
— потливость;
— постоянные головные боли;
— ощущение внутренней дрожи, беспокойство;
— общая слабость, снижение трудоспособности.
Характерны кризы с резким повышением АД в сочетании с нервно-психическими, эндокринно-обменными, желудочно-кишечными и гематологическими симптомами (пароксизмальная форма заболевания). Во время приступа клиника напоминает симптоматику симпатико-адреналового криза: появляются чувство страха, беспокойство, дрожь, озноб, бледность кожных покровов, головная боль, боль за грудиной, в области сердца, тахикардия, экстрасистолия, тошнота, рвота, повышение температуры тела, потливость, сухость во рту. В крови — лейкоцитоз, лимфоцитоз, эозинофилия, гипергликемия. Приступ завершается полиурией. Продолжительность криза от нескольких минут до нескольких часов. Криз может осложниться кровоизлиянием в сетчатку глаза, нарушением мозгового кровообращения, отеком легких. Приступы возникают, как правило, внезапно и могут провоцироваться эмоциональным стрессом, физическим напряжением, пальпацией опухоли, резким изменением положения тела. При стабильной форме заболевания отмечается постоянно высокая артериальная гипертензия, возможны нарушения функционального состояния почек, изменения глазного дна. Наблюдаются повышенная возбудимость, лабильность настроения, утомляемость, головная боль. При злокачественной опухоли — феохромобластоме — нередки похудание, боли в животе. Возможно развитие сахарного диабета.
Диагностика.
В диагностических целях проводят ультразвуковое исследование надпочечников, компьютерную томографию, ретропневмоперитонеум (топическая диагностика), определяют экскрецию с мочой (в течение суток или в трехчасовой порции мочи, собранной после приступа) катехоламинов и их метаболитов: адреналина, норадреналина, ванилилминдальной кислоты, проводят фармакологические пробы с гистамином или тропафеном. Определение свободных катехоламинов в плазме.
Лечение.
Для купирования криза применяют тропафен. Оперативное лечение и лучевая терапия
Профилактика.
Диагностика и преждевременное обследование органов брюшной полости.
Вопрос 70:
Эндокринная артериальная гипертензия. Определение. Этиология. Патогенез. Клиника. Диагностика. Лечение.
Определение.
Эндокринная артериальная гипертензия- это гипертензия в основе которой лежит избыточная продукция и секреция гормонов, оказывающих прямое или косвенное прессорное влияние.
Этиология. Патогенез.

Клиника.
Обычно, симптомы болезни проявляются во время гипертонических кризов (головная боль, головокружения и другие неврологические расстройства, боли в груди, одышка, чувство страха). Более выраженная клиническая картина наблюдается при установлении поражений в органах мишенях:
• Поражение сердца: признаки ишемической болезни сердца и прогрессирующей сердечной недостаточности;
• Поражение мозга: прогрессирующие неврологические расстройства, гипертоническая энцефалопатия, нарушения зрения;
• Поражение почек: признаки почечной недостаточности;
• Поражение периферических сосудов: перемежающаяся хромота.
Диагностика.
Для диагностики эндокринной артериальной гипертензии, а также для определения поражений внутренних органов проводят дополнительно обследование: общий анализ крови, общий анализ мочи, специфические анализы крови и мочи, УЗИ сердца и внутренних органов, ЭКГ, различные пробы и пр.
Лечение.
Лечение начинается с поврежденного органа, который привел к гипертензии + диуретики.
Вопрос 71:
Диф. диагноз по синдрому артериальной гипертензии ( первчный гиперальдостеронизм, феохромоцитома, коартация аорты, стеноз почечной артерии)
Атеросклеротическое поражение почечных артерий — наиболее частая причина реноваскулярных артериальных гипертензий (около 70%). Обычно развивается у мужчин старше 50 лет. Диагноз устанавливается на основании выявления продолжительного систолического или систолодиа-столического шума над проекцией почечных артерий (в эпигастрии на 2—3 см выше пупка, а также на этом же уровне справа и слева от средней линии живота). Шум выявляется примерно у 50—60% больных. Верифицируется диагноз объективными методами исследования: изотопной ренографией, экскреторной урографией, компьютерной томографией, брюшной аортографией, катетеризацией почечных вен (повышение содержания ренина в венозной крови пораженной почки). Данные аортографии имеют решающее значение не только в окончательной постановке диагноза, но и в выборе метода лечения (баллонная ангиопластика, хирургическая коррекция стеноза).
Феохромоцитома — опухоль, как правило, доброкачественная, состоящая из хромаффинных клеток и продуцирующая катехоламины. В период кризовых состояний при феохромоцитоме артериальное давление повышается внезапно и в течение нескольких секунд достигает очень высокого уровня (250—300/150—130 мм рт. ст.). Появляются резко выраженная тахикардия, бледность лица, холодный пот, нарушается зрение. Возникает сильная жажда, позывы к мочеиспусканию. В крови — лейкоцитоз и гипергликемйя. Кризы могут провоцироваться холодовой пробой, глубокой пальпацией живота, приведением нижних конечностей к животу, приемом допегита, резерпина, клофелина. Последний может использоваться для проведения дифференциальной диагностики. При приеме 0,3 мг клофелина у лиц без феохромоцитомы уровень катехоламинов в крови (через 2—3 ч) и моче (при приеме препарата в 21ч моча собирается в интервале от 21 до 7 ч) резко снижается. У больных с опухолью содержание катехоламинов в крови и моче не изменяется. Предположение о наличии феохромоцитомы подтверждается определением повышенной экскреции катехоламинов и их метаболитов в суточной моче: адреналина — более 50 мкг, норадрсналина — более 100—150 мкг, ванилилминдальной кислоты — более 6 мкг, в том числе в течение 3 ч после очередного криза.
Верифицируется диагноз с помощью компьютерной томографии, ультразвукового исследования. В последние годы все более широкое применение находит сцинтиграфия с 1-131 — аналогом гуанитидина, который избирательно захватывается опухолью.
Первичный алъдостеронизм (синдром Конна) проявляется клинически стабильной артериальной гипертензией, чаще диастолического типа вследствие увеличения синтеза альдостерона в клубочковом слое коры надпочечников. Заболевание чаще встречается у женщин.
В диагностике первичного альдостеронизма и его дифференциальной диагностике следует учитывать уровень калия (гипокалиемия) и натрия в сыворотке крови, состояние кислотно-основного равновесия, суточный диурез, который может составлять от 2 до 7 л в сутки, плотность мочи, обычно значительно сниженную, никтурию, изостенурию, щелочную реакцию мочи. Сниженная или нулевая активность ренина плазмы и увеличение экскреции с мочой альдостерона являются характерными признаками первичного альдостеронизма. Гипокалиемия может подтверждаться пробой с гипотиазидом. Из фармакологических проб для подтверждения диагноза может еще использоваться прием антагонистов альдостерона (верошпирон по 100 мг/сут в течение 4—5 недель), в результате приводящий к снижению диастолического АД не менее чем на 20 мм рт. ст. Диагностический поиск завершается применением компьютерной томографии.
Коарктация аорты — один из врожденных пороков сердца. Сужение аорты чаще всего бывает в месте перехода ее в нисходящий отдел, реже оно находится между устьем левой сонной и левой подключичной артерий. Если порок в детстве не диагностирован и не проведена его хирургическая коррекция, то к 20—30-летнему возрасту у больных развивается стойкая, высокая гипертензия с повышением как систолического, так и диастолического давления. Есть ряд симптомов, которые позволяют заподозрить коарктацию аорты и своевременно ее диагностировать. Хорошо физически развита верхняя половина туловища, полнокровны лицо и шея, в то же время отмечаются гипотрофия и бледность нижних конечностей. Четко различается величина пульса на руках и ногах, значительно ослаблен пульс на бедренных и подколенных артериях, не определяется пульс на тыльных артериях стоп. Иногда имеется различие пульса на обеих руках — на правой он I больше, на левой — меньше. При выявлении такого рода симптомов необходимо измерить давление на руках и ногах. В норме систолическое давление на ногах выше, чем на руках, на 15—20 мм рт. ст., при коарктации аорты все наоборот: на руках АД выше, чем на ногах. При аускультации сердца и сосудов определяется шум изгнания, который лучше всего выслушивается во II—III межреберьях слева от грудины, нередко также и в межлопаточном пространстве. Рентгенологически отмечаются выраженная пульсация аорты выше места сужения, постстенотическое расширение аорты, аортальная конфигурация сердца, узурация нижних краев IV—VIII ребер. Решающим методом является аортография, которая позволяет уточнить место коарктации и ее протяженность.
Атеросклеротическая гипертония. Диагностика этой формы симтоматической гипертензии несложна, однако очень часто в этом случае ошибочно ставится диагноз гипертонической болезни. Главной отличительной чертой атеросклеротической гипертонии является ее систолический характер — систолическое давление повышается до 160—170 мм рт. ст., диастолическое — нормальное или снижено, а пульсовое давление высокое.
Вопрос 72:
Железодефицитная анемия. Определение. Этиология. Патогенез. Классификация. Клиника. Диагностика. Лечение. Профилактика.
Железодефицитная анемия — это анемия, обусловленная дефицитом железа в сыворотке крови, костном мозге и депо.
Этиология
Хронические кровопотери
маточные – гиперполименорея, эндометриоз, из ЖКТ- язва, полипоз, опухоль, дивертикулы,
почечные - гломерулонефрит с выраженной гематурией, опухоль
геморрагические диатезы (наследственная геморрагическая телеангиэктазия — болезнь Рандю-Ослера, тромбоцитопатия, тромбоцитопеническая пурпура, гемофилия,
Кровопотери при заболеваниях легких — часто повторяющиеся кровохарканья и легочные кровотечения при туберкулезе легких, бронхоэктазах, раке легкого, Синдром Гудпасчера характеризуется продукцией аутоантител к базальным мембранам клубочковых капилляров почек и альвеол легких и развитием клиники гломерулонефрита в сочетании с легочным кровотечением (кровохарканьем)
Ятрогенные кровопотери — это кровопотери, обусловленные врачебный манипуляциями, пример частые кровопускания у больных полицитемией
Истерические кровопотери (синдром Ластени де Фержоля) — искусственно вызываемые кровотечения улиц с психопатическими отклонениями.
Повышенная потребность в железе
Беременность, роды, лактация
Период полового созревания и роста. Развитие железодефицитной анемии обусловлено повышением потребности в железе в связи с интенсивным ростом органов и тканей, усиленным ростом тела в длину, началом менструаций.
повышенная потребность в железе на фоне лечения витамином В12, что объясняется интенсификацией нормобластического кроветворения и использованием для этих целей больших количеств железа.
Интенсивные занятия_спортом анемия обусловлена повышением потребности в железе при больших физических нагрузках, увеличением мышечной массы (использованием большего количества железа для синтеза миоглобина)
Недостаточность поступления с пищей
Нутритивная (алиментарная) железодефицитная анемия, у вегетарианцев, у людей с низким социально – экономическим статусом
частое употребление крепкого чая, который снижает всасывание железа в тонком кишечнике.)
Нарушение всасывания
хронические энтериты и энтеропатии с развитием синдрома мальабсорбции;
резекция тонкой кишки;
резекция желудка по методу Бильрот II (конец в бок), когда
происходит выключение части 12-перстной кишки.
Нарушение транспорта
обусловлено снижением содержания в крови трансферина при:
врожденной гипо- и атрансферинемии
гипопротеинемиях различного генеза (нефротический синдром;
нарушение белковообразовательной функции печени при циррозах печени, тяжело протекающих хронических гепатитах; синдром мальабсорбции; алиментарная недостаточность);
появлении антител к трансферину и его рецепторам.
Патогененез
• Наиболее важными патогенетическими факторами развития ЖДА являются:
• Нарушение синтеза Hb.
• Генерализованный дефект в клеточной пролиферации.
• Уменьшение продолжительности жизни эритроцитов.
• Вследствие недостаточного взаимодействия железа в синтезе гема снижается синтез Hb и возникает дефектность эритропоэза.
• Наблюдается снижение активности железосвязывающего протеина цитохрома и сукцинат дегидрогеназы.
• При падении насыщения трансферрина ниже 16 %, нарушается снабжение железом КМ.
• Повышается СЭП, что отражает избыток протопорфирина над гемовым железом. Каждая клетка содержит меньшее количество Hb, в результате чего образуются микроциты и развивается гипохромия эритроцитов.
• Может развиваться неврологическая симптоматика с возникновением парестезий, нарушением интеллектуальной деятельности и поведения у детей.
• Секреция в желудке соляной кислоты снижается, и часто — необратимо.
• Развиваются трофические нарушения органов и тканей.
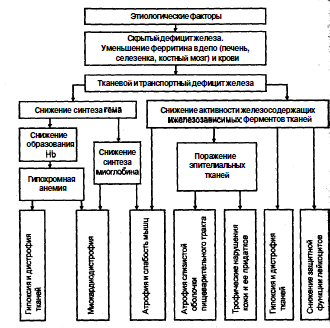
Классификация

КЛИНИЧЕСКАЯ КАРТИНА
• У больных наблюдаются характерные для анемии симптомы, но существует слабая корреляция между уровнем Hb и тяжестью симптоматики. У некоторых больных с тяжелым дефицитом железа могут отсутствовать такие проявления анемического синдрома, как слабость, бледность или утомляемость.
• У детей могут наблюдаться ослабление внимания, ответа на сенсорные раздражители, отсталость развития, нарушение поведения, задержка роста.
• Появляются парастезий и чувство жжения языка, возможно, вследствие тканевого дефицита железа.
• Развиваются сидеропенические симптомы, свойственные только ЖДА: извращение вкуса (пика хлоротика), пристрастие к необычным продуктам, таким как земля, глина (геофагия); накрахмаленному белью (амилофагия); льду (пагофагия); извращение обоняния (пристрастие к запаху бензина, ацетона, типографской краски).
• Нарушение иммунитета проявляется снижением резистентности организма к инфекции. Осмотр больного выявляет:
• бледность
• сглаженный красный язык; в более тяжелых случаях на языке обнаруживают участки покраснения неправильной формы («географический язык»)
• ангулярный хейлит ("заеды")
• койлонихии (редко)
• кровоизлияния из сосудов сетчатки (при тяжелой анемии)
• Характерно наличие затруднения при проглатывании сухой и плотной пищи, иногда — чувство першения и ощущение инородного тела в глотке (синдром Пламмера-Винсона).
Диагностика
Диагностика основана на клинических (наличие анемического и сидеропенического синдромов) и лабораторных методах исследования:
Эритроциты
• Количество эритроцитов, уровень Hb и величина Ht пропорционально снижены., анизоцитоз эритроцитов.
• Умеренный гипохромный овалоцитоз, наличие в мазках крови мишеневидных клеток.
• Прогрессирующая гипохромия (низкий ц. п., МСН) и микроцитоз (низкий MCV), показатель МСНС изменяется вариабельно.
• Количество ретикулоцитов в норме или слегка снижено.
Лейкоциты
• Количество лейкоцитов обычно в норме, но у небольшого количества больных наблюдается лейкопения (3,0-4,0•109/л) за счет снижения уровня гранулоцитов.
Тромбоциты
• Тромбоцитопения развивается у 30 % детей, но может появляться и у взрослых.
• Тромбоцитоз находят у 35 % детей, у 50-75 % взрослых вследствие хронической потери крови и усиления кроветворения КМ.
Концентрация железа сыворотки
• Обычно низкая, но может быть и нормальной (12,5-30,4 мкмоль/л). Необходимо помнить, что концентрация железа может быть сниженной при наличии сопутствующего хронического или острого воспаления, малигнизации, острого инфаркта миокарда, даже при отсутствии дефицита железа.
Общая железосвязывающая способность
• Норма 30,6-84,6 мкмоль/л.
• При дефиците железа обычно повышена.
Сывороточный ферритин
• Норма 10-250 нг/л.
• При уровне от 10 до 20 нг/л можно предполагать наличие ЖДА.
• Для ЖДА характерен уровень менее 10 нг/л.
Свободный эритроцитарный протопорфирин
• Норма 2,7-9,0 мкмоль/л.
• Концентрация обычно повышена при дефиците железа.
• Очень специфичен для диагностики дефицита железа и пригоден для широкого скрининга у детей при установлении дефицита железа и отравлении свинцом.
Принципы лечения
• При выявлении причины развития ЖДА лечение должно быть направлено на её устранение (оперативное лечение, коррекция алиментарной недостаточности и др.).
• В большинстве случаев радикальное устранение причины ЖДА не представляется возможным (меноррагии, беременность, усиленный рост). В таких случаях основное значение приобретает терапия железосодержащими препаратами.
• В большинстве случаев для коррекции дефицита железа следует назначать железосодержащие препараты для внутреннего употребления.
Ожидать:
• появление пика ретикулоцитов через 1-2 недели; хотя ответ ретикулоцитов может быть минимальным
• значительное повышение концентрации Hb на 3-4 неделе
• 50 % часть коррекции дефицита железа на 4-5 неделе лечения
• нормализации уровня Hb через 2-4 месяца от начала лечения.
ОСНОВНЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯ ПРЕПАРАТАМИ ЖЕЛЕЗА
• Пищевое железо не корригирует дефицит железа.
• Предпочтительно назначение препаратов железа с достаточным (30-100 мг) содержанием двухвалентного железа
•Предпочтительно назначение препаратов железа с достаточным (30-100 мг) содержанием двухвалентного железа: Актиферрин Гемоферпролонгатум Ировит Иррадан Сорбифер-Дурулес Тардиферон Ферроплекс
• Назначение препаратов железа, содержащих вещества, усиливающие всасывание железа.
• Нецелесообразность одновременного назначения витаминов группы В и фолиевой кислоты.
• Избегать одновременного приема пищевых веществ (с большим содержанием фосфорной кислоты, солей кальция, фитина, танина) и лекарственных препаратов (тетрациклины, альмагель, соли магния), которые уменьшают всасывание железа.
• Препараты железа не рекомендуется назначать с едой, антацидами или ингибиторами образования соляной кислоты.
• Достаточная продолжительность курса терапии: лечение необходимо продолжать в течение 12 месяцев после нормализации содержания Hb для пополнения запасов железа.
• Необходимость проведения поддерживающей терапии препаратами железа после нормализации показателя Hb.
ПАРЕНТЕРАЛЬНАЯ ТЕРАПИЯ
• Обычно используется редко, только у 10-20 % больных.
• Показаниями для парентерального лечения препаратами железа являются:
• Нарушение всасывания при патологии кишечника (энтериты, синдром недостаточности всасывания, резекция тонкого кишечника).
• Необходимость снижения дозы препарата для внутреннего приема.
• Обострение язвенной болезни желудка или двенадцатиперстной кишки.
• Непереносимость препаратов железа для приема внутрь.
• Необходимость более быстрого насыщения организма железом (больные ЖДА, которым предстоят оперативные вмешательства).
• Для определения ориентировочной дозы парентерального железа используется формула:
(150-Нв больного (г/л)) х вес тела (кг) х 3.
Профилактика
- Периодическое наблюдение за картиной крови; - употребление пищи с высоким содержанием железа (мясо, печень и др.); - профилактический прием препаратов железа в группах риска. - ликвидация этиологических факторов анемии
Особенности у пожилых
АН у стариков не связана с возрастными изменениями кроветворной ткани [3], а является в большинстве случаев проявлением различных заболеваний, одни из которых чаще встречаются в позднем возрасте (опухоли, дивертикулез кишечника), а другие не имеют строгой возрастной привязанности, но характеризуются рядом особенностей в позднем возрасте (инфекционно-воспалительные процессы, эрозивно-язвенные поражения желудочно-кишечного тракта). Характер и выраженность клинической симптоматики при АН определяются, с одной стороны, неспецифическими проявлениями самого анемического состояния (одышка, головокружение и др.), а с другой – симптоматикой заболевания, лежащего в основе АН.
АН в позднем возрасте характеризуются целым рядом особенностей, которые имеют важное значение для своевременной диагностики и адекватного лечения:
• у пожилых и стариков это заболевание имеет те же патогенетические механизмы развития, что и в других возрастных группах;
• часто возникает в результате многих патогенетических и этиологических факторов (сочетанный дефицит железа, витамина B12, фолиевой кислоты и др.), что следует учитывать при диагностическом поиске и ведении больных;
• неспецифические проявления АН у стариков могут маскироваться симптоматикой основного заболевания, часто встречающегося в позднем возрасте (одышка при сердечной и дыхательной недостаточности, головокружения у больных с сосудистой патологией головного мозга и т.д.);
• развитие АН усугубляет симптоматику часто встречающихся в позднем возрасте заболеваний сердечно-сосудистой (стенокардия, сердечная недостаточность) и центральной нервной систем (дисциркуляторная энцефалопатия);
• заболевание у стариков чаще, чем у молодых, является одним из проявлений хронических воспалительных процессов (инфекционных и неинфекционных), злокачественных опухолей, алиментарного дефицита;
• АН может нарушать качество жизни пожилых и стариков в значительно большей степени, чем у лиц более молодого возраста, не отягощенных множественной сопутствующей патологией;
• терапия АН у стариков требует комплексного подхода с использованием методов лечения основного заболевания, патогенетической (заместительной) и симптоматической терапии
Профилактика.
Периодическое наблюдение за картиной крови;
- употребление пищи с высоким содержанием железа (мясо, печень и др.);
- профилактический прием препаратов железа в группах риска.
- оперативная ликвидация источников кровопотерь.
73.Картина периферической крови при железодефицитной анемии. Железодефицитная анемия — это анемия, обусловленная дефицитом железа в сыворотке крови, костном мозге и депо.
Диагностика основана на клинических (наличие анемического и сидеропенического синдромов) и лабораторных методах исследования:
Эритроциты
• Количество эритроцитов, уровень Hb и величина Ht пропорционально снижены., анизоцитоз эритроцитов.
• Умеренный гипохромный овалоцитоз, наличие в мазках крови мишеневидных клеток.
• Прогрессирующая гипохромия (низкий ц. п., МСН) и микроцитоз (низкий MCV), показатель МСНС изменяется вариабельно.
• Количество ретикулоцитов в норме или слегка снижено.
Лейкоциты
• Количество лейкоцитов обычно в норме, но у небольшого количества больных наблюдается лейкопения (3,0-4,0•109/л) за счет снижения уровня гранулоцитов.
Тромбоциты
• Тромбоцитопения развивается у 30 % детей, но может появляться и у взрослых.
• Тромбоцитоз находят у 35 % детей, у 50-75 % взрослых вследствие хронической потери крови и усиления кроветворения КМ.
Концентрация железа сыворотки
• Обычно низкая, но может быть и нормальной (12,5-30,4 мкмоль/л). Необходимо помнить, что концентрация железа может быть сниженной при наличии сопутствующего хронического или острого воспаления, малигнизации, острого инфаркта миокарда, даже при отсутствии дефицита железа.
Общая железосвязывающая способность
• Норма 30,6-84,6 мкмоль/л.
• При дефиците железа обычно повышена.
Сывороточный ферритин
• Норма 10-250 нг/л.
• При уровне от 10 до 20 нг/л можно предполагать наличие ЖДА.
• Для ЖДА характерен уровень менее 10 нг/л.
Свободный эритроцитарный протопорфирин
• Норма 2,7-9,0 мкмоль/л.
• Концентрация обычно повышена при дефиците железа.
• Очень специфичен для диагностики дефицита железа и пригоден для широкого скрининга у детей при установлении дефицита железа и отравлении свинцом.
74. В12 дефицитная анемия. Этиология, патогенез, клиника, диагностика, лечение.
B12-дефицитная анемия или мегалобластная анемия или болезнь Аддисона-Бирмера ( малокро́вие) - заболевание, обусловленное нарушением кроветворения из-за недостатка в организме витамина B12. Особенно чувствительны к дефициту этого витамина костный мозг и ткани нервной системы
Эпидемиология: развитие заболевания характерно преимущественно для возраста 60-70 лет. По данным Herbert (1985), в возрасте 30-40 лет заболевание встречается с частотой 1 случай на 5000 человек, в возрасте 60-70 лет — 1 на 200 человек. По данным Carmell (1996), среди населения стран Северной Европы частота В12-дефицитной анемии составляет 0.1 %, а среди лиц пожилого возраста — 1 %.
Этиология
Основные причины развития Вп-дефицитной анемии:
I. Нарушение секреции желудком «внутреннего фактора» — гастромукопротеина.
1. Атрофический аутоиммунный гастрит с продукцией антител к париетальным клеткам и гастромукопротеину.
2. Тотальная гастрэктомия (реже — субтотальная резекция желудка).
3. Врожденное нарушение секреции гастромукопротеина.
4. Рак желудка.
5. Полипоз желудка.
6. Токсическое действие высоких доз алкоголя на слизистую оболочку желудка.
II. Нарушение всасывания витамина В12 в тонком кишечнике:
1. Резекция участка подвздошной кишки (более 60 см).
2. Синдром мальабсорбции различного генеза (ферментные энтеропатии, целиакия, тропическое спру, энтериты, болезнь Крона, амиоидоз кишечника).
3. Рак тонкого кишечника, лимфома тонкой кишки.
4. Хронический панкреатит с нарушением секреции трипсина.
5. Врожденное отсутствие рецепторов к комплексу «витамин В12+гастромукопротеин» в подвздошной кишке (болезнь Иммерслунд-Грзсбека).
6. Нарушение всасывания витамина В12, вызванное лекарственными средствами (колхицин, неомицин, бигуаниды, циметидин, ПАСК и др.).
III.Конкурентное расходование витамина В12:
1. Инвазия широким лентецом.
2. Инвазия власоглавом, паразитирующим в нижних отделах подвздошной кишки и в слепой кишке.
3. Множественные дивертикулы тонкого кишечника с дивертикулитом.
4. Операции на тонкой кишке с образованием «слепых петель».
IV. Повышенный расход витамина В12:
1. Многоплодная беременность.
2. Хроническая гемолитическая анемия.
3. Множественная миелома и другие новообразования.
4. Миелопролиферативные заболевания.
5. Тиреотоксикоз.
V. Нарушение поступления витамина В12 с пищей. Строгое вегетарианство.
VI. Снижение запасов витамина В12. Выраженный цирроз печени.
VII. Нарушение транспорта витамина В12. Отсутствие транскобаламина II или появление антител к нему.
Патогенез B12-дефицитной анемии:
Роль цианкобаламина и фолиевой кислоты в развитии мегалобластной анемии связана с их участием в широком спектре обменных процессов и обменных реакций в организме. Фолиевая кислота в форме 5,10 - метилентетрагидрофолата участвует в метилировании дезоксиуридина, необходимого для синтеза тимидина, при этом образуется 5-метилтетрагидрофолат. Цианокобаламин является кофактором метилтрасферазной каталитической реакции, осуществляющей ресинтез метионина и одновременно регенерацию 5-метилтетрагидрофолата в тетрагидрофолат и 5,10 метилентетрагидрофолат. При недостаточности фолатов и (или) цианкобаламина нарушается процесс включения уридина в ДНК развивающихся гемопоэтичеких клеток и образования тимидина, что обуславливает фрагментацию ДНК (блокирование ее синтеза и нарушение клеточного деления). При этом возникает мегалобластоз, происходит накопление больших форм лейкоцитов и тромбоцитов, их раннее внутрикостномозговое разрушение и укорочение жизни циркулирующих клеток крови. В результате гемопоэз оказывается неэффективным, развивается анемия, сочетающаяся с тромбоцитопенией и лейкопенией. Кроме того, цианкобаламин является коферментом в реакции превращения метилмалонил-КоА в сукцинил-КоА. Эта реакция необходима для метаболизма миелина в нервной системе, в связи с чем при дефиците цианкобаламина наряду с мегалобластной анемией отмечается поражение нервной системы, в то время как при недостаточности фолатов наблюдается только развитие мегалобластной анемии. Цианкобаламин содержится в пищевых продуктах животного происхождения - печени, почках, яйцах, молоке. Запасы его в организме взрослого человека (главным образом в печени) велики - около 5 мг, и если учесть, что суточная потеря витамина составляет 5 мкг, то полное истощение запасов при отсутствии поступления (нарушение всасывания, при вегетарианской диете) наступает только через 1000 дней. Цианкобаламин в желудке связывается (на фоне кислой реакции среды) с внутренним фактором - гликопротеином, продуцируемым париетальными клетками желудка, или другими связывающими белками - R-факторами, присуствующими в слюне и желудочном соке. Эти комплексы предохраняют цианкобаламин от разрушения при транспорте по ЖКТ. В тонкой кишке при щелочном значении рН под влиянием протеиназ панкреатического сока цианкобаламин отщепляется от R-протеинов и соединяется с внутренним фактором. В пдовздошной кишке комплекс внутреннего фактора с цианкобаламином связывается со специфическими рецепторами на поверхности эпителиальных клеток, освобождение цианкобаламина из клеток кишечного эпителия и транспорт к тканям происходит с помощью особых белков плазмы крови - транскобаламинов 1,2,3, причем транспорт цианкобаламина к гемопоэтическим клеткам осуществляется преимущественно транскобаламином 2. Фолиевая кислота содержится в зеленых листьях растений, фруктах, печени, почках. Запасы фолатов составляют 5-10 мг, минимальная потребность - 50 мкг в день. Мегалобластная анемия может развиться через 4 месяца полного отсутствия поступления фолатов с пищей.
Клиническая картина В12-дефицитной анемии характеризуется поражением трех систем: пищеварительной, кроветворной и нервной.
Поражение пищеварительной системы .У подавляющего большинства больных симптомы поражения системы органов пищеварения (прежде всего субъективные) могут быть наиболее ранними признаками заболевания. Больные жалуются на снижение, иногда даже отсутствие аппетита, ощущение тяжести и полноты в подложечной области после еды, отрыжку съеденной пищей и воздухом, боль и жжение в языке, в области десен, губ, иногда в области прямой кишки. Указанные жалобы больных обусловлены развитием глоссита, атрофического гастрита и атрофическими изменениями слизистой оболочки кишечника. Отсутствие аппетита некоторые гематологи объясняют гипоксией мозга и угнетением центра аппетита в гипоталамической зоне.
При осмотре полости рта обращают на себя внимание воспалительно-атрофические изменения слизистой оболочки полости рта и языка. Для В12-дефицитной анемии характерен гладкий «лакированный» язык с атрофированными сосочками, потрескавшийся, с участками воспаления ярко-красного цвета (воспаленным и красным может оказаться весь язык), иногда с изъязвлениями (глоссит Hunter). Следует подчеркнуть, что глоссит наблюдается только при значительном и длительном дефиците витамина В12, приблизительно у 25% больных (А. В. Демидова, 1993). Глоссит характерен не только для В12-дефицитной анемии, он может наблюдаться и при железодефицитной анемии. Слизистая оболочка полости рта бледна, могут отмечаться
явления афтозного стоматита.
При пальпации живота определяется неинтенсивная боль в эпигастральной области (непостоянный признак), нередко наблюдается увеличение печени и селезенки. Если развитие В12-дефицитной анемии обусловлено нарушением всасывания витамина В12 в тонком кишечнике, то в клинической картине наряду с синдромом анемии обычно имеется четко выраженная симптоматика синдрома мальабсорбции.
Поражение кроветворной системы Нарушение системы кроветворения является ведущим в клинической картине заболевания и характеризуется анемией различной степени выраженности. Больные жалуются на значительную общую слабость; одышку и сердцебиения (при нетяжелой анемии преимущественно при физической нагрузке, при выраженной анемии — даже в покое); головокружение; иногда обморочные состояния; шум в ушах, потемнение в глазах и мелькание мушек пред глазами. Эти субъективные проявления неспецифичны, они наблюдаются также и при других видах анемий. При осмотре обращают на себя внимание цвет кожи и внешний вид больных. Кожа обычно бледная, очень часто с лимонно-желтым оттенком (в связи с гипербилирубинемией, обусловленной гемолизом). Легкую желтушность склер можно заметить даже тогда, когда степень анемии невелика. Характерно несколько одутловатое лицо, часто наблюдается пастозность в области голеней и стоп. Как правило, больные не худеют, за исключением,
Диагностика болезней системы крови разумеется, тех ситуаций, когда В12-дефицитная анемия обусловлена
раком желудка или резко выраженным синдромом мальабсорбции. Анемия обусловливает развитие синдрома миокардиодистрофии, которая проявляется тахикардией, иногда экстрасистолической аритмией, небольшим расширением границы относительной тупости сердца влево, приглушенностью тонов сердца, негромким систолическим шумом в области верхушки, изменениями ЭКГ. Вследствие анемии, особенно если она значительно выражена, снижается память, умственная работоспособность. Иногда при В12-дефицитной анемии повышается температура тела (не выше 38°С).
Поражение нервной системы Изменения нервной системы при В12-деф;:цитной анемии яляются характерным признаком этого заболевания и, как правило, наблюдаются при тяжелом и длительном течении. Поражение нервной системы при В12-дефицитной анемии называет- % фуникулярным миелозом и характеризуется вовлечением вАроцесс задних и боковых столбов спинного мозга. Наступает демиелинизация, а затем дегенерация нервных волокон в спинном мозге и спинномозговых нервах Больные жалуютс : на слабость в ногах, особенно при подъеме по лестнице, при быстрой ходьбе, ощущение ползания мурашек^по ногам, онемение ног. Больным кажется, что они не чувствуют! при ходьбе опоры под ногами («не чувствуют земли под ногами»). |Создается впечатление, что нога наступает не на твердую землю, а на что-то рыхлое, мягкое, как вата. Это заставляет больных неоднократно как бы «пробовать землю ногой». Указанные жалобы обусловлены нарушением проприоцептивной чувствительности. Неврологическая симптоматика во многом определяется преимущественным поражением задних или боковых столбов спинного мозга. При преобладании поражения задних столбов нарушается глубокая, пространственная, вибрационная чувствительность; появляются сенсорная атаксия, затруднения при ходьбе; снижаются сухожильные рефлексы; наблюдается атрофия мышц нижних конечностей. При выраженном поражении задних столбов спинного мозга может наступить нарушение функции тазовых органов (недержание мочи, недержание кала).
При преобладании поражения боковых столбов спинного мозга неврологическая симптоматика иная: развивается нижний спастический парапарез с резким повышением сухожильных рефлексов и тонуса мышц нижних конечностей; нарушение функции тазовых органов характеризуется задержкой мочеиспускания и дефекации. Очень редко при В12-дефицитной анемии наблюдаются нарушения обоняния, слуха, функции верхних конечностей, а также психические расстройства (бред, галлюцинации, психозы, депрессия).
Диагностика В12-дефицитной анемии: 1. Клинический анализ крови - снижение количества эритроцитов - снижение гемоглобина - повышение цветного показателя (выше 1.05) - макроцитоз (относится к группе макроцитарных анемий) - базофильная пунктация эритроцитов, наличие в них телец Жолл и колец Кебота - появление ортохромных мегалобластов - снижение ретикулоцитов - лейкопения - тромбоцитопения - снижение моноцитов - анэозинфилия 2. В окрашенных мазках - типичная картина: наряду с характерными овальными макроцитами встречаются эритроциты нормального размера, микроциты и шизоциты - пойкило- и анизоцитоз. 3. Уровень билирубина в сыворотке повышен за счет непрямой фракции 4. Обязательна пункция костного мозга так как такая картина на периферии может быть при лейкозе, гемолитической анемии, апластических и гипопластических состояниях (однако, необходимо отметить, что гиперхромия характерна именно для В12-дефицитной анемии). Костный мозг клеточный, число ядросодержащих эритроидных элементов увеличено в 2-3 раза противо нормы, однако эритропоэз неэффективный, о чем свидетельствует снижение числа ретикулоцитов и эритроцитов на периферии и укорочение их продолжительности жизни (в норме эритроцит живет 120-140 дней). Находят типичные мегалобласты - главный критерий постановки диагноза В12-дефицитная анемия. Это клетки с "ядерно-цитоплазматической диссоциацией" (при зрелой гемоглобинизированной цитоплазме нежное, сетчатого строения ядро с нуклеолами); также обнаруживаются клетки гранулоцитарного ряда большого размера и гигантские мегакариоциты.
Анализ мочи и кала — при развитии гемолиза в моче выявляется уробилин, в кале — увеличено количество стеркобилина. Тест Шеллинга — позволяет оценить всасывание витамина В12 в кишечнике в присутствии гастромукопротеина или без него и сделать заключение о патогенетическом варианте В12-дефицитной анемии (обусловлена она дефицитом гастромукопротеина или нарушением всасывания витамина В12). Различают два вида теста — «Шеллинг-1» и «Шеллинг-П». «Шеллинг-1» — больному дают принять внутрь витамин В 1 2 , меченный "'Со, и спустя 1-6 часов внутримышечно вводят «ударную дозу» немеченого витамина В12 для насыщения печеночного депо. Затем измеряют содержание радиоактивного витамина В12 в суточной моче. Снижение его экскреции указывает на нарушение всасывания витамина В12 в кишечнике.
«Шеллинг-П» — проводится повторение теста «Шеллинг-1» с использованием гастромукопротеина, меченого радиоактивным кобальтом. Повышение экскреции радиоактивного витамина В12 будет указывать на дефицит гастромукопротеина в качестве основного механизма развития В12-дефицитной анемии. Если экскреция радиоактивного витамина В12 в тесте «Шеллинг-П» не увеличилась, можно считать, что причиной развития В12-дефицитной анемии является не дефицит гастромукопротеина, а нарушение всасывания витамина В12 в кишечнике.
Инструментальные исследования
Эзофагогастродуоденоскопия — наблюдаются атрофические изменения слизистой оболочки пищеварительного тракта. Наиболее характерно развитие диффузного атрофического гастрита, дуоденита, может обнаруживаться атрофический эзофагит (значительно реже). Биопсия слизистой оболочки подтверждает наличие атрофического гастрита.
Исследование желудочной секреции — выявляется резкое уменьшение количества желудочного сока, отсутствие соляной кислоты (ахилия) и пепсина, иногда соляная кислота обнаруживается, но уровень ее очень низкий. При В 12 -дефицитной анемии, обусловленной нарушением всасывания витамина В 1 2 в тонком кишечнике или инвазией широкого лентеца, секреция соляной кислоты значительно снижена, однако стимуляторы желудочной секреции (гистамин, пентагастрин) повышают уровень соляной кислоты в желудочном соке.
УЗИ печени и селезенки — выявляется незначительное увеличение размеров селезенки, иногда печени. Указанные изменения наблюдаются не всегда.
Рентгеноскопия желудка — обнаруживаются нарушения эвакуаторной функции желудка, уплощение и сглаженность складок слизистой оболочки.
Лечение B12-дефицитной анемии:
Комплекс лечебных мероприятии при В12 - дефицитной анемии следует проводить с учетом этиологии, выраженности анемии и наличия неврологических нарушений. При лечении следует ориентироваться на следующие положения: - непременным условием лечения В12 - дефицитной анемии при глистной инвазии является дегельминтизация (для изгнания широкого лентеца назначают фенасал по определенной схеме или экстракт мужского папоротника). - при органических заболеваниях кишечника и поносах следует применять ферментные препараты (панзинорм, фестал, панкреатин), а также закрепляющие средства (карбонат кальция в сочетании с дерматолом). - нормализация кишечной флоры достигается приемом ферментных препаратов (панзинорм, фестал, панкреатин), а также подбором диеты, способствующей ликвидации синдромов гнилостной или бродильной диспепсии. - сбалансированное питание с достаточным содержанием витаминов, белка, безусловным запрещением алкоголя - непременное условие лечения В12 и фолиеводефицитной анемии. - патогенетическая терапия осуществляется с помощью парентерального введения витамина В12 (цианкобаламин), а также нормализации измененных показателей центральной гемодинамики и нейтрализации антител к гастромукопротеину ("внутреннему фактору") или комплексу гастромукопротеин + витамин В12 (кортикостероидная терапия). Гемотрансфузии проводят лишь при значительном снижении гемоглобина и проявлении симптомов коматозного состояния. Рекомендуется вводить эритроцитную массу по 250 - 300 мл (5 - 6 трансфузий). Преднизолон (20 - 30 мг/сут) рекомендуется при аутоиммунной природе заболевания. Принципы терапии:
насытить организм витамином - поддерживающая терапия - предупреждение возможного развития анемии Чаще пользуются цианкобаламином в дозах 200-300 микрограмм (гамм). Данная доза применяется если нет осложнений (фуникулярный миелоз, кома). Сейчас применяют 500 микрограмм ежедневно. Вводят 1-2 раза в день. При наличии осложнений 1000 микрограмм. Через 10 дней доза уменьшается. Инъекции продолжаются 10 дней. Затем, в течение 3 месяцев еженедельно вводят 300 микрограмм. После этого, в течение 6 месяцев делается 1 инъекция в 2 недели. Критерии оценки эффективности терапии: - резкий ретикулоцитоз через 5-6 инъекций, если его нет, то имеется ошибка диагностики; - полное восстановление показателей крови происходит через 1.5 - 2 месяца, а ликвидация неврологических нарушений в течение полугода.
Прогноз: Благоприятный.
Профилактика B12-дефицитной анемии:
Профилактика у практически здоровых людей обеспечивается рациональным питанием, включающим мясные и рыбные продукты. Вегетарианцам полезно регулярное включение в рацион молока и сои. После лабораторных исследований (см. выше) можно рекомендовать парентеральное введение 50—100 мкг препарата витамина В12 1—2 раза в месяц или ежедневный прием таблеток, содержащих цианокобаламин. С целью профилактики важно также своевременно выявлять больных дифиллоботриозом (носителей широкого лентеца); производить дегельминтизацию. При заболеваниях (и после операций), сопровождающихся нарушением всасывания цианокобаламина, следует под контролем лабораторных исследований (содержание витамина В12 в моче и крови) назначать лечебные или профилактические курсы витаминотерапии.
75.Картина периферической крови при в12-дефицитной анемии.
Общий анализ крови при витамин B12-дефицитной анемие
Характерны панцитопения (анемия, лейкопения, тромбоцитопения), сдвиг в лейкоцитарной формуле влево.
Микроскопия мазка периферической крови при витамин B12-дефицитной анемие
Типичен макроцитоз, анизоцитоз, пойкилоцитоз. Обнаруживают мегалоциты (гиперхромные эритроциты диаметром 11-12 мкм без просветления в центре), тельца Жолли (мелкие тёмно-фиолетовые включения в эритроците, представляющие собой разрушенное ядерное вещество) и кольца Кэбота, ги-персегментированные нейтрофилы. Количество ретикулоцитов в норме или несколько снижено.
Биохимический анализ крови
Содержание витамина B12 в плазме крови составляет менее 100 пг/мл (в норме 160-950 пг/мл). Характерны увеличение содержания ферритина в сыворотке крови, гипербилирубинемия за счёт непрямой фракции, уменьшение содержания гаптоглобина, увеличение активности ЛДГ. Возможно обнаружение AT к внутреннему фактору Касла и париетальным клеткам желудка.
76.Дифференциальный диагноз по анемическому синдрому
ДИФЕРЕНЦИАЛЬНИЙ ДИАГНОЗ ПРИ АНЕМИЯХ.
ПАТОГЕНЕЗ
ВАЖНЕЙШИЕ КЛИНИЧЕСКИЕ ФОР
МЫ
Гематологическая характеристика
Функциональное состояние костного мозга
I. Анемии вследствие кровопо-терь (постгеморрагические)
Острая Хроническая
Нормохром-ная, нормоци-тарная Гипохромная, микроцитарная
Гиперрегенераторная Различного характера в зависимости от длительности кровопотерь, но чаще гиперрегенераторная
II. Анемии вследствие повышенного кроверазрушения (гемолитические)
1. Анемии, обусловленные вну-трисосудистым гемолизом А. Острые: а) токсические (отравление ге-молитическими ядами); б) инфекционные (сепсис, малярия и др.); в) посттрансфузионные (вследствие переливания несовместимой крови): г) гемолитическая болезнь новорожденных; д) гемоглобинурии Б. Хроническая гемолитическая анемия с пароксизмальной гемо-глобинурией (болезнь Маркиафа-вы— Микели)
Нормохромные, нормо-микроцитар-ные
Гиперрегенераторные
.
2. Анемии, обусловленные внутриклеточным гемолизом а) врожденная хроническая гемолитическая анемия (болезнь Минковского — Шоффара); б) приобретенная гемолитическая анемия; в) гемоглобинозы
Гипохромная, микросферо-цитарная
Гиперрегенераторные
.
3.Анемии со смешанной (внутриклеточной и внутрисосуди-стой) локализацией гемолиза
Нормохром-ная, нормо-цитарная
.
III. Анемии вследствие нарушенного кровообразования
1. Железодефицитные анемии: а) хлороз ранний и поздний; б) анемия беременных; в) гастроэнтерогенная анемия; г) агастрическая анемия;
Гипохромные, микроцитарные
Гипорегенераторные
.
2. в12 (фолиево)-дефицитные анемии: а) болезнь Аддисона— Бирмера; б) глистная пернициозная анемия;
Гиперхром-ные, макро-мегалоцитар-ные
Гиперрегенераторные
в)пернициозная анемия беременных; г)анемия при спру; д)агастрическая пернициозная анемия; е)при атрофии слизистой желудка (рак, сифилис)
.
.
.
3. Гипопластические (апластические) анемии.А. Анемии вследствие токсического угнетения костного мозга: а) ионизирующая радиация; б) бензольная интоксикация; в) лекарственные воздействия; г) аутоагрессивные; д) неизвестной этиологииБ. Анемии, обусловленные метаплазией костного мозга; а) при лейкозах; б) при миеломной болезни; в) при метастазах рака в костный мозг
Нормохромные, нормоцитарные
Арегенераторные
при постгеморрагической анемии — клинические проявления основного заболевания как источника кровопотери (язва или опухоль желудочно-кишечного тракта, геморрой, анкилостомидоз, мено- или метроррагии и т. п.); при железодефицитных анемиях — извращение вкуса, ряд трофических расстройств (сухость кожи, ломкость ногтей, выпадение волос) и часто — желудочную ахилию; при гемолитической анемии — гемолитическую желтуху, а в случае массивного распада эритроцитов — гемоглобинурию; при В12(фолиево)-дефицитной анемии — нарушение со стороны желудочно-кишечного тракта в виде глоссита, органической ахилии, а также поражение нервной системы типа фуникулярно-го миелоза; при гипопластической анемии — геморрагические проявления и реже — септицемию с некрозами в полости рта, зева, и т.д. Острая постгеморрагическая анемия — нормохромная, нормоцитарная, регенераторная. Железодефицитная (в том числе хроническая постгеморрагическая) анемия — гипохромная, микроцитарная (реже макроци-тарная), гипорегенераторная. В12(фолиево)-дефицитная анемия — гиперхромная, макромегалоцитарная, гипорегенераторная. Гемолитическая анемия — нормогипохромная (реже гиперхромная), микроцитарная, гиперрегенераторная. Гипопластическая анемия — нормохромная, нормоцитарная, арегенераторная.
77.Острые лейкозы. Определение, этиология, патогенез, клиника, диагностика, лечение, профилактика.
Острые лейкозы – гетерогенная группа опухолевых заболеваний, при которых костный мозг поражается бластами – морфологически незрелыми клетками, при этом вытесняются элементы кроветворения в костном мозге и инфильтрация бластами внутренних органов.
Частота встречаемости 5 на 100 000 населения в год
ЭТИОЛОГИЯ Неизвестна
Предрасполагающие факторы: Ионизирующее излучение Химио- и радиотерапия других опухолей 20% ОЛ следствие курения Бензол При врождённых заболеваниях за счёт повышенной хромосомной нестабильности Т-клеточный вирус – 1 Обменная (эндогенная) теория: накопление метаболитов триптофана и тирозина
Классификация:
Миелоидные лейкозы
Мо—с недифференцированными бластными клетками
М, — ОМЛ без признаков созревания бластов
М2 — ОМЛ с признаками созревания бластов
М,—промиелоцитарный лейкоз
М4—миеломоноцитарный лейкоз; М4-Е„—с аномальными эозинофилами
М5—моноцитарный (монобластный) лейкоз
Мы—недифференцированный лейкоз (более 80% составляют клетки типа монобластов)
Ма—с признаками дифференциации клеток моноцитарного ряда (монобластов менее 80%, остальные клетки —промоноциты и моноциты)
М,—острый эритролейкоз
М,—острый мегакариобластный лейкоз
Лимфобластные лейкозы L1 — с малыми размерами бластов (чаще у детей)
L2 — с крупными размерами бластов (чаще у взрослых)
L3—с бластными клетками типа клеток при лимфоме Беркитта
ОМЛ- острый миелобластный лейкоз.
ПАТОГЕНЕЗ 1) ОЛ - следствие мутации в генетическом материале кроветворной клетки, которая, размножаясь, образует опухолевый клон 2) Диссеминация опухолевых клеток – метастазирование по кроветворной системе 3) Опухолевая прогрессия – в её основе повышенная изменчивость хромосом и образование новых субклассов, из-за которых изменяются свойства опухоли
КЛАССИФИКАЦИЯ ФАБ – классификация: I – Нелимфобластные, миелогенные (миелоидные) лейкозы, подразделяются на 8 типов; II – Лимфобластные – 3 типа; III – Миелопоэтические дисплазии или миелодиспластический синдром – 4 типа
ЛЕЧЕНИЕ Основной принцип лечения – максимально полное удаление лейкозных клеток на всех этапах.
Стадии ОЛ: начальная, разгара, ремиссия полная, неполная, рецидив, терминальная
Есть 2 популяции клеток – пролиферирующая и непролиферирующая. Пролиферирующая находится в митотической фазе цикла, на неё действует полихимиотерапия. Определённые препараты действуют в определённые фазы цикла – 6-меркаптопурин, циклозан; некоторые на весь цикл – винкристин, циклофосфан, преднизолон.
Терапия должна быть: интенсивной, длительной, сочетать циклоспецифические и циклонеспецифические препараты
!!Стабильная и длительная ремиссия – это 5 лет и более
Программа CALGB
Курс I – индукция ремиссии (4 нед). Препараты дают на мг/м2
Курс II – ранняя интенсификация (4 нед)
Курс III – ЦНС-профилактика и межкурсовая поддерживающая терапия (12 нед)
Курс IV – поздняя интенсификация (8 нед)
Курс V – длительная поддерживающая терапия (до 24 месяцев от момента установления диагноза)
Если есть рецидив или рефрактерные формы, используют специальные схемы – 5-дневная RACOP, COAP, COMP, а затем основная схема
Терапия нелимфобластного лейкоза – «7+3»: цитозин-арабинозид 7 дней, затем даунорубицин 3 дня
Препараты, применяемые для лечения ОЛ: 1) Алкилирующие соединения, нарушающие синтез НК – циклофосфан 2) Антиметаболиты – предшественники НК: - 6-меркаптопурин - метотрексат 3) Антимитотические средства – блокируют митоз в стадии метафазы путём денатурации тубулина винкристин 4) Противоопухолевые а/б – антрациклины, подавляют синтез ДНК и РНК рубомицин 5) Ферменты: L-аспарагиназа разрушает L-аспарагин, т.к. у бластов в нём повышенная потребность 6) ГКС - преднизолон 60 мг/м2
На фоне полихимиотерапии обязательна терапия прикрытия: А/б терапия, Дезинтоксикационная терапия, включая гемосорбцию, плазмаферез, Заместительная компонентная терапия при глубокой цитопении (переливание Эр-массы, тромбоцитов), Аллопуринол 600 мг/м2 из-за массивного клеточного распада, Увеличение объёма жидкости до 3 литров, Растворы АК и жировые эмульсии, Профилактика вирусных и грибковых осложнений
78.Хронический лимфолейкоз. Определение, этиология, патогенез, клиника, диагностика, лечение, профилактика.
Хронический лимфолейкоз (ХЛЛ)
Хронический лимфолейкоз (ХЛЛ) –клональное лимфопролиферативное неопластическое заболевание, характеризующиеся пролиферацией и увеличение в периферической крови кол-ва зрелых лимфоцитов на фоне лимфоцитарной инфильтрации костного мозга, лимфатических узлов, селезенки и других органов.
Эпидемиология ХЛЛ – наиболее распространенный вид лейкемии, составляющий 30% всех случаев. Распространенность составляет 3,9 и 2,0 на 100 000 мужчин и женщин соответственно. 90% больных старше 50 лет старше 50 лет, хотя в редких случаях заболевание возникает у детей.
Этиология ХЛЛ неизвестна. Хотя непосредственное участие не установлено, родственники первой степени родства больных с ХЛЛ имеют в 3 раза больший, чем в остальной популяции, риск развития ХЛЛ и других лимфоидных опухолей. Участие радиации и вирусов в развитии ХЛЛ не обнаружено.
Патогенез хронического лимфолейкоза
На уровне предшественника В-клетки происходит хромосомная аберрация, приводящая к трисомии хромосомы 12 либо к структурным нарушениям хромосом 6, 11, 13 или 14. Патологические клетки дифференцируются до уровня рециркулирующих В-клеток или В-клеток памяти. Их нормальные клеточные аналоги — длительноживущие, иммунологически аре-активные, митотически пассивные В-клетки Т-независимого пути диффе-ренцировки и В-клетки памяти соответственно. Последующие деления генетически нестабильных лимфоцитов могут привести к появлению новых мутаций и соответственно новых биологических свойств, т.е. субклонов лейкозных клеток. Клинически это проявляется наличием симптомов интоксикации, трансформации ХЛЛ в злокачественную и агрессивную лим-фоидную опухоль, что наблюдается (по сравнению с другими лимфомами) крайне редко, в 3% случаев. Болезнь иногда сопровождается появлением моноклональных IgM или IgG.
Клиническое течение
Доброкачественная
Прогрессирующая
Селезенчатая (спленомегалическая)
Абдоминальная
Опухолевая
Костномозговая
Пролимфоцитарная
Клиническая картина
Основные критерии начального периода
Незначительное увеличение нескольких лимф. узлов одной или нескольких групп
Лейкоз не превышающий 50
Нет тенденции к увеличению лейкоцитоза
Удовлетворительное состояние больного (состояние компенсации)
Период выраженных клинических проявлений
Жалобы: слабость, снижение работоспособности, повышение температуры
Лимфоаденопатия
Лимфоидные инфильтраты кожи (чаще при Т-клеточном варианте ХЛЛ)
Органы и системы (поражение обусловлено лейкемической инфильтрацией)
Спленомегалия
Инфильтрация слизистой ЖКТ
Инфилтр. верхних и нижних дыхательных путей
Почки
ЦНС
Сердце (поражается редко)
ОАК
Лейкоцитоз 50-100
Резкое увеличение кол-ва лимфоцитов 10 и более (характерный признак ХЛЛ)
Появление клеток Боткина-Гумпрехта (полуразрушиные ядра лимфоцитов)
Нормохромная анемии
Увеличение СОЭ
Терминальная стадия
Резкое ухудшение состояния, истощение, выроженная интоксикация, исчезновение аппетита, высокая температура тела. Возникновение инфекционно-воспалительных процессов с локализацией в различных органах и системах. Тяжелая почечная недостаточность. т
ОАК
Выраженная анемия
Тромбоцитопения
Бластный криз
Частая трансформация в другие лимфопролиферотивные заболевания
Лечение
Лечебная программа
Режим
Цитостатики
Лимфоцитофарез
Лучевая терапия
Спленэктомия
ГКС
Лечение инфекционных осложнений
Цитостатики
Хлорбутин – таблетки по 0.002 и 0.005г 4-10 мг в день
Циклофосфан – таб по0.05г и амп по0.2 г в/в или в/м по 400мгежедневно
Пафенцил – таб по 0.025г по 25-75 мг ежедневно курсовая доза 500-1200
Цитостатическая схема ЦВП – циклофосфан в течение 5 дней сут доза по 400мг/м, винкристин в 1-й день 1,4мг/м, преднизолон в течение 5 дней в сут дозе 40 мг/м.
Прогноз. В отдельных случаях комплексная химиотерапия позволяет получить многолетние ремиссии. Продолжительность жизни больных колеблется в очень широких пределах – от нескольких месяцев до 2-3 десятилетий, в среднем 75 месяцев.
79.Лабораторные диагностика хронического миелолейкоза.
Хронический миелойдный лейкоз – опухоль кроветворной ткани, исходящая из клеток-предшественниц миелопоэза, морфологическим субстратом которой являются дифференцирующиеся и зрелые гранулоциты.
Лабораторная диагностика
1. В гемограмме характерны гранулоцитарный лейкоцитоз (20—250 • 109/л и выше) со значительным содержанием миелоцитов, промиелоцитов, иногда - бластов, эозинофильно-базофильная ассоциация; у многих больных тромбоцитоз до 400—600•109/л, относительная, а позже, в III ст. абсолютная лимфопения. Например: эр. — 3,15 • 1012/л, Hb — 98 г/л, ЦП — 0,9, ретик. — 0,5 ‰, тромб. — 648 • 109/л, лейк. — 99,0 • 109/л: бласты — 6, базофилы — 2, э — 4, промиелоциты — 8, миелоциты — 15, ю — 12, п — 12, с — 38, л — 2, м — 1, СОЭ — 18 мм/ч.
2. Снижение щелочной фосфатазы в нейтрофилах менее 10 ед.
3. Костный мозг весьма богат клеточными элементами (иногда более 200 • 109/л) за счет гиперплазии незрелых гранулоцитов. Кариотип 46 XX t (9; 22), Ph‘-хромосома положительная.
4. В специализированных гематологических центрах проводятся кариологические исследования для выявления Ph-хромосомы (маркера хронического миелолейкоза).
80. Идиопатическая тромбоцитопеническая пурпура. Определение, этиология патогенез, клиника, диагностика, лечение.
ИДИОПАТИЧЕСКАЯ ТРОМБОЦИТОПЕНИЧЕСКАЯ ПУРПУРА (БОЛЕЗНЬ ВЕРЛЬГОФА) (Morbus maculosus Werlhofi)
Идиопатическая тромбоцитопеническая пурпура--одно из наиболее распространенных геморрагических заболеваний.
Этиология до сих пор не установлена.
Патогенез. В основе заболевания лежит разрушение тромбоцитов антителами, синтезирующимися в органах иммунокомпетентной системы (прежде всего, в селезенке, а также в костном мозге, печени и других органах, содержащих лимфоидную ткань). Антитела, присоединяясь к определенному участку мембраны тромбоцитов, формируют с ними иммунный комплекс, который в дальнейшем разрушается в клетках системы мононуклеарных фагоцитов, в основном в селезенке, являющейся активной зоной макрофагальной системы, а в тяжелых случаях -- также в печени и костном мозге. Возможна внутрисосудистая агглютинация тромбоцитов
Радиоизотопными методами установлено резкое укорочение продолжительности жизни тромбоцитов (до нескольких часов вместо 8--12 дней).
Повышенное разрушение тромбоцитов ведет к стимуляции тромбоцитопоэза путем увеличения выработки тромбопоэтинов. При идиопатической тромбоцитопенической пурпуре увеличено содержание мегакариоцитов в костном мозге; количество тромбоцитов, образующихся в единицу времени, не снижено, как это предполагали раньше, а, наоборот, повышено по сравнению с нормой в 2--6 раз. В связи с этим какое-то время существует равновесие между продукцией и деструкцией тромбоцитов, нарушить которое могуч различные стрессовые ситуации -- инфекция, интоксикация, лекарственные препараты, обладающие свойствами гаптена, а также некоторые физиологические состояния -- беременность, климакс и т д.
В патогенезе кровоточивости при тромбоцитопенической пурпуре ведущую роль играют тромбоцитопения и связанные с ней нарушения коагуляционных cвойств крови и проницаемости стенки сосудов. При этом нарушается i фаза свертывания крови--образование тромбопластина, а также ретракция сгустка крови за счет дефицита ретрактозима.
Повышение проницаемости стенки сосудов объясняется также тромбоцитопенией. отсутствием краевого стояния тромбоцитов, нарушением их ангиотрофической функции и дефицитом серотонина, вырабатываемого тромбоцитами и обладающего мощным сосудосуживающим действием.
Клиника. Заболевание встречается чаще всего в молодом возрасте и преимущественно среди женщин. Основными клиническими симптомами являются кровоизлияния в кожу и кровотечения из слизистых оболочек, возникающие или спонтанно, или под влиянием незначительных травм Кожные геморрагии имеют различную величину -- от петехий до крупных пятен и даже кровоподтеков, которые располагаются обычно на передней поверхности туловища и конечностей В зависимости от давности кровоизлияния первоначальная багрово-красная окраска его постепенно приобретает различные оттенки -- синий, зеленый и желтый, что придает коже характерный вид ("шкура леопарда").
Довольно частым симптомом заболевания являются кровотечения из слизистых оболочек Первое место по частоте занимают кровотечения из носа и десен, а у женщин-- мено- и метроррагии. Кровотечения из слизистых оболочек обычно комбинируются с кожными геморрагиями и носят нередко множественный и профузный характер, сопровождаясь развитием постгеморрагической анемии.
В начальном периоде они могут быть единственным признаком заболевания Возможны также кровоизлияния в сетчатку и другие отделы глаза, в головной мозг, пищевой канал, легкие и почки
Непостоянным симптомом заболевания является незначительное увеличение селезенки, которая, как правило, при тромбоцитопенической пурпуре не прощупывается. Выраженная спленомегалия скорее противоречит диагнозу болезни Верльгофа. В большинстве подобных случаев имеется лишь симптоматическая тромбоцитопения, сопутствующая спленопатии различного характера.
Картина крови характеризуется значительным снижением количества тромбоцитов (в отдельных случаях до полного исчезновения), изменением их морфологических и функциональных свойств (анизо- и пойкилоцитоз, уменьшение зернистости, снижение активности лактатдегидрогеназы, глюкозо-6-фосфатдегидрогеназы, ?-глицерофосфатазы, снижение агрегационной и адгезивной способности).
Показатели красной крови и количество лейкоцитов обычно в норме. Лишь в тяжелых случаях, при длительных или профузных кровотечениях, развивается постгеморрагическая анемия.
В крови могут выявляться антитела к тромбоцитам (тромбоагглютинины и тромболизины).
При исследовании пунктата костного мозга отмечается повышенное, реже нормальное, содержание мегакариоцитов, вокруг которых тромбоциты, как правило, отсутствуют. Последнее обстоятельство связано не с уменьшением образования кровяных пластинок, как это трактовалось раньше, а с ускоренным поступлением их в кровь.
Нередко наблюдаются морфологические изменения мегакариоцитов (потеря гранул, вакуолизация, асинхронизм созревания), объясняемые повышенной тромбоцитообразовательной функцией их. В отдельных случаях аутоиммунной тромбоцитопении количество мегакариоцитов бывает снижено, что, по-видимому, связано с наличием антител, направленных против мегакариоцитов.
Следует отметить также ослабление или отсутствие ретракции сгустка крови. Если в норме кровь из вены свертывается с отделением сыворотки через 2 ч, то при тромбоцитопенической пурпуре сгусток остается рыхлым в течение 6 ч и даже суток. Наряду с этим отмечаются увеличение времени кровотечения (до 10-- 20 мин и более) при неизмененном времени свертывания крови и положительный симптом жгута (Кончаловского -- Румпеля -- Лееде). Однако надо иметь в виду, что геморрагические тесты обычно выражены только на высоте кровотечения, почти исчезая в стадии ремиссии.
Диагноз устанавливают на основании множественного характера геморрагии, рецидивирования болезни и ряда положительных геморрагических тестов (тромбоцитопении, замедления ретракции сгустка крови, увеличения времени кровотечения) при полной сохранности и даже гиперплазии мегакариоцитарного аппарата костного мозга.
Дифференциальный диагноз проводят с геморрагическим васкулитом, гемофилией, гипопластической анемией, острым лейкозом, миелокарцинозом.
От геморрагического васкулита и гемофилии тромбоцитопеническая пурпура отличается наличием тромбоцитопении, отсутствием суставных проявлений, нормальным временем свертывания крови (последнее при гемофилии замедлено).
При гипопластической анемии помимо снижения количества тромбоцитов наблюдаются анемия, лейкопения и гранулонитопения, а в костномозговом пунктате и трепанате -- гипо- или аплазия.
Острый лейкоз характеризуется тяжелым состоянием больных, некротическими изменениями на слизистых оболочках, анемией, появлением в лейкограмме бластных клеток, бластной метаплазией костного мозга.
Отличительными признаками миелокарциноза являются следующие: тяжелое общее состояние, лихорадка, исхудание, боль в костях, поражение костей с типичными рентгенологическими изменениями, нередко сопровождающееся патологическими переломами. При исследовании крови определяется анемия, степень которой не адекватна кровопотере, часто -- лейкопения, появление в лейкограмме молодых форм (метамиелоцитов, миелоцитов и даже миелобластов), наличие эритробластов. В мазках костномозгового пунктата можно обнаружить атипичные клетки.
Течение заболевания в основном хроническое, с чередованием обострений и ремиссий различной продолжительности, во время которых исчезают геморрагические явления, нередко нормализуется количество тромбоцитов, ретракция сгустка и др. Наряду с этим наблюдаются хронические формы заболевания с монотонным течением, постоянными геморрагиями на коже или слизистых оболочках и тромбоцитопенией.
Примерно у 1/3 больных встречаются острые формы заболевания, характеризующиеся внезапным началом, интенсивными геморрагическими проявлениями, но в большинстве случаев заканчивающиеся быстрым выздоровлением.
Прогноз при тромбоцитопенической пурпуре в общем благоприятный. В отдельных случаях острые формы заболевания или очередные его рецидивы могут сопровождаться профузными кровотечениями из слизистых оболочек с последующей тяжелой анемией, а иногда -- кровоизлиянием в головной мозг, что может привести к смерти.
Лечение должно быть направлено на купирование геморрагических проявлений, устранение анемии и предотвращение рецидивов. Для борьбы с кровоточивостью назначают сосудоукрепляющие средства (препараты кальция, аскорбиновую кислоту, рутин, аскорутин, черноплодную рябину, этамзилат -- дицинон по 1--2 табл. 3 раза в день или по 2--4 мл внутримышечно или внутривенно и др.). Применяют также аминокапроновую кислоту внутрь или внутривенно, серотонина адипи- нат 0,5--1 мл в сутки 1 °/о раствора внутривенно или внутримышечно; местно -- гемостатическую губку, тромбин, гемофобие и др. При наличии анемии и кровоточивости рекомендуется переливание крови наименьших сроков хранения. При хронической постгеморрагической анемии показаны препараты железа.
Трансфузии тромбоцитной массы следует ограничить лишь ургентными случаями и не производить вообще при наличии у больного антител к тромбоцитам ввиду возможного усиления кровоточивости.
В качестве патогенетической терапии широко применяют кортикостероиды. Механизм их действия сводится к уменьшению проницаемости стенки сосудов и угнетению иммунных реакций, что особенно важно при иммунной форме тромбоцитопении, при которой возможно увеличение количества тромбоцитов под влиянием кортикостероидов. Преднизолон назначают в суточной дозе 1 -- 1,5 мг/кг. После купирования кровоточивости дозу постепенно снижают до 20--25 мг в сутки. Поддерживающая терапия в этих дозах длится 1-- 3 месяца. При новом обострении проводится повторный курс. Наблюдение за больными в течение последующего года определяет дальнейшую терапевтическую тактику. В случае неэффективности консервативной терапии, наличии частых обострений, сопровождающихся обильными кровотечениями (особенно -- в жизненно важные органы), анемии показана спленэктомия, которая дает ремиссии в 75--80% случаев и наиболее эффективна у лиц молодого возраста.
Терапевтический эффект спленэктомии объясняется устранением тормозящего влияния селезенки на костный мозг и удалением источника образования антител.
Операцию следует производить, по возможности, в неактивной фазе заболевания.
При тромбоцитопенической пурпуре, рефрактерной ко всем видам терапии, включая лечение кортикостероидами и спленэктомию, назначаются иммунодепрессивные средства (меркаптопурин, азатиоприн). Однако неблагоприятные последствия угнетения иммунологической реактивности больных и угнетающее действие этих препаратов на гемопоэз ограничивают их применение.
81.Геморрагические диатезы. Определение, этиология, классификация, патогенез, клиника, диагностика, лечение.
Причины заболевания
Геморрагии наблюдаются при различных заболеваниях: язвенной болезни желудка, геморрое, туберкулезе легких, болезнях матки и т. д. Если у человека появляются частые кровотечения от незначительных ранений, травм (ушибов) при совершенно здоровых органах и эти кровотечения трудно остановить, то говорят о склонности организма к геморрагиям. Диатезом называется предрасположение организма (иногда наследственное) к определенным заболеваниям. Геморрагическим диатезом, или кровоточивостью, называются заболевания, сопровождающиеся кровотечениями, возникающими от понижения свертываемости крови, недостатка в крови тромбоцитов или от повреждения капилляров (воспалительные, токсические или дистрофические). Нарушение свертываемости крови может происходить под влиянием разных причин: от уменьшения количества тромбоцитов, недостатка тромбокиназы, протромбина и т. д. Поэтому к геморрагическим диатезам относятся многие заболевания, например тромбоцитопеническая пурпура, геморрагический васкулит, гемофилия.
Патогенез наследственных геморрагических состояний определяется нарушением нормальных гемостатических процессов: аномалиями мегакариоцитов и тромбоцитов, дефицитом или дефектом плазменных факторов свертывания крови, неполноценностью мелких кровеносных сосудов.
Приобретенные геморрагические диатезы обусловлены ДВС-синдромом, иммунными поражениями сосудистой стенки и тромбоцитов, токсикоинфекционными поражениями кровеносных сосудов, заболеваниями печени, воздействиями лекарственных средств.
Симптомы и виды
Различают наследственные и приобретенные геморрагические диатезы.
Наследственные проявляются у детей (например, гемофилия), приобретенные возникают в любом возрасте, чаще они являются осложнением других заболеваний, например болезней печени, системы крови с нарушением образования тромбоцитов. Повышенная кровоточивость может наблюдаться при передозировке гепарина, непрямых антикоагулянтов (фенилина и др.), тромболитических препаратов, ацетилсалициловой кислоты (аспирина).
Из генетически обусловленных форм геморрагических диатезов этой группы наиболее часто встречается наследственная телеангиэктазия (Ослера-Рандю болезнь), при которой из-за истончения и множественных дефектов базальной мембраны мелких кровеносных сосудов на слизистых оболочках, губах, коже, а иногда и на внутренних органах образуются мелкие узловатые или ветвистые (в виде паучков) легко кровоточащие сосудистые образования. Особенно опасны интенсивные и трудно купируемые носовые кровотечения, прогрессирующие в возрасте старше 7-10 лет. У многих больных развиваются также артериовенозные шунты в легких (при рентгенологическом исследовании видны очаговые затемнения) и в печени, что может приводить к появлению вторичного эритроцитоза, цианотической гиперемии кожи лица и слизистых оболочек. Более редкими формами являются телеангиэктазии, сочетающиеся с мозжечковыми расстройствами и иммунной недостаточностью, например синдром Луи-Бар.
Среди приобретенных геморрагических диатезов, характеризующихся преимущественным поражением кровеносных сосудов, доминируют инфекционные и иммунные формы. При приобретенных геморрагических диатезах очаги поражения располагаются симметрично, высыпания имеют воспалительную основу (иногда с некрозами), нередко возникают другие виды сыпей (волдыри, папулы), лихорадка, артралгии, гематурия, абдоминальные нарушения (болевой синдром, кишечные кровотечения). К ним легко присоединяется тромбогеморрагический синдром.
По патогенезу различают следующие группы геморрагических диатезов:
1) обусловленные нарушениями свертываемости крови, стабилизации фибрина или повышенным фибринолизом, в том числе при лечении антикоагулянтами, стрептокиназой, урокиназой, препаратами дефибринирующего действия (арвином, рептилазой, дефибразой и др.);
2) обусловленные нарушением тромбоцитарно-сосудистого гемостаза (тромбоцитопений, тромбоцитопатии);
3) обусловленные нарушениями как коагуляционного, так и тромбоцитарного гемостаза: а) болезнь Виллебранда; б) диссеминированное внутрисосудистое свертывание крови (тромбогеморрагический синдрома); в) при парапротеинемиях, гемобластозах, лучевой болезни и др. ;
4) обусловленные первичным поражением сосудистой стенки с возможным вторичным вовлечением в процесс коагуляционных и тромбоцитарных механизмов гемостаза (наследственная телеангиэктазия Ослера-Рандю, гемангиомы, геморрагический васкулит Шенлейна-Геноха, эритемы, геморрагические лихорадки, гиповитаминозы С и В и др.). В особую группу включают различные формы так называемой невротической, или имитационной, кровоточивости, вызываемой у себя самими больными вследствие расстройства психики путем механической травматизации ткани (нащипывание или насасывание синяков, травмирование слизистых оболочек и т. д.), тайным приемом лекарственных препаратов геморрагического действия (чаще всего антикоагулянтов непрямого действия – кумаринов, фенилина и др.), самоистязанием или садизмом на эротической почве и т. д. Реже встречаются близкие к ДВС-синдрому тромбогеморрагические заболевания, протекающие с выраженной лихорадкой-тромботическая тромбоцитопеническая пурпура (болезнь Мошкович) и гемолитико-уремический синдром. Выделяют 5 типов кровоточивости: гематомный, капиллярный (микроциркуляторный), смешанный (гематомный и капиллярный одновременно), пурпурный и микроангиоматозный.
При гематомном типе, который характерен для гемофилии, отмечаются кровоизлияния в суставы, массивные гематомы различной локализации, послеоперационная кровоточивость.
Капиллярный тип кровоточивости встречается при тромбоцитопениях и тромбоцитопатиях. Для него характерны мелкие кровоизлияния на коже (петехии и экхимозы), носовые, десневые и маточные кровотечения, возможны гемитурия и желудочные кровотечения, кровоизлияния в вещество мозга.
Смешанный тип кровоточивости проявляется образованием гематом, петехиально-пятнистыми высыпаниями на коже, носовыми, десневыми и маточными кровотечениями. Наиболее часто он наблюдается при тромбогеморрагическом синдроме, а также при передозировке антикоагулянтов.
При пурпурном типе кровоточивости отмечаются мелкие симметрично расположенные преимущественно на нижних конечностях кровоизлияния в виде сыпи. Этот тип кровоточивости выявляется при геморрагических васкулитах.
Микроангиоматозный тип кровоточивости в виде упорно повторяющихся кровотечений одной и той же локализации обусловлен наследственными, реже приобретенными нарушениями развития мелких сосудов.
Осложнения при геморрагические диатезы зависят от локализации геморрагий. При повторных кровоизлияниях в суставы возникают гемартрозы при образовании обширных гематом в области прохождения крупных нервных стволов возможно сдавление нервов с развитием параличей, парезов при кровоизлияниях в головной мозг появляются симптомы, характерные для нарушения мозгового кровообрашения. При повторных переливаниях крови и плазмы может развиться сывороточный гепатит. У больных с полным отсутствием факторов свертывания возможно образование антител, что значительно ументшает эфективность трансфузий; возможны посттранфузионные реакции.
Диагностика
Общая диагностика геморрагических заболеваний и синдромов базируется на следующих основных критериях: 1) определение сроков возникновения, давности, длительности и особенностей течения заболевания (появление в раннем детском, юношеском возрасте либо у взрослых и пожилых людей, острое или постепенное развитие геморрагического синдрома, недавнее или многолетнее (хроническое, рецидирующее) его течение и т. д. ;
2) выявление по возможности семейного (наследственного) генеза кровоточивости (с уточнением типа наследования) либо приобретенного характера болезни;
3) уточнение возможной связи развития геморрагического синдрома с предшествовавшими патологическими процессами, воздействиями (в том числе и лечебными с лекарственные препараты, прививки и др.) и фоновыми заболеваниями (болезни печени, лейкозы, инфекционно-септические процессы, травмы, шок и т. д.);
4) определение преимущественной локализации, тяжести и типа кровоточивости. Так, при болезни Ослера-Рандю преобладают и часто являются единственными упорные носовые кровотечения; при патологии тромбоцитов-синяковость, маточные и носовые кровотечения, при гемофилиях- глубокие гематомы и кровоизлияния в суставы.
Лечение и профилактика
Лечение при наследственных геморрагических диатезах проводят с помощью средств, устраняющих дефицит отдельных факторов свертывающей системы крови.
Приобретенные геморрагические диатезы лечат с учетом причин их развития. Обязательно отменяют те препараты, которые вызвали кровоточивость, вводят антидоты. Профилактика. В профилактике наследственных геморрагических диатезов большое значение имеет медико-генетическое консультирование, а приобретенных – предупреждение заболеваний, способствующих их возникновению, рациональное использование средств, снижающих свертывание крови.
82.Дифференциальная диагностика по геморрагическому синдрому. Типы кровоточивости.Геморрагический синдром возникает как следствие изменений в одном или нескольких звеньях гемостаза. Это может быть поражение сосудистой стенки, нарушение структуры, функции и количества тромбоцитов, нарушение коагуляционного гемостаза.Из наследственных нарушений гемостаза наиболее часто встречаются тромбоцитопатии, гемофилия А, болезнь Виллебранда, гемофилия В, телеангиэктазия.причины приобретенных форм- вторичная тромбоцитопения и тромбоцитопатии, ДВС-синдром, дефицит факторов протромбинового комплекса и геморрагический васкулит.Различают 5 типов геморрагического синдрома.1.Гематомный. Типичен для гемофилии А и В, характеризуется возникновением болезненных напряженных кровоизлияний в мягкие ткани и суставы, постепенным развитием нарушений функции опорно-двигательного аппарата..2.Петехиально-пятнистый (синячковый). Возникает при тромбоцитопении, тромбоцитопатии, нарушении свертывающей систем.3.Смешанный синячково-гематомный. Развивается при тяжелом дефиците факторов протромбинового комплекса и фактора XIII, болезни Виллебранда ,характеризуется сочетанием петехиально-пятнистых кожных геморрагии с отдельными большими гематомами в забрюшинном пространстве, стенке кишечника. В отличие от гематомного типа, кровоизлияние в полость суставов возникает крайне редко. Синяки могут быть обширными и болезненными.4.Васкулито-пурпурный тип. Наблюдается при инфекционных и иммунных васкулитах, легко трансформируется в ДВС-синдром и характеризуется геморрагией в виде сыпи или эритемы на воспалительной основе, возможным присоединением нефрита и кишечного кровотечения.5.Ангиоматозный тип. Развивается в зонах телеангиэктазий, ангиом, артериовенозных шунтов и характеризуется упорными локальными геморрагиями, связанными с зонами сосудистой патологии.
1. При гемофилии А и В (дефицит факторов VIII и IX) определяются болезненные обширные кровоизлияния в подкожную клетчатку, под апоневрозы, в серозные оболочки, в мышцы и суставы обычно после травм с развитием деформирующих артрозов, контрактур, патологических переломов. Наблюдаются длительные, профузные посттравматические и послеоперационные кровотечения, реже - спонтанные. Выражен поздний характер кровотечений, то есть спустя несколько часов после травмы.
2. При тромбоцитопениях и тромбоцитопатиях, наблюдается питехии, экхимозы на коже и слизистых оболочках, спонтанные (возникающиеся преимущественно по ночам несимметричные кровоизлияния в кожу и слизистые оболочки) или возникающиеся при малейших травмах кровотечения: носовые, десневые, маточные, почечные. Гематомы образуются редко, опорно-двигательный аппарат не страдает. Послеоперационные кровотечения не отмечаются (кроме тонзиллэктомии). Часты и опасны кровоизлияния в мозг;им предшествуют петехиальные кровоизлияния в кожу и слизистые оболочки.3. Васкулитно-пурпурный тип обусловлен экссудативно-воспалительными явлениями в микрососудах на фоне иммуно-аллергических и инфекционно-токсических нарушений. Наиболее распространенное заболевание-геморрагический васкулит синдром Шенлейна-Геноха. Геморрагический синдром представлен симметрично расположенными, преимущественно на конечностях в области крупных суставов, элементами, четко отграниченными от здоровой кожи, выступающими над ее поверхностью, представленными папулами, волдырями, пузырьками, которые могут сопровождаться некрозом и образованием корочек. Может быть волнообразное течение, "цветение" элементов от багряного до желтого цвета с последующим мелким шелушением кожи. При васкулитно-пурпурном типе возможны абдоминальные кризы с обильными кровотечениями, рвотой, макро- и микрогематурией , часто трансформирующиеся в ДВС-синдром.
83.Гломерулонефриты. Определение, этиология, патогенез, классификация, клиника, диагностика, лечение, профилактика. ОСТРЫЙ ГЛОМЕРУЛОНЕФРИТ ОГ— циклически протекающее, инфекционно-аллерги-ческое заболевание почек, характеризующееся при типичном течении внезапным началом с видимыми гематурией и отеками, гипертензией ЭтиологияОбычно началу болезни за 1-3 нед предшествует стрептококковая инфекция в виде фарингита, тонзиллита, скарлатины, кожных поражений — импетиго-пиодермия.охлаждение, респираторная вирусная инфекция у ребенка с хроническим тонзиллитом или носительством кожного нефритогенного стрептококка А могут привести к активации инфекции
Патогенез.Активированный иммунными комплексами комплемент, обладая хемотак-сической активностью, привлекает в очаг поражения нейтрофилы. Освободившиеся из лизосом полинуклеоляров энзимы повреждают эндотелиальный покров базальной мембраны клубочка, что приводит к разрывам ее, появлению в пространстве Боумена белков плазмы, эритроцитов, фрагментов мембраны. Активированный комплемент способствует также активации факторов Хагемана, агрегации тромбоцитов., в капиллярах клубочков проис-ходит свертывание крови, отложение фибрина. Полинуклеоляры, обладая фибринолитической активностью, разрушают фибрин, но все же при тяжелом течении депозиты фибрина закономерно находят в сосудах почек.
Клиническая картина развивается приблизительно через 10-14 дней после перенесенной ангины, скарлатины или другого острого стрептококкового заболевания, охлаждения и складывается из двух групп симптомов — экстраренальных и ренальных.доминируют экстпраренальные симптомы: недомогание, плохой аппетит, вялость, тошнота; ребенок бледнеет, у него появляется умеренный отечный синдром (пастоз-нях, в области лодыжек). Резко выраженные отеки в начале бывают редко. Иногда отмечают повышение температуры тела до субфебрильной, умеренное увеличение печени. гипер-тензионный синдром: головная боль, изменения сердечно-сосудистой систе-мы, заключающиеся в тахикардии, систолическом шуме на верхушке, тошноте, иногда рвоте, а при обследовании — в разной степени выраженности повышении артериального давления< изменении сосудов глазного дна Бледность лица в сочетании с его отечностью, набуханием шейных вен создает у части больных специфический вид лица — fades nephritica.Ренальные симптомы в начале следующие: олигурия, изменение цвета мочи (покраснение) или гематурия лишь при анализе мочи, боли в области поясницы (из-за растяжения капсулы почек) или недифференцированные боли в животе, азотемия.Мочевой синдром (олигурия, протеинурия, гематурия, цилиндрурия). Олигурия (уменьшение диуреза на 50-80% или менее 300 мл/м2 в сутки) возникает при гломерулонефрите вследствие уменьшения массы функционирующих нефронов. Кроме того, внутрисосудистые тромбы, отечность сосудистого эндотелия и подоцитов, выраженная пролиферация эндотелия и мезангиума приводят к снижению фильтрации и в функционирующих клубочках. Следствием этого является задержка в кровяном русле жидкости (гиперволемия) и далее гиперальдостеронизм, уменьшение натрийурии. Определенную роль в патогенезе олигурии играет и повышение обратной дистальной реабсорб-ции воды, то есть развитие «антидиуреза» из-за повышенной секреции АДГ. Относительная плотность мочи высока (выше 1,030).Отеки. В патогенезе отеков у больных ОСГН имеют значение 4 фактора:1. Повышение гидродинамического давления вследствие:а) увеличения объема циркулирующей крови,б) гипертензии.2. Уменьшение коллоидно-осмотического давления крови, связанного:а) с тем, что при гиперволемии одновременно развивается гидремия,б) с диспротеинемией (сдвиг отношения альбумины/глобулины крови в сторону глобулинов),в) с дисэлектролитемией.3. Повышение проницаемости капилляров, которое объясняют наличием у больных значительного повышения гиалуронидазной активности крови и «диффузным капилляритом».4. Увеличение реабсорбции воды и уменьшение экскреции натрия с мочой
Лечение.Режим. При постельном режиме все тело больного должно находиться в равномерном тепле. Диета. Наиболее принципиальным в диете при является ограничение соли и водыСуточное количество жидкости в разгар болезни должно быть равно вчерашнему диурезу, а при отсутствии сведений о нем — около 15 мл/кг (400 мл/м2) — неощутимые потери воды в сутки.
Антибиотикотерапию назначают при поступлении в стационар всем больным. Антибиотик (полусинтетические пенициллины, макролиды) назначают в среднетерапевтических дозах на 8-10 дней. При наличии хронических очагов инфекции, интеркуррентных заболеваний также целесообразнее использовать цикловое назначение антибиотиков (3-4 цикла). К патогенетической терапии относят мероприятия по улучшению почечного кровотока: режим, электрофорез с 1% никотиновой кислотой или гепарином и внутривенные вливания эуфиллина либо теофиллина, трентала.Мочегонные средства назначают лишь больным с выраженными отеками, гипертензионным синдромом. При умеренных отеках достаточно применения электрофореза с никотиновой кислотой на область почек или эуфиллина, трентала. лазикс (фуросемиду), вводимому внутримышечно или внутривенно (разовая доза 1-1,5-2 мг/кг), в комбинации его с ги-потиазидом (разовая доза 0,5-1 мг/кг внутрь одновременно с фуросемидом) или амилоридом (школьникам 5 мг внутрь), назначаемым за 2 ч до приема фуросемида. Указанные комбинации препаратов, действуя на различные отделы нефрона, увеличивают натрийуретический и диуретический эффекты. Комбинация фуросемида и амилорида обладает калийсберегающим действием. Длительность эффекта препаратов 3-4 ч, но в связи с тем, что у больных диффузным гломерулонефритом имеется никтурия, вечером им мочегонных не дают. Можно использовать и такую схему назначения мочегонных: в 8 ч — фуросемид, в 10 ч — гипотиазид или триампур и в 16 ч — верошпирон. Для снижения повышенного артериального давления у больных ОСГН используют препараты центрального действия (клофелин, резерпин) или ингибиторы ангиотензин-превращающего фермента (капотен и др.), а- или (3-блокаторы (пироксан, лабеталол, анаприлин и др.), блокаторы кальциевых каналов (нифедипин и др.). Гипотензивные средства дают 2-3 раза в день.
ХРОНИЧЕСКИЕ ГЛОМЕРУЛОНЕФРИТЫ— группа разнородных первичных гломерулопатий, характеризующихся персистирующими прогрессирующими воспалительными, склеротическими и деструктивными процессами с последующим поражением и других отделов нефрона, в частности, и тубуло-интерстициальным склерозом.
Этиология
= нерациональная лекарственная терапия (длительный прием нефротоксических медикаментов, полипрогмазия, злоупотребление гепарином, нестероидными противовоспалительными препаратами при лечении ОСГН, отсутствие антибактериальной терапии при стрептококковой инфекции и др.)
= хронические очаги инфекции, персистирующие вирусные инфекции, чрезмерные антигенные нагрузки (сочетанные и рецидивирующие инфекции, повторные введения иммуноглобулинов, неправильно проводимые профилактические прививки)
=тяжелые полигиповитаминозы,охлаждения, нерациональное питание
Патогенез
При этом решающее значение может иметь либо повреждение почки, ведущее к длительному и массивному поступлению почечных антигенов в кровоток (вызванному как иммунологическими причинами — иммунными комплексами, аутоантителами, цитоток-сическими лимфоцитами, так и неиммунными — нестабильностью мембран нефрона, повреждением гистогематического барьера разными факторами, в том числе лекарствами, дисплазией почек разного генеза), либо расстройства иммунологической реактивности, при которых возможен аутоиммунный процесс к неповрежденной ткани (чаще это системные болезни, при которых поражение почек вторично, то есть является одним из проявлений болезни).
Классификация
Различаются клинические формы течения:
1) гематурическая,
2) отечно-протеинурическая (нефротическая),
3) смешанная.
Клиническая картина
При гематурическом варианте течения иногда начало болезни неясно: при плановом обследовании или после перенесенного заболевания в анализах мочи обнаруживают микрогематурию и небольшую протеинурию. Эритроциты — выщелоченные, реже свежие, покрывают все поля зрения (либо количество их невелико), но при пробе Аддиса суточная эритроцитурия при повторных обследованиях выше 1-2 млн. Жалоб ребенок обычно не предъявляет, артериальное давление нормальное, а функциональные пробы почек не выявляют отклонений от нормы. Нередко у больных находят скрытые очаги инфекции (хронический тонзиллит и др.), небольшую анемию. Периодически у некоторых больных могут быть жалобы на нерезкие боли в пояснице, отеки, боли в животе, утомляемость, головную боль. гломерулонефрит, IgA-нефропатию.При отечно-протеинурической форме симптоматика гораздо более отчетливая и диагностика ее при плановом обследовании уже достаточно редка. Основными симптомами болезни являются массивная протеинурия и разной выраженности отеки. Не всегда имеется четкая связь между тяжестью протеинурии и отечного синдрома. Эта форма ХГН чаще имеет острое начало: после перенесенной респираторной инфекции, ангины, охлаждения, вакцинации, а иногда и внешне беспричинно развивается клиника острого нефрита с массивной протеинурией. Несмотря на лечение, существенного обратного развития протеинурии и отеков не происходит, хотя гипертензия и азотемия обычно исчезают. Развиваются гипопротеинемия, гиперлипидемия и другие симптомы, изложенные в разделе «Нефротический синдром». При биопсии почек типичен мезангио-пролиферативный гломерулит. Заболевание протекает длительно, волнообразно, с выраженной склонностью к интеркуррентным инфекциям. Длительное время азотовыделительная функция почек не нарушается, но в конце концов наступает ХПН.Смешанная форма ХГН (сочетание гематурии, отеков, гипертензии, массивной протеинурии) протекает особенно неблагоприятно, рано развивается ХПН. Обычно начало болезни протекает как острый нефрит, но курабель-ность процесса невелика. К упомянутой выше симптоматике присоединяются проявления гипертензии: боли в пояснице, головная боль, головокружение, раздражительность или вялость, ухудшение зрения. Иногда паралич лицевого нерва может быть единственным проявлением тяжелой гипертензии. Гипертензионной энцефалопатии может предшествовать (или сопровождать ее) рвота, гиперрефлексия, атаксия и очаговые или генерализованные судороги. Границы относительного сердечного притупления расширены влево, часто выслушивают систолический шум на верхушке. У больного часто отмечают анемию. При рентгенографии обнаруживают сердце в виде «сидячей утки», на ЭКГ — признаки перегрузки левого желудочка. Артериальное давление значительно превышает возрастные нормативы (максимальное давление в мм рт. ст. = 90 + 2п, где п — число лет, минимальное = '/2 максимального + 10). Результаты исследования глазного дна свидетельствуют о наличии гипертонической ангиоретинопатии. При этом течении хронического нефрита ХПН наступает через 1-2 года болезни, а то и раньше. При биопсии почек обычен пролиферативно-фибропластический гломерулит.ЛечениеДиета зависит от функционального состояния почек. При отсутствии нарушения функции почек целесообразно некоторое ограничение поваренной соли (не более 30-35 мг/кг в день), исключение из питания всех продуктов промышленного консервирования, грибов и блюд из них, мясных и рыбных бульонов, пряностей, копчений, солений, продуктов, содержащих много гис-тамина или вызывающих его освобождение.
Медикаментозное лечение. Глюкокортикоиды изолированно при ХГН не применяют. При морфологически мембранозном гломерулите диетическое лечение с добавлением курантила (10 мг/кг в сутки в 3 приема) или индометацина (3 мг/кг в сутки в 3 приема), но если имеются даже начальные признаки почечной недостаточности или гипертензия, то целесообразна комплексная терапия глюко-кортикоидами, цитостатиками и антиагрегантом. Из иммунодепрессоров в последние годы все больше рекомендуют циклоспорин А в дозах 3-10 мг/кг в сутки, то есть постепенно повышая дозу, под контролем уровня препарата в крови, который не должен превышать 400-450 нг/мл.
Мезангио-пролиферативный ХГН при первой атаке НС лечат глюкокорти-коидами, при повторных с помощью 4-компонентной терапии (глюкокортикоиды + цитостатик + гепарин + антиагрегант).
Фокально-сегментарный гломерулосклероз — наиболее резистентная к терапии форма ХГН, а потому есть две точки зрения:1) поддерживающая и симптоматическая терапия,
2) активная комплексная 4-компонентная терапия с периодическими курсами пульс-терапий глюкокортикоидами.
85.Критерии диагностики острого гломерулонефрита

85.Критерии диагностики хронического гломерулофрита.
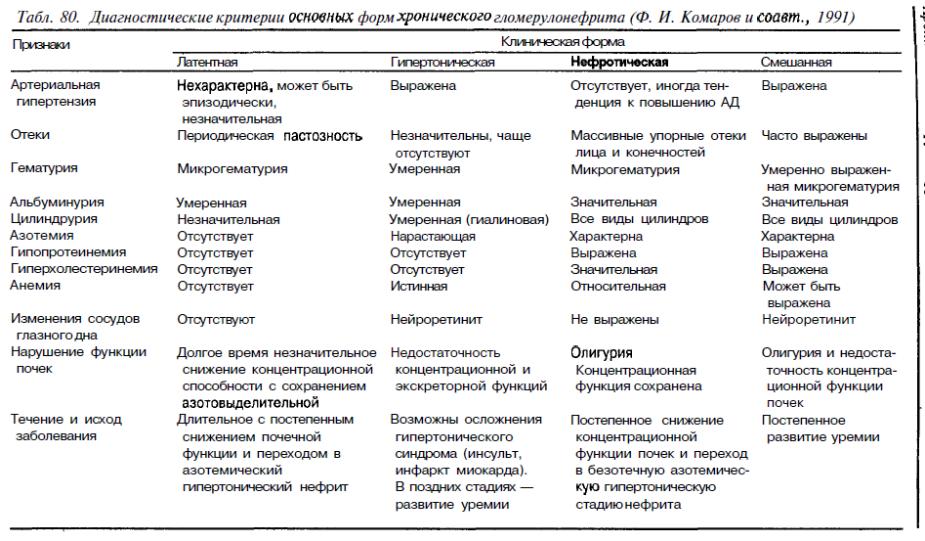
86.Дифференциальный диагноз по нефротическому синдрому. Нефротический синдром — клинико-лабораторный симптомокомплекс, включающий массивную протеинурию (более 3,5 г белка в сутки), нарушения белкового и липидного обмена (гипопротеинемия, диспротеинемия, гипоальбуминемия, ги- перлипидемия, липидурия) и отеки вплоть до анасарки.Нефротический синдром возникает при затянувшемся течении острого гломерулонефрита. Наблюдается длительное (более 6—12 мес) течение болезни, нередко — с переходом в хронический гломерулонефрит. Для острого гломерулонефрита характерно медленное нарастание отеков (иногда — вплоть до анасарки). Преобладают клинико-лабораторные признаки нефротического синдрома. При этом выраженность артериальной гипертонии и гематурии невелика. Выявляются основные лабораторные данные, характеризующие любой вариант развития нефротического синдрома. Потеря белка с мочой может достигать 20—50 г в сутки. Основным компонентом в мочевом белке является альбумин.
При сахарном диабете причиной появления нефротического синдрома служит диабетический гломерулоскле- роЗ), который чаще всего развивается при инсулинзависимом типе сахарного диабета и значительно реже наблюдается при инсулин- независимом типе. Возникает он преимущественно у женщин.Наиболее ранний симптом — перемежающаяся селективная протеинурия, которая может сохраняться в течение 10—15 лет на фоне высоких цифр клубочковой фильтрации.
При длительности течения диабета более 10—15 лет протеинурия становится неселективной, снижается клубочковая фильтрация. Для диагностики важна биопсия почки.
Развернутый нефротический синдром встречается редко (6,3— 30,6 %)4 и является тяжелым прогностическим признаком. Мочевой осадок (эритроциты, цилиндры) скудный. Повышение артериального давления происходит параллельно степени нарастания протеинурии. Через 5—6 лет после появления постоянной протеи- нурии развивается терминальная уремия.
При первичном амилоидозе долгое время жалобы отсутствуют. Затем возникают отеки, которые становятся все более распространенными и выраженными. Появляются общая слабость, адинамия. Повышается артериальное давление. Развивается нефротический синдром. Формируется почечная недостаточность. У некоторых больных обнаруживают симптомы амилоидного поражения сердца (аритмии, тахикардия, одышка), нервной системы (нарушения чувствительности), органов пищеварения (диарея, симптомы нарушенного всасывания, макроглос- сия), увеличиваются размеры печени и селезенки.
ПД В отличие от протеинурии при хроническом нефрите протеинурия при амилоидозе сохраняется даже после развития хронической почечной недостаточности. В начале болезни с потерей преимущественно альбуминов селективная протеинурия сменяется затем неселективной. Протеинурия может достигать 20—30 г в сутки. У некоторых больных в моче обнаруживается белок Бенс-Джонса.
Соответственно степени протеинурии обнаруживаются гиалиновые и (реже) зернистые цилиндры, дающие резко положительную ШИК-реакцию. Иногда выявляются гематурия и лейкоцитурия. Типичны гипер-а2- и у-глобулинемия, гипоаль- буминемия, появление в моче у-гликопротеидов. Проводится биопсия почки, печени, селезенки, лимфатических узлов, прямой кишки, ткани десны.
Ревматоидный артрит в настоящее время является одной из наиболее частых причин амилоидоза и связанного с ним нефротического синдрома. Описано формирование нефротического синдрома при ювенильном ревматоидном артрите.
При системной склеродермии нефротический синдром возникает редко. У некоторых больных нефротический синдром связан с формирующимся при этой болезни амилоидозом.
При узелковом периартериите нефротический синдром встречается очень редко. При этом характерно сочетание нефротического синдрома со значительным повышением артериального давления, ретинопатией и выраженной гематурией. Отечный синдром выражен слабее, чем при нефротическом синдроме другого происхождения.
87.Дифференциальный диагноз по отечному синдрому (хронический пиелонефрит, хронический гломерулонефрит, хроническая сердечная недостаточность). Отеки — избыточное накопление жидкости в тканях организма и серозных полостях. Различают местные (локализованные) и общие отеки, а также скрытые и явные отеки. Скрытыми могут быть отеки объемом менее 2—4 л. Для их обнаружения необходимы сопоставление суточного диуреза и выпитой жидкости, взвешивание больного.От истинных отеков следует отличать псевдоотеки при ожирении, склеродермии, увеличение отдельных частей тела при парциальном гигантизме и т. д. Чаще всего встречаются кардиальные отеки как проявление сердечной недостаточности. У больных выявляются различ-ные заболевания сердца (пороки, атеросклеротический кардиосклероз, перенесенный инфаркт миокарда, аневризма сердца, застойная кардиомиопатия и др.). Определяются увеличение сердца той или иной степени, гепатомегалия. Часто отмечаются аритмии, особенно — мерцание предсердий.
Характерны положение ортопноэ, олигурия, никтурия, застойные явления в легких, набухание шейных вен. Развитию отеков, как правило, предшествует одышка. Отеки нарастают медленно, распространяются обычно снизу вверх. Они симметричны, мало смещаются.
Учитывается выраженная зависимость отеков от положения тела: появление на ногах у ходячих и на пояснице у лежачих больных. Отеки обычно сильнее к вечеру. Их характеризует тестоватая консистенция, при надавливании остается долго не исчезающая ямка. Кожа над областью отеков холодная, цианотичная. При длительном существовании отеков возникают трофические изменения кожи, трещины, дерматит.
В выраженных случаях (анасарка) внешние отеки сочетаются с асцитом (в брюшной полости может накопиться 5—10 л транссудата), гидротораксом, чаще — правосторонним (по 2—3 л транссудата с каждой стороны), реже — с гидроперикардом (накопление до 1 л жидкости в полости перикарда).
Проводят исследования, уточняющие характер кардиальной патологии (ЭКГ, ФКГ, рентгеноскопия грудной клетки, эхо- кардиография и др.), а также исследования, оценивающие степень нарушения гемодинамики (измерение венозного давления, объема циркулирующей крови, величины сердечного выброса и т. п.). Отеки при нефротическом синдроме появляются в первую очередь в местах с наиболее рыхлой подкожной клетчаткой: на лице (особенно — в области век), на передней брюшной стенке, в области гениталий. Одышка не характерна. Нет зависимости отеков от положения тела. Постепенно отеки могут доходить до степени анасарки. Часто они сопровождаются асцитом, реже — гидротораксом. Олигурия необязательна.
ПД. Характерны высокая протеинурия (суточная — более 3 г), гипопротеинемия, диспротеинемия, гиперлипидемия, нередко — обилие в моче разнообразных цилиндров (зернистых, жировых, восковидных) и жироперерожденного почечного эпителия. При неясной причине нефротического синдрома показана биопсия почки.
8.Диф.диагноз при мочевом синдроме. Мочевой синдром может проявляться в различных вариантах. Приведенные ниже особенности изменений мочи представляют собой условную схему, и очень редко каждая отдельная особенность встречается в чистом виде. Высокой считается протеинурия, если суточная потеря белка составляет более 3 г.Выраженный нефротический синдром как клиническая форма острого гломерулонефрита характеризуется большими отеками с анасаркой, асцитом и гидротораксом. Имеются и другие клинические признаки острого нефрита.
ПД. Выявляется суточная протеинурия более 3,5 г. В моче обнаруживаются гиалиновые, зернистые и восковидные цилиндры. В сыворотке крови выявляются гипопротеинемия (менее 6 г/л), гипоаль- буминемия (менее 3 г/л), гиперлипидемия и гиперхолестеринемия.
Хронический гломерулонефрит, протекающий с нефротическим синдромом, сопровождается выраженными отеками лица, конечностей и поясничной области. Артериальное давление нормальное или периодически повышается и легко купируется гипотензивными средствами. Могут быть признаки гипертрофии левого желудочка.
Определяются другие клинические признаки хронического нефрита. Эта клиническая форма чаще наблюдается у больных с мембранозно-пролиферативным и мембранозным хроническим гломерулонефритом. Особенно она характерна для нефрита с минимальными изменениями (для липоидного нефроза).Отмечаются суточная протеинурия более 3,5 г, стойкая и выраженная цилиндрурия, эритроцитурия и лейкоцитурия. В крови выявляются гипопротеинемия и гипоальбуминемия, гиперхолестеринемия и повышение уровня фибриногена.Для с м е ш а н н о й формы хронического гломерулонефрита, когда сочетаются гипертензивный и нефротический синдромы, характерны повышение артериального давления, головная боль, головокружение, иногда — сниженный аппетит, тошнота, рвота, жажда. Имеются и другие признаки хронического нефрита (соответствующий анамнез, отечный синдром).
ПД. Выявляют лабораторные признаки нефротического синдрома, которые описаны выше Вторичный амилоидоз почек возникает у больных туберкулезом ( особенно при легочных формах), нагнои- тельными заболеваниями, сифилисом, ревматоидным артритом, малярией, эндокардитом, раком легкого, раком желудка, лимфогранулематозом.
В первой стадии амилоидоза преобладают симптомы основного заболевания. Протеинурия вариабельна, нарастает после нагрузок и простудных заболеваний. Появляются отеки, постепенно формируется развернутый нефротический синдром. Диурез сохранен. Иногда до умеренных цифр повышается артериальное давление. Увеличиваются в размерах печень и селезенка. Терминальная стадия амилоидоза характеризуется развитием почечной недостаточности. Артериальное давление имеет тенденцию к повышению. Прогрессирует сердечная недостаточность.
Умеренная протеинурия характеризуется суточной потерей белка от 0,5 до 3 г.
При трактовке причин умеренной протеинурии нужно учитывать возможность ложноположительных реакций и появления протеинурии непочечного происхождения. Осадочные белковые пробы могут давать ложноположительные результаты при наличии в моче йодистых контрастных веществ, большого количества продуктов метаболизма пенициллина, цефалоспоринов и сульфаниламидов.
При выраженной лейкоцитурии и особенно гематурии положительная реакция на белок может быть следствием распада форменных элементов при длительном стоянии мочи.. Латентная стадия хронического гломерулонефрита проявляется изолированным мочевым синдромом. Продолжительность латентной стадии колеблется от несколь-ких лет до 10—15 лет и более. Характерно, что, чем старше возраст, в котором развился гломерулонефрит, тем короче латентная стадия. Для этой формы нефрита экстраренальные проявления не типичны. Возможны преходящие подъемы артериального давления, пастозность лица. Отсутствуют признаки длительной гипертензии (изменения глазного дна, гипертрофия левого желудочка).
Морфологическими формами хронического гломерулонефрита при наличии изолированного мочевого синдрома могут быть мезанги- ально-пролиферативная, мембранозно-пролиферативная, реже — мембранозная форма.
ПД. Суточная протеинурия не превышает 3,0—3,5 г. Выраженность гематурии, цилиндрурии и лейкоцитурии может быть различной.
Гипертоническая болезнь может сопровождаться изменениями в моче при развитии артериолосклероза почек. Клиническая характеристика гипертонической болезни описана выше.
Д. В поздних стадиях гипертонической болезни иногда отмечаются суточная протеинурия около 1 г, небольшая гематурия и цилиндрурия. Более выражен мочевой синдром у больных гипертонической болезнью во время интеркуррентных заболеваний, при повышении температуры тела, гипертензивных кризах, появлении застойной недостаточности кровообращения, развитии атеросклероза почечных артерий. Стойкие изменения в моче, особенно у больных с умеренной и выраженной гипертензией, являются показанием к тщательному обследованию почек и мочевыводящих путей для диагностики других заболеваний (гломерулонефрита, пиелонефрита, мочекаменной болезни, диабетического гломерулосклероза и т. д.). Острый гломерулонефрит сизолированным эчевым синдромом и в развернутой форме нередко начинается >сле ангины, острого респираторного заболевания, острого фарин- [та (в среднем через 10 сут).
При развернутой форме появляются слабость, недомогание, ажда, отеки, уменьшается выделение мочи. При повышении ар- риального давления больные жалуются на головную боль. Воз- )жны боли в пояснице ноющего характера.
ПД. При исследовании мочи определяются эритроцитурия [ногда — выраженная; моча приобретает цвет „мясных помоев“), ютеинурия, цилиндрурия и лейкоцитурия.
Хронический пиелонефрит в боль случаев является следствием острого пиелонефрита. С са чала он может протекать со стертой симптоматикой. Жеш болевают гораздо чаще мужчин.
Отмечаются субфебрильная или фебрильная темпера- ноб или познабливание, быстрая утомляемость, слабость, вие аппетита, тошнота, рвота, похудание. У 45—60 % бол вышается артериальное давление.4 Типичны боли в п< полиурия или олигурия, дизурия, поллакиурия.
ПД. В анализе мочи выявляются лейкоцитурия, бакт< снижение относительной плотности, нередко — протеину матурия. Для определения источника бактериурии и лейко у женщин исследуется средняя порция мочи, а у мужчин п ся двустаканная проба.
Количественное содержание лейкоцитов оцениваю мощью проб Нечипоренко и Аддиса—Каковского. Отм снижение концентрации водородных ионов, концентра способности почек, осмолярности мочи, нарушение эк аммиака. Для уточнения характера возбудителя делаютс; мочи.
В анализе крови определяются нормохромная анемия цитоз, увеличение СОЭ. Для выявления пузырно-мочеточ! рефлюкса и других изменений в мочевыводящих путях npi цистоуретерографию или цистореносцинтиграфию. Мочекаменная болезнь часто сопровожу нием камней в мочеточниках с развитие лики. При локализации конкремента в лоханке hj боль иррадиирует в паховую область, в область нар; органов, в бедро. При нахождении камня в нижней ника боль у мужчин иррадиирует в половой член, область больших половых губ. При этом возникаю! позывы на мочеиспускание, моча выделяется по каг не выделяется.
ПД. При локализации конкремента в мочеточн выявлены остановка контрастной жидкости над кам ние на этом уровне мочеточника. У ратные камни oi только на экскреторных урограммах или ретроград] мах в виде дефекта наполнения соответственно раз зации камня.
89. Диагностические критерии хронической почечной недостаточности
прогрессирующее снижение клубочковой фильтрации (N 100-120 мл/мин)
параллельно нарастающий уровень креатинина крови (N 150 мкмоль/л);
дисэлектролитемия (гипер-К, Р-емия, гипо-Са, Na-емия);
метаболический ацидоз;
анемия, тромбоцитопения, увеличение СОЭ;
вторичные изменения различных внутренних органов и систем (артериальная гипертензия, "уремическое легкое", перикардит, энцефалопатия, остеит, стоматит и другие);
изменение концентрационной функции почек по результатам пробы с нагрузкой белком, пробы на разведение и концентрацию.
90.Клиника и неотложная помощь при кетоацидотической и гипогликемической комах.
.Кетоацидотическая кома- грозное осложнение сахарного диабета, являющееся следствием резко выраженной инсулиновой недостаточности и снижения утилизации глюкозы тканями, что приводит к тяжелейшему кетоацидозу, нарушению всех видов обмена веществ, расстройству функции всех органов и систем, в первую очередь нервной системы и потере сознания.
Различают три последовательно развивающиеся и сменяющие друг друга стадии гиперкетонемической комы:
• стадия умеренного кетоацидоза;
• стадия гиперкетонемической прекомы;
• стадия гиперкетонемической комы.
Клиникаразвивается постепенно, в течение нескольких часов и даже нескольких суток. Может быть продромальный период, характеризующийся утомляемостью, слабостью, сухостью во рту, жаждой, полиурией, головными болями, угнетением аппетита, тошнотой, рвотой, болями в животе. Возможны нарушения сознания: от оглушенности до сопора, далее развивается кома с полной потерей сознания и отсутствием реакции на раздражители.
Кожа сухая, горячая; лицо гиперемировано; дыхание Куссмауля — глубокое и шумное; в выдыхаемом воздухе содержится запах ацетона; тургор тканей снижен; глазные яблоки при надавливании мягкие; мышечный тонус снижен. Язык сухой, жесткий, шершавый. Тахикардия. Артериальное давление снижается, пульс слабый, мягкий. Сухожиль ные рефлексы снижены или отсутствуют. Зрачковые и корнеальные рефлексы вялые.
По преобладанию симптомокомплекса выделяют клинические варианты:
Желудочно-кишечная Форма с псевдо-перитонеальными явлениями: боли в животе, напряжение мышц брюшной стенки, положительные симптомы раздражения брюшины. При проведении адекватного лечения симптомы исчезают. Сердечно-сосудистая форма — коллапс, нарушения сердечного ритма.Почечная форма с развитием олигоанурии. Энцефалопатическая Форма напоминает инсульт.
Лечебная программа при выведении больного из гиперкетонемической комы.
1.1. Устранение дефицита инсулина и нормализация углеводного обмена
-препараты инсулина короткого, но быстрого действия. Рекомендуется метод лечения "малыми" дозами инсулина. Применяются две модификации этого метода.
1. 1. 1. Постоянная внутривенная инфузия небольших доз инсулина
Вначале инсулин вводят внутривенно струйно в дозе 8-10 ЕД, а затем внутривенно капельно — со скоростью 6-10 ЕД в час. Для этого готовят раствор, содержащий 50 ЕД инсулина в 500 мл изотонического раствора натрия хлорида, вводят капельно со скоростью 60-100 мл в час, т.е. 6-10 ЕД инсулина в час. Если уровень глюкозы в крови не снижается через 2 ч, то дозу увеличивают до 12-16 ЕД в.
После достижения гликемии 11 ммоль/л внутривенное введение инсулина прекращают и назначают инсулин подкожно по 4-6 ЕД каждые 3-4 ч под контролем гликемии. Уровень гликемии поддерживают в пределах 8-10 ммоль/л.
1.1.2. Частые внутримышечные инъекции малых доз инсулина
Лечение начинают с внутримышечного введения 20 ЕД инсулина, лучше в дельтовидную мышцу плеча. В последующем каждый час внутримышечно вводят 6-8 ЕД инсулина. Если при внутримышечном введении инсулина в течение 2 ч гликемия не снижается, то необходимо перейти на внутривенное капельное введение инсулина. После достижения уровня гликемии 11 ммоль/л назначают инсулин подкожно по 4-6 ЕД каждые 3-4 ч.
1.2. Усиленная регидратация организма
- внутривенно изотонический раствор натрия хлорида, раствора Рингера. В течение 1-го часа вводится внутривенно капельно 1.5 л; в течение 2-го часа — 1 л; в течение 3-го и 4-го часов — по 0.5 л; в дальнейшем — по 0.25-0.3 л каждый час в течение 8 ч. После достижения уровня гликемии 11.1-14 ммоль/л целесообразно подключить введение 5% раствора глюкозы.
Общее количество жидкости, перелитой за 12 ч лечения, должно составлять около 6-7 л.
1.3. Восстановление электролитного баланса
1.3.1. Борьба с гипокалиемией
калия хлорид 1-2% раствором, Начальная доза калия хлорида, вводимого внутривенно капельно, составляет 20 ммоль/ч (1.5 г/ч) в течение 4-5 ч, а затем он вводится по 0.5 г/ч.
1.3.2. Борьба с другими электролитными нарушениями
-Заместительная терапия фосфорсодержащими препаратами - внутривенно капельно калия фосфат со скоростью 10 ммоль/ч., употребление молока.
- дефицит магния. 5-10% раствора магния сульфата по 6-8 мл в течение 3 ч под контролем АД.
1.4. Восстановление нормального КЩР
- 2.5% раствор натрия гидрокарбоната, внутривенно со скоростью 100 ммоль/ч .В среднем за сутки приходится ввести около 400-600 мл 2.5% раствора натрия гидрокарбоната.
- Для борьбы с ацидозом можно применять трисамин внутривенно капельно со скоростью 20 капель в минуту в дозе не более 1.5 г/кг (500 мл в течение суток).
1.5. Нормализация деятельности сердечно-сосудистой системы
- внутривенное капельное вливание полиглюкина, плазмы, 40-80 мг допмина в 300 мл изотонического раствора натрия хлорида со скоростью 20 капель в минуту.
-внутривенно 30-60 мг преднизолона.
-внутривенно медленно 0.5 мл 0.05% раствора строфантина в 20 мл изотонического раствора натрия хлорида.
1.6. Восстановление запасов глюкозы в организме
- Инфузии раствора глюкозы производят в количестве 500 мл в
1.7. Лечение патологических состояний, вызвавших гиперкетонемическую кому, симптоматическое лечение
- Олигурия и признаки почечной недостаточности являются показанием к внутривенному введению 50-100 мг фуросемида.
-В связи с выраженной склонности к гиперкоагуляции и развитию ДВС-синдрома рекомендуется внутривенное введение 5000 ЕД гепарина каждые 6-8 ч.
- осложнением комы является отек головного мозга. внутривенного введения 10 мл 2.4% раствора эуфиллина в 10 мл изотонического раствора натрия хлорида, 80 мг фуросемида
Гипогликемическая кома
ГГК – состояние организма, обусловленное резким падением содержания сахара в крови с последующим снижением утилизации глюкозы мозговой тканью и гипоксией мозга.
Гипогликемическая кома обычно возникает у больных сахарным диабетом как результат:
1) передозировки инсулина
2) голодания
3) интенсивной физической нагрузки
4) при приеме внутрь гипогликемизирующих сульфаниламидных препаратов (бутамид, букарбан, манинил)
У больного появляются предвестники: чувство голода, дрожь, головная боль, потливость. Коматозное состояние развивается очень быстро, возбуждение переходит в сопор и в кому.
Появляются дрожание конечностей, ощущение сердцебиения.
Весьма характерны для этого состояния диплопия и чувство онемения губ.
Тонус мышц повышен, развиваются тонические и клонические судороги.
Зрачки широкие, тонус глазных яблок нормальный.
Запаха ацетона нет.
Кожные покровы влажные, тургор сохранен, язык влажный, дыхание поверхностное. Глюкозурии нет, кетоновых тел нет, есть гипогликемия.
1. Больному вводят медленно внутривенно струйно 40-100 мл 40%-ного раствора глюкозы; при гипогликемическом состоянии дают внутрь сладкий чай, мед, варенье.
2. При отсутствии эффекта после введения 100 мл 40% глюкозы перейти на инфузии 5% раствора глюкозы до 2 г/кг.
3. Если после дозы глюкозы 1 г/кг эффект отсутствует, ввести 100 мг гидрокортизона и 1 мг глюкагона в/в капельно.
