
Важнейшие соединения
|
Al2O3 |
Sc2O3 |
Y2O3 |
La2O3 |
DHобр. |
-1675 |
-1908 |
-1904 |
-1795 |
tпл. |
2050 |
2300 |
2415 |
2320 |
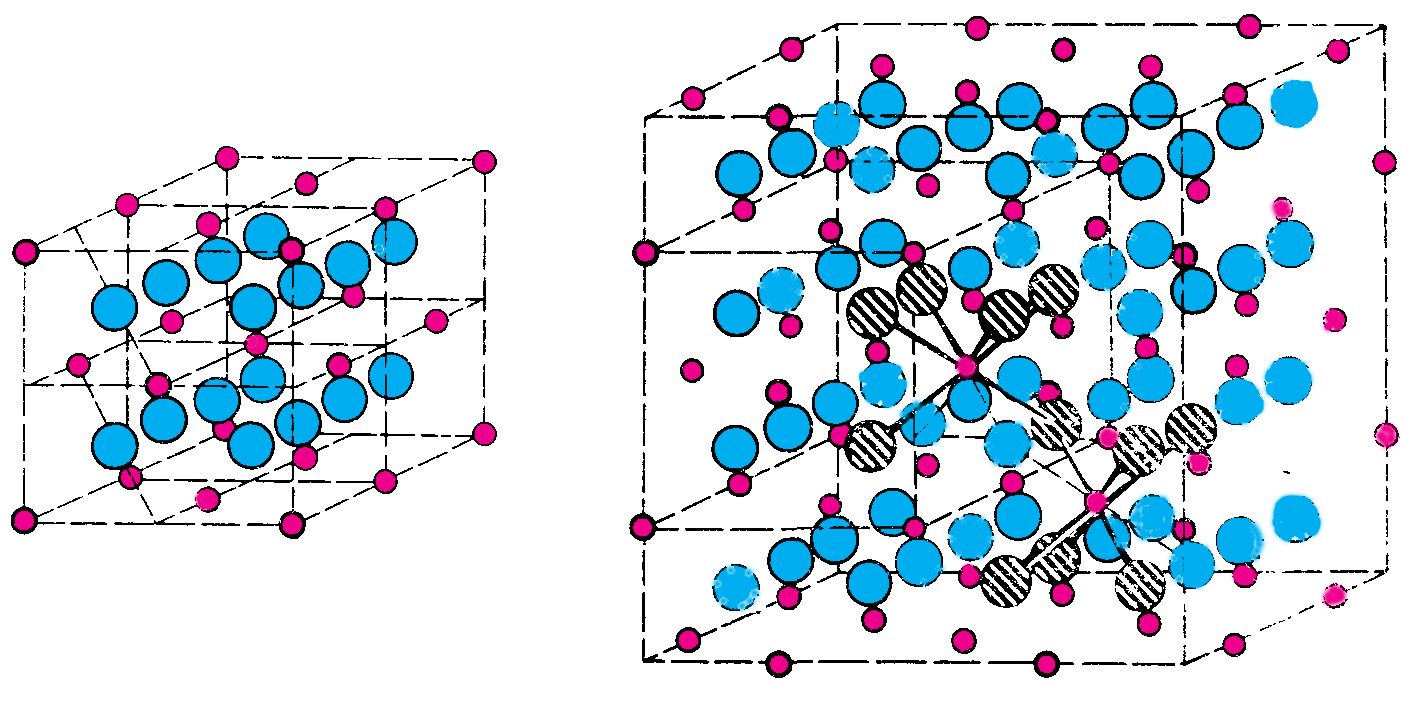
 ксиды
- тугоплавкие белые кристаллические
вещества с очень низкими обр.
и высокими температурами плавления,
близкими к таковым оксида алюминия. Они
имеют собственную структуру, не похожую
на структуру корунда, и родственную
флюориту. Получить их можно либо прямым
путем (хотя, конечно, так их не получают),
либо разложением гидроксидов или солей
(карбонатов, нитратов). В оксидах
ухудшаются объемные отношения, поэтому
их растворимость в воде растет и заметно
улучшается реакционная способность.
Стремлением к улучшению объемных
отношений можно объяснить способность
оксидов иттрия и в особенности лантана
поглощать из воздуха углекислый газ.
Оксид скандия как наименее реакционноспособный
из обсуждаемых оксидов наиболее надежно
вступает в реакции в расплавах, проявляя
при этом основные свойства с признаками
амфотерности. Оксиды иттрия и лантана
основны и способны проявлять свои
свойства в растворах.
ксиды
- тугоплавкие белые кристаллические
вещества с очень низкими обр.
и высокими температурами плавления,
близкими к таковым оксида алюминия. Они
имеют собственную структуру, не похожую
на структуру корунда, и родственную
флюориту. Получить их можно либо прямым
путем (хотя, конечно, так их не получают),
либо разложением гидроксидов или солей
(карбонатов, нитратов). В оксидах
ухудшаются объемные отношения, поэтому
их растворимость в воде растет и заметно
улучшается реакционная способность.
Стремлением к улучшению объемных
отношений можно объяснить способность
оксидов иттрия и в особенности лантана
поглощать из воздуха углекислый газ.
Оксид скандия как наименее реакционноспособный
из обсуждаемых оксидов наиболее надежно
вступает в реакции в расплавах, проявляя
при этом основные свойства с признаками
амфотерности. Оксиды иттрия и лантана
основны и способны проявлять свои
свойства в растворах.
La2O3 + xH2O ® La2O3·xH2O
L a2O3
+ 3CO2
®
La2(CO3)3
a2O3
+ 3CO2
®
La2(CO3)3
Sc2O3 + 3K2S2O7 ® Sc2(SO4)3 + 3K2SO4
Sc2O3 + 2KOH ® 2KScO2 + H2O
Э 2O3
+ 3H2SO4
®
Э2(SO4)3
+ 3H2
2O3
+ 3H2SO4
®
Э2(SO4)3
+ 3H2
ПР(Э2O3·xH2O) |
Sc |
Y |
La |
|
10-27 |
10-24 |
10-19 |
Sc2O3·xH2O + NaOH ® не идет
Э2O3·xH2O + 3H2SO4 ® Э2(SO4)3 + (х+3)H2O
Галогениды элементов подгруппы также похожи на галогениды алюминия. Так, фториды тугоплавки, негигроскопичны, нерастворимы в воде, зато хлориды, бромиды и иодиды гигроскопичны, легко обратимо гидролизуются. В ряду однотипных галогенидов основные свойства усиливаются: например, фторид скандия легко взаимодействует с растворами фторидов щелочных металлов. С фторидами иттрия и тем более лантана подобная реакция возможна лишь в расплавах и только с CsF, RbF.
Подобно алюминию, скандий и его аналоги образуют двойные соли типа квасцов М[Э(SO4)2], а также М2+[Э+3(NO3)5], М+[Э+3(CO3)2]. Известны сульфаты и нитраты, которые при нагревании разлагаются до оксидов.
Лантаноиды
К лантаноидам относятся 14 элементов, расположенных в периодической системе непосредственно после лантана. У них достраивается 4f-подуровень, то есть общая их электронная формула 4f1-145d0-16s2. 4f- и 5d-подуровни весьма близки по энергии, поэтому единственный d-электрон без труда проваливается на f-подуровень и остается на d-подуровне только в тех случаях, если f-подуровень либо наполовину, либо полностью заполнен.
14 f-элементов принято делить на два подсемейства: церия и тербия. Судя по количеству f-электронов, у атомов очень большие валентные возможности. Однако большинство электронов f-подуровня не могут принимать участие в образовании связей, ведь f-подуровень является кайносимметричным, третьим снаружи и поэтому малодоступным. Обычно с f-подуровня на d-возбуждается один электрон, следовательно, наиболее характерная степень окисления лантаноидов +3 за счет возникающей 5d16s2-электронной конфигурации. Возможны и другие степени окисления. Так, первые f-элементы церий и празеодим из-за особой близости f-подуровня способны проявлять и степень окисления +4, причем для церия она даже более характерна, чем +3. Для европия – атома с наполовину заполненным f-подуровнем, более характерна степень окисления +2. Эта степень окисления, правда, в меньшей мере, чем +3, уже проявляется у самария. Примерно такая же картина наблюдается и в семействе тербия.
Подсемейство церия |
Ce 4f25d06s2 +3+4 |
Pr 4f35d06s2 +3+4 |
Nd 4f45d06s2 +3 |
Pm 4f55d06s2 +3 |
Sm 4f65d06s2 +2+3 |
Eu 4f75d06s2 +2+3 |
Gd 4f75d16s2 +3 |
Подсемейство тербия |
Tb 4f95d06s2 +3+4 |
Dy 4f105d06s2 +3+4 |
Ho 4f115d06s2 +3 |
Er 4f125d06s2 +3 |
Tm 4f135d06s2 +2+3 |
Yb 4f145d06s2 +2+3 |
Lu 4f145d16s2 +3 |
Л антаноиды
совместно с иттрием, лантаном и иногда
скандием за сходство свойств простых
веществ и многих соединений объединяют
в одно семейство – РЗЭ. Существенные
отличия большинства лантаноидов от
иттрия и лантана проявляется в цвете,
магнитных свойствах, устойчивости
различных степеней окисления. Так,
большинство соединений лантаноидов
окрашены, что определяется возможностью
f-f-переходов. Неокрашены только соединения
лантаноидов с наполовину и полностью
заполненным f-подуровнем.
антаноиды
совместно с иттрием, лантаном и иногда
скандием за сходство свойств простых
веществ и многих соединений объединяют
в одно семейство – РЗЭ. Существенные
отличия большинства лантаноидов от
иттрия и лантана проявляется в цвете,
магнитных свойствах, устойчивости
различных степеней окисления. Так,
большинство соединений лантаноидов
окрашены, что определяется возможностью
f-f-переходов. Неокрашены только соединения
лантаноидов с наполовину и полностью
заполненным f-подуровнем.
