
- •1. Ферменты. Понятие. Строение. Понятие об активном центре. Коферменты.
- •2. Обмен фенилаланина и тирозина. Синтез катехоламинов, тироксина, меланинов. Биологическое значение.
- •Вопрос 1:
- •Вопрос 2:
- •Билет № 2
- •1. Обратимое и необратимое ингибирование ферментов, ферментные яды. Примеры.
- •2. Воздействие факторов физической природы на организм человека.
- •Вопрос 1:
- •1. Конкурентное ингибирование
- •1. Специфические и неспецифические ингибиторы
- •Вопрос 2:
- •Билет № 3
- •1. Конкурентное ингибирование. Принцип. Примеры. Пути реактивации ферментов при конкурентном ингибировании.
- •2. Гемоглобин. Синтез гема. Транспорт кислорода и со2. Типы и функциональные формы гемоглобина. Гемоглобинопатии.
- •Вопрос 1:
- •Вопрос 2:
- •Билет № 4
- •1. Понятие об аллостерических ферментах. Особенности строения и регуляции. Примеры.
- •2. Компоненты гуморального врожденного иммунитета. Механизмы защитного действия.
- •Вопрос 1:
- •Вопрос 2:
- •Билет № 5
- •1. Дезаминирование аминокислот. Обезвреживания аммиака. Токсичность аммиака.
- •2. Иммуноферментный анализ. Принцип. Применение для идентификации микроорганизмов.
- •Вопрос 1:
- •Вопрос 2:
- •Билет 6.
- •1.Оксидоредуктазы. Строение коферментов. Биологическая роль.
- •2. Биогенные амины как нейромедиаторы (катехоламины, серотонин, гамк, гистамин), их метаболизм. Нарушение обмена биогенных аминов при психических заболеваниях.
- •Вопрос1:
- •Вопрос 2:
- •Билет № 7
- •1. Общие принципы взаимодействия регуляторов с клетками-мишенями. Сигнальные пути.
- •2. Катаболизм гема, образование желчных пигментов. Нарушение обмена билирубина.
- •Вопрос 1:
- •1. Передача гормональных сигналов через мембранные рецепторы
- •2. Передача сигналов через внутриклеточные рецепторы
- •3. Передача сигналов через рецепторы, сопряжённые с ионными каналами
- •Вопрос 2:
- •Билет № 8
- •1. Факторы, определяющие нормальный уровень ферментативной активности биологических жидкостей. Причины, приводящие к изменению количества и активности ферментов в биологических жидкостях.
- •2. Воздействие факторов биологической природы на организм человека.
- •Вопрос 1:
- •Вопрос 2:пока засекречен Билет № 9
- •1. Окислительное декарбоксилирование пировиноградной кислоты. Характеристика мультиферментного комплекса пируватдегидрогеназы. Значение процесса.
- •2. Биохимические механизмы токсичности металлов (Pb, Cd, Hg).
- •Вопрос 1:
- •Вопрос2:пока засекречен Билет № 10
- •Вопрос 1:
- •Вопрос2:
- •Билет № 11
- •2. Классы иммуноглобулинов, классификация, функции в иммунном ответе. Клонально-селекционная теория синтеза антител.
- •Вопрос1:
- •Вопрос 2:
- •Билет № 17
- •Гормоны щитовидной железы. Тироксин и трийодтиронин. Строение, метаболизм. Механизм действия на клетки-мишени. Влияние на обмен веществ.
- •Фотометрический метод определения содержания аналитов и активности ферментов в биологических жидкостях. Принцип метода.
- •Вопрос 1:
- •Вопрос 2:пока засекречен Билет № 18
- •1 Регуляция уровня глюкозы в крови.
- •2 Витамин а. Потребность, источники, условия всасывания, транспорт. Биохимические функции. Признаки недостаточности.
- •Вопрос 1:
- •Вопрос 2:
- •Билет № 19
- •1. Глюконеогенез. Характеристика основных стадий, субстраты глюконеогенеза, регуляция, значение.
- •2. Метаболизм этанола. Биохимические механизмы токсического действия этанола.
- •Вопрос 1:
- •А. Реакции глюконеогенеза
- •1. Образование фосфоенолпирувата из пирувата - первая из необратимых стадий глюконеогенеза
- •2. Гидролиз фруктозо-1,6-бисфосфата и глюкоза-6-фосфата
- •3.Энергетический баланс глюконеогенеза из пирувата
- •Вопрос 2:
- •1. Синтез гликогена. Ход процесса, регуляция. Биологическое значение.
- •2. Витамины рр и в2. Потребность, источники. Коферментные формы и биохимические функции. Признаки недостаточности.
- •Вопрос 1:
- •Вопрос2:
- •Билет № 21
- •1. Глюкоза-6-фосфат – ключевое соединение в обмене углеводов. Источники и пути использования глюкозо-6-фосфата в клетке.
- •2. Основные этапы биосинтеза нуклеотидов. Биологическая роль. Антиметаболиты – ингибиторы процесса.
- •Вопрос 1:
- •Билет № 22
- •1. Распад гликогена. Регуляция. Биологическое значение. Гликогенозы.
- •2. Репликация. Основные этапы. Биологическая роль процесса.
- •Вопрос 1:
- •Вопрос 2:
- •1 Этап репликации: инициация
- •2 Этап репликации: элонгация
- •3 Этап репликации: терминация
- •Билет № 23
- •1. Молекулярная организация биологических мембран. Трансмембранный перенос веществ.
- •2. Структурная организация монооксигеназной системы окисления. Семейства цитохрома р450. Основные реакции, катализируемые изоферментами цитохрома р450.
- •Вопрос 1:
- •2. Трансмембранная асимметрия липидов
- •3. Жидкостность мембран
- •1. Первично-активный транспорт
- •2. Вторично-активный транспорт
- •Вопрос 2:
- •1. Основные ферменты микросомальных электронтранспортных цепей
- •2. Функционирование цитохрома р450
- •3. Свойства системы микросомального окисления
- •Билет № 24
- •1. Инсулин. Синтез. Механизм действия на клетки-мишени. Физиологические эффекты.
- •2. Переваривание белков и всасывание аминокислот. Биохимическая ценность белков.
- •Вопрос 1:
- •1. Инсулин. Строение, синтез и секреция
- •2. Биологические функции инсулина
- •3. Механизм действия инсулина
- •Вопрос 2:
- •1. Образование и роль соляной кислоты
- •2.Механизм активации пепсина
- •Билет № 25
- •1. Переваривание липидов. Всасывание. Роль желчи. Нарушение процессов переваривания и всасывания липидов.
- •2. Транскрипция. Основные этапы, регуляция, значение. Посттрансляционный процессинг белка.
- •Вопрос 1:
- •Вопрос 2:
- •Билет №26
- •Вопрос 1:
- •Использование холестерина в организме
- •Вопрос 2:
- •Билет № 27
- •Вопрос 1:
- •Вопрос 2:пока засекречен Билет № 28
- •Вопрос 1:
- •Вопрос 2:
- •Билет № 30
- •1. Метаболизм кетоновых тел. Роль кетоновых тел в норме и патологии.
- •2. Трансляция. Основные этапы. Антибиотики – ингибиторы трансляции.
- •Вопрос 1:
- •Вопрос 2:
- •Билет № 31
- •1. Депонирование и мобилизация триацилглицеринов. Регуляция.
- •2. Метаболическая биотрансформация ксенобиотиков. Реакции I фазы метаболизма.
- •Вопрос1:
- •Вопрос 2:
- •1. Основные ферменты микросомальных электронтранспортных цепей
- •2. Функционирование цитохрома р450
- •3. Свойства системы микросомального окисления
- •Билет № 32
- •Вопрос 1:
- •Вопрос2:
- •Билет № 33
- •1. Липолиз. Регуляция, значение. Бетта-окисление высших жирных кислот. Энергетическая
- •2. Витамин д. Потребность, источники, метаболизм. Биохимические функции.
- •Вопрос 1:
- •Вопрос 2:
- •Билет № 34
- •1. Биосинтез высших жирных кислот. Характеристика мультиферментного комплекса пальмитат-синтетазы. Значение процесса.
- •Вопрос 1:
- •1. Синтез пальмитиновой кислоты
- •2. Регуляция синтеза жирных кислот
- •3. Синтез жирных кислот из пальмитиновой кислоты
- •Вопрос 2:
- •Билет № 35
- •1. Эссенциальные жирные кислоты как предшественники синтеза эйкозаноидов. Простагландины, их биологическая роль.
- •2. Биохимические основы канцерогенеза.
- •Вопрос 1:
- •Вопрос 2:
- •Билет № 36
- •1. Синтез нсi и его регуляция. Роль соляной кислоты в переваривании белков.
- •2. Система «ренин-ангиотензин-альдостерон», вазопрессин. Функции.
- •Вопрос 1:
- •1. Образование и роль соляной кислоты
- •2.Механизм активации пепсина
- •3.Возрастные особенности переваривания белков в желудке
- •4. Нарушения переваривания белков в желудке
- •Вопрос 2:
- •1. Синтез и секреция антидиуретического гормона
- •2. Механизм действия
- •3. Несахарный диабет
- •1. Механизм действия альдостерона
- •2. Роль системы ренин-ангиотензин- альдостерон в регуляции водно-солевого обмена
- •3. Восстановление объёма крови при обезвоживании организма
Билет № 30
1. Метаболизм кетоновых тел. Роль кетоновых тел в норме и патологии.
2. Трансляция. Основные этапы. Антибиотики – ингибиторы трансляции.
Вопрос 1:
ОБМЕН КЕТОНОВЫХ ТЕЛ
При голодании, длительной физической работе и в случаях, когда клетки не получают достаточного количества глюкозы, жирные кислоты используются многими тканями как основной источник энергии. В отличие от других тканей мозг и другие отделы нервной ткани практически не используют жирные кислоты в качестве источника энергии. В печени часть жирных кислот превращается в кетоновые тела, которые окисляются мозгом, нервной тканью, мышцами, обеспечивая достаточное количество энергии для синтеза АТФ и уменьшая потребление глюкозы. К кетоновым телам относят β-гидроксибутират, ацетоацетат и ацетон. Первые две молекулы могут окисляться в тканях, обеспечивая синтез АТФ. Ацетон образуется только при высоких концентрациях кетоновых тел в крови и, выделяясь с мочой, выдыхаемым воздухом и потом, позволяет организму избавляться от избытка кетоновых тел.
Синтез кетоновых тел в печени.
При низком соотношении инсулин/глюкагон в крови в жировой ткани активируется распад жиров. Жирные кислоты поступают в печень в большем количестве, чем в норме, поэтому увеличивается скорость β-окисления (рис. 8-32). Скорость реакций ЦТК в этих условиях снижена, так как оксалоацетат используется для глюконеогенеза. В результате скорость образования ацетил-КоА превышает способность ЦТК окислять его. Ацетил-КоА накапливается в митохондриях печени и используется для синтеза кетоновых тел. Синтез кетоновых тел происходит только в митохондриях печени.
Синтез кетоновых тел начинается с взаимодействия двух молекул ацетил-КоА, которые под действием фермента тиолазы образуют ацетоацетил-КоА (рис. 8-33). С ацетоацетил-КоА взаимодействует третья молекула ацетил-КоА, образуя 3-гидрокси-3-метилглутарил-КоА (ГМГ-КоА). Эту реакцию катализирует фермент ГМГ-КоА-синтаза. Далее ГМГ-КоА-лиаза катализирует расщепление ГМГ-КоА на свободныйацетоацетат и ацетил-КоА.
Ацетоацетат может выделяться в кровь или превращаться в печени в другое кетоновое тело - β-гидроксибутират путём восстановления.
В клетках печени при активном β-окислении создаётся высокая концентрация NADH. Это способствует превращению большей части ацетоацетата в β-гидроксибутират, поэтому основное кетоновое тело в крови - именно β-гидроксибутират. При голодании для многих тканей жирные кислоты и кетоновые тела становятся основными топливными молекулами. Глюкоза используется в первую очередь нервной тканью и эритроцитами.
При высокой концентрации ацетоацетата часть его неферментативнодекарбоксилируется, превращаясь в ацетон. Ацетон не утилизируется тканями, но выделяется с выдыхаемым воздухом и мочой. Таким путём организм удаляет избыточное количество кетоновых тел, которые не успевают окисляться, но, являясь водорастворимыми кислотами, вызывают ацидоз.
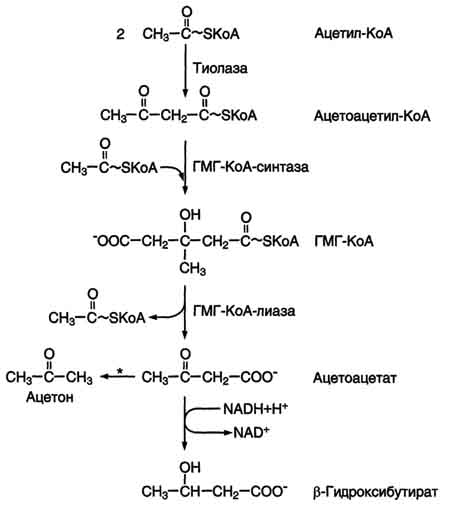
Рис. 8-33. Синтез кетоновых тел в митохондриях гепатоцитов. Регуляторный фермент синтеза кетоновых тел (ГМГ-КоА-синтаза) ингибируется свободным КоА. - реакция идёт неферментативно при высокой концентрации кетоновых тел в крови.
Регуляция синтеза кетоновых тел
. Регуляторный фермент синтеза кетоновых тел - ГМГ-КоАсинтаза.
ГМГ-КоА-синтаза - индуцируемый фермент; его синтез увеличивается при повышении концентрации жирных кислот в крови. Концентрация жирных кислот в крови увеличивается при мобилизации жиров из жировой ткани под действием глюкагона, адреналина, т.е. при голодании или физической работе.
ГМГ-КоА-синтаза ингибируется высокими концентрациями свободного кофермента А.
Когда поступление жирных кислот в клетки печени увеличивается, КоА связывается с ними, концентрация свободногоКоА снижается, и фермент становится активным.
Если поступление жирных кислот в клетки печени уменьшается, то, соответственно, увеличивается концентрация свободногоКоА, ингибирующего фермент. Следовательно, скорость синтеза кетоновых тел в печени зависит от поступления жирных кислот.
Окисление кетоновых тел в периферических тканях
При длительном голодании кетоновые тела становятся основным источником энергии для скелетных мышц, сердца и почек. Таким образом
глюкоза сохраняется для окисления в мозге и эритроцитах. Уже через 2-3 дня после начала голодания концентрация кетоновых тел в крови достаточна для того, чтобы они проходили в клетки мозга и окислялись, снижая его потребности в глюкозе.
β-Гидроксибутират (рис. 8-34), попадая в клетки, дегидрируется NAD-зависимой дегидрогеназой и превращается в ацетоацетат. Ацетоацетат активируется, взаимодействуя с сук-цинил-КоА - донором КоА:
Ацетоацетат + Сукцинил-КоА → Ацетоацетил-КоА + Сукцинат.
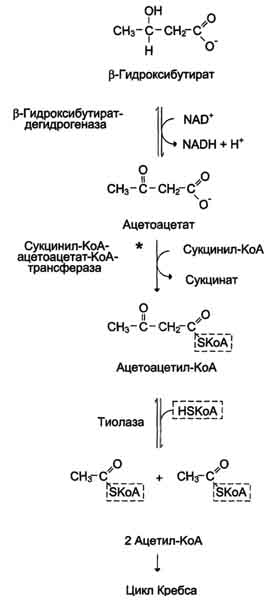
Рис. 8-34. Окисление кетоновых тел в тканях.
Реакцию катализирует сукцинил-КоА-ацето-ацетат-КоА-трансфераза. Этот фермент не синтезируется в печени, поэтому печень не использует кетоновые тела как источники энергии, а производит их "на экспорт". Кетоновые тела - хорошие топливные молекулы; окисление одной молекулы β-гидроксибутирата до СО2 и Н2О обеспечивает синтез 27 молекул АТФ. Эквивалент одной макроэргической связи АТФ (в молекуле сукцинил-КоА) используется на активацию ацетоацетата, поэтому суммарный выход АТФ при окислении одной молекулы β-гидроксибутирата - 26 молекул.
Кетоацидоз. В норме концентрация кетоновых тел в крови составляет 1-3 мг/дл (до 0,2 мМ/л), но при голодании значительно увеличивается. Увеличение концентрации кетоновых тел в крови называют кетонемией, выделение кетоновых тел с мочой - кетонурией. Накопление кетоновых тел в организме приводит к кетоацидозу: уменьшению щелочного резерва (компенсированному ацидозу), а в тяжёлых случаях - к сдвигу рН (некомпенсированному ацидозу), так как кетоновые тела (кроме ацетона) являются водорастворимыми органическими кислотами (рК~3,5), способными к диссоциации:
СН3-СО-СН2-СООН ↔ СН3-СО-СН2-СОО- + Н+.
Ацидоз достигает опасных величин при сахарном диабете, так как концентрация кетоновых тел при этом заболевании может доходить до 400-500 мг/дл. Тяжёлая форма ацидоза - одна из основных причин смерти при сахарном диабете. Накопление протонов в крови нарушает связывание кислорода гемоглобином, влияет на ионизацию функциональных групп белков, нарушая их кон-формацию и функцию.
