
- •Органическая химия
- •1. Классификация органических соединений
- •3. Типы химических реакций
- •Циклоалканы (циклопарафины)
- •1. Получение
- •2. Физические свойства
- •3. Химические свойства
- •Диеновые углеводороды (алкадиены)
- •1. Получение
- •2. Химические свойства
- •Ароматические углеводороды (арены)
- •1 Строение молекулы бензола
- •2. Изомерия и номенклатура
- •3. Получение
- •4. Химические свойства
- •5. Реакции присоединения. В реакции присоединения, приводящие к разрушению ароматической структуры бензольного кольца, арены могут вступать с большим трудом:
- •Галогенопроизводные углеводородов
- •1. Классификация
- •2. Изомерия и номенклатура
- •3. Получение
- •4. Физические свойства
- •5. Химические свойства
- •6. Применение
- •Карбоновые кислоты
- •Основные карбоновые кислоты
- •1. Изомерия
- •2. Получение
- •3. Физические свойства
- •4. Химические свойства
- •Азотсодержащие органические соединения
- •1 Амины
- •1. Номенклатура
- •2. Химические свойства
- •2 Ароматические амины
- •1. Анилин (фениламин)
- •1. Физические свойства
- •2. Химические свойства
- •Высокомолекулярные соединения (вмс) или полимеры
- •1. Физические свойства
- •2. Классификация
- •П олимеризационные полимеры
- •Поликонденсационные полимеры
- •3. Химические свойства
- •4. Применение
2. Изомерия и номенклатура
При замещении водородных атомов в молекуле бензола различными радикалами образуются гомологи бензола: метилбензол (толуол) и этилбензол, пропилбензол и т.д. Если в молекуле бензола атомы водорода замещены двумя радикалами, то образуются ор-
то-, мета- и пара-производные бензола. Другой способ наименования таких веществ состоит в том, что атомы углерода в формулах нумеруют. Обозначения орто, мета и пара пишут сокращенно: о-, м-, n-. Известны ароматические соединения, в боковых цепях которых имеются радикалы непредельных углеводородов. Простейшим представителем таких углеводородов является винилбензол, или стирол (С6Н5 ─ СН = СН2).
3. Получение
Важнейшими источниками ароматических углеводородов являются каменноугольная смола, газы, образующиеся при коксовании (пиролизе) углей, продукты переработки нефти.
1. Ученый Н. Д. Зелинский доказал, что бензол образуется из циклогексана, выделяемого из некоторых сортов нефти
С6Н12
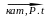 С6Н6 + 3Н2↑
С6Н6 + 3Н2↑
2. В присутствии оксидных катализаторов н-гексан тоже превращается в бензол
С6Н14 С6Н6 + 4Н2↑
3. Если пропустить ацетилен при 450—500 °С над активированным углем, то он превращается в бензол
3НС
≡ СН
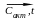 С6Н6
С6Н6
4. Перегонка солей бензойной кислоты со щелочами
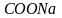


+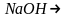 +
+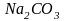
5. Гомологи бензола получают по реакции Шарля Вюрца (1817-1884) – Рудольфа Фиттига (1835-1910)
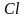
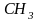
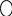
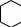 +2NaCℓ
+ CℓCH3 →
+ 2NaCℓ
+2NaCℓ
+ CℓCH3 →
+ 2NaCℓ
хлорбензол толуол
6. По реакции Шарля Фриделя (1832-1899) - Джеймса Крафтса (1839-1917) – Гавриила Гаврииловича Густавсона (1842-1908), реакции алкилирования бензола протекает по схеме
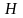
+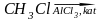 + НСℓ
+ НСℓ
бензол толуол
7. Алкилирование бензола непредельными соединениями протекает по схеме
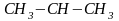
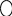 +
+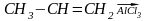
бензол изопропилбензол (кумол)
4. Химические свойства
По химическим свойствам арены отличаются от предельных и непредельных углеводородов. Это объясняется особенностями строения бензольного кольца. Делока-лизация шести π-электронов в циклической системе понижает энергию молекулы, что обусловливает повышенную устойчивость (ароматичность) бензола и его гомологов.
Поэтому арены не склонны вступать в реакции присоединения или окисления, которые ведут к нарушению ароматичности. Для них наиболее характерны реакции, идущие с сохранением ароматической системы, а именно, реакции замещения атомов водорода, связанных с циклом. Наличие областей повышенной π-электронной плотности с двух сторон плоского ароматического цикла ведет к тому, что бензольное кольцо является нуклеофилом и в связи с этим склонно подвергаться атаке электрофильным реагентом. Таким образом, для ароматических соединений наиболее типичны реакции электро-фильного замещения. Другие реакции (присоединение, окисление) идут с трудом:
1. Галогенирование. Замещение атома водорода в бензольном кольце на галоген происходит в присутствии катализаторов (кислот Гильберта Льюиса (1875-1946))
С6Н6
+ Cℓ2
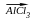 C6H5Cℓ
+ HCℓ
C6H5Cℓ
+ HCℓ
хлорбензол
2. Нитрование. Бензол реагирует с нитрующей смесью (смесью концентрированных азотной и серной кислот)
С6Н6
+ НОNO2
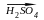 C6H5NO2
+ H2O
C6H5NO2
+ H2O
нитробензол
3. Алкилирование (реакция Фриделя-Крафтса). Замещение атома водорода в бен-зольном кольце на алкильную группу (алкилирование) происходит под действием алкилгалогенидов или алкенов в присутствии катализаторов (кислот Льюиса) (см. получение).
4. Реакции замещения производных бензола. Метильный радикал в молекуле толуола - донор электронов (индуктивное влияние (I+)) смещает электронную плотность в сторону бензольного кольца. Это приводит к повышению электронной плотности в орто- и пара-положениях, тем самым облегчая реакции электрофильного замещения в этих положениях. Поэтому, если бензол нитруется, галогенируется с образованием монозаме-щенных производных, то толуол нитруется и галогенируется, с образованием трех заме-щенных
 О2N
NO2
О2N
NO2
 +
+
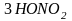 + 3Н2О
+ 3Н2О
NO2
тринитротолуол
