
- •Введение в физическую химию. История развития физической и коллоидной химии.
- •2. Понятие термодинамики. Системы, виды систем.
- •3.Параметры состояния системы. Экстенсивные и интенсивные параметры.
- •17.Внутренняя энергия и Энтальпия.
- •18.Изобарно-изотермический и изохорно изотермические потенциалы, и их формулы.
- •20.Теромодинамический критерий, характеризующий равновесие.
- •21.Смещение термодинамического равновесия. Принцип Ле-Шатлье.
- •24.Уравнение изохоры и изобары хим. Реакции.
- •26)Фазовое равновесие и основные термины.
- •28)Термический анализ.Построение кривых охлаждения.
- •29)Хар-ка понятий эвтектика,Эвт. Точка,Эвтектич. Температура.
- •30)Растворы. Концентрированные растворы.
- •31)Виды концентрации и формулы.
- •32)Осмотическое давление.
- •Реакция нулевого порядка
- •Реакция первого порядка
- •Реакция второго порядка
- •36. Формулы определения порядка химической реакции и кинетические уравнения.
- •37. Влияние температуры на скорость реакции. Аррениуса. Энергия активации.
- •39. Методы получения лиофобных коллоидных систем.
- •40. Методы получения лиофобных коллоидных систем: пептизация….
- •41.Классификация дисперсных систем по взаимодействию дисперсной фазы и дисперсной среды.
- •42.Классификация дисперсных систем по взаимодействию между частицами.
- •43. Молекулярно-кинетическое свойство коллоидных систем. Броуновское движение.
- •44. Диффузия в коллоидных системах. Закон Фика.
- •46)Уравнение Эйнштейна - Смолуковского.
- •47)Оптические свойства коллоидных систем. Уравнение Феллея и его применение.
- •Поверхностное явление работы Адгезии – когезии.
- •Уравнение Юнга. Правило смачивания.
- •Оптические свойства. Уравнение Бугера – Ламберта- Бера.
20.Теромодинамический критерий, характеризующий равновесие.
Состояние термодинамического равновесия называется устойчивым, если в этом состоянии не происходит изменения макроскопических параметров системы.
Критерии термодинамической устойчивости различных систем:
Изолированая (абсолютно не взаимодействующая с окружающей средой) система — максимум энтропии.
Замкнутая (обменивается с термостатом только теплом) система — минимум свободной энергии.
Система с фиксированными температурой и давлением — минимум потенциала Гиббса.
Система с фиксированными энтропией и объёмом — минимум внутренней энергии.
Система с фиксированными энтропией и давлением — минимум энтальпии.
21.Смещение термодинамического равновесия. Принцип Ле-Шатлье.
Принцип Ле Шателье — Брауна (1884 г.) — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия. Влияние температуры зависит от знака теплового эффекта реакции. При повышении температуры химическое равновесие смещается в направлении эндотермической реакции, при понижении температуры — в направлении экзотермической реакции. В общем же случае при изменении температуры химическое равновесие смещается в сторону процесса, знак изменения энтропии в котором совпадает со знаком изменения температуры. Зависимость константы равновесия от температуры в конденсированных системах описывается уравнением изобары Вант-Гоффа:
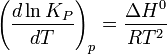
в системах с газовой фазой — уравнением изохоры Вант-Гоффа
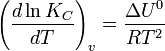
Давление существенно влияет на положение равновесия в реакциях с участием газообразных веществ, сопровождающихся изменением объёма за счёт изменения количества вещества при переходе от исходных веществ к продуктам: При повышении давления равновесие сдвигается в направлении, в котором уменьшается суммарное количество молей газов и наоборот. Введение в реакционную смесь или образование в ходе реакции инертных газов действует так же, как и понижение давления, поскольку понижается парциальное давление реагирующих веществ. Следует отметить, что в данном случае в качестве инертного газа рассматривается газ, не участвующий в реакции. В системах с уменьшением количества молей газов инертные газы смещают равновесие в сторону исходных веществ, поэтому в производственных процессах, в которых могут образовываться или накапливаться инертные газы, требуется периодическая продувка газоводов. Влияние концентрации на состояние равновесия подчиняется следующим правилам:
При повышении концентрации одного из исходных веществ равновесие сдвигается в направлении образования продуктов реакции; При повышении концентрации одного из продуктов реакции равновесие сдвигается в направлении образования исходных веществ.
22.Влияни концентрации и температуры на хим. равновесие. При увеличении температуры химическое равновесие смещается в сторону эндотермической (поглощение) реакции, а при понижении в сторону экзотермической (выделение) реакции.
CaCO3=CaO+CO2 -Q t↑ →, t↓ ←
N2+3H2↔2NH3 +Q t↑ ←, t↓ →
концентрация исходных веществ и продуктов реакции
При увеличении концентрации одного из исходных веществ химическое равновесие смещается в сторону продуктов реакции, а при увеличении концентрации продуктов реакции-в сторону исходных веществ.
S2+2O2=2SO2 [S],[O]↑ →, [SO2]↑ ←
23.Влияние давления на хим. равновесие. При увеличении давления химическое равновесие смещается в сторону меньшего объёма веществ, а при понижении в сторону большего объёма. Этот принцип действует только на газы, т.е. если в реакции участвуют твердые вещества, то они в расчет не берутся.
CaCO3=CaO+CO2 P↑ ←, P↓ →
1моль=1моль+1моль
