
1. Гидроксид хрома (VI) относится к классу неорганических соединений
1)кислая соль
2)основание
3)амфотерный гидроксид
+ 4)кислота
5)средняя соль
6)основная соль
2. Гидроксид хрома (III) относится к классу неорганических соединений:
1)кислая соль
2)основание
+ 3)амфотерный гидроксид
4)кислота
5)средняя соль
6)основная соль
3. Гидроксид железа (II) относится к классу неорганических соединений:
1)кислая соль
+ 2)основание
3)Амфотерный гидроксид
4)кислота
5)средняя соль
6)основная соль
4. С гидроксидом натрия реагирует
1)хлорид лития
2)сульфат натрия
+ 3)нитрат меди
+ 4)оксид серы (VI)
5)оксид меди (II)
6)гидроксид меди (II)
5. Реакция, уравнение которой СаСО3 + СО2 + Н2О = Са(НСО3)2 является реакцией
1)обмена
+ 2)соединения
3)разложения
4)замещения
5)окисления-восстановления
6. Реакция, уравнение которой 2NаНСО3 = Nа2СО3 + СО2 + Н2О является реакцией
1)Обмена
2)соединения
+ 3)разложения
4)Замещения
5)окисления-восстановления
7. Реакция, уравнение которой Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O относится к реакциям
+ 1)обмена
2)Соединения
3)разложения
4)замещения
5)окисления-восстановления
8. Гидроксиды, формулы которых KOH и Al(OH)3, являются по характеру свойств соответственно
1)кислота и основание
+ 2)основание и амфотерный гидроксид
3)основание и кислота
4)амфотерный гидроксид и кислота
5)кислота и амфотерный гидрокисд
6)амфотерный гидроксид и основание
9. Гидроксиды, формулы которых H2SO4 и Be(OH)2, являются по характеру свойств соответственно
1)кислота и основание
2)основание и амфотерный гидроксид
3)основание и кислота
4)амфотерный гидроксид и кислота
+ 5)кислота и амфотерный гидрокисд
6)амфотерный гидроксид и основание
10. Гидроксиды, формулы которых Cu(OH)2 и H2CrO4, являются по характеру свойств соответственно
1)кислота и основание
2)основание и амфотерный гидроксид
+ 3)основание и кислота
4)амфотерный гидроксид и кислота
5)кислота и амфотерный гидрокисд
6)амфотерный гидроксид и основание
11. Гидроксиды, формулы которых HMnO4 и Ba(OH)2, являются по характеру свойств соответственно
+ 1)кислота и основание
2)основание и амфотерный гидроксид
3)основание и кислота
4)амфотерный гидроксид и кислота
5)кислота и амфотерный гидрокисд
6)амфотерный гидроксид и основание
12. Какая группа веществ состоит только из оснований:
1)Cu(OH)2, (CuOH)2SO4, H2SO4
2)NaOH, Na2O, Na2SO4
+ 3)NaOH, Cu(OH)2, Ca(OH)2
4)Ca(OH)2, CaO, CaCO3
5)NaOH, Cu(OH)2, CaCO3
6)(CaOH)2CO3, CaSO4, NaOH
13. Для какого соединения фактор эквивалентности равен 1/3
1)CuSO4
2)Al2(SO4)3
+ 3)Al(OH)3
4)CaO
5)Al2O3
6)HNO3
14. Чему равен фактор эквивалентности Н4Р2О7 при взаимодействии кислоты с одним молем NаОН
ОТВЕТ: 1/4
15. Чему равна молярная масса эквивалента ортофосфорной кислоты (г/моль) при взаимодействии ее с двумя молями NаОН
ОТВЕТ: 49
16. Чему равен фактор эквивалентности Н4Р2О7 при взаимодействии кислоты с двумя моль NаОН
ОТВЕТ: 1/2
17. Химический элемент - это:
1)совокупность одинаковых молекул
+ 2)совокупность атомов с одинаковым зарядом ядра
3)простое вещество
4)вид атомов
5)чистое вещество
6)электронейтральная неделимая частица
18. Молекулы - это:
1)химически неделимые частицы, из которых состоят вещества
+ 2)электронейтральные частицы вещества, определяющие его химические свойства
3)частицы, до которых разрушаются все вещества при плавлении и испарении
4)частицы, до которых разрушаются вещества при химических явлениях
5)совокупность атомов с одинаковым зарядом ядра
6)положительно заряженные элементарные частицы
19. Атом - это:
1)наименьшая частица вещества, сохраняющая его свойства
+ 2)наименьшая частица элемента, сохраняющая его свойства
3)электронейтральная неделимая частица вещества
4)положительно заряженная частица вещества
5)частица, до которой разрушаются все вещества
20. Какой из химических терминов определяет «простое вещество»:
1)чистое вещество
+ 2)вещество, построенное атомами одного химического элемента
3)вещество, построенное атомами разных химических элементов
4)отдельные атомы одного химического элемента
5)совокупность атомов с одинаковым зарядом ядра
6)вид атомов
21. Количество вещества - это:
+ 1)отношение массы вещества к его молярной массе
2)отношение молярной массы вещества к его массе
3)отношение молярного объема газообразного вещества к его объему
4)произведение числа Авогадро на число молекул
5)совокупность одинаковых молекул
6)совокупность атомов с одинаковым зарядом ядра
22. Формула сернистого газа:
1)H2S
+ 2)SO2
3)SO3
4)S8
5)H2SO3
6)H2S2O3
23. Кислотными являются оксиды
1)только металлов
2)только неметаллов
+ 3)металлов с высокой валентностью и неметаллов
4)металлов с низкой валентностью и неметаллов
5)взаимодействующие с водой
6)взаимодействующие с водой с образованием кислоты
24. Формуле соли Ba(HSO3)2 соответствует название:
ОТВЕТ: гидросульфит бария
25. Какой оксид является ангидридом азотной кислоты
1)N2O
2)NO
3)N2O3
4)NO2
5)N2O4
+ 6)N2O5
26. Только кислотные оксиды содержатся в ряду
1)ZnO, CO2, N2O
2)CO, SiO2, SnO2
+ 3)CrO3, N2O3, SiO2
4)N2O5, P2O3, Cs2O
5)NO2, P2O5, SO3
6)CaO, Al2O3, Mn2O7
27. При взаимодействии хрома с соляной кислотой образуются
+ 1)CrCl2 и H2
2)CrCl3 и H2O
3)CrCl2 и H2O
4)CrCl3 и H2
5)CrO и H2
6)Cr2O3 и H2
28. Оксид кремния реагирует с
1)карбонатом натрия
2)фтороводородной кислотой
3)сульфатом меди
4)магнием
5)водой
+ 6)гидроксидом калия
29. С каким из веществ будет реагировать SO2
1)H2SiO3
2)NaCl
3)CrO3
4)KNO3
+ 5)KOH
6)P2O5
30. Какой кислоте соответствует формула оксида фосфора Р2О3
1)НРО3
+ 2)Н3РО3
3)Н3РО4
4)Н4Р2О7
5)Н3РО2
31. Гидроксид железа (II) реагирует с
1)KOH
2)NaCl
3)Ca(OH)2
+ 4)H2SO4
5)Na2O
6)Cu(OH)2
32. При прокаливании Cr(OH)3 образуется
1)Cr2O3 и H2
+ 2)Cr2O3 и H2О
3)CrO и H2
4)CrO и H2О
5)CrO3 и H2
6)CrO3 и H2О
33. Чему равно количество вещества аммиака (моль), массой 1 г (округлять до сотых долей)_____
ОТВЕТ: 0,06
34. Какова масса (г) 2 л водорода (округлять до сотых долей)______
ОТВЕТ: 0,18
35. Сумма коэффициентов в уравнении реакции взаимодействия гидроксида натрия с сульфатом меди______
ОТВЕТ: 5
36. Чему равна плотность хлора по воздуху ( округлить до сотых)_______
ОТВЕТ: 2,45
37. Масса 2,24 л газа (условия нормальные) равна 2,8 г. Чему равна молекулярная масса газа (г/моль)______
ОТВЕТ: 28
38. Какой объем (л) при нормальных условиях занимают 27·1021 молекул газа____
ОТВЕТ: 1
39. Какова формула соединения азота с кислородом, если плотность этого газа по водороду равна 15
+ 1)NO
2)N2O
3)N2O3
4)NO2
5)N2O4
6)N2O5
40.
В цепочке превращений
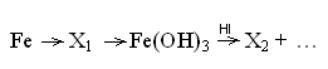 веществами
Х1
и Х2
являются…
веществами
Х1
и Х2
являются…
1)Fe(OH)2 и FeI3
2)FeCl3 и Fe2O3
+ 3)FeCl3 и FeI2
4)FeSO4 и Fe
5)Fe2O3 и FeI3
6)FeCl3 и Fe
41.
Для цепочки превращений конечным
веществом
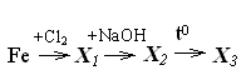 Х3
является
Х3
является
+ 1)Fe2O3
2)Fe(OH)2
3)Fe(OH)3
4)FeO
5)Fe3O4
42. При взаимодействии оксида серы (IV) с избытком раствора NaOH образуется
+ 1)Na2SO3 и H2O
2)NaHSO3
