
- •«Молекулярные основы биоэнергетических процессов и общие пути катаболизма в организме человека . Ферменты»
- •Мультиферментные комплексы
- •Факторы, влияющие на скорость ферментативных реакций
- •Способы регуляции активности ферментов
- •Ковалентная (химическая) модификация
- •Диагностика энзима в моче
- •1. Обратимое 2. НеобратимоеА. Конкурентное а. Специфическое б. Неконкурентное б. Неспецифическое
- •Наследственные энзимопатии по типу нарушений метаболизма делят на:
- •Стадии метаболизма
- •Обмен веществ.Метаболические пути. Унификация питательных веществ.
- •Роль в организме
- •Энергетический эффект цикла Кребса Итак, при распаде 1 моль ацетил-КоА образуется 12 моль атф, следовательно, из 2 моль ацетил-КоА - 24 моль атф.
- •Механизм : Окислительное фосфорилирование
- •Специфические и общие пути катаболизма
- •Окислительное декарбоксилирование пировиноградной кислоты (пвк)
- •Окислительное декарбоксилирование пировиноградной кислоты (пвк)
Окислительное декарбоксилирование пировиноградной кислоты (пвк)
Окисление ПВК до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс».
Процесс окислительного декарбоксилирования ПВК происходит в матриксе митохондрий. В нем принимают участие (в составе пируватдегидрогеназного комплекса) 3 фермента (пируватдегидрогеназа, дигидролипоилдегидрогеназа и дигидролипоилацетилтрансфераза) и 5 коферментов (тиаминпирофосфат (ТПФ (витамин В1)), амид липоевой кислоты, коэнзим А (СоА (витамин В3)), ФАД (флавинадениндинуклеотид (витамин В2)),НАД+(никотинамидадениндинуклеотид (витамин РР)).
Суммарную реакцию, катализируемую пируватдегидрогеназным комплексом, можно представить следующим образом:

Образовавшийся в процессе окислительного декарбоксилирования ацетил-СоА окисляется далее в цикле трикарбоновых кислот с образованием СО2 и АТФ.
42.Окислительное декарбоксилирование пировиноградной кислоты. Его биологическое значение.
Окислительное декарбоксилирование пировиноградной кислоты (пвк)
Окисление ПВК до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс».
Процесс окислительного декарбоксилирования ПВК происходит в матриксе митохондрий. В нем принимают участие (в составе пируватдегидрогеназного комплекса) 3 фермента (пируватдегидрогеназа, дигидролипоилдегидрогеназа и дигидролипоилацетилтрансфераза) и 5 коферментов (тиаминпирофосфат (ТПФ (витамин В1)), амид липоевой кислоты, коэнзим А (СоА (витамин В3)), ФАД (флавинадениндинуклеотид (витамин В2)),НАД+(никотинамидадениндинуклеотид (витамин РР)).
Суммарную реакцию, катализируемую пируватдегидрогеназным комплексом, можно представить следующим образом:

Образовавшийся в процессе окислительного декарбоксилирования ацетил-СоА окисляется далее в цикле трикарбоновых кислот с образованием СО2 и АТФ.
Биологическая роль окислительного декарбоксилирования пирувата заключается в том, что оно является важным этапом катаболизма, позволяющим включаться в цикл Кребса тем веществам, при распаде которых образуется ПВК. Образовавшаяся молекула НАДН2 окисляется в длинной дыхательной цепи с образованием 3-х молекул АТФ. Окислительное декарбоксилирование пирувата протекает внутри митохондрий.
43.Специфические и общие пути катаболизма углеводов, липидов, белков. Цикл трикарбоновых кислот (цикл Кребса), его роль в обмене углеводов, липидов, аминокислот.
В катаболизме различают три стадии:
1). Полимеры превращаются в мономеры (белки – в аминокислоты, углеводы в моносахариды, липиды – в глицерол и жирные кислоты). Химическая энергия при этом рассеивается в виде тепла.
2). Мономеры превращаются в общие продукты, в подавляющем большинстве в ацетил-КоА. Химическая энергия частично рассеивается в виде тепла, частично накапливается в виде восстановленных коферментных форм (НАДН, ФАДН2), частично запасается в макроэргических связях АТФ (субстратное фосфорилирование).
1-ая и 2-ая стадии катаболизма относятся к специфическим путям, которые уникальны для метаболизма белков, липидов и углеводов.
3). Заключительный этап катаболизма, сводится к окислению ацетил-КоА до СО2 и Н2О в реакциях цикла трикарбоновых кислот (цикла Кребса) – общий путь катаболизма. Окислительные реакции общего пути катаболизма сопряжены с цепью тканевого дыхания. При этом энергия (40-45%) запасается в виде АТФ (окислительное фосфорилирование).
В результате специфических и общих путей катаболизма биополимеры (белки, углеводы, липиды) распадаются до СО2, Н2О и NH3, которые являются основными конечными продуктами катаболизма.
ЦИКЛ КРЕБСА(цикл лимонной и трикарбоновой кислот), система биохимических реакций, посредством которой большинство организмов ЭУКАРИОТОВ получают основную энергию в результате окисления пищи. Происходит в КЛЕТКАХ МИТОХОНДРИЙ. Включает несколько химических реакций, в результате которых высвобождается энергия. Этот процесс называется системой ПЕРЕНОСА ЭЛЕКТРОНОВ по аналогии с переходом АДЕНОЗИНТРИФОСФАТА (АТФ) в АДЕНОЗИН ДИФОСФАТ (АДФ). АТФ обеспечивает реакции МЕТАБОЛИЗМА химической энергией. Цикл Кребса важная часть процесса ДЫХАНИЯ и ОБМЕНА ВЕЩЕСТВ клетки.
Цикл трикарбоновых кислот (цикл Кребса)
образовавшийся в результате окислительного декарбоксилирования пирувата ацетил-КоА вступает в цикл Кребса. Данный цикл состоит из восьми последовательных реакций
В первой реакции, катализируемой ферментом цитратсинтазой, ацетил-КоА конденсируется с оксалоацетатом. В результате образуется лимонная кислота:
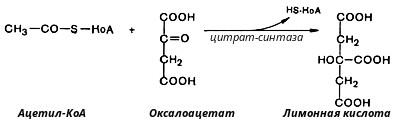
По-видимому, в данной реакции в качестве промежуточного продукта образуется связанный с ферментом цитрил-КоА. Затем последний самопроизвольно и необратимо гидролизуется с образованием цитрата и HS-KoA.
Во второй реакции цикла образовавшаяся лимонная кислота подвергается дегидратированию с образованием цис-аконитовой кислоты, которая, присоединяя молекулу воды, переходит в изолимонную кислоту. Катализирует эти обратимые реакции гидратации-дегидратации фермент аконитат-гидратаза:

В третьей реакции, которая, по-видимому, лимитирует скорость цикла Кребса, изолимонная кислота дегидрируется в присутствии НАД-зависимой изоцитратдегидрогеназы:

(В тканях существует два типа изоцитратдегидрогеназ: НАД- и НАДФ-зависимые. Установлено, что роль основного катализатора окисления изолимонной кислоты в цикле Кребса выполняет НАД-зависимая изоцитратдегидрогеназа.)
В ходе изоцитратдегидрогеназной реакции изолимонная кислота декарбоксилируется. НАД-зависимая изоцитратдегидрогеназа является аллостерическим ферментом, которому в качестве специфического активатора необходим АДФ. Кроме того, фермент для проявления своей активности нуждается в ионах Mg2+или Мn2+.
В четвертой реакции происходит окислительное декарбоксилирование α-кетоглутаровой кислоты до сукцинил-КоА. Механизм этой реакции сходен с реакцией окислительного декарбоксилирования пирувата до ацетил-КоА. α-Кетоглутаратдегидрогеназный комплекс напоминает по своей структуре пируватдегидрогеназный комплекс. Как в одном, так и в другом случае в ходе реакции принимают участие пять коферментов: TДФ, амид липоевой кислоты, HS-KoA, ФАД и НАД. Суммарно данную реакцию можно написать так:

Пятая реакция катализируется ферментом сукцинил-КоА-синтетазой. В ходе этой реакции сукцинил-КоА при участии ГДФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Одновременно происходит образование высокоэргической фосфатной связи ГТФ1 за счет высокоэргической тиоэфирной связи сукцинил-КоА:

(Образовавшийся ГТФ отдает затем свою концевую фосфатную группу на АДФ, вследствие чего образуется АТФ. Образование высокоэргического нуклеозидтрифосфата в ходе сукцинил-КоА-синтетазной реакции - пример фосфорилирования на уровне субстрата.)
В шестой реакции сукцинат дегидрируется в фумаровую кислоту. Окисление сукцината катализируется сукцинатдегидрогеназой, в молекуле которой с белком ковалентно связан кофермент ФАД:

В седьмой реакции образовавшаяся фумаровая кислота гидратируется под влиянием фермента фумаратгидратазы. Продуктом данной реакции является яблочная кислота (малат). Следует отметить, что фумаратгидратаза обладает стереоспецифичностью, - в ходе данной реакции образуется L-яблочная кислота:

Наконец, в восьмой реакции цикла трикарбоновых кислот под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат:

Как видно, за один оборот цикла, состоящего из восьми ферментативных реакций, происходит полное окисление ("сгорание") одной молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА, а коферменты (НАД и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться. Это окисление осуществляется в системе переносчиков электронов (или в цепи дыхательных ферментов), локализованной в митохондриях.


СВЯЗЬ МЕЖДУ ОБМЕНОМ УГЛЕВОДОВ И ЖИРОВ
Единство в обмене углеводов и жиров доказывается возникновением общих промежуточных продуктов распада. При распаде углеводов образуется пировиноградная кислота, а из нее -активная уксусная кислота -ацетил-КоА, который может быть использован в синтезе жирных кислот. Последние при своем распаде дают ацетил-КоА.
