
Биохимия.ру полный курс лекций
.pdf
biokhimija.ru |
Тимин О.А. Лекции по биологической химии |
331 |
|
|
|
ФИЗИОЛОГИЧЕСКИЕ СИСТЕМЫ
Удаление кислоты через легкие
Газообмен в легких заключается в постоянном обмене кислородом и углекислым газом между двумя соприкасающимися компартментами – легочными альвеолами и кровеносными капиллярами. (см Газообмен в легких и тканях)
Углекислый газ быстро диффундирует из плазмы и эритроцитов в альвеолярное пространство. В то же время в альвеолярном воздухе имеется высокая концентрация кислорода, который, проникая в эритроциты, вытесняет СО2 из комплекса с гемоглобином с образованием оксигемоглобина – более сильной кислоты, чем угольная. "Кислый" оксигемоглобин отдает ионы Н+ в ассоциацию с ионом HCO3–, образуется H2CO3, которая вступает в карбоангидразную реакцию с появлением СО2, удаляемого в плазму и в альвеолы.
Таким образом, легочная вентиляция обеспечивает удаление H2CO3 и повышение уровня pH. Она работает в тесном контакте с гемоглобиновой и бикарбонатной буферной системами.
Главным фактором для активации дыхательной системы является концентрация ионов Н+, влияющих на рецепторы в каротидных тельцах. Закисление крови уже через 1-2 минуты вызывает стимуляцию дыхательного центра, повышая его активность в 4-5 раз. Снижение кислотности крови понижает активность дыхательного центра в 2-4 раза.
Чувствительные хеморецепторы для CO2 находятся в продолговатом мозгу, аортальном и каротидных тельцах.
Сдвиги концентрации O2 в крови не являются существенными для изменения легочной вентиляции. Но в случае хронической гиперкапнии (увеличении CO2) рецепторы дыхательного центра теряют чувствительность к CO2 (десенсибилизация) и низкое pO2 становится основным стимулом. Также избирательное снижение кислорода в артериальной крови на 40% от нормы стимулирует активность дыхательного центра.
Удаление кислоты через почки
Почки играют ведущую роль в регуляции уровня рН плазмы крови. Движущей силой в почечных влияниях на уровень pH играют потоки ионов Na+. Ионы Na+ перемещаются внутрь клеток по концентрационному градиенту, который создается при работе фермента Na+/К+-АТФазы на базолатеральной мембране.
Благодаря почкам
o регулируется концентрация ионов HCO3- в плазме крови,
o удаляются ионы Н+ в мочу в реакциях ацидогенеза и аммониегенеза.
Здесь активно протекают три процесса, связанных с уборкой кислых эквивалентов: o Реабсорбция бикарбонатных ионов HCO3–.
o Ацидогенез – удаление ионов Н+ с титруемыми кислотами (в основном в составе дигидрофосфатов H2PO4–).
o Аммониегенез – удаление ионов Н+ в составе ионов аммония NH4+.
Реабсорбция бикарбонат-ионов
Ионы HCO3–, находящиеся в плазме крови, непрерывно фильтруются и оказываются в первичной моче.
Одновременно в канальцевую жидкость при участии Na+/H+-обменника из эпителиоцитов активно выводятся ионы H+ в обмен на ионы Na+.

Кислотно-основное состояние |
332 |
|
|
Секретируемые ионы Н+ и ионы HCO3–, находящиеся в первичной моче, ассоциируют до угольной кислоты Н2СО3, которая распадается на СО2 и H2O. Используя возникающий градиент концентрации между просветом канальцев и цитозолем эпителиоцитов, СО2 диффундирует в клетки. Внутриклеточная карбоангидраза направляет входящий СО2 для образования угольной кислоты. После диссоциации кислоты ионы НСО3– выносятся в кровь, подщелачивая ее, ионы Н+ секретируются обратно в мочу. В итоге происходит обратное всасывание ионов НСО3–, при этом каждый добавляемый в плазму НСО3– соответствует экскреции одного иона Н+.
Пороговое значение реабсорбции бикарбонатов соответствует их нормальной концентрации в крови. Это значит, что при превышении нормального уровня бикарбонаты не будут реабсорбироваться и окажутся в моче.
Впроксимальных канальцах реабсорбируется 80% профильтрованного НСО3–. В целом
впочечных канальцах происходит реабсорбция более 99% от фильтруемого бикарбонатиона.
Ацидогенез
В процессе ацидогенеза в сутки выделяется 10-30 ммоль кислотных веществ, названных титруемыми кислотами. Фосфаты, являясь одной из этих кислот, играют роль буферной системы в моче. Роль ее состоит в экскреции кислых эквивалентов без потерь бикарбонатионов за счет дополнительного иона H+ в составе выводимого H2РO4– (по сравнению с
HCO3):
HРO42– + Н2СО3 H2РO4– + НСО3
biokhimija.ru |
Тимин О.А. Лекции по биологической химии |
333 |
|
|
|
Бикарбонат натрия в почечных канальцах реабсорбируется, а кислотно-основная реакция мочи зависит только от содержания дигидрофосфата. Хотя в крови соотношение HРO42–/ H2РO4– равно 4:1, начиная от клубочкового фильтрата к дистальным канальцам оно может достигать 50-кратного перевеса доли ионов H2РO4– (1:50).
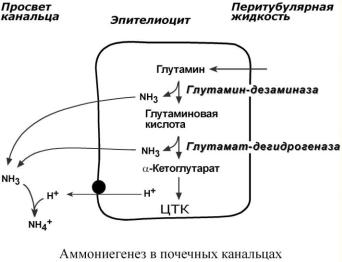
Аммониегенез
Аммониегенез происходит на протяжении всего почечного канальца, но более активно идет в дистальных отделах – дистальных канальцах и собирательных трубочках коркового и мозгового слоев. В этих сегментах секреция ионов Н+ происходит активно с участием Н+-АТФазы, локализованной на апикальной мембране эпителиоцита.
Глутамин и глутаминовая кислота, попадая в клетки канальцев, быстро дезаминируются глутаминазой и глутаматдегидрогеназой с образованием аммиака. Являясь гидрофобным соединением, аммиак диффундирует в просвет канальца и связывает экскретируемые ионы Н+ с образованием иона NH4+ , который удаляется с мочой.
Влияние костной ткани
Это наиболее медленно реагирующая система. Механизм ее участия в регуляции рН крови состоит в возможности обмениваться с плазмой крови ионами Са2+ и Na+ в обмен на протоны Н+. Происходит растворение гидроксиапатитных кальциевых солей костного матрикса, освобождение ионов Са2+ и связывание ионов HPO42– с Н+ с образованием дигидрофосфата, который уходит с мочой.
8Н+ + Ca10(PO4)6(OH)2 → 2H2O + 10Ca2+ + 6HPO42––
Параллельно при снижении рН (закисление) происходит поступление ионов H++внутрь остеоцитов, а ионов K+ – наружу.
Печень
Существенную, но пассивную роль в регуляции кислотно-основного состояния крови берет на себя печень, в которой происходит метаболизм низкомолекулярных органических кислот (молочная кислота и др). Кроме этого, кислые и щелочные эквиваленты выделяются с желчью.
Г А З Ы К Р О В И
Несмотря на то, что исследование кислотно-основного состояния, строго говоря, подразумевает исследование только величины pH (концентрации ионов H+), в реальности в него также включается исследование физиологически важных газов, присутствующих в крови –
Кислотно-основное состояние |
334 |
|
|
O2 и CO2. Анализ газов показывает эффективность газообмена по величинам парциальных давлений – pO2 и pCO2.
Величина парциального давления – это процентная доля газа в общем объеме.
Газы атмосферного воздуха поступают в кровь диффузно через альвеолярную мембрану. Молекулы O2 поступают из альвеол в кровь, а молекулы CO2 из крови в альвеолы пока парциальные давления не выровняются.
КИСЛОРОД
Вопросы, связанные с оксигенацией крови и транспортом кислорода довольно сложны. Связано это с тем, что в виде свободных (растворенных) молекул O2 находится лишь небольшая доля общего кислорода крови. Поэтому показатель pO2 не отражает содержание кислорода в крови!
Основная часть кислорода связана с гемоглобином (Hb) и истинное содержание кислорода в крови зависит от двух дополнительных параметров – концентрации Hb и сатурации гемоглобина (насыщении) кислородом (HbOsat или SO2). Показатель насыщения кислородом показывает процент доступных мест связывания на гемоглобине.
Оксигемоглобин
Оксигемоглобин (HbО2) – процентное содержание в крови, является отношением фракции оксигемоглобина (HbО2) к сумме всех фракций (общему гемоглобину).
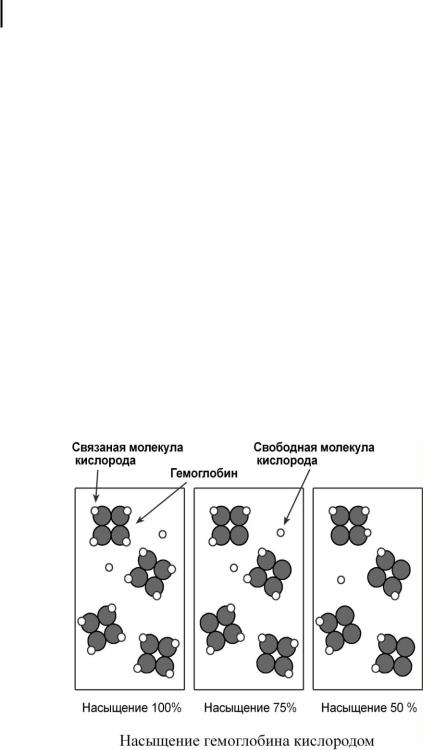
Насыщение гемоглобина кислородом
Насыщение (сатурация) гемоглобина кислородом (HbOSAT, SО2), представляет собой отношение фракции оксигенированного гемоглобина к тому количеству гемоглобина в крови, который способен транспортировать О2.
Отличия между двумя показателями HbО2 и HbOSAT заключаются в том, что у пациентов возможно наличие в крови фракции такой формы гемоглобина, которая не способна акцептировать О2 (Hb-CO, metHb, сульфоHb). Например, если при отравлении нитритами количество metHb составляет 15%, тогда величина HbО2 никогда не сможет превысить 85%, но насыщение (HbOsat) может быть различно – от максимума (HbOsat=95-98%) при полном насыщении до низких величин при отсутствии кислорода.
Но так как большинство больных не имеют в крови повышенного содержания этих форм гемоглобина, значения HbО2 и SО2 обычно очень близки.
biokhimija.ru |
Тимин О.А. Лекции по биологической химии |
335 |
|
|
|
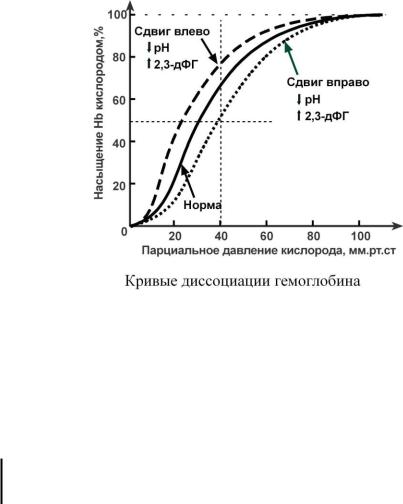
Парциальное давление O2 выступает как движущая сила, приводящая к насыщению гемоглобина кислородом. Хотя в целом, чем выше pO2 тем выше HbOsat, эта зависимость не является линейной.
В центральной части кривой диссоциации малейшие сдвиги pO2 приводят к резким изменениям насыщения гемоглобина. И наоборот, при высоком pO2 (70-90 мм рт.ст) кривая становится плоской, насыщение гемоглобина практически не зависит от количества кислорода в плазме.
Сдвиг влево происходит при защелачивании и снижении концентрации 2,3-дифосфоглицерата и сигнализирует о повышении сродства кислорода к гемоглобину (в легких). Сдвиг вправо - это снижение сродства кислорода к гемоглобину (в тканях), обеспечивается закислением среды и накоплением 2,3-дифосфоглицерата.
Хотя pO2 не показывает количество кислорода в крови, но это количество зависит от pO2 через показатель сатурации гемоглобина.
В свою очередь имеются факторы, влияющие на величину pO2:
1.Альвеолярная вентиляция. Хотя она влияет как на pO2 так и на pCO2, но доля кислорода в альвеолах при гипервентиляции может лишь слегка увеличиться, приближаясь к
pO2 атмосферного воздуха, при гиповентиляции – стремительно падает, вытесняясь CO2. В то же время доля pCO2 быстро снижается при усиленной вентиляции.
2.Вентиляционно-перфузионное соотношение, определяется тем, что
oне вся кровь, притекающая к легким, соприкасается с хорошо вентилируемыми альвеолами (спадение,альвеол, уплотнение).
oне все хорошо вентилируемые альвеолы получают достаточно крови.
3.Концентрация кислорода во вдыхаемом воздухе (FiO2, fraction of inspired oxygen).
УГЛЕКИСЛЫЙ ГАЗ
Концентрация СО2 в альволярном воздухе столь низка, а в крови столь высока, что диффузия этого газа в альвеолы чрезвычайно эффективна и скорость его удаления зависит только от альвеолярной вентиляции – общего объема воздуха, транспортируемого в минуту между альвеолами и атмосферой ("скорости выдувания").
Следовательно, при усиленной вентиляции легких углекислый газ выводится, и показатель pCO2 в крови снижается. Это автоматически означает потерю организмом угольной кислоты (ионов H+), что является причиной защелачивания крови – алкалоза, называемого дыхательным или респираторным. Повышение концентрации СО2 в крови свидетельствует
Кислотно-основное состояние |
336 |
|
|
о недостаточной альвеолярной вентиляции; в этом случае повышение показателя рСО2 в кро-
ви является причиной дыхательного ацидоза.
Б У Ф Е Р Н Ы Е О С Н О В А Н И Я
Общим показателем, характеризующим КОС, является концентрация буферных оснований (bufer bases, ВВ), включающая сумму всех оснований крови, хотя большую часть этих оснований представляют анионы бикарбоната и белковые анионы.
Более узким показателем является концентрация бикарбонат-ионов. При дыхательных нарушениях количество бикарбонатов мало изменяется, т.к. угольная кислота, образуемая из CO2, очень плохо диссоциирует и изменение ее концентрации не влияет на содержание иона HCO3-. Но, например, при накоплении в крови метаболических кислот (молочной кислоты) ион HCO3- будет активно расходоваться на их буферизацию, показатель снизится.
На практике главным и наиболее информативным показателем служит избыток буферных оснований (base excess, BE). Изменение величины BE отражает степень использования буферных оснований для удержания гомеостаза при смещении уровня ионов H+. При алкалозе использование буферных оснований не требуется, показатель возрастает. При закислении среды основания расходуются и показатель BE снижается, т.е. возникает дефицит оснований.
О С Т А Т О Ч Н Ы Е А Н И О Н Ы
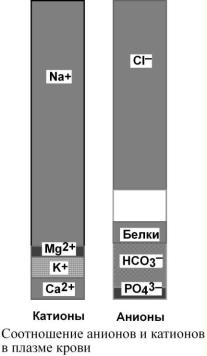
Если посчитать сумму всех ионных зарядов в плазме крови, будет обнаружено, что количество положительных зарядов равно количеству отрицательных зарядов. Данный закон электронейтральности иллюстрируется диаграммой Gamble. Смысл диаграммы в том, что общий заряд анионов, представленных в плазме в довольно высоких концентрациях (Cl–,
HCO3–, белки) и обычно измеряемых в лабораториях, не полностью нейтрализует измеряе-
мые катионы (Na+, K+, Ca2+, Mg2+).
Катионы (мэкв/л) |
Анионы (мэкв/л) |
||
|
|
|
|
Na+ |
140 |
Cl– |
100 |
|
|
|
|
2+ |
1,5 |
Белки |
15 |
Mg |
|||
|
|
|
|
K+ |
4,5 |
HCO3– |
24 |
|
|
|
|
2+ |
5,0 |
3– |
3 |
Ca |
PO4 |
||
|
|
Остаточные |
12 |
|
|
анионы |
|
|
|
|
|
Всего |
151 |
Всего |
151 |
Часть анионов остается "за кадром", это и есть т.н. неизмеряемые или остаточные анионы (ОА) или, что то же самое, анионный интервал (АИ). Остаточные анионы представлены анионами органических (молочная, щавелевая, мочевая и др.) и неорганических (серная и др.) кислот. Остаточные анионы (или анионный интервал) отражают накопление
biokhimija.ru |
Тимин О.А. Лекции по биологической химии |
337 |
|
|
|
каких-либо кислот в плазме крови. Они возрастают при кетоацидозе (анионы ацетоуксусной и -гидроксимасляной кислот), лактоацидозе (лактат-анионы), отравлении этанолом (ацетатанионы), интоксикациях (салицилаты, метанол, этиленгликоль).
ОСНОВНЫЕ ПОКАЗАТЕЛИ КИСЛОТНО-ОСНОВНОГО СОСТОЯНИЯ
Показа- |
|
Характеристика |
Нормальные |
|
тель |
|
|
величины |
|
|
Отрицательный десятичный логарифм концентрации во- |
7,37-7,44 (артерии) |
||
|
дородных |
ионов. Главный показатель кислотно- |
||
рН |
|
|||
основного состояния, характеризует состояние алкалоза |
|
|||
|
7,34-7,43 (вены) |
|||
|
или ацидоза. |
|||
|
|
|||
|
Парциальное давление углекислого газа. Показывает |
|
||
рСО2 |
суммарную концентрацию СО2, растворенного в плазме |
35-45 мм рт. ст. |
||
крови, H2CO3 и HCO3-. Основной критерий дыхательных |
||||
|
|
|||
|
нарушений. |
|
||
|
Парциальное давление кислорода. Показывает концен- |
|
||
рО2 |
трацию О2 |
растворенного в плазме крови. Основной кри- |
83-108 мм рт. ст. |
|
|
терий при характеристике гипоксии. |
|
||
ВВ |
Буферные |
основания. Показывает концентрацию всех |
43,7-53,5 ммоль/л |
|
буферных оснований в цельной крови. |
||||
|
|
|||
|
концентрация бикарбонат-ионов. Показывает количество |
|
||
[HCO3-] |
бикарбонат-ионов в плазме крови. Основной критерий |
21-24 ммоль/л |
||
|
для диагностики метаболических нарушений. |
|
||
|
Избыток оснований. Показывает колебания количества |
|
||
|
основных эквивалентов. Положительные величины сви- |
|
||
BE |
детельствуют о дефиците кислот и потере ионов Н+. |
0 2,5 ммоль/л |
||
|
Отрицательные величины говорят об избытке некарбо- |
|
||
|
новых кислот и ионов Н+. |
|
||
|
Остаточные анионы (анионный интервал). Показывает |
|
||
ОА (АИ) |
накопление каких-либо кислот (кроме угольной и соля- |
12 4 ммоль/л |
||
|
ной) в плазме крови. |
|
||
НА Р У Ш Е Н И Я К И С Л О Т Н О - О С Н О В Н О Г О С О С Т О Я Н И Я
ИИ Х К О М П Е Н С А Ц И Я
ПРИЧИНЫ НАРУШЕНИЙ
Суммируя и группируя все причины нарушений кислотно-основного состояния, можно выделить следующие причины:
1.Повышенное поступление кислых продуктов или недостаточность их удаления.
2.Изменение количества иона НСО3– в сторону увеличения или снижения.
3.Изменение концентрации ионов К+ в крови.
МЕТАБОЛИЧЕСКИЙ АЦИДОЗ
Причины
1. Повышение содержания кислот в крови Кетоацидоз развивается при сахарном диабете 1 типа, при отравлении алкоголем, при
голодании, при кетогенной диете (значительное снижение углеводов в пище при нормальном или избыточном потреблении белков и жиров).
Кислотно-основное состояние |
338 |
|
|
Механизм развития кетоацидоза состоит в избыточном количестве окисляемых жирных кислот, поступающих в печень из жировой ткани (после активации липолиза) либо недостаточно эффективное сжигание "алкогольного" ацетил-S-КоА.
Лактоацидоз развивается при гипоксии тканей любого происхождения (соотношение лактат : пируват составляет 10 : 1) – при сепсисе, шоке, кровотечении, отеке легких, сердечной недостаточности, при повышении вязкости крови из-за водопотери, лейкемии.
2. Потеря бикарбонатов
Потери бикарбонатов возможны вместе с кишечным, панкреатическим и билиарным секретами при диареях и фистулах кишечника и желчного пузыря, дренировании поджелудочной железы.
Из лекарственных средств потерю бикарбонатов вызывают ингибиторы карбоангидразы (диакарб), препятствующие их реабсорбции в почках.
3. Задержка ионов Н+
Возникает при хронической почечной недостаточности – поражение канальцев или уменьшение числа функционирующих нефронов.
Также причиной задержки ионов Н+ является уменьшение количества натрия в первичной моче, что ограничивает антиперенос ионов Na+ и H+, и снижение фосфатов в крови, которые связывают и выводят ионы Н+.
Компенсация
1. Действие вне- и внутриклеточных буферов
o внеклеточные буферы – карбонатный и гемоглобиновый.
o костная ткань обеспечивает нейтрализацию ионов водорода бикарбонатами. Процесс сопровождается выходом кальция в кровь,
o обмен ионов Н+ и К+ через плазматическую мембрану любых клеток.
2. Дыхательная система
Закисление среды стимулирует дыхательный центр и возникает компенсаторная гипервентиляция. Гипервентиляция выводит избыток СО2 (угольной кислоты), снижая рСО2, что нормализует отношение НСО3– : Н2СО3=20 : 1.
3. Почечные механизмы компенсации (только при внепочечных нарушениях)
o накопление Н+ повышает активность глутаминазы и, следовательно, скорость аммониегенеза,
o усиление синтеза ионов НСО3– в реакциях ацидо- и аммониегенеза и переход его в плазму,
o реабсорбция всего канальцевого НСО3–.
МЕТАБОЛИЧЕСКИЙ АЛКАЛОЗ
Причины
1. Эндогенный синтез и повышенная секреция в кровь ионов НСО3–:
o обкладочными клетками желудка при неукротимой рвоте, фистуле желудка, кишечной непроходимости,
o клетками почечного эпителия в результате гиперальдостеронизма, при гиповолемии, при использовании петлевых диуретиков (фуросемид, тиазиды).
2. Ятрогенное создание высоких концентраций ионов НСО3– при внутривенном введении щелочных растворов.
Компенсация
1. Реакция дыхательной системы, направленная на снижение частоты и глубины дыхания:
o гиповентиляция повышает концентрацию рСО2, и, следовательно, H2CO3. Благодаря этому емкость карбонатного буфера возрастает и соотношение НСО3–/Н2СО3 нормализуется до 20:1, величина pH снижается.

biokhimija.ru |
Тимин О.А. Лекции по биологической химии |
339 |
|
|
|
2. Реакция почек
o реабсорбция НСО3–, имеет пороговое значение, поэтому при алкалозе и избытке в крови ионов НСО3– в конечной моче сохраняется НСО3–, что может увеличивать ее рН до 8.
РЕСПИРАТОРНЫЙ АЦИДОЗ
Причины
Причиной является нарушение вентиляции легких:
o повреждения или заболевания легких (пневмония, фиброз, отек легких, инородное тело),
o бронхиальная астма, эмфизема, бронхит.
o повреждения или заболевания дыхательных мышц (нехватка калия, боли после операции, травмы, накопление жировых отложений),
o угнетение дыхательного центра (опиаты, барбитураты), неправильный режим ИВЛ,
Компенсация
1. В основном компенсацию осуществляют почечные реакции:
o усиление ацидо- и аммониегенеза, создающих резерв ионов НСО3– и удаляющие избыток ионов Н+,
oмаксимально возможная реабсорбция HCO3–.
2.Задействуется костная ткань, в обмен на ионы Н+ в кровь высвобождаются ионы кальция.
3.Бикарбонатная и гемоглобиновая буферные систем неэффективны, т.к. имеется нарушение функции легких.
РЕСПИРАТОРНЫЙ АЛКАЛОЗ
Причины
1. Возбуждение дыхательного центра. Причин этого возбуждения может быть несколько:
o субарахноидальное кровотечение, при этом происходит стимуляция дыхательного центра продуктами гемолиза,
o при циррозе печени и сепсисе происходит стимуляция дыхательного центра токсинами и циркулирующими вредными метаболитами.
o изолированный ацидоз церебральной жидкости, который является остаточным явлением после компенсации метаболического ацидоза крови при помощи вливаний раствора НСО3–.
Дело в том, СО2 легко проходит через гематоэнцефалический барьер, а ионы НСО3– – плохо. Поэтому при быстрой инфузии в кровь раствора НСО3– и компенсации КОС в крови ацидоз цереброспинальной жидкости сохраняется. Поэтому дыхательный центр стимулируется еще некоторое время.
2.Лихорадочные состояния.
3.Неправильный режим искусственной вентиляции легких.
Компенсация
1. В основном компенсацию осуществляют почечные реакции:
oзамедление скорости ацидо- и аммониегенеза, что снижает реабсорбцию ионов НСО3–
ипрепятствует экскреции ионов Н+,
2.Бикарбонатная и гемоглобиновая буферные систем неэффективны, т.к. имеется гипервентиляция.
Кислотно-основное состояние |
340 |
|
|
ДИ А Г Н О С Т И К А Н А Р У Ш Е Н И Й
КИ С Л О Т Н О - О С Н О В Н О Г О С О С Т О Я Н И Я
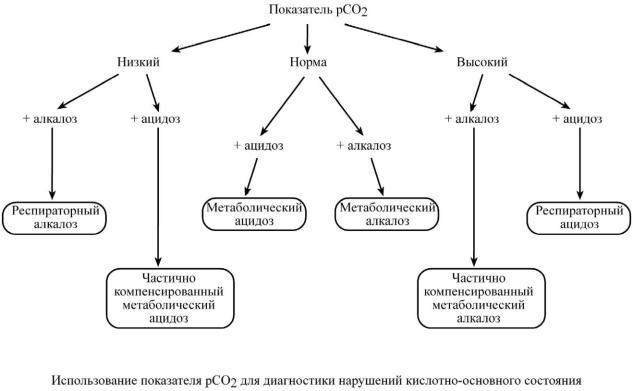
Ниже приводится упрощенный алгоритм первичной диагностики нарушений КОС.
1 шаг
Определение рН. На основании этого сразу ставится диагноз ацидоза или алкалоза. В клинике может быть третий вариант – нормальный рН при удовлетворительной компенсации нарушений КОС, но здесь это не обсуждается.
2 шаг
Определение величины рСО2. Могут быть три ситуации: высокий рСО2, низкий рСО2 и норма.
3 шаг
Сопоставление того или иного уровня величины рСО2 с ацидозом или алкалозом:
1.При нормальной величине рСО2 сдвиги КОС могут быть только метаболические.
2.При низком значении рСО2 и
o алкалозе – респираторный алкалоз,
oацидозе – метаболический ацидоз с дыхательной компенсацией.
3.При высоком значении рСО2 и
o ацидозе – респираторный ацидоз,
o алкалозе – метаболический алкалоз с дыхательной компенсацией.
4 шаг
Поиск клинических причин нарушений кислотно-основного равновесия.
