
- •1. Теоретические основы метода атомно-эмиссионной спектроскопии (аэс)
- •2. Связь интенсивности спектральной линии с концентрацией элемента в пробе
- •3. Спектральные приборы
- •4. Источники атомизации и возбуждения
- •5. Способы регистрации спектров. Основы фотографического метода аэс
- •6. Характеристическая кривая фотопластинки и способы ее построения
- •7. Основы количественного атомно-эмиссионного анализа
- •Литература
1. Теоретические основы метода атомно-эмиссионной спектроскопии (аэс)
Атомно-эмиссионным спектральным анализом называют метод исследования элементного (качественного или количественного) состава вещества по спектру излучения его атомов.
С точки зрения современных представлений, атом может находиться в различных, но строго определенных энергетических состояниях. Состояние с минимальной энергией является наиболее устойчивым и называется нормальным или основным. Молекулы анализируемого вещества, переведенного в источнике света в парообразное состояние, расщепляются на атомы. Последние под действием высоких температур переходят в возбужденное состояние. Переход атома из возбужденного состояния в основное или другое возбужденное состояние, но с меньшей энергией, сопровождается излучением кванта света, частота которого определяется соотношением
![]() , (1.1)
, (1.1)
выражающим закон сохранения энергии. Из (1.1) частота или длина волны излучения выразятся, соответственно, как
![]() (1.2)
(1.2)
или
![]() , (1.3)
, (1.3)
где ![]() – постоянная Планка, равная 6.6238×10-27
эрг/с,
– постоянная Планка, равная 6.6238×10-27
эрг/с,
![]() и
и
![]() – энергии до и после излучения кванта
света,
– энергии до и после излучения кванта
света,
![]() – скорость света
– скорость света
![]() .
.
Подставляя вместо
и
их численные значения, выражая
![]() в Ангстремах, а
и
в электронволыпах, получаем
соотношение
в Ангстремах, а
и
в электронволыпах, получаем
соотношение
![]() , (1.4)
, (1.4)
связывающее длину водны с энергией уровней. Из этого выражения следует, что набор длин волн спектральных линий, излучаемых атомом, строго определяется набором энергетических состояний, в которых он может находиться.
Энергия, необходимая для возбуждения атома, называется потенциалом возбуждения. Энергия, приводящая к отрыву от атома его внешнего валентного электрона, называется потенциалом ионизации. Избыточную энергию атом получает в источнике света в результате столкновения с различными частицами (ионами, электронами).
Процессы, происходящие в светящемся облаке источника, приводят к установлению определенной концентрации возбужденных атомов и ионов. При большой плотности паров в источнике все компоненты плазмы (электроны, атомы, ионы) характеризуются близкой температурой Т. В такой плазме устанавливается термодинамическое равновесие: частицы всех сортов движутся со скоростью, определяемой по закону Максвелла, и распределяются по энергетическим уровням в соответствии с законом Больцмана. Поэтому концентрация возбужденных атомов определяется по формуле Больцмана
![]() , (1.5)
, (1.5)
где
![]() ,
,
![]() – концентрация атомов в возбужденном
и нормальном состояниях;
– концентрация атомов в возбужденном
и нормальном состояниях;
![]() ,
,
![]() – статистические веса возбужденного
и нормального состояний;
– статистические веса возбужденного
и нормального состояний;
![]() – энергия данного уровня;
– энергия данного уровня;
![]() – постоянная Больцмана.
– постоянная Больцмана.
Интенсивность излучения за одну секунду при переходе атомов между двумя энергетическими состояниями определяется соотношением
![]() , (1.6)
, (1.6)
где – число излучающих атомов в 1см3;
![]() – вероятность спонтанного излучения;
– вероятность спонтанного излучения;
![]() – энергия кванта.
– энергия кванта.
С учетом того, что при термическом механизме возбуждения определяется формулой Больцмана (1.5) соотношение (1.6) принимает следующий вид:
![]() . (1.7)
. (1.7)
Таким образом, интенсивность спектральных
линий зависит от температуры плазмы
(Т), потенциала возбуждения данного
уровня (
)
и вероятности соответствующего перехода
(
).
Причем, с увеличением температуры плазмы
интенсивность излучения должна
возрастать. Однако экспериментальные
данные (рис. 1.1) указывают, что первоначально
увеличение температуры приводит к
увеличению интенсивности, но затем
наблюдается ее спад, и на кривых
зависимости
![]() от Т появляются максимумы, положение
которых определяется потенциалами
ионизации элементов. Это объясняется
тем, что наряду с возбуждением атомов
возможны процессы ионизации, которые
приводят к ослаблению атомного спектра.
от Т появляются максимумы, положение
которых определяется потенциалами
ионизации элементов. Это объясняется
тем, что наряду с возбуждением атомов
возможны процессы ионизации, которые
приводят к ослаблению атомного спектра.
К
3000 5000 10000 Т,
К
Рис. 1.1. Влияние
температуры плазмы на интенсивность
спектральных линий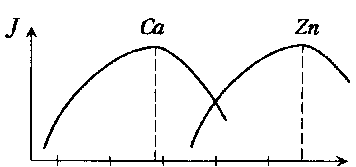
![]() .
.
Число ионов (N+) при условии термодинамического равновесия определяется известной формулой Саха:
![]() ,
,
где
![]() – число электронов в 1см3;
– число электронов в 1см3;
![]() – потенциал ионизации.
– потенциал ионизации.
Величина а определяется по формуле:
Рис. 2.1. Зависимость
интенсивности спектральной линии от
концентрации элемента в пробе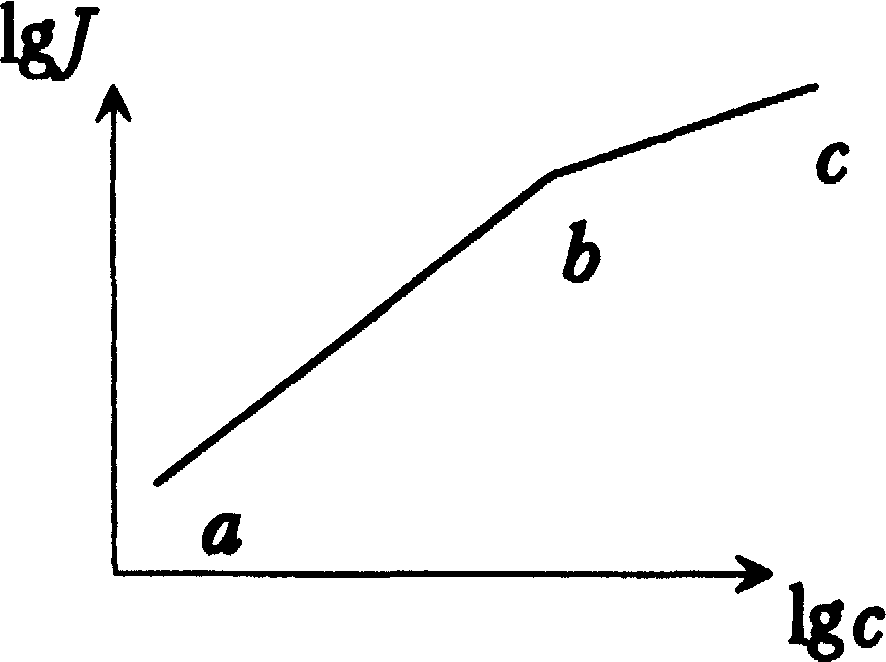
![]() ,
,
где m – масса электрона.
При наличии процесса ионизации интенсивность линий ионов по мере возрастания степени ионизации будет возрастать, и определяться соотношением:
![]() .
.
Таким образом, если рассматривать разряд с различной температурой, то будет наблюдаться последовательное усиление и ослабление интенсивности линий различных атомов в зависимости от их потенциалов ионизации.
