- •1)Рабочие тела. Параметры состояния
- •2) Первый закон термодинамики. Внутренняя энергия. Энтальпия.
- •3)Теплоемкость
- •4)Второй закон термодинамики. Энтропия тела.
- •5)Водяной пар. Основные понятия и определения.
- •6) Определение основных параметров водяного пара
- •7) Диаграммы водяного пара
- •9) 1 Закон термодинамики. Внутренняя энергия. Энтальпия.
- •10) Истечение газов и паров.
- •11) Дросселирование газов и паров.
- •12) Нагнетание газов и паров
- •13) Классификация циклов тсу
- •15) Цикл гту с подводом теплоты при постоянном давлении.
- •16)Циклы гту с подводом теплоты при постоянном объеме.
- •18) Цикл Ренкина.
- •19) Регенеративный цикл псу.
- •23)Цикл пароэжекторной холодильной установки.
- •24) Цикл абсорбционной холодильной установки .
- •25) Тепловой насос.
1)Рабочие тела. Параметры состояния
Рабочие тела – в технической термодинамике рассматриваются системы(тела), при помощи которых происходит взаимное преобразование теплоты и работы(процессы в тепловых машинах)
В качестве рабочих тел, как правило используют газы и пары, которые способны значительно изменить свой объем при изменении внешних условий.
 Г
Г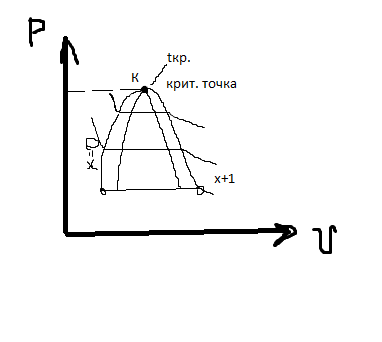 аз
можно рассматривать как пар соответствующей
жидкости, находящийся далеко от
состояния(сильно перекрытый пар), а
пар- как реальный газ, близкий к состоянию
сжижения.
аз
можно рассматривать как пар соответствующей
жидкости, находящийся далеко от
состояния(сильно перекрытый пар), а
пар- как реальный газ, близкий к состоянию
сжижения.
Параметры состояния:Термические: PV=u(нью)(M)RT терм. Уравнение состояния отношение силы к площади, на которую действует Pбар<Pабс (“+”) Pабс=Pизб+Pбар.
Pа – абсолютное давление [Па; H/м^2]
V – удельный объем [м^3/кг; V/m]
Ta – абсолютная температура [K(t+273)] является мерой интенсивности теплового движения молекул тела и окружающей среды кинетической энергией движения молекул газа.
Калорические: H=U+PV (зависит только от начального и конечного состояния) [Дж/кг]
H- энтальпия h(i). При постоянном давлении изменении энтальпия равно количеству теплоты, подведенной к системе.
S – энтропия [кДж/К*кг] мера упорядоченности системы.
U – внутренняя энергия, напряжение [кДж/кг]
2) Первый закон термодинамики. Внутренняя энергия. Энтальпия.
Первый закон термодинамики
Q=A+дельтаU (первая форма записи с учетом дельтаU)
В термодинамическом процессе подведенная теплота в общем случае расходится на изменении внутренней энергии и на совершении внешней работы.
Вторая форма, исходя из понятия энтальпии.
h=U+pV
dh>=d(U+pV)
Q=0 адиабата dq=0; S=const, PV=const. A=-дельтаU осуществляется без теплообъема.
A=0 dV=0 изохора V=const. подача жидкости насосом
дельтаU=0 изотерма (T=const) A=Q
3)Теплоемкость
Подвод теплоты к рабочему телу или отвод от него в каком –либо процессе приводит в общем случае к изменению температуры тела
Отношение количества теплоты q подведенной или отведенной в процессе, к соответствующему изменению температуры дельтаt=t2-t1 называется теплоемкостью тела
C=q/дельта T [кДж/К]
Массовая, отнесенная к 1кг рабочего тела
Cm=q/mдельтаT [кДж/К*кг]
Объемная, отнесенная к 1м^3 при нормальных условиях Cv=q/VдельтаT [кДж/м^3*К]
Мольная, отнесенная к 1 молю вещества
|
MCv |
MCp |
1 |
3 |
5 |
2 |
5 |
7 |
3 |
7 |
9 |
4)Второй закон термодинамики. Энтропия тела.
dQ/T=pdV+dU/T
dQ=dS=TdS
Создание вечного двигателя второго рода невозможна.
Теплота не может сама собой переходить от менее нагретого тела к более нагретому.
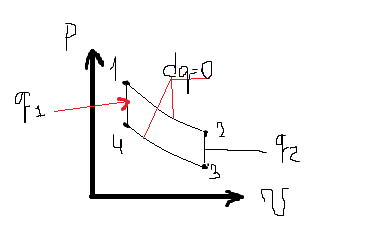
Процесс расширения рабочего тела с подводом теплоты q, будет сопровождаться увеличением энтропии
Процесс возвращения рабочего тела в начальное состояние по часовой стрелке сопровождается уменьшением энтропии, т.е. отводом теплоты q2
Отношение превращенной в работу теплоты q0 к теплоте, подведенной к рабочему телу за цикл (затраченной) q, называется термическим КПД
n(с хвостиком))t=(q1-q2)/q1=1-q2/q1=Ац/q1
Ац-работа цикла