
- •Органическая химия
- •Программа цели и задачи учебной дисциплины, её место в учебном процессе Цели и задачи изучения дисциплины
- •Краткая характеристика дисциплины, её место в учебном процессе
- •Связь с предшествующими дисциплинам
- •Связь с последующими дисциплинами
- •Содержание дисицплины ( Лекционный курс)
- •При выполнении задания рекомендуется использовать следующую литературу:
- •Конспеты лекций Органические соединения
- •Значение органической химии
- •Основные положения теории химического строения Бутлерова:
- •Формулы строения
- •Структурные изомеры
- •Стереоизомеры
- •Горение.
- •Галогенирование алканов.
- •Алкены, алкадиены, алкины (ненасыщенные углеводороды).
- •Номенклатура алкенов
- •Общие свойства ненасыщенных (непредельных) углеводородов
- •Другие реакции алкенов и алкинов.
- •Отличительные реакции алкинов.
- •Методы получения алкинов
- •Система является циклической Цикл является плоским
- •Ниже приведены примеры ароматических систем
- •Номенклатура ароматических соединений.
- •Номенклатура замещенных бензолов
- •Окисление
- •Методы получения бензола и его гомологов
- •Система является циклической Цикл является плоским
- •Производные углеводородов Галогеналканы.
- •Строение галогеналканов
- •Способы получения галогеналканов
- •Реакции нуклеофильного замещения при насыщенном атоме углерода Реакции нуклеофильного замещения (примеры)
- •Одноатомные спирты
- •Строение и свойства спиртов
- •Получение спиртов
- •Свойства спиртов
- •Алкоголяты
- •Основность спиртов
- •Водородные связи
- •Нуклеофильность
- •Многоатомные спирты
- •Получение
- •Химические свойства
- •Простые эфиры
- •Получение
- •Свойства
- •Этиленоксид
- •Краун-эфиры
- •Металлоорганические соединения
- •Получение металлорганических соединений
- •Свойства реактивов Гриньяра Основность
- •Нуклеофильность
- •Альдегиды и кетоны
- •Альдегиды
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Применение
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Применение
- •Карбоновые кислоты
- •Получение
- •5. Гидролиз функциональных производных (сложных эфиров, ангидридов, галогенангидридов, амидов). Химические свойства
- •Применение
- •Физические свойства
- •Химические свойства
- •Азотсодержащие соединения (амины)
- •Номенклатура
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Пептиды. Белки
- •Химические свойства
- •Углеводы. Генетический d- ряд сахаров
- •Генетический d- ряд сахаров
- •Построение формул Хеуорса для d- галактозы
- •Рассмотрим построение формул Хеуорса на примере d- галактозы.
- •Получение
- •2. Восстановление.
- •II. Реакции по гидроксильным группам
- •III. Специфические реакции
- •Дисахариды
- •Полисахариды
- •Крахмал
- •Целлюлоза (клетчатка)
- •Электронные эффекты и механизмы некоторых реакций
- •Нуклеофильное замещение у насыщенного атома углерода sn1 и sn2 реакции.
- •Мономолекулярное нуклеофильное замещение (sn1)
- •Бимолекулярное нуклеофильное замещение (sn2)
- •Реакции элиминирования (е1,е2)е1е2
- •Мономолекулярное элиминирование е1.
- •Бимолекулярное элиминирование е2.
- •Реакции конденсации
- •Реакция Канниццаро
- •Бензоиновая конденсация
- •Конденсация Перкина
- •Кляйзена-Шмидта реакция
- •Cложноэфирная конденсация
- •Конденсация Дикмана
- •Нуклеофильное замещение у насыщенного атома углерода sn1 и sn2 реакции.
- •Примеры решения задач
- •Перечень вопросов по самоконтролю Углеводороды
- •Алкилгалогениды и спирты
- •Альдегиды и кетоны
- •Карбоновые кислоты
- •Электрофильное и нуклеофильное замещение в ароматическом ряду
- •Амины и диазосоединения
- •1.Расположите следующие азотсодержащие соединения по возрастанию их основности:
- •Перечень вопросов к экзамену по всему курсу
Свойства реактивов Гриньяра Основность
Реактивы Гриньяра можно рассматривать как смешанные магниевые соли галогенно-водородных кислот и алканов, т.е. как источники почти свободных карбанионов. Алкильный анионявляется сильным сопряженным основанием слабой кислоте - алкану (рКа 35-50). Поэтому реактивы Гриньяра и другие металлоорганические соединения участвуют в химических превращениях как мощнейшие основания и нуклеофилы. Как основания, они реагируют с соединениями, содержащими кислый атом водорода. При этом реактивы Гриньяра превращаются в углеводороды. Донорами протонов могут быть вода, спирты, аммиак, первичные и вторичные амины, ацетилены, т.е. даже очень слабокислые соединения. На этой реакции основан газообъемный метод определения кислых атомов водорода (реакция Чугаева-Церевитинова). Исследуемое соединение или смесь обрабатывают метилмагниййодидом и, измерив объем выделившегося метана, рассчитывают количество кислых протонов в соединении или соответствующих компонентов в смеси.
![]()
При взаимодействии реактивов Гриньяра с ацетиленом образуется бис-(магнийиодид)-ацетилен, называемый комплексом Иоцича.
![]()
Последний применяют в органическом синтезе для получения, например, дейтероацет-альдегида
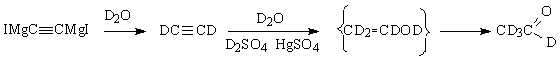
или замещенных алкинов
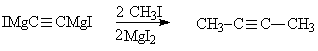
Нуклеофильность
Нуклеофильность металлоорганических соединений проявляется в превращениях, аналогичных реакции Вюрца (SN2).
![]()
В этом превращении электрофилом могут быть не только органические галогениды но также галогениды металлов и неметаллов.

Реакция с молекулярным йодом приводит к замещению магнийгалогенидного фрагмен-та йодом, что используется для синтеза йодпроизводных.
![]()
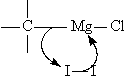
Нуклеофильный характер реактивов Гриньяра и других металлоорганических соедине-ний иллюстрируют реакции присоединения к СО2 и к другим соединениям, содержащим группы с электронодефицитным углеродом.
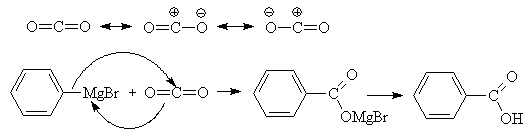

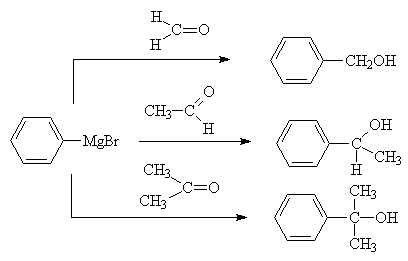
Реактивы Гриньяра легко присоединяются к карбонильной группе альдегидов и кетонов. При этом реакция с формальдегидом дает первичные спирты, с другими альдегидами – вторичные, с кетонами – третичные спирты. Реакция начинается с нуклеофильной атаки углеродного атома, связанного с магнием, на электронно-дефицитный атом карбонильной группы. Как и в вышеприведенных примерах, изначально образуется смешанная магниевая соль, в данном случае алкоголят, которую затем гидролизуют (обычно, хлоридом аммония).
При взаимодействии с кислородом реактивы Гриньяра окисляются до гидроперокси-дов, которые аналогично выделяют после гидролиза соответствующей смешанной соли.
![]()
Если гидропероксид реагирует со второй молекулой реактива Гриньяра, то образуется смешанный алкоголят, гидролизующийся затем до спирта.
![]()
Данная реакция, разумеется, не имеет практического значения и представляет собой процесс, иллюстрирующий разложение магнийорганического соединения на воздухе. Это объясняет необходимость использования реактивов Гриньяра сразу же после приготовления или хранения их в инертной атмосфере.
Альдегиды и кетоны
Органические
соединения, молекулы которых содержат
карбонильную группу ![]() ,
называются карбонильными соединениями.
В зависимости от характера связанных
с карбонильной группой заместителей
карбонильные соединения делятся на
альдегиды, кетоны, карбоновые кислоты
и их функциональные производные.
,
называются карбонильными соединениями.
В зависимости от характера связанных
с карбонильной группой заместителей
карбонильные соединения делятся на
альдегиды, кетоны, карбоновые кислоты
и их функциональные производные.
