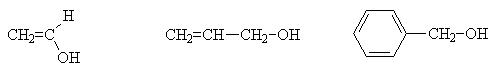- •Органическая химия
- •Программа цели и задачи учебной дисциплины, её место в учебном процессе Цели и задачи изучения дисциплины
- •Краткая характеристика дисциплины, её место в учебном процессе
- •Связь с предшествующими дисциплинам
- •Связь с последующими дисциплинами
- •Содержание дисицплины ( Лекционный курс)
- •При выполнении задания рекомендуется использовать следующую литературу:
- •Конспеты лекций Органические соединения
- •Значение органической химии
- •Основные положения теории химического строения Бутлерова:
- •Формулы строения
- •Структурные изомеры
- •Стереоизомеры
- •Горение.
- •Галогенирование алканов.
- •Алкены, алкадиены, алкины (ненасыщенные углеводороды).
- •Номенклатура алкенов
- •Общие свойства ненасыщенных (непредельных) углеводородов
- •Другие реакции алкенов и алкинов.
- •Отличительные реакции алкинов.
- •Методы получения алкинов
- •Система является циклической Цикл является плоским
- •Ниже приведены примеры ароматических систем
- •Номенклатура ароматических соединений.
- •Номенклатура замещенных бензолов
- •Окисление
- •Методы получения бензола и его гомологов
- •Система является циклической Цикл является плоским
- •Производные углеводородов Галогеналканы.
- •Строение галогеналканов
- •Способы получения галогеналканов
- •Реакции нуклеофильного замещения при насыщенном атоме углерода Реакции нуклеофильного замещения (примеры)
- •Одноатомные спирты
- •Строение и свойства спиртов
- •Получение спиртов
- •Свойства спиртов
- •Алкоголяты
- •Основность спиртов
- •Водородные связи
- •Нуклеофильность
- •Многоатомные спирты
- •Получение
- •Химические свойства
- •Простые эфиры
- •Получение
- •Свойства
- •Этиленоксид
- •Краун-эфиры
- •Металлоорганические соединения
- •Получение металлорганических соединений
- •Свойства реактивов Гриньяра Основность
- •Нуклеофильность
- •Альдегиды и кетоны
- •Альдегиды
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Применение
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Применение
- •Карбоновые кислоты
- •Получение
- •5. Гидролиз функциональных производных (сложных эфиров, ангидридов, галогенангидридов, амидов). Химические свойства
- •Применение
- •Физические свойства
- •Химические свойства
- •Азотсодержащие соединения (амины)
- •Номенклатура
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Пептиды. Белки
- •Химические свойства
- •Углеводы. Генетический d- ряд сахаров
- •Генетический d- ряд сахаров
- •Построение формул Хеуорса для d- галактозы
- •Рассмотрим построение формул Хеуорса на примере d- галактозы.
- •Получение
- •2. Восстановление.
- •II. Реакции по гидроксильным группам
- •III. Специфические реакции
- •Дисахариды
- •Полисахариды
- •Крахмал
- •Целлюлоза (клетчатка)
- •Электронные эффекты и механизмы некоторых реакций
- •Нуклеофильное замещение у насыщенного атома углерода sn1 и sn2 реакции.
- •Мономолекулярное нуклеофильное замещение (sn1)
- •Бимолекулярное нуклеофильное замещение (sn2)
- •Реакции элиминирования (е1,е2)е1е2
- •Мономолекулярное элиминирование е1.
- •Бимолекулярное элиминирование е2.
- •Реакции конденсации
- •Реакция Канниццаро
- •Бензоиновая конденсация
- •Конденсация Перкина
- •Кляйзена-Шмидта реакция
- •Cложноэфирная конденсация
- •Конденсация Дикмана
- •Нуклеофильное замещение у насыщенного атома углерода sn1 и sn2 реакции.
- •Примеры решения задач
- •Перечень вопросов по самоконтролю Углеводороды
- •Алкилгалогениды и спирты
- •Альдегиды и кетоны
- •Карбоновые кислоты
- •Электрофильное и нуклеофильное замещение в ароматическом ряду
- •Амины и диазосоединения
- •1.Расположите следующие азотсодержащие соединения по возрастанию их основности:
- •Перечень вопросов к экзамену по всему курсу
Реакции нуклеофильного замещения при насыщенном атоме углерода Реакции нуклеофильного замещения (примеры)
Примеры реакций нуклеофильного замещения весьма многочисленны, при этом в качестве субстрата может выступать не только галогеналкан, но и соединения других классов. В ряду галогеналканов возможны реакции замещения другим галогеном, гидроксилом, алк(ар)оксилом-, нитро-, циано-, аминогруппой и др.
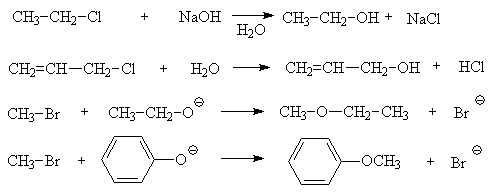
Для замещения галогена цианогруппой применяют цианиды щелочных металлов, реагентом для замещения нитрогруппой служат нитриты щелочных металлов или серебра.
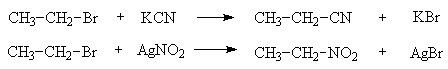
Цианид- и нитрит-ион относятся к амбидентным анионам, т. е. таким, которые имеют по два нуклеофильных центра. Каждый из них образует два изомерных продукта взаимодействия с галогеналканами - нитрил и изонитрил, нитросоединение и алкилнитрит, соответственно.
![]()
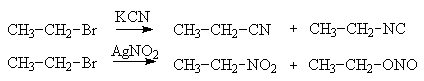
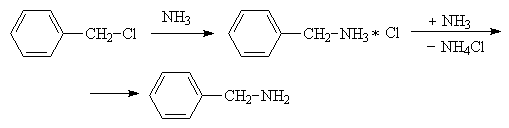
Взаимодействие галогеналкана с аммиаком и аминами приводит сначала к образованию соответствующей аммониевой соли. Последняя превращается в амин при действии основания, роль которого часто выполняет сам амин, взятый в избытке.
Нужно обратить внимание, что данная реакция имеет ограниченное препаративное значение и сопровождается побочным образованием большого количества ди- и триалкиламинов, т.к. алифатические заместители, в большинстве случаев обладающие донорным индуктивным эффектом, повышают нуклеофильность аминогруппы.
Одноатомные спирты
Гидроксипроизводные предельного алифатического ряда называют спиртами (алканолами, например, «этанол, бутанол-2»), т.е названия спиртов образуют путем прибавления окончания -ол к названию соответствующего углеводорода. Кроме официальной номенклатуры используют другие: русскую (по названию углеводородного радикала, например, «этиловый спирт»), тривиальную (например, древесный спирт), карбинольную (карбинол – метанол, а другие спирты – как его производные, т.е. трет-бутанол может быть назван триметилкарбинолом).
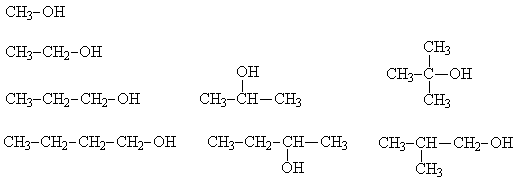
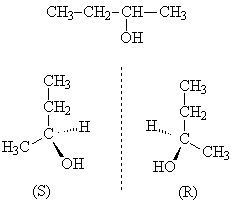
В гомологическом ряду алканолов наблюдается два вида изомерии структурная (изомерия цепи и изомерия положения гидроксила) и оптическая.
Непредельные спирты бывают двух типов: с гидроксилом при двойной связи и аллильные спирты. Ароматические спирты рассматривают как алканолы, в молекулах которых присутствуют ароматические кольца. Те спирты, в которых кратные связи отделены от ОН-группы более чем одним sp3-гибридным атомом углерода, по свойствам не отличаются от обычных алканолов.
|
||
Виниловый |
Аллиловый |
Бензиловый |
Нужно отметить, что виниловые спирты, не содержащие сильных акцепторов в молекуле, крайне неустойчивы, они, по сути, являются таутомерной формой соответствующих кетонов, которая присутствует в веществе в незначительной концентрации:
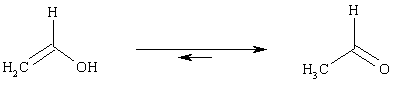
Спиртовая молекула может содержать несколько гидроксильных групп. В соответствии с их количеством различают двух- трех-, многоатомные спирты. Официальные названия многоатомных спиртов образуются путем прибавления окончания -диол, -триол к названию соответствующего углеводорода. Часто применяются тривиальные названия, особенно для 1,2-диолов, называемых гликолями.