
- •И.В.Самсонова, м.Н.Медведев, в.В.Голубцов, с.В.Малашенко
- •Министерство образования республики беларусь уо «витебский государственный медицинский университет»
- •Патологическая анатомия инфекционных заболеваний Пособие
- •210602, Витебск, пр. Фрунзе, 27.
- •210602, Витебск, пр. Фрунзе, 27.
- •Оглавление
- •Предисловие
- •Глава 1. Клинико-морфологические основы инфекционных болезней
- •I. Основной источник возбудителя:
- •II. Механизм передачи инфекции:
- •Глава 2. Вирусные воздушно-капельные инфекции грипп – острое респираторное вирусное заболевание, протекающее с явлениями общей интоксикации и поражением верхних дыхательных путей.
- •Глава 3. Бактериальные воздушно-капельные инфекции
- •Глава 4. ВирусНые воздушно-капельные инфекции с поражением кожи и слизистых оболочек
- •Глава 5. Инфекции с преимущественным поражением нервной системы
- •Глава 6. Инфекции с преимущественным поражением Желудочно-кишечного тракта
- •Глава 7. АнтРоПонозные, зоонозные и трансмиссивные инфекции
- •Глава 8. Инфекции, передающиеся половым путем
- •Глава 9. Вирусные гепатиты
- •Глава 10. Туберкулез
- •Глава 10. Вич-инфекция
- •Приложение 1. Тест-задания по патологической анатомии инфекционных заболеваний
- •Приложение 2 ситуационные задачи по клинической патоморфологии инфекционных заболеваний
- •Ответы на ситуационные задачи
- •Литература
Глава 6. Инфекции с преимущественным поражением Желудочно-кишечного тракта
КИШЕЧНАЯ КОЛИ-ИНФЕКЦИЯ (ЭШЕРИХИОЗ) – острое заболевание, вызываемое некоторыми типами кишечных палочек, протекающее с синдромом гастроэнтерита или гастроэнтероколита.
Этиология, эпидемиология, патогенез. Возбудители – кишечные палочки (E.coli, род Escherichia, семейство Enterobacteriaceae) – являются грам-отрицательными палочками, не образуют спор, имеют микрокапсулу; факультативные анаэробы, реже аэробы. Род Escherichia представлен 7 видами, основное значение имеет вид E.coli.
Вид включает условно-патогенные кишечные палочки, которые являются постоянными обитателями кишечника человека, животных, птиц, рыб. E.coli как нормальные обитатели кишечника синтезируют витамины групп К, В, Е и другие, являются антагонистами патогенных бактерий (выделяют колицины), участвуют в пристеночном пищеварении, стимулируют иммунитет. При подавлении E.coli антибиотиками развивается дисбактериоз. При снижении иммунитета E.coli могут вызывать гнойно-воспалительные процессы в различных органах (цистит, пиелит, холецистит, коли-сепсис) и эшерихиозы. E.coli – санитарно-показательный микроорганизм, наличие которого в воде, пище, на предметах обихода указывает на фекальное загрязнение.
Эшерихии имеют соматический О-Аг, жгутиковый Н-Аг и поверхностный соматический К-Аг. На практике используют упрощенную классификацию патогенных штаммов кишечной палочки по видам О-Аг (всего изучено 170 О-Аг, из которых более 80 выделены у патогенных для человека эшерихий).
Факторами патогенности возбудителя являются: плазмида К88 (обеспечивает синтез факторов адгезии, колонизации, которые необходимы для прикрепления к клеткам эпителия кишечника), факторы инвазии (это белки наружной мембраны; с их помощью энтероинвазионные E.coli проникают в эпителиальные клетки, размножаются в них и вызывают их разрушение), экзотоксины (энтеротоксины, синтез которых зависит от плазмиды Ent. Среди них различают цитотоксины и цитотонины).
В настоящее время принято подразделять патогенные для человека E.coli на следующие группы:
Энтеротоксигенные Е. соli включают 70 серогрупп. Эти возбудители имеют факторы патогенности (пили или фимбрии), способствующие адгезии и колонизации нижних отделов тонкого кишечника; имеют энтеротоксины, синтез которых кодируется плазмидными генами. Они вызывают нарушение водно-солевого обмена. Заболевание протекает по типу холерной диареи. Пути распространения - водный, реже - алиментарный. Чаще болеют дети от 1 года до 3-х лет и взрослые (путешественники).
Энтероинвазивные Е. соli включают 9 серогрупп, они вызывают геморрагический колит. Их патогенность связана со способностью внедряться в эпителиоциты слизистой оболочки толстой кишки, размножаться внутри клеток и разрушать их. Эти свойства кодируются хромосомными и плазмидными генами. Одна из плазмид кодирует синтез белков наружной мембраны, которые определяют инвазию. Они имеют сходство с соответствующими белками шигелл. Как и шигеллы, они неподвижны и не способны ферментировать лактозу. Локализация процесса – нижний отдел подвздошной и толстая кишка. Поражение характеризуется абдоминальными болями, профузной водянистой диареей с примесью крови. Болеют дети 1-2 лет, подростки и взрослые. Чаще заболевание вызывают серовары О124 О144. Пути передачи – водный, пищевой.
Энтеропатогенные Е. соli включают 20 серогрупп. Патогенез поражений обусловлен адгезией бактерий к эпителию тонкой кишки, повреждением микроворсинок, но не инвазией в клетку. У большинства серотипов имеются плазмиды, которые обеспечивают синтез факторов адгезии и колонизации. Для заболевания характерна водянистая диарея и выраженное обезвоживание. Чаще болеют дети первого года жизни. Путь передачи – контактно-бытовой, реже алиментарный.
Энтерогеморрагические Е. соli представлены 4 серогруппами, которые выделяют цитотоксин; его образование кодирует ген, переносимый бактериофагом. Фактором патогенности являются плазмиды, облегчающие адгезию к клеткам эпителия толстой кишки. Токсичность обусловлена способностью синтезировать шигаподобные токсины, которые разрушают клетки эндотелия мелких кровеносных, сосудов. Это нарушает кровоток и вызывает некроз клеточной стенки. Возникает диарея с примесью крови при отсутствии лейкоцитов в испражнениях и признаков лихорадки. Помимо диареи возникает гемолитическая анемия, которая сочетается с почечной недостаточностью. Болеют дети и взрослые. Заболевание передается алиментарным путем.
Энтеропатогенные штаммы Е. соli могут вызывать сепсис, менингиты, инфекции мочевыводящих путей у новорожденных и лиц с ослабленным иммунитетом.
Источник инфекции при эшерихиозах – больной человек и бактерионоситель. Механизм передачи – фекально-оральный, пути распространения в первую очередь пищевой (чаще через молоко и молочные продукты), затем водный, в некоторых случаях, особенно при ЭПКП – контактно-бытовой.
Клиническая картина. Инкубационный период длится 3–6 дней (чаще 4–5 дней). Эшерихиозы могут протекать в следующих клинических формах: 1) кишечные заболевания детей; 2) кишечные заболевания взрослых; 3) сепсис. У детей кишечные формы эшерихиоза протекают в виде различной тяжести энтеритов (стул обильный, пенистый, водянистый, нередко оранжевого цвета) и энтероколитов в сочетании с синдромом общей интоксикации.
У взрослых заболевание, вызванное эшерихией 0124, напоминает по течению и клиническим симптомам острую дизентерию. Протекает чаще в стертой и легкой формах, реже (15–20 %) встречается среднетяжелая и тяжелая (3 %) формы. Тенезмы и ложные позывы бывают реже, чем при дизентерии. Стул жидкий с примесью слизи, у некоторых больных с кровью.
Патоморфологические изменения: микроскопические изменения органов пищеварительного тракта однотипны, но степень их выраженности в различных его отделах различна. В желудке изменения укладываются в картину катарального гастрита с уплощением покровного эпителия, дистрофическими изменениями эпителия желез, лимфоплазмоцитарной инфильтрацией с примесью нейтрофилов собственной пластинки слизистой оболочки. В тонкой кишке, особенно в тощей и в подвздошной, отмечают выраженные дистрофические и некробиотические изменения в эпителии ворсинок с десквамацией его в виде пластов, в результате чего ворсинки становятся оголенными. В собственной пластинке слизистой оболочки отмечается умеренный отек, очаговая инфильтрация лимфоцитами, плазмоцитами, эозинофилами и нейтрофилами. Если процесс затягивается, ворсинки утолщаются и укорачиваются и в них появляются разрастания соединительной ткани. При электронно-микроскопическом исследовании иногда в цитоплазме энтероцитов обнаруживают патогенные эшерихии, но в основном они размножаются в просвете кишки и на внутренней поверхности энтероцитов. Изменения в толстой кишке выражены значительно слабее.
Макроскопически желудок и тонкая кишка в первые дни растянуты водянистым содержимым с беловатыми и зеленоватыми хлопьями, иногда с примесью крови. Максимальные изменения выявляются в подвздошной кишке. Толстая кишка визуально не изменена, либо с точечными кровоизлияниями в слизистой оболочке. Иногда обнаруживаются изъязвления слизистой оболочки размерами 0,2–2,0 см, неглубокие, с плоскими краями и дном. Язвочки располагаются вблизи крепления брыжейки, поэтому полагают, что их возникновение связано с сосудистыми расстройствами и неспецифично. Помимо описанного для кишечной коли-инфекции характерно развитие пневматоза, возникновение которого связано со способностью эшерихий к газообразованию в стенке кишки. В редких случаях в слизистой оболочке толстой кишки развивается геморрагическое воспаление.
В связи с потерей организмом большого количества жидкости, токсикозом, а также интраканаликулярной диссеминацией возбудителя в организме при коли-инфекции отмечаются и изменения других органов (общие изменения). Кожа становится сухой, морщинистой. В печени и в миокарде развивается жировая дистрофия, в селезенке и в лимфатических узлах – гиперплазия ретикулоцитов, полнокровие, отек, иногда клетки миелоидного ряда. В вилочковой железе – акцидентальная инволюция с последующей атрофией и склерозом, в надпочечниках – атрофия коркового вещества за счет пучковой зоны. В почках определяется белковая дистрофия, в легких – острая эмфизема как следствие гиперветикулляции при ацидозе и гипоксии, в головном мозге – расстройства кровообращения в капиллярном русле, отек.
Осложнения. При интраканаликулярной диссеминации кишечные палочки попадают в легкие и участвуют наряду с другой бактериальной флорой в развитии очаговой пневмонии. Если заболевание вызывают энтероинвазивные штаммы эшерихий, то клинически и морфологически заболевание протекает как шигеллез. В связи с этим развиваются осложнения, характерные для дизентерии.
Смерть наступает при резком обезвоживании или от осложнений.
Иммунитет после заболевания группоспецифический, слабовыраженный. Естественный иммунитет против возбудителей колиэнтерита у детей раннего возраста обеспечивается sIgA-антителами грудного молока матери, а также бифидобактериями, которые являются антагонистами патогенных Е. соli. Материнские антитела IgМ против патогенных Е. соli не проходят через плаценту. При дизентериеподобных заболеваниях передается пассивный иммунитет от матери антителами- IgG проходящими через плаценту. Поэтому новорожденные легко заболевают колиэнтеритами, но невосприимчивы к дизентериеподобным инфекциям. У взрослых резистентность определяется антагонизмом нормальной флоры кишечника и IgА-антителами против патогенных штаммов.
Диагностика. Материал – фекалии, моча, кровь, рвотные массы, желчь, секционный материал. Основной метод – бактериологический; для обнаружения энтеротоксинов может быть использован ИФА.
Иерсиниоз – острое инфекционное заболевание, относящееся к зоонозам и характеризующееся поражением желудка и кишечника со склонностью к генерализации процесса и поражением различных органов.
Этиология, эпидемиология, патогенез. Возбудитель – Yersinia enterocolitia и Yersinia pseudotuberculosis – это грам- неспорообразующие палочки, факультативные анаэробы, не образуют капсул и спор.
Иерсинии Yersinia enterocolitia делятся на 5 биотипов, 10 фаготипов, а по О-антигену более чем на 30 серотипов. Наибольшее значение в патологии человека имеют 2-й и 4-й биотипы, 3, 5, 8-й и 9-й серотипы. Иерсинии экспрессируют различные фаторы вирулентности, обладающие пирогенной, гемолитической т провоспалительной активностью. Некоторые серовары продуцируют энтеротоксин.
Иерсинии чувствительны к нагреванию и высушиванию, дезсредствам, устойчивы к холоду, переносят температуру до -250С. Могут расти при температуре 5°С. Вне организма в молоке сохраняются до 16 дней, могут размножаться; в хлебе 24 дня; в масле 145 дней; в воде до 244 дней. Долго сохраняются на свежих овощах, фруктах, в квашениях и могут там размножаться.
Источник инфекции – дикие и домашние (кошки, собаки, свиньи, крупный и мелкий рогатый скот) животные, птицы, грызуны. Грызуны выделяют иерсинии во внешнюю среду с калом, мочой загрязняя ее.
Основной путь заражения человека алиментарный. Люди инфицируются через продукты, чаще овощи и фрукты (чаще при употреблении овощных салатов), загрязненные калом и мочой грызунов, без термической обработки. Возможно инфицирование при контакте с больными домашними животными. Больной человек опасности для окружающих не представляет.
Иерсиниоз, вызываемый Yersinia enterocolitia, встречается как в виде спорадических заболеваний, так и в виде небольших вспышек. Чаще болеют дети в возрасте от 3-х лет и старше в любой сезон года, но чаще в осенне-зимнее время.
Внедрение возбудителя происходит в нижних отделах тонкой кишки (преимущественно в области илеоцекального угла и червеобразного отростка), где они, проникая в стенку, вызывают терминальный илеит, могут быть язвенные изменения. Лимфогенно возбудитель достигает мезентериальных лимфатических узлов, размножаются там, накапливаются, способствуя развитию мезентериального лимфаденита с тенденцией к абсцедированию. Далее происходит прорыв бактерий из лимфатического русла в кровь, что ведет к диссеминации инфекции, поражению внутренних органов и интоксикации. Адекватная иммунная реакция обычно ведет к выздоровлению.
Клиническая картина и патоморфологические изменения. Инкубационный период длится от 15 ч. до 4 сут. (чаще 1–2 дня). Основными клиническими формами являются: 1) гастроэнтероколитическая, 2) аппендикулярная, 3) септическая, 4) субклиническая. Заболевание начинается остро. Температура тела повышается до 38–40°С, лихорадка длится до 5 дней, при септических формах – дольше. Наблюдаются симптомы общей интоксикации (озноб, головная боль; боль в мышцах, суставах). Боли в животе более сильные, чем при других острых кишечных инфекциях (ОКИ), вследствие поражения дистального отдела тонкой и слепой кишки клиническая картина часто похожа на аппендицит, на фоне кишечного синдрома характерно появление сыпи в большей степени в области суставов; часто бывает желтуха и катаральная ангина.
При гастроэнтероколитической форме на этом фоне появляется схваткообразная боль в животе, чаще в нижних отделах справа или в пупочной области. Могут быть тошнота и рвота. Преобладающим симптомом является острая водянистая диарея до 10 раз в сутки, продолжающаяся 3– 14 дней. У части детей в испражнениях обнаруживают кровь. Может быть примесь слизи, крови обычно не бывает. В отличие от дизентерии нет также тенезмов, ложных позывов, спазма и болезненности сигмовидной кишки. Эта форма развивается у младенцев и детей раннего возраста. Морфологические изменения обнаруживают в желудке, тонкой и толстой кишке, однако преимущественно страдает терминальный отдел подвздошной кишки, в которой развивается катаральный, реже катарально-язвенный энтерит. При этом слизистая оболочка кишки отечна, просвет ее сужен, в области гиперплазированных групповых лимфоидных фолликулов определяются округлые язвы. Иногда в процесс вовлекается слепая кишка и в ней возникают изменения по типу псевдомембранозного колита. Гистологически во всех слоях стенки кишки выявляется инфильтрация нейтрофилами, эозинофилами, макрофагами, плазматическими клетками и лимфоцитами. В дне язв находят иерсинии и полиморфно-ядерные лейкоциты.
Мезентериальные лимфатические узлы увеличены, спаяны в пакеты, микроскопически в них отмечается диффузная нейтрофильная инфильтрация. Иногда обнаруживают микроабсцессы. Печень увеличена, гепатоциты в состоянии жировой дистрофии, изредка развивается острый гепатит. Селезенка увеличена в 1,5–2 раза, в ней отмечаются гиперплазия красной пульпы и редукция лимфоидной ткани. Выявляются крупные зародышевые центры. Очень часто поражаются сосуды. В связи с иммунокомплексным поражением развиваются васкулиты, тромбоваскулиты, фибриноидный некроз. Следствием системных васкулитов является сыпь, которая при иерсиниозе развивается у 95 % больных, реже гломерулонефрит.
Аппендикулярная форма характерна для детей старшего возраста и молодых людей. При этой форме, кроме общих симптомов, появляются симптомы аппендицита (иногда гнойного), характерны высокая температура и лейкоцитоз. В стенке отростка находят густую инфильтрацию нейтрофилами, эозинофилами, гистиоцитами, а иногда иерсиниозные гранулемы из макрофагов, эпителиоидных клеток, гигантских клеток типа Пирогова–Лангханса и характерное для них гнойное расплавление с кариорексисом.
Септическая форма развивается у ослабленных лиц, протекает по типу септицемии с лихорадкой неправильного типа, отмечаются повторные ознобы, профузный пот, увеличение печени и селезенки, нарастает анемизация, появляется желтуха. В печени и селезенке развиваются расстройства кровообращения, появляются мелкие абсцессы и участки некроза с умеренной гранулематозной реакцией. Возможны деструкция и воспалительная инфильтрация желчных протоков, системное поражение сосудов с участками фибриноидного некроза и наличием вокруг них гигантоклеточных или эпителиоидноклеточных гранулем, а также частое поражение суставов вплоть до тяжелых инвалидизирующих гнойных артритов. Эта форма заканчивается летально в 50% случаев.
Субклинические формы выявляются, как правило, в очагах лабораторным путем. Они характеризуются слабой выраженностью и даже отсутствием некоторых клинических симптомов иерсиниоза.
Иерсиниоз, вызываемый У. pseudotuberculosis, сходен по клинико-морфологическим проявлениям с гастроэнтероколитическим, но прогноз при нем значительно благоприятнее. Эта форма иерсиниоза обычно встречается у лиц старше 40 лет, чаще женщин. Гистологически обнаруживают изменения, характерные для одной из форм острого аппендицита, терминальный илеит и брыжеечный лимфаденит.
Осложнения. В раннем периоде болезни возможны перфорация язв, перитонит, пневмония, желтуха, в позднем периоде – узловатая эритема, синдром Рейтера, миокардит.
Исход обычно благоприятный, но болезнь может рецидивировать или принимать хронический характер.
Смерть наступает при септической форме.
Иммунитет после перенесенного заболевания нестойкий, возможны повторные случаи.
Диагностика. Материал для исследования – любой, но обязательно фекалии. Методы: бактериологический, биобактериологический, серологический на 7-14 дни болезни, экспресс-метод РПГА и МИФ.
дизентерия (Шигеллез) – острое инфекционное заболевание из группы острых кишечных инфекций, вызываемых бактериями рода Shigellae, протекающих с явлениями общей интоксикации и преимущественным поражением дистального отдела толстой кишки.
Этиология, эпидемиология, патогенез. Возбудители – бактерии рода шигелл – грам-отрицательные неспорообразующие палочки, различающиеся по своим антигенным и некоторым культуральным свойствам, имеющие пили, которые обеспечивают адгезию. Выделяют 4 вида: 1) S.dysenteriae – серогруппа А, серовары 1-10; 2) S.flexneri серогруппа В, серовары 1-8; 3) S.boydii серогруппа С, серовары 1-15; 4) S.sonnei серогруппа Д.
В настоящее время возбудителями дизентерии чаще являются бактерии серогрупп В и Д (Флекснера и Зоне), изредка – бактерии Ньюкастла и очень редко Григорьева – Шига.
Факторы патогенности – экзотоксин (токсин Шига), вызывающий гибель клеток и приток жидкости в очаги поражения (наиболее выражено его количество у S.dysenteriae), эндотоксин, оказывающий энтеротропное (повреждение энтероцитов), нейротропное (повреждение интрамуральных ганглиев кишки) и пирогенное действие, и микрокапсула.
Резистентность: невысокая устойчивость к действию различных факторов, наиболее устойчивы S.sonnei, которые в водопроводной воде сохраняются до 2,5 месяцев, в воде открытых водоемов – до 1,5 месяца, в продуктах, особенно молочных, могут не только сохраняться, но и размножаться.
Источник инфекции – человек, больной острой или хронической дизентерией, а также реконвалесцент или бактерионоситель. Дизентерия относится к типичным кишечным инфекциям с фекально-оральным механизмом заражения; возможен также и контактно-бытовой механизм передачи («болезнь грязных рук»). Основные факторы передачи возбудителей: пищевые продукты, питьевая вода, белье, посуда, игрушки, зараженные фекалиями больного. При дизентерии Зоне преобладает пищевой путь, при дизентерии Флекснера – водный. Пассивными переносчиками инфекции являются насекомые – мухи, тараканы и др., переносящие возбудителей на пищевые продукты.
Дизентерийные бактерии, проникнув через рот, поселяются в клетках эпителия нижнего отдела толстой кишки. Патогенез поражений обусловлен способностью шигелл прикрепляться с помощью пилей и белков наружной мембраны к эпителиальным клеткам слизистой оболочки толстого кишечника. Благодаря инвазивному фактору возбудители проникают внутрь клеток, размножаются там и инфицируют соседние клетки. Шигеллы способны покидать фагосомы и выходить в цитоплазму нейтрофилов и макрофагов. Размножение шигелл в эпителиальных клетках вызывает их гибель, приводит к проникновению бактерий в подлежащие ткани с развитием эрозий и язв и воспалительной реакции подслизистой оболочки. Кровь из образовавшихся эрозивных язв попадает в испражнения. Эндотоксин, освобождающийся при разрушении бактерий, проникает в кровь и вызывает общее проявление интоксикации, усиление перистальтики, понос. Дизентерийные токсины воздействуют на стенки сосудов, делая их более проницаемыми и ломкими, на ЦНС, периферические нервные ганглии, симпато-адреналовую систему. В результате действия экзотоксина наблюдается более выраженное нарушение водно-солевого обмена, деятельности ЦНС, поражение почек. Поражения слизистой оболочки толстой кишки (отечность, геморрагии, эрозии, язвы, реже фибринозные изменения) являются также следствием трофических расстройств, которые возникают в результате действия дизентерийного токсина на периферические нервные ганглии.
Клиническая картина и патоморфологические изменения. Инкубационный период длится от 1 до 3 дней (чаще 1–2). Развитию острых проявлений болезни нередко предшествует продромальный период (общая слабость, недомогание, потеря аппетита). Затем повышается температура тела (37–37,8°), возникают боли в животе, локализующиеся главным образом в левой подвздошной области, жидкий стул, обычно калового характера. В последующие часы или на другой день стул учащается, в нем обнаруживаются примеси слизи и прожилки крови, иногда примесь слизи может быть обильной, а кровь примешивается в виде небольших комочков. Возникают также своеобразные болевые ощущения – тенезмы (тянущие боли в области прямой кишки, отдающие в крестец во время акта дефекации) и ложные позывы.
В последнее время у большинства больных (около 80%) острая дизентерия протекает легко, с маловыраженными явлениями.: острое начало, выраженный, но кратковременный интоксикационный синдром, стул в 1-е сутки жидкий, на 2-3 день характерный – всегда скудный (синдром «ректального плевка»), с примесью слизи, кровь в виде капелек или красной ниточки, также характерно наличие тенезмов – болезненные сокращения прямой кишки, ложные тенезмы, болезненность в левой подвздошной области, уплотнение сигмы, гепатоспленомегалия, возможно выпадение прямой кишки.
Клинически наиболее тяжело протекает дизентерия, вызываемая S.dysenteriae, при которой морфологически определяются изменения местного и общего характера.
Местные изменения развиваются в слизистой оболочке толстой кишки, главным образом в прямой и сигмовидной, реже – в нисходящей ободочной, но степень выраженности изменений убывает по направлению к слепой кишке. В развитии колита различают 4 стадии: 1) катаральный колит; 2) фибринозный колит; 3) стадия образования язв (язвенный колит); 4) стадия заживления язв.
Стадия катарального колита продолжается 2—3 дня. При этом в просвете кишки обнаруживаются полужидкие или кашицеобразные массы с примесью слизи, иногда с кровью; кишка местами растянута, местами спазмирована, слизистая оболочка набухшая, неравномерно полнокровная, покрыта крупными хлопьями слизи, после удаления которой иногда видны мелкие кровоизлияния. Микроскопически отмечаются десквамация эпителия, гиперемия, отек, кровоизлияния и диффузная лейкоцитарная инфильтрация.
Стадия фибринозного колита продолжается 5—10 дней. На высоте складок и между ними появляется фибринозная пленка, первоначально в виде нежных отрубевидных хлопьев, легко отделяющихся от слизистой оболочки. Иногда процесс этим ограничивается. В других случаях стенка кишки повреждается в значительной степени и оказывается покрытой пленками грязно-желтого или грязно-зеленого цвета, которые в случаях кровоизлияний становятся черными. Стенка кишки утолщена, просвет сужен. Микроскопически определяется проникающий на значительную глубину некроз, густая инфильтрация некротических масс полиморфно-ядерными лейкоцитами и пропитывание их фибрином (дифтеритический колит). В подслизистой основе отмечаются отек, кровоизлияния; в нервных сплетениях кишки – дистрофические и некротические изменения (вакуолизация, кариолизис нервных клеток, распад нервных волокон с размножением леммоцитов).
Стадия образования язв (язвенный колит) развивается на 10–12-й день болезни и характеризуется отторжением пленок и расплавлением фибринозно-некротических масс. Это приводит к образованию язв сначала в прямой кишке, затем в сигмовидной и выше. Язвы имеют причудливую форму и разную глубину, края их неровные, дно покрыто желтоватыми массами. Больший диаметр язв направлен поперек просвета кишки.
Стадия заживления язв характеризуется процессами регенерации, которые продолжаются в течение 3–4-й недели заболевания. Дефекты стенки кишки заполняются грануляционной тканью, которая в последующем созревает. В случае небольших язвенных дефектов регенерация может быть полной, при глубоких и обширных – образуются рубцы, деформирующие стенку и сужающие просвет кишки.
В регионарных лимфатических узлах при дизентерии развивается лимфаденит с явлениями миелоидной метаплазии.
Классическая схема стадийных изменений слизистой оболочки толстой кишки может прерваться на любой стадии, в том числе и на стадии катарального колита самостоятельно (абортивная форма), но чаще – на фоне антибактериальной терапии. В отдельных случаях дизентерия носит затяжной или хронический характер течения. При хронических формах дизентерии, которые встречаются нечасто (около 2—3%), отмечаются глубокие нарушения функций всех отделов желудочно-кишечного тракта: поражения желудка (обычно развивается ахилия) и поджелудочной железы; нарушения секреторной и ферментативной деятельности кишечника; атрофические процессы в толстой кишке; нарушения функций печени, что ведет к расстройствам всех видов обмена. Однако хроническая форма дизентерии признается не всеми, и изменения кишки, отмечаемые у данной категории больных, расцениваются как постдизентерийный колит. В этих случаях регенерация язв затягивается, образуются псевдополипы слизистой оболочки. У таких больных из краев язв высевают шигеллы, а также обнаруживают положительную реакцию агглютинации с дизентерийным антигеном.
Дизентерия, вызванная S.flexneri и S.sonnei, протекает гораздо легче, процесс имеет характер катарального гастроэнтероколита с преобладанием изменений в дистальных отделах кишки.
Особенностью дизентерии у детей является поражение лимфоидного аппарата стенки кишки, проявляющееся гиперплазией лимфоидной ткани солитарных и групповых фолликулов (фолликулярный колит) с развитием центрального некроза и гнойного расплавления. После удаления гноя на месте каждого фолликула образуется язвочка с нависшими краями (фолликулярно-язвенный колит), причем выходное отверстие уже, чем дно этой язвы, в связи с грушевидной формой фолликула.
При наслоении на дизентерию стафилококковой или иной инфекции характерно развитие нагноительных и деструктивных морфологических изменений кишечника. В этих случаях возникают обширные сливающиеся язвы, которые при заживлении образуют грубые рубцы, деформирующие стенку кишки. Крайне редко у ослабленных больных возможно развитие гангренозного колита вследствие присоединения анаэробной инфекции на стадии фибринозного воспаления.
Общие изменения проявляются гиперплазией лимфоидной ткани селезенки, развитием жировой дистрофии в сердце и печени. Кроме того, в печени иногда возможны мелкоочаговые некрозы, а в почках – некроз эпителия канальцев. При хроническом течении дизентерии обнаруживаются известковые метастазы, макро- и микролиты, образование которых связано с нарушениями минерального обмена.
О сложнения
при дизентерии связаны, главным образом,
с изменениями в стенке кишки – так
называемые кишечные осложнения. К ним
относят перфорацию язв с развитием
перитонита (если язвы высокие) или
парапроктита (при локализации язв в
прямой кишке), флегмону кишки, реже –
внутрикишечное кровотечение, рубцовые
стенозы кишки. Среди внекишечных
осложнений встречаются бронхопневмонии,
пиелит и пиелонефрит, серозные
(токсические) артриты, пилефлебитические
абсцессы печени. При хроническом течении
развиваются интоксикация, кахексия,
амилоидоз. Подобные осложнения нередко
возникают на фоне активации аутоинфекции.
сложнения
при дизентерии связаны, главным образом,
с изменениями в стенке кишки – так
называемые кишечные осложнения. К ним
относят перфорацию язв с развитием
перитонита (если язвы высокие) или
парапроктита (при локализации язв в
прямой кишке), флегмону кишки, реже –
внутрикишечное кровотечение, рубцовые
стенозы кишки. Среди внекишечных
осложнений встречаются бронхопневмонии,
пиелит и пиелонефрит, серозные
(токсические) артриты, пилефлебитические
абсцессы печени. При хроническом течении
развиваются интоксикация, кахексия,
амилоидоз. Подобные осложнения нередко
возникают на фоне активации аутоинфекции.
Смерть больных дизентерией может наступить от кишечных и внекишечных осложнений.
Иммунитет – непрочный и непродолжительный, он не только видо-, но и вариантоспецифичен.
Диагностика. Основной метод – бактериологический; для диагностики стертых и бессимптомных форм можно использовать РПГА. Для экспресс-диагностики используются РИФ, РПГА, ИФА.
САЛЬМОНЕЛЛЕЗ
Сальмонеллами вызываются 3 группы поражений: брюшной тиф и паратифы, собственно сальмонеллез (гастроэнтериты и септицемии). Развитие их зависит от вирулентности возбудителя, его инфицирующей дозы и состояния иммунитета макроорганизма. Среди сальмонелл есть виды, патогенные только для человека: S.typhi, S.paratyphi A, S.paratyphi В (S.schottmuelleri) S.paratyphi C (S.hirschfeldii) вызывающие брюшной тиф и паратифы А, В, C. Многие виды обитают в организме домашних и диких животных, птиц, рыб и вызывают у человека поражение кишечника – сальмонеллезы.
Все сальмонеллы – грам-отрицательные неспорообразующие, подвижные палочки, факультативные анаэробы, имеют три основных антигена: О-АГ, Н-АГ, Vi-АГ. Во внешней среде сальмонеллы долго сохраняют свою жизнеспособность: в воде открытых водоемов они живут 11-120 суток, в морской воде – до месяца, в почве до 9 месяцев, в комнатной пыли до 1,5 лет, в колбасных изделиях 2-4 месяца, в замороженном мясе и яйцах до 1 года, но в замороженных овощах и фруктах до 2,5 месяца. В продуктах сальмонеллы не только сохраняются, но и размножаются (молоко, сметана, творог, мясной фарш). В заражении пищевых продуктов могут играть роль мухи. Бактерии хорошо переносят низкие температуры, при нагревании до 60˚С погибают через 30 минут, при 100˚С – почти мгновенно. Дезинифицирующие средства (хлорамин, гипохлорит, лизол) в обычных концентрациях убивают возбудителей через несколько минут.
Для развития заболевания достаточно 103-109 бактерий, но при высокой вирулентности возбудителя или при иммунодефицитном состоянии человека инфицирующая доза может быть во много раз меньше. Основные факторы вирулентности: факторы колонизации (пили) 1, 3, 4, типов, обеспечивающие адгезию к эпителию кишечника (1), к пейеровым бляшкам и солитарным фолликулам (4), к различным субстратам (3); факторы инвазивности – способствуют проникновению в эпителий, бокаловидные клетки слизистой оболочки и макрофаги; плазмида вирулентности – обеспечивает ускоренное размножение вне желудочно-кишечного тракта; плазмидные и/или хромосомные факторы резистентности к бактерицидному действию сыворотки крови; энтеротоксины – повышают уровень цАМФ, активируют синтез простагландинов или нарушают синтез белка; эндотоксин – оказывает пирогенное действие, угнетает ЦНС, может привести к развитию миокардита, миокардиодистрофии и инфекционно-токсическому шоку.
САЛЬМОНЕЛЛЕЗ – вызываемое сальмонеллами острое инфекционное заболевание человека, животных и птиц, характеризующееся разнообразными клиническими проявлениями (от бессимптомного носительства до тяжелейших септических форм) с преимущественным поражением желудочно-кишечного тракта (гастроэнтериты, колиты) и сопровождающееся диареей.
Этиология, эпидемиология, патогенез. Возбудитель – большая группа сальмонелл (основные возбудители – S.enterica var. typhimurium, var. heidelberg, var. anatum, var.derby и др.), насчитывающая в настоящее время около 2000 серотипов. Относительно часто у человека встречаются около 90 серотипов, причем 10 из них обусловливают 85–91 % всех сальмонеллезов человека. Большинство возбудителей выделяют у различных животных (основной резервуар) и человека, но регистрируют также серовары, имеющие одного хозяина, например, S.sendai обитает только у человека.
Источник заражения человека чаще всего домашние птицы (50%), особенно куры и утки, а также их яйца (сальмонеллы могут проникать через скорлупу внутрь). Носительство сальмонелл выявлено у домашнего скота, собак, кошек, грызунов, у многих диких животных и птиц. Инфицированные животные выделяют бактерии с мочой и калом, молоком, слюной, загрязняя окружающую среду.
Основной путь передачи сальмонелл – пищевой. Заболевание возникает у человека в связи с употреблением мясных продуктов (говядина, свинина – до 20% случаев), яиц, реже – рыбы, овощей, фруктов, моллюсков, раков, крабов. Мясо может инфицироваться эндогенно при жизни животного во время его болезни, а также экзогенно в процессе транспортировки, переработки, хранения. Иногда продукты питания инфицируются при неправильной их кулинарной обработке, приготовлении пищи.
При несоблюдении санитарно-гигиенических норм может реализовываться контактно-бытовой путь передачи, который характерен для нозокомиальных вспышек сальмонеллеза. Такие вспышки отмечены в родовспомогательных помещениях, хирургических, детских, и других стационарах. При госпитальных сальмонеллезах чаще выделяется S.haifa. Возбудители госпитальных сальмонеллезов отличаются высокой полирезистентностью к химиотерапевтическим препаратам и антибиотикам.
Наиболее восприимчивы к сальмонелезу дети в возрасте от 1 года и лица с различными иммунодефицитами. Группу риска составляют также лица с ахлоргидрией, пациенты после гастрэктомий, ваготомий и лица, регулярно употребляющие антациды.
Подъем заболеваемости отмечается в теплый сезон – с мая по октябрь.
Воротами инфекции является преимущественно слизистая оболочка тонкой кишки, в которой сальмонеллы с помощью пилей прикрепляются к клеткам эпителия и путем эндоцитоза проникают в них. Бактерии достигают базальной мембраны и попадают в lamina propria, где размножаются, захватываются фагоцитами и ретикулоцитами, вызывают развитие местной воспалительной реакции. Внутри макрофагов бактерии не только размножаются, но и частично погибают с освобождением эндотоксина, поражающего нервно-сосудистый аппарат кишечника и повышающего проницаемость клеточных мембран. Это способствует распространению сальмонелл по лимфатическим путям и проникновению в мезентериальные лимфатические узлы. Эндотоксин обуславливает также развитие симптомов общей интоксикации организма. Продуцируемый сальмонеллами энтеротоксин приводит к активации аденилатциклазы и гуанилатциклазы энтероцитов с последующим нарастанием внутриклеточной концентрации цАМФ, цГМФ и др. это влечет за собой поступление в просвет кишечника большого количества жидкости, калия, натрия, хлоридов. У больных развивается рвота и понос. В большинстве случаев в этой стадии инфекционный процесс может завершиться (гастроинтестинальная форма). При тяжелых формах может развиться обезвоживание, а также инфекционно-токсический шок.
При глубоком нарушении барьерной функции лимфатического аппарата кишечника сальмонеллы проникают в кровь (возникает бактериемия), происходит генерализация процесса, что наиболее характерно для S.typhimurium и S.enteritidis. При септикопиемическом варианте генерализации сальмонеллы заносятся в различные органы, где образуются вторичные гнойные очаги. Выделяющийся сальмонеллами эндотоксин обусловливает также дистрофические изменения внутренних органов.
Клиническая картина и патоморфологические изменения. Инкубационный период от 2 часов до 3-х суток (чаще 12—24 ч). Для сальмонеллезов характерно острое начало, выраженный токсикоз (в большей степени, чем при других острых кишечных инфекциях), нейротоксикоз, поражение любого отдела желудочно-кишечного тракта, но преимущественно тонкой кишки (развивается энтерит); стул всегда обильный, часто зловонный, пенистый, зеленого, коричневого или желтого цвета. Выделяют три формы течения сальмонеллезов:
1. гастроинтестинальная форма: гастритический, гастроэнтеретический, гастроэнтероколитический варианты;
2. генерализованная форма: тифоподобный, септикопиемический варианты;
3. бактерионосительство (острое; хроническое; транзиторное), которое рассматривают как субклиническую форму сальмонеллеза.
Наиболее распространенная гастроинтестинальная форма (раньше ее относили к пищевым токсикоинфекциям) начинается остро, с повышения температуры тела до 38–40˚С, озноба и симптомов общей интоксикации. Эта форма протекает с обильной рвотой и поносами до 10–15 раз в сутки, приводящими к быстрому и значительному обезвоживанию организма, отчего эту форму еще называют домашней холерой (cholera nostras). Выделяют 3 варианта ее течения:
• гастритический – заболевание ограничивается субфебрильной температурой, однократной рвотой и небольшим послаблением стула, потерей жидкости не более 3 %; все явления проходят через 1–2 дня;
• гастроэнтеритический (средней тяжести);
• гастроэнтероколитический (тяжелый вариант течения с продолжительной, более 5 дней, высокой температурой тела, профузной рвотой, обильной и длительной диареей с потерей жидкости до 7–10% массы тела, что приводит к развитию синдрома обезвоживания, олигурии и даже острой почечной недостаточности. Характерны жажда, олигурия, цианоз губ, запавшие глаза, сморщенная кожа, судороги, снижение АД.
Желудок и особенно тонкая кишка при этом резко расширены, иногда даже паралитически. В их просвете содержатся полужидкие (при тяжелом варианте жидкие) массы с примесью слизи и резким гнилостным запахом. Слизистая оболочка желудка и кишечника отечна, полнокровна, с мелкими кровоизлияниями, иногда с эрозиями или нежными пленчатыми наложениями. При тяжелом варианте течения воспаление приобретает геморрагический характер. Регионарные лимфатические узлы пораженной кишки с явлениями гиперплазии. При гастроэнтероколитическом варианте в толстой кишке отмечаются максимально тяжелые изменения.
Септикопиемический вариант генерализованной формы («сальмонеллезный сепсис») протекает наиболее тяжело и характеризуется гематогенной генерализацией возбудителя с заносом его во все внутренние органы и развитием в них многочисленных гнойников разной величины на фоне типичных изменений в кишечнике. Вторичные гнойные очаги часто развиваются в опорно-двигательном аппарате (остеомиелиты, артриты, спондилиты), но особенно часто – в печени, легких и почках. Иногда наблюдаются септический сальмонеллезный эндокардит, аортит с последующим развитием аневризмы аорты, гнойные менингиты, реже возникают абсцессы печени, гнойный струмит, инфицированная киста яичника. У детей раннего возраста нередко наблюдается менингит. Для этого варианта характерен резко выраженный токсикоз, лихорадка неправильного типа, с большими суточными размахами, повторными ознобом и потом. Заболевание длится в течение многих недель. В связи с развитием септического состояния развивается гиперплазия селезенки, однако без значительного увеличения ее, а также дистрофические изменения во внутренних органах, часты диапедезные кровоизлияния. Заболевание плохо поддается антибиотикотерапии; встречается редко, но нередко приводит к летальным исходам.
Брюшнотифозный, или тифоподобный вариант по своим проявлениям почти не отличается от брюшного тифа; диагноз уточняется после выделения гемокультуры сальмонелл. В кишечнике, селезенке и лимфатических узлах развиваются изменения, сходные с таковыми при брюшном тифе, но выраженные гораздо менее интенсивно.
Осложнения. При тяжелых формах может развиться обезвоживание, инфекционно-токсический шок, острая почечная недостаточность; на фоне неадекватной терапии – дисбактериоз, который обычно часто наблюдается при хроническом бактерионосительстве.
Иммунитет – постинфекционный, непродолжительный, нестойкий, типоспецифический.
Диагностика. Материал для исследования – испражнения, рвотные массы, промывные воды желудка, кровь, моча, остатки пищи, исходные продукты, смывы с оборудования и предметов. Основной метод исследования – бактериологический; серологический используется для диагностики и выявления носительства, экспресс-методы – при групповых заболеваниях (РИФ, РПГА, ИФА).
К группе острых инфекционных заболеваний с фекально-оральным механизмом передачи, вызванных сальмонеллами, относятся ТИФО-ПАРАТИФОЗНЫЕ ЗАБОЛЕВАНИЯ (брюшной тиф, паратифы А и В). Они имеют сходные клинические проявления, характеризуются лихорадкой, обшей интоксикацией, бактериемией, увеличением печени и селезенки, энтеритом и своеобразным поражением лимфатического аппарата кишечника. Относятся к кишечным антропонозам. Возбудителями заболевания являются несколько видов сальмонелл – Salmonella typhi, S.paratyphi A, S.paratyphi В (S.schottmuelleri) S.paratyphi C (S.hirschfeldii. Инфицирующая доза колеблется от 10 млн. до 1 млрд. микробных клеток. Основным источником инфекции в последние годы являются хронические бактерионосители сальмонелл.
БРЮШНОЙ ТИФ – острое инфекционное заболевание, характеризующееся поражением лимфоидного аппарата кишечника (главным образом тонкой кишки), бактериемией и протекающее с выраженной интоксикацией, гепатоспленомегалией и часто с розеолезной сыпью.
Этиология, эпидемиология, патогенез. Вызывается S.typhi. Брюшной тиф – строгий антропоноз. Единственным источником заболевания является больной человек или бактерионоситель, которые выделяют возбудителя с испражнениями, мочой, потом, грудным молоком у кормящих матерей, слюной.
Основной механизм заражения – фекально-оральный, который реализуется водным, пищевым или контактно-бытовым путем. Возбудитель при заглатывании попадает в тонкую кишку, размножается там, выделяя эндотоксин, и вызывает развитие специфического энтерита. Затем сальмонелла интерэпителиально проникает в слизистую оболочку кишки, вызывая минимальные повреждения энтероцитов, и поражает лимфатические образования тонкой кишки (одиночные и групповые фолликулы). Далее по лимфатическим сосудам возбудитель проникает в мезентериальные лимфатические узлы и дальше в кровоток. Эта первичная бактериемия возникает через 24–72 ч после заражения, клинически не документируется, быстро прекращается в связи с фагоцитозом возбудителя макрофагами. Однако часть сальмонелл сохраняется и после внутриклеточного размножения вновь попадает в кровоток, вызывая продолжающуюся в течение нескольких дней и даже недель повторную бактериемию, которой манифестирует брюшной тиф. В эти сроки диагноз можно поставить, выделив сальмонеллу из крови (гемокультура).
Бактериемия определяет генерализацию инфекта и начало становления иммунитета, о чем свидетельствует наличие со 2-й недели заболевания в крови антител к возбудителю, определяемых с помощью реакции агглютинации. сальмонеллы с током крови попадают в печень, а далее – в желчные пути, где находят благоприятную среду для своего существования. Не вызывая клинически выраженного холецистита, брюшнотифозные палочки в большом количестве размножаются в желчи (бактериохолия), с которой и выделяются в просвет тонкой кишки. С этого момента сальмонеллы обнаруживают во всех экскретах больных (фекалии, моча, пот, молоко лактирующих женщин). Посевы фекалий (копрокультура) становятся положительными на 3-й, иногда на 4-й неделе, когда выделение возбудителей с желчью достигает пика.
Попадая с желчью естественным путем в тонкую кишку, бактерии в групповых и солитарных лимфоидных фолликулах вызывают гиперергическую реакцию в связи с сенсибилизацией их при заражении (первая встреча) и бактериемий (вторая встреча). Эта реакция выражается некрозом лимфатического аппарата тонкой (иногда и толстой) кишки, подобным таковому при феномене Артюса.
При распаде сальмонелл выделяется эндотоксин, который обуславливает симптомы общей интоксикации и играет важную роль в генезе язв тонкого кишечника, лейкопении и может обусловить развитие инфекционно-токсического шока.
Клиническая картина и патоморфологические изменения. Инкубационный период составляет 10—14 дней. При типичном течении болезнь начинается постепенно. Нарастают слабость, головная боль, симптомы интоксикации, с каждым днем повышается температура тела, достигая наибольших цифр к 7–9-му дню болезни. В период разгара отмечаются заторможенность больных, головная боль, снижение аппетита, умеренно выраженный кашель.
Патоморфологические изменения при брюшном тифе делят на местные и общие. Местные изменения при брюшном тифе наблюдаются прежде всего в терминальном отделе подвздошной кишки на протяжении 1–1,5 м и максимально выражены у самого илеоцекального клапана (илеотиф). Нередко изменения развиваются и в толстой кишке (колотиф), но чаще поражаются и тонкая, и толстая кишка (илеоколотиф) с преобладанием изменений в тонкой кишке. Для брюшного тифа характерна цикличность течения, и изменения в кишечнике укладываются в 5 стадий, или периодов, заболевания: мозговидного набухания, некроза, образования язв, чистых язв и заживления. Каждая стадия продолжается примерно неделю.
В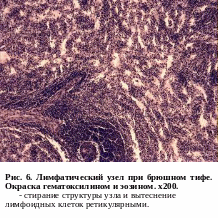 стадии
мозговидного набухания
в просвете кишки обнаруживаются
полужидкие и кашицеобразные массы с
примесью слизи (картина катарального
воспаления). Регионарные лимфатические
узлы заметно увеличены, сочные, мягкие,
красноватого цвета. Макроскопически
слизистая оболочка подвздошной кишки
полнокровна, групповые фолликулы
увеличиваются в размерах, выступая над
поверхностью слизистой оболочки в виде
плоских мягко-эластических бляшек
серого цвета с неровной поверхностью
в виде борозд и извилин, напоминающих
мозг ребенка. На разрезе они сочные,
розовато-серые. Микроскопически
в
групповых фолликулов лимфоциты
определяются в небольшом количестве;
они вытеснены моноцитами и тифозными
(брюшнотифозные) клетками (очень крупные
одноядерные макрофаги со светлой
цитоплазмой и бледным ядром, фагоцитирующие
брюшнотифозные палочки). Источником
макрофагов являются пролиферирующие
моноциты. Тифозные клетки образуют
очаговые скопления, или брюшнотифозные
гранулемы ("тифомы"), в которых
помимо тифозных клеток видны в небольшом
количестве моноциты, гистиоциты и
ретикулярные клетки. Гранулемы сливаются
между собой, полностью вытесняя лимфоидную
ткань. Таким образом, морфологическим
выражением мозговидного набухания
является острое продуктивное воспаление
с образованием макрофагальных гранулем,
отражающих реакцию гиперчувствительности
замедленного типа в ответ на инфекционный
агент.
стадии
мозговидного набухания
в просвете кишки обнаруживаются
полужидкие и кашицеобразные массы с
примесью слизи (картина катарального
воспаления). Регионарные лимфатические
узлы заметно увеличены, сочные, мягкие,
красноватого цвета. Макроскопически
слизистая оболочка подвздошной кишки
полнокровна, групповые фолликулы
увеличиваются в размерах, выступая над
поверхностью слизистой оболочки в виде
плоских мягко-эластических бляшек
серого цвета с неровной поверхностью
в виде борозд и извилин, напоминающих
мозг ребенка. На разрезе они сочные,
розовато-серые. Микроскопически
в
групповых фолликулов лимфоциты
определяются в небольшом количестве;
они вытеснены моноцитами и тифозными
(брюшнотифозные) клетками (очень крупные
одноядерные макрофаги со светлой
цитоплазмой и бледным ядром, фагоцитирующие
брюшнотифозные палочки). Источником
макрофагов являются пролиферирующие
моноциты. Тифозные клетки образуют
очаговые скопления, или брюшнотифозные
гранулемы ("тифомы"), в которых
помимо тифозных клеток видны в небольшом
количестве моноциты, гистиоциты и
ретикулярные клетки. Гранулемы сливаются
между собой, полностью вытесняя лимфоидную
ткань. Таким образом, морфологическим
выражением мозговидного набухания
является острое продуктивное воспаление
с образованием макрофагальных гранулем,
отражающих реакцию гиперчувствительности
замедленного типа в ответ на инфекционный
агент.
В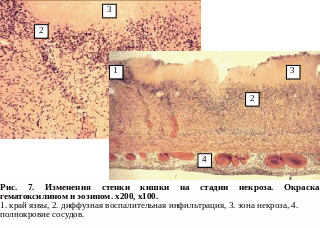 стадии некроза
групповых фолликулов
брюшнотифозные
гранулемы подвергаются некрозу, который
начинается с поверхностных отделов и
постепенно углубляется, достигая
мышечной и даже серозной оболочек.
Некротические массы грязно-серые, а
затем имбибируются желчью и приобретают
зеленовато-желтую или коричневатую
окраску.
стадии некроза
групповых фолликулов
брюшнотифозные
гранулемы подвергаются некрозу, который
начинается с поверхностных отделов и
постепенно углубляется, достигая
мышечной и даже серозной оболочек.
Некротические массы грязно-серые, а
затем имбибируются желчью и приобретают
зеленовато-желтую или коричневатую
окраску.
Некротические массы начинают постепенно отторгаться на 3-й неделе заболевания (стадия образования язв) и образуются изъязвления ("грязные язвы"), очертания которых повторяют форму фолликулов. первоначально они появляются в терминальной части подвздошной кишки, затем – в вышележащих отделах. Края свежих язв имеют форму валика и нависают над дном. Дно неровное, с остатками некротизированной ткани. При отторжении некротических масс возможны обнажение и разрушение стенок сосудов с последующим кровотечением.
На 4-й неделе изъязвления становятся неглубокими, с низкими закругленными краями и гладким, свободным от некроза дном (стадия чистых язв); они имеют правильную овальную форму и вытянуты вдоль кишки. В этой стадии иногда происходит перфорация язвы с последующим развитием перитонита.
На 5-й неделе заболевания идет заживление язв с разрастанием в дне язвы грануляционной ткани, эпителизацией поверхности за счет регенерации эпителия и «наползания» его с краев. В результате образуется нежный рубчик. При гистологическом исследовании в стенке кишки отмечается лишь отсутствие лимфоидной ткани в месте бывшей язвы.
Изменения лимфатических узлов брыжейки, прежде всего области илеоцекального угла, развиваются в той же последовательности, что и в лимфоидном аппарате кишки: сначала они увеличиваются за счет полнокровия, пролиферации моноцитарных фагоцитов и ретикулярных клеток, вытесняющих лимфоциты, затем появляются тифозные клетки и формируются брюшнотифозные гранулемы. Гранулемы некротизируются, а затем происходит их организация или петрификация. Иногда только такие петрифицированные лимфатические узлы являются свидетельством перенесенного брюшного тифа.
Следует учитывать, что в разных участках тонкой кишки одного больного можно одновременно увидеть структурные изменения, характерные для двух, иногда трех стадий брюшного тифа. Чем проксимальнее расположены изменения, тем они "моложе", чем дистальнее, ближе к илеоцекальному углу, тем они "старее". Таким образом, о стадии брюшного тифа следует судить по наиболее "старым изменениям", наблюдаемым в терминальном отрезке подвздошной кишки.
Общие изменения обусловлены персистирующей бактериемией, которая длится несколько дней (а иногда несколько недель), с неоднократным попаданием брюшнотифозных палочек в кожу и внутренние органы и развитием в них типичных изменений. Типичным признаком брюшного тифа является брюшнотифозная экзантема, которая появляется на 8–10-й день заболевания на коже живота, боковых поверхностей груди и на спине. Она представляет собой единичные розеолы диаметром 3–6 мм, возвышающиеся над уровнем кожи с четкими границами, исчезающие при надавливании. Микроскопически в сосочковом слое дермы находят гиперемию сосудов, отек и воспалительные инфильтраты из лимфоцитов, плазмоцитов, гистиоцитов и лаброцитов. Эпидермис разрыхлен, с явлениями гиперкератоза. В элементах сыпи выявляются сальмонеллы. Через 3–5 дней розеолы бесследно исчезают. Могут периодически появляться новые элементы сыпи. У ослабленных больных, особенно на фоне авитаминоза С, сыпь приобретает геморрагический характер.
Во внутренних органах (печени, селезенке, костном мозге, лимфатических узлах, легких, желчном пузыре) появляются брюшнотифозные гранулемы. В редких случаях местные (кишечные) изменения при брюшном тифе уступают общим, причем из внекишечных очагов гранулематозного поражения высеваются сальмонеллы. Ведущими клиническими проявлениями заболевания становятся поражение легких (пневмотиф), гортани (ларинготиф) или желчных путей (холангиотиф).
Помимо типичных, при брюшном тифе находят изменения, характерные для любого инфекционного заболевания: гиперпластические процессы в органах лимфатической системы и дистрофические – в паренхиматозных. Селезенка, как правило, увеличена в 3–4 раза, капсула ее напряжена, на разрезе пульпа вишневого цвета, дает обильный соскоб, иногда образуются инфаркты. Выражены гиперплазия красной пульпы, пролиферация моноцитарных элементов и ретикулярных клеток, а также характерные брюшнотифозные гранулемы. В миокарде, печени, почках находят дистрофические изменения. Изредка развивается холецистит.
Осложнения при брюшном тифе подразделяются на две группы: кишечные и внекишечные. Среди кишечных осложнений наиболее частые и наиболее грозные осложнения – перфорация кишечных язв и кишечное кровотечение. Перфорация кишечника возникает у 0,5–8 % больных обычно в период с 11-го по 25-й день болезни. Очень опасна 4-я неделя болезни, когда в процессе очищения от некротических масс язва углубляется. В последние годы перфорация кишечника чаще возникает на фоне нормальной температуры и хорошего самочувствия больного, нередко при расширении в этот период двигательного режима и нарушении диеты.
Кровотечение возникает обычно на 3-й неделе и может быть смертельным. Обычно основные изменения развиваются в слизистой оболочке в области групповых фолликулов, но гранулемы по ходу лимфатических сосудов проникают до серозной оболочки и именно в области гранулем развивается некроз и перфорация язвы с развитием перитонита. Неоднократно описывали перитонит на фоне "амбулаторного брюшного тифа", переносимого больными на ногах. В этих случаях причиной перитонита может быть попадание в брюшную полость распадающихся мезентериальных лимфатических узлов при их некрозе или пульпы селезенки при надрыве ее капсулы (последнее возникает при субкапсулярном расположении брюшнотифозных гранулем).
И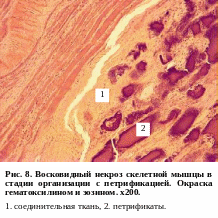 з
внекишечных осложнений возможны
пневмония, инфекционный психоз, острый
холецистит, реже другие осложнения
(гнойный перихондрит гортани, восковидные
(ценкеровские) некрозы прямых мышц
живота, периоститы большеберцовой
кости, ребер и межпозвоночных дисков,
остеомиелиты, артриты, цистит, простатит),
большинство из которых отмечали в
до-антибиотический период и сейчас они
представляют лишь исторический интерес.
В настоящее время в связи с присоединением
вторичной инфекции, прежде всего
стафилококков, пневмококков, стрептококков,
возможно развитие очаговой пневмонии
чаще с поражением нижних долей,
внутримышечных абсцессов.
з
внекишечных осложнений возможны
пневмония, инфекционный психоз, острый
холецистит, реже другие осложнения
(гнойный перихондрит гортани, восковидные
(ценкеровские) некрозы прямых мышц
живота, периоститы большеберцовой
кости, ребер и межпозвоночных дисков,
остеомиелиты, артриты, цистит, простатит),
большинство из которых отмечали в
до-антибиотический период и сейчас они
представляют лишь исторический интерес.
В настоящее время в связи с присоединением
вторичной инфекции, прежде всего
стафилококков, пневмококков, стрептококков,
возможно развитие очаговой пневмонии
чаще с поражением нижних долей,
внутримышечных абсцессов.
Брюшнотифозный сепсис встречается крайне редко, при этом местные (кишечные) изменения могут отсутствовать (typhus sine typho), но ярко выражен "тифозный статус" больного: бред, потеря сознания, нарушение слуха, гектическая температура. В настоящее время при брюшном тифе "тифозный статус" встречается крайне редко (не более 2,8 %).
Прогноз. При современных методах лечения благоприятный. Трудоспособность восстанавливается через 1,5–2 мес. от начала болезни. До применения антибиотиков летальность при брюшном тифе достигала 20 %. При тяжелых формах и наличии осложнений (особенно перфорации кишечника, перитонит, пневмония, сепсис) прогноз хуже: смерть наступает в 1–3 %. При перитоните, который имеет вялое течение, погибают до 50 % больных.
Возможно развитие осложнений в связи с передозировкой антибиотиков, когда одномоментная гибель большого числа сальмонелл приводит к коллапсу, парезу сосудистой стенки, развитию ДВС-синдрома. После перенесенного заболевания возможно развитие бактерионосительства, которое проходит спонтанно в течение года, однако 3% больных остаются бактерионосителями пожизненно (хроническое носительство) с локализацией возбудителя в желчных путях.
Иммунитет – после перенесенной инфекции стойкий, но могут быть рецидивы, повторные заболевания, часто наблюдается бактерионосительство. Такие люди опасны как источник инфекции.
Диагностика. Клиническая диагностика в начальный период заболевания затруднительна, особенно в легких и атипичных случаях. В этот период доказательством служит выделение или обнаружение возбудителей в крови. При типичной клинической картине диагностика не вызывает затруднений.
Материалом для исследования является кровь, испражнения, моча, дуоденальное содержимое, желчь, соскоб розеол, костный мозг. Методы: бактериологический – гемокультура в период бактериемии (1-я неделя заболевания); серологический – РПГА для выявления нарастания титра антител (с 5-7 дня заболевания). Для выявления бактерионосительства используют РПГА. При эпидемических вспышках с целью экспресс-диагностики для выявления антигенов в крови, костном мозге и другом материале применяют РИФ и ИФА.
ХОЛЕРА – острое инфекционное заболевание из группы карантинных (особо опасных инфекций) инфекций, характеризующееся эпидемическим распространением в летне-осенний период, токсическим поражением тонкого кишечника, развитием тяжелого гастроэнтерита, выраженной рвотой и диареей с быстрой потерей жидкости и солей, нарушением водно-электролитного обмена, обезвоживанием организма, развитием гиповолемического шока с расстройством функции почек. Относится к особо опасным инфекциям.
Этиология, эпидемиология, патогенез. Возбудителем холеры является Vibrio cholerae, представленный двумя биоварами – V. cholerae 0139 biovar cholerae (классический) и V. cholerae biovar El Tor, сходные по морфологическим и тинкториальным свойствам. Это Грам-отрицательные неспорообразующие палочки, весьма подвижны. Возбудитель холеры является факультативным анаэробом, имеет термостабильный О (соматический) и термолабильный (жгутиковый) Н-АГ. Последний является групповым, а по О-антигену холерные вибрионы разделяются на 3 серологических типа: тип Огава (содержит антигенную фракцию В), тип Инаба (фракцию С), промежуточный тип Гикошима (фракции В и С). Эти серотипы наблюдаются как у классических вибрионов, так и у биотипа Эль-Тор. Действием экзотоксина холерного вибриона на эпителий слизистой оболочки тонкой кишки обусловлена потеря жидкости организмом.
Факторы патогенности: энтеротоксин, молекула которого состоит из 5 связующих пептидов В и катализирующего пептида А; жгутики (обеспечивают подвижность вибриона); муциноза (разжижает слизь и облегчает доступ к эпителию); нейраминидаза (обеспечивает взаимодействие с микроворсинками).
Резервуаром и источником инфекции являются человек, больной различными клиническими формами холеры, и вибриононоситель.
Основной механизм заражения – фекально-оральный, который реализуется водным, алиментарным и контактно-бытовым путями. Возбудитель проникает в пищеварительный тракт человека с инфицированной водой (ведущий путь передачи) как при питье, так и при использовании ее для мытья овощей, фруктов и во время купания, с пищевыми продуктами, а также может быть занесен руками, загрязненными выделениями больного холерой. Недостаточная термическая обработка продуктов приводит к заражению. Определенную роль играют мухи, способные переносить возбудителя с испражнений на пищевые продукты. Как и при других кишечных инфекциях, заболеваемость холерой увеличивается в летне-осенний период.
В последние годы распространена холера, вызванная вибрионом Эль-Тор. Особенностью ее является возможность длительного вибриононосительства, а также большое количество больных легкими и стертыми формами.
Восприимчивость людей к холере высокая. Наиболее подвержены заболеванию лица с пониженной кислотностью желудочного сока, с анацидными гастритами.
Воротами инфекции является пищеварительный тракт. Попадающие через рот с водой или пищей холерные вибрионы частично погибают в желудке под действием кислой среды. Оставшиеся возбудители достигают тонкой кишки, локализуются в ее просвете или в поверхностных слоях слизистой оболочки, где размножаются, чему способствует выделение эпителиальными клетками щелочного секрета, высокое содержание пептонов и желчи. Воспалительная реакция не развивается.
Холерные вибрионы образуют эндо- и экзотоксины. Термостабильный эндотоксин обладает иммуногенным действием, индуцирует синтез вибриоцидных антител. Однако основную роль в патогенезе холеры играет экзотоксин (холероген) – термостабильный белок, устойчивый к действию протеолитических ферментов. Молекула экзотоксина состоит из двух компонентов – А и В. Компонент В обеспечивает проникновение в клетку токсического компонента А через связывание с рецептором на энтероцитах; компонент А приводит к активации аденилатциклазы, повышению в клетках уровня цАМФ, что приводит к подавлению всасывания NaCl, выходу жидкости и электролитов из железистых клеток в просвет кишечника. Толстая кишка не успевает всасывать огромное количество изотонической жидкости, секретируемой тонкой кишкой, что проявляется профузным поносом (холерная диарея) и приводит к большим потерям воды и электролитов. В результате этих потерь снижается объем объем циркулирующей крови, развиваются гиповолемия со сгущением крови и нарушением микроциркуляции, развиваются обезвоживание, артериальная гипотензия, сердечная недостаточность, нарушение сознания, гипотермия, гиповолемический шок. Сгущение крови нередко сопровождается острой почечной недостаточностью и тяжелыми метаболическими расстройствами.
Клиническая картина, патоморфологические изменения. Инкубационный период колеблется от нескольких часов до 5 дней (чаще 2–3 дн). Клиническая картина холеры отличаются полиморфизмом и варьируют от легкого поноса до тяжелейших алгидных форм, заканчивающихся смертью. Тяжесть течения определяется процентом потерянной жидкости по отношению к массе тела (I степень дегидратации: потеря жидкости не превышает 1-3% массы тела; II степень до 4-6%; III 7% и более). Особенность современной холеры в мировой практике – преобладание легких форм, тяжелые составляют лишь 10–12%.
Заболевание начинается остро с появления поноса, к которому несколько позже присоединяется рвота. При легких и стертых формах холеры стул нечастый, общее состояние не нарушено, обезвоживание отсутствует. В более выраженных случаях понос вначале носит каловый характер, затем теряет каловый характер и запах и принимает вид белесоватой водянистой с плавающими хлопьями («рисовый отвар») или окрашенной желчью в желтый или зеленый цвет жидкости. Относительно часто в выделениях имеется примесь слизи и крови. Рвотные массы имеют тот же химический состав, что и выделения из кишечника. Потеря жидкости при рвоте и поносе быстро приводит к обезвоживанию организма, вследствие чего меняется внешний вид больного: черты лица заостряются, слизистые оболочки рта суховатые, голос становится хриплым, кожа теряет обычный тургор и легко собирается в складки, развивается цианоз кожи и слизистых оболочек, появляются гемодинамические нарушения (тахикардия, одышка, тоны сердца становятся приглушенными, снижается АД), уменьшается количество мочи, снижается температура тела до 34–35,5˚С. Часто возникают тонические судороги, болезненные судороги мышц конечностей.
В развитии холеры различают три стадии (периода): холерный энтерит, холерный гастроэнтерит и алгидный период.
Холерный энтерит имеет серозный или серозно-геморрагический характер. Слизистая оболочка становится набухшей, отечной и полнокровной; отмечается гиперсекреция бокаловидных клеток, цитоплазматические мембраны которых разрываются и секрет выбрасывается в просвет кишки. На этом фоне появляются единичные или множественные кровоизлияния. При своевременном лечении энтерит (особенно вызванный вибрионом Эль-Тор) нередко заканчивается выздоровлением, однако он может смениться холерным гастроэнтеритом.
При холерном гастроэнтерите явления энтерита нарастают, эпителиальные клетки вакуолизируются и теряют микроворсинки; некоторые из них погибают и десквамируются. К энтериту присоединяется серозный или серозно-геморрагический гастрит. Прогрессирующее обезвоживание в этот период связано не только с диареей, но и рвотой.
Наиболее отчетливые морфологические изменения выражены в алгидный период. При этом петли тонкой кишки растянуты, в просвете их содержится большое количество (3– 4 л) жидкости, в которой удается обнаружить вибрионы. Серозная оболочка кишки сухая, с точечными кровоизлияниями, матовая, окрашена в розово-желтый цвет. Между петлями гонкой кишки обнаруживается прозрачная, липкая, тянущаяся в виде нитей слизь. Микроскопически в стенке кишки отмечаются резкое полнокровие, отек, некроз и слущивание эпителиальных клеток ворсин, инфильтрация слизистой оболочки лимфоцитами, плазматическими клетками, нейтрофилами, очаги кровоизлияний.
Проявления эксикоза ярко обнаруживаются как при осмотре, так и при внутреннем исследовании трупа (Н. И. Пирогов, А. И. Полунин). Трупное окоченение наступает быстро и сохраняется в течение нескольких дней. В результате этого мышцы резко контурированы («поза гладиатора»). Кожа, как правило, сухая, морщинистая, особенно на пальцах рук («руки прачки»). Вследствие быстро наступающего трупного окоченения она иногда напоминает «гусиную». Слизистые оболочки, подкожная клетчатка, мышцы сухие, причем мышцы становятся темно-красными. Кровь в венах густая и темная. Серозные оболочки также сухие, покрыты липкой, прозрачной слизью, которая тянется в виде нитей. С обезвоживанием связаны изменения многих внутренних органов – селезенки, печени, желчного пузыря, почек, миокарда, головного мозга. Селезенка уменьшается, капсула ее морщиниста, фолликулы атрофичны, отмечается гемосидероз пульпы. В печени развиваются дистрофия гепатоцитов и очаговые некрозы паренхимы; желчеобразование нарушается. Желчный пузырь растянут прозрачной светлой желчью («белая желчь»). В почках выявляется некроз эпителия канальцев главных отделов нефрона (т. е. изменения, наблюдаемые при олигурии или острой почечной недостаточности); в миокарде, головном мозге – дистрофические и некробиотические изменения.
Осложнения холеры принято делить на специфические (холерный тифоид и постхолерную уремию) и неспецифические. Холерный тифоид развивается как гиперергическая реакция на повторное поступление вибрионов. Не исключено значение и патогенной флоры кишечника. Клинико-морфологические проявления алгидного периода при тифоиде исчезают. Основные изменения наблюдаются в толстой кишке и представлены дифтеритическим колитом, похожим на дизентерийный. Селезенка увеличивается, помимо гиперплазии пульпы, в ней находят инфаркты. В печени появляются множественные различной величины очаги некроза в связи с тромбозом междольковых сосудов. Изменения почек характеризуются подострым экстракапиллярным гломерулонефритом или некрозом эпителия почечных канальцев. Эти изменения обусловливают развитие уремии при холерном тифоиде.
Постхолерная уремия — своеобразное осложнение посталгидной холеры, при котором в корковом веществе почек появляются множественные инфарктоподобные некрозы.
К неспецифическим осложнениям холеры относятся пневмония, абсцессы, флегмона, рожа, сепсис.
Иммунитет: прочный, длительный, повторные случаи наблюдаются редко.
Диагностика: Распознавание в очаге холеры при наличии характерных проявлений болезни трудности не представляет. Диагностика первых случаев холеры в местности, где она ранее не регистрировалась, всегда затруднительна и требует обязательного бактериологического подтверждения. Материал – испражнения, рвотные массы, желчь, секционный материал, вода, смывы с объектов окружающей среды, пищевые продукты и т.д. – следует доставлять в лабораторию не позднее 2 часов после забора, при невозможности это сделать образцы помещают в специальные транспортные среды.
Серологические исследования имеют вспомогательное значение и могут быть применены в основном для ретроспективной диагностики.
Дифференцировать холеру необходимо с острыми гастроэнтеритами, вызванными сальмонеллами, кишечной палочкой, отравлением бледной поганкой и некоторыми ядохимикатами.
Прогноз при своевременном и правильном лечении благоприятный. При тяжелых формах с осложнениями (отек легких, почечная недостаточность) могут быть летальные исходы. Смерть больных холерой обычно наступает в алгидный период от обезвоживания, комы, уремии, интоксикации. В настоящее время в связи с ранним и адекватным лечением (введение воды и электролитов, прием антибиотиков) летальность при холерном алгиде значительно снижена. Возможна смерть и от осложнений холеры, среди которых наиболее частым является уремия.
АМЕБИАЗ (амебная дизентерия) – хроническое протозойное заболевание, характеризующееся язвенным поражением толстого кишечника, иногда осложняющееся абсцессами печени, поражением легких и других органов в основе которого лежит язвенный колит.
Этиология, эпидемиология, патогенез. Возбудитель заболевания – дизентерийная амеба Entamoeba histolytica – относится к классу Саркодовых (Sаrcodina). Это единственный патогенный для человека вид амеб. Амебы передвигаются с помощью псевдоподий, размножаются бинарным делением, половой путь отсутствует, при неблагоприятных условиях образуют цисту.
может находиться в четырех формах:
1. большая вегетативная форма;
2. тканевая (эритрофаг) – вызывает специфическое поражение стенки толстой кишки; выявляется эта форма в гистологических срезах, иногда в жидких испражнениях;
3. инвазивные формы (гемофаги или эритрофаги) – содержат в эндоплазме эритроциты на разных стадиях переваривания;
4. просветная форма – основная форма E.histolytica, в ее цитоплазме отсутствуют эритроциты; образует цисты. Эту форму выявляют у больных хроническим амебиазом или у реконвалесцентов.
Большая вегетативная форма способна фагоцитировать эритроциты и встречается только у больных; просветная форма и стадия цисты встречаются у носителей амеб.
Основной хозяин – человек. В верхнем отделе толстой кишки в микроаэрофильных условиях обитают просветные формы амебы, которые питаются бактериями и остатками клеток. С кишечным содержимым амебы продвигаются в нижние отделы кишечника и образуют цисты, которые с фекалиями попадают в воду, на руки, пищу (с мухами) и снова попадают в организм человека. В тонкой кишке происходит растворение оболочки цисты, и при делении из каждого ядра образуется 8-ядерная амеба, из которой возникают восемь дочерних особей.
Таким образом, источником амебиаза является человек-цистоноситель. Ежедневно он выделяет до 45 млн. (в среднем около 8 млн.) цист. Механизм заражения фекально-оральный, через зараженные воду и пищу. Амебиаз распространен в тропических и субтропических странах. В Европе есть спорадические, как правило, завозные случаи.
Заражение наступает при попадании цист в пищеварительный тракт человека. Поражается преимущественно слепая (хронический язвенный колит) и восходящая ободочная кишка, далее по частоте следуют сигмовидная кишка, прямая кишка и аппендикс. Нередки случаи, когда язвы образуются на всем протяжении толстой кишки и даже в подвздошной кишке. В толстой кишке циста превращается в просветную форму, наступает носительство. Заболевание развивается лишь при переходе просветной формы в тканевую. E.histolytica проникает в подслизистую оболочку слепой и ободочной кишок, выделяет некротоксин, который разрушает эпителий кишечника и вызывает некроз тканей. Амебы выделяют ферменты, которые также играют роль в инвазии. Проникая в кровеносные и лимфатические капилляры, амебы вызывают образование серозно-фибринозного экссудата в подслизистой и ишемию отдельных участков кишечника с развитием некроза. В результате образуется кратерообразные язвы, которые могут вторично инфицироваться кишечными бактериями. Гематогенно (примерно у 40% больных) дизентерийная амеба может проникнуть в ветви портальной вены, а затем в виде эмболов – в печень, реже в другие органы и вызвать там специфические абсцессы.
Клиническая картина и патоморфологические изменения. Инкубационный период продолжается от 1 нед. до 3 мес. Симптомы похожи на бактериальную дизентерию. Болезнь начинается относительно остро: повышается температура до субфебрильных цифр, появляются слабость, головная боль, умеренная боль в животе, стул становится жидким красно-бурого цвета с примесью стекловидной слизи и крови («малиновое желе»). Температура субфебрильная. После острого периода, как правило, бывает длительная ремиссия, затем заболевание обостряется вновь и принимает хроническое течение.
Морфологически в стенке толстой кишки обнаруживаются отек и гистолиз, некроз слизистой оболочки, образование язв, наиболее часто и резко выраженные в слепой кишке. Участки некроза слизистой оболочки несколько выбухают над ее поверхностью, они окрашены в грязно-серый или зеленоватый цвет. Зона некроза проникает глубоко в подслизистый и мышечный слои. При образовании язвы края ее становятся подрытыми и нависают над дном. По мере прогрессирования некроза размеры язвы увеличиваются. На границе между омертвевшими и сохранившимися тканями находят амебы. Клеточная воспалительная реакция в стенке кишки выражена слабо, однако по мере присоединения вторичной инфекции развивается лейкоцитарная реакция, появляется гной. Иногда развивается флегмонозная и гангренозная форма колита. Заживление глубоких язв происходит с образованием рубцов, которые могут привести к сужению кишечника.
Регионарные лимфатические узлы несколько увеличены, но амебы в них не обнаруживаются; обычно амебы находят в кровеносных сосудах стенки кишки.
В печени могут обнаруживаться одиночные, реже множественные абсцессы. Амебные абсцессы печени, достигающие иногда 10 см в диаметре (и заметные при ультразвуковом исследовании), имеют в краевых зонах выраженную воспалительную реакцию и «ворсистую» окантовку из фибрина. В их центральной зоне часто происходят кровоизлияния, которые, смешиваясь с гнойно-некротическим материалом, образуют тестообразную массу шоколадного вида. Наслаивающиеся бактериальные инфекции могут значительно усиливать гнойную реакцию в амебных абсцессах.
Осложнения амебиаза делят на кишечные и внекишечные. Из кишечных наиболее опасны перитонит вследствие перфорации кишечника, кровотечение, образование стенозирующих рубцов после заживления язв, развитие воспалительных инфильтратов вокруг пораженной кишки – амебома, которые нередко симулируют опухоль.
Из внекишечных осложнений наиболее частым и опасным является развитие абсцесса печени. Он может развиться как во время острого периода, так и спустя длительное время, когда уже нет выраженных поражений кишечника. Амебный абсцесс может прорваться в окружающие органы и привести к образованию поддиафрагмального абсцесса, перитонита, гнойного плеврита.
Диагностика. Исследование нужно проводить не позднее 20 мин после дефекации или взятия материала. Лабораторным подтверждением диагноза служит обнаружение в испражнениях большой вегетативной формы амебы с фагоцитированными эритроцитами. При микроскопии испражнений обнаруживают цисты E.histolytica, окрашенные раствором люголя. Характерную подвижность вегетативных форм выявляют в нативных препаратах. Гистологические препараты окрашивают по Гейденгайну.
При серологическом исследовании высокие титры антител выявляют у 90% больных с внекишечными поражениями. Используют РПГА, РИФ. У бессимптомных носителей антитела обычно не обнаруживают.
ЛЯМБЛИОЗ (Д.Ф.Лямбль), или жиардиаз (Giardiasis) – паразитарная инфекция, протекающая в виде дисфункции кишечника или как бессимптомное паразитоносительство. Возбудитель lamblia intestinalis (Giardia lamblia), относится к роду Giardia.
Этиология, эпидемиология, патогенез. Возбудитель – лямблия – относится к простейшим. Существует в виде вегетативной (трофозоиты) и цистной стадий развития. Лямблия вегетативной стадии грушевидной формы, длина 8–18 мкм, ширина 6–7 мкм, имеет четыре пары жгутиков и присасывательный диск, при помощи которого они присасываются к эпителию кишечника. Два ядра и парабазальное тело трофозоита вместе придают телу паразита вид «лица с гримасой». Во внешней среде быстро погибает. Цисты паразита неподвижны, имеют толстую оболочку, отслоенную от самой цисты, что является дифференциально-диагностическим признаком. В зрелых цистах содержится четыре ядра, четыре парабазальных тела, присасывательный диск. Цисты сохраняются во внешней среде до 3 мес.
Ворота инфекции – верхние отделы тонкой кишки. Инфицирующая доза – более 100 цист лямблий. У большей части инвазированных никаких симптомов не выявляется, поэтому ряд исследователей сомневаются в патогенности лямблий. Вегетативная форма лямблий может существовать только на поверхности слизистой оболочки верхнего отдела тонкой кишки. В нижних отделах они образуют цисты и выделяются с фекалиями. Лямблии не могут существовать в желчевыводящих путях (желчь их убивает). Они могут вызывать изменения слизистой оболочки в месте прикрепления и оказывать рефлекторные воздействия.
Развитие заболевания зависит от вирулентности инфекционной дозы возбудителя, от pH желудочного сока и состояния системы иммунитета макроорганизма. При попадании в организм цист гиардии быстро размножаются в верхних отделах тонкой кишки (на 1 см2 слизистой оболочки могут находиться более 1 млн. гиардий). инфицированные люди с фекалиями выделяют огромное количество паразитов (до 18 млрд. цист в сутки). Вегетативные формы гиардий нарушают пристеночное пищеварение и перистальтику тонкой кишки. Возможно, они разрушают микроворсинки, в результате чего ухудшается всасывание жиров, углеводов, витаминов.
Клиническая картина и патоморфологические изменения. Инкубационный период продолжается 10–15 дней. Паразиты начинают выделяться через 9 дней после инфицирования. Общее самочувствие больных остается хорошим, температура тела нормальная. Нарушения всасывания (синдром мальабсорбции) приводит к диарее (стул жидкий, водянистый), снижению аппетита, усталости, апатии, отекам, снижению массы тела: иногда могут быть парестезии, кровотечения, мышечные подергивания, боли в правом подреберье.
Морфологическая картина в кишечнике варьирует от абсолютно нормальной до явно патологической. В большинстве случаев лямблии вызывают утолщение концов ворсин, снижение соотношения длины ворсин и крипт, а также пеструю воспалительную инфильтрацию в собственной пластинке слизистой оболочки. Кроме того, наблюдается неравномерное повреждение щеточной каемки всасывающих энтероцитов и гипертрофия лимфоидных фолликулов.
Через несколько дней все эти симптомы постепенно исчезают.
Диагностика. Доказательством лямблиоза является обнаружение вегетативных форм лямблий (в дуоденальном содержимом, жидком стуле) или цист (в оформленном стуле). Необходимо учитывать возможность сочетания носительства лямблий с каким-либо другим заболеванием.
