
- •И.В.Самсонова, м.Н.Медведев, в.В.Голубцов, с.В.Малашенко
- •Министерство образования республики беларусь уо «витебский государственный медицинский университет»
- •Патологическая анатомия инфекционных заболеваний Пособие
- •210602, Витебск, пр. Фрунзе, 27.
- •210602, Витебск, пр. Фрунзе, 27.
- •Оглавление
- •Предисловие
- •Глава 1. Клинико-морфологические основы инфекционных болезней
- •I. Основной источник возбудителя:
- •II. Механизм передачи инфекции:
- •Глава 2. Вирусные воздушно-капельные инфекции грипп – острое респираторное вирусное заболевание, протекающее с явлениями общей интоксикации и поражением верхних дыхательных путей.
- •Глава 3. Бактериальные воздушно-капельные инфекции
- •Глава 4. ВирусНые воздушно-капельные инфекции с поражением кожи и слизистых оболочек
- •Глава 5. Инфекции с преимущественным поражением нервной системы
- •Глава 6. Инфекции с преимущественным поражением Желудочно-кишечного тракта
- •Глава 7. АнтРоПонозные, зоонозные и трансмиссивные инфекции
- •Глава 8. Инфекции, передающиеся половым путем
- •Глава 9. Вирусные гепатиты
- •Глава 10. Туберкулез
- •Глава 10. Вич-инфекция
- •Приложение 1. Тест-задания по патологической анатомии инфекционных заболеваний
- •Приложение 2 ситуационные задачи по клинической патоморфологии инфекционных заболеваний
- •Ответы на ситуационные задачи
- •Литература
Глава 8. Инфекции, передающиеся половым путем
ХЛАМИДИОЗЫ – это группа заболеваний, вызванных микроорганизмами, относящимися к семейству Chlamidiaceae.
В настоящее время выделено четыре семейства Chlamidiaceae, включающее два патогенных для человека рода микроорганизмов – Chlamydia и Chlamydophila и три родственных хламидиям семейства микроорганизмов – Parachlamydiaceae, Simcaniacae, Waddliaceae.
Наибольшую роль в патологии человека из рода Chlamydia играет C.trachomatis, имеющая 15 сероваров. Серовары L-1, L-2, L-3 являются возбудителями пахового лимфогранулематоза; сероварианты А, Ва, В и С – возбудители трахомы. Остальные (от D до К) вызывают различные урогенитальные заболевания. Путь передачи – контактный.
Из рода Chlamydophila патогенными для людей являются C.pneumoniae, C.psittaci, C.abortus.
C.pneumoniae имеет 4 вида сероварианта – TWAR, AR, KA, CWZ – и вызывает пневмонии, ОРВИ; изучается их участие в патогенезе атеросклероза, бронхиальной астмы, саркоидоза. Путь передачи данных инфекций – воздушно-капельный.
C.abortus распространены среди животных, они колонизируют плаценту, вызывают аборты у животных, реже у женщин, работающих с овцами.
C.psittaci имеют восемь серовариантов. Они вызывают орнитоз (пситтакоз). Путь передачи – воздушно-капельный. Источник инфекции – птицы (для орнитоза – голуби, для пситтакоза – попугаи).
Хламидии и хламидофилы – строгие внутриклеточные паразиты, не способны синтезировать АТФ ( т.е. являются энергетическими паразитами). По химическому составу хламидии сходны с грам-отрицательными бактериями, имеют в своем составе ДНК и РНК. Способны персистировать, могут переходить в L-формы, неподвижны, нет спор и капсул.
Хламидии имеют уникальный двухфазный цикл развития: до проникновения в клетку они инертны – это спороподобное состояние (элементарные тельца), однако могут заражать клетки (т.е. обладают инфекциозностью). Вначале элементарные тельца адгезируются на клетках-мишенях, а затем захватываются везикулами фагоцитов. В клетке везикулы с хламидиями двигаются в перинуклеарном пространстве и формируют включения внутри цитоплазмы. Элементарные тельца превращаются в большие метаболически активные неинфекционные ретикулярные тельца. Они оттесняют ядро клетки-хозяина к периферии. Сами располагаются около ядра и окружаются оболочкой клеточного происхождения «хламидой». Затем ретикулярное тельце делится, образуются дочерние формы, которые превращаются опять в элементарные тельца и выделяются из клетки. Весь цикл развития занимает около трех суток.
Хламидии имеют белковый термолабильный антиген и термостабильный родоспецифический антиген (ЛПС). Первый находится в наружной мембране, проявляет свойства поринов и включает детерминанты, которые распознаются видо-, типо- и сероварспецифическими антителами. Родоспецифический антиген (ЛПС) состоит из специфической и групповой детерминант; последняя дает реакцию с некоторыми сальмонеллами.
Факторами патогенности хламидий являются эндотоксин и экзотоксин, термолабильные мембранные эффекторы, которые связаны с типоспецифическими хламидийными антигенами и обеспечивают адгезию на клетках-мишенях, тропизм к определенным тканям. Выделяют нейраминидазу, которая разрушает сиаловую кислоту рецепторов, реагирующих с возбудителем. В результате увеличивается проницаемость тканей. Факторами патогенности являются и метаболиты, которые угнетают функции клеток-хозяина.
Клинические проявления, патоморфологические изменения.
Урогенитальные хламидиозы по клиническим проявлениям мало отличаются от поражения урогенитального тракта другими возбудителями. Хламидиозный уретрит чаще дает симптоматику у мужчин, чем у женщин. У некоторых мужчин этот возбудитель может привести к появлению синдрома Рейтера (H.Reiter), представляющего собой триаду симптомов – уретрит, конъюнктивит и полиартрит. У женщин урогенитальные хламидиозы часто приводят к трубному бесплодию. Внутриклеточные включения хламидий лучше всего выявлять с помощью окраски флюоресцирующими антителами к этому возбудителю и после культивирования на среде Мак-Коя. Диагноз устанавливают после определения в сыворотке пациента антихламидийных антител.
Паховый (венерический) лимфогранулематоз (4-я венерическая болезнь, паховая лимфогранулема) сначала проявляется мелким эпидермальным пузырьком, возникающим на гениталиях в области входных ворот инфекции. Пузырек изъязвляется и из него начинает сочиться экссудат, богатый нейтрофилами. В дальнейшем на основе язвы развивается хроническое, часто гранулематозное воспаление. Возникает первичный комплекс. В процесс вовлекаются паховые, тазовые и ректальные лимфатические узлы. Тканевая реакция в них имеет смешанное, гранулематозное и гнойное выражение. Гнойные изменения представлены абсцессами характерной неправильной формы (звездчатые абсцессы), имеющими некротический центр и окруженными зонами грануляционной ткани. Гигантские многоядерные клетки, как правило, отсутствуют. Поражения напоминают таковые при болезни кошачьих царапин, вызываемой полиморфными грам-отрицательными микробами. На поздних стадиях в очагах пахового лимфогранулематоза гранулем значительно меньше, появляются плазмоцитарные инфильтраты, прогрессирует фиброз.
Болезнь Рейтера – системный хламидиоз. На фоне дефектов системы иммунитета одновременно развивается триада симптомов – уретрит, конъюнктивит, артрит.
Все хламидийные и хламидофильные инфекции сопровождаются вторичными иммунодефицитами, возможна персистенция возбудителя.
Лабораторная диагностика. Материал зависит от формы заболевания. При трахоме - соскоб конъюнктивы глаза, при орнитозе – мокрота, при урогенитальных поражениях - соскоб, отделяемое уретры, влагалища, моча.
Методы: цитологический, иммуноцитологический, молекулярно-биологический, бактерио-серологический, аллергический – с 3 дня выявляют ПЧЗТ.
Примечание. Хламидийная инфекция в зависимости от пути заражения может протекать в виде хламидийного коньюктивита новорожденных, орнитоза, трахомы.
Хламидийный коньюктивит новорожденных характеризуется воспалительной инфильтрацией конъюнктивы нижнего века, часто заканчивается спонтанным выздоровлением. Реже развивается доброкачественный фолликулярный конъюнктивит, который продолжается около года. Взрослые могут инфицироваться при купании в водоемах, загрязненных хламидиями.
Орнитоз впервые описан в конце XIX века у лиц, контактировавших с попугаями. Пути передачи – воздушно-капельный или воздушно-пылевой. Выражен тропизмом к тканям дыхательных путей и лимфатическим узлам. Наблюдается гибель зараженных эпителиальных клеток, местная воспалительная реакция. Возбудитель поглощается макрофагами и транспортируется в печень, селезенку. Здесь он размножается и диссеминирует с кровью в легкие и другие ткани. Формируются очаги некротического гранулематозного поражения с большим количеством геморрагий.
Трахома – это хроническое инфекционное заболевание, характеризующееся поражением клеток конъюнктивы глаза и прилегающих тканей с образованием фолликулов, рубцов, первичным поражением нервных окончаний в конъюнктиве и регионарных лимфатических узлах. Заболевание часто приводит к слепоте. Иммунитет нестойкий.
СИФИЛИС – хроническое венерическое заболевание, имеющее рецидивирующее течение с характерной периодизацией клинических симптомов, способное поражать все органы и системы (кожу, слизистые оболочки внутренних органов, кости и нервную систему), передающееся преимущественно половым путем. С момента заражения является общим инфекционным заболеванием, которое длится у нелеченных больных многие годы со сменой периодов обострения скрытыми периодами. Во время обострения на коже, слизистых оболочках, во внутренних органах наблюдаются активные проявления болезни. Для скрытого периода характерно отсутствие клинических признаков болезни, и только положительные серологические реакции крови свидетельствуют о наличии инфекционного процесса.
Этиология, эпидемиология, патогенез. Возбудитель – бледная трепонема (Treponema pallidum, бледная спирохета) – спиралевидный микроб длиной 5–20 мкм и диаметром 0,09—0,5 мкм, относится к микроаэрофильным спирохетам. Трепонемы содержат около 40% липидов, очень мало нуклеопротеидов, вследствие чего плохо окрашиваются анилиновыми красителями, грам-отрицательны, при окраске по Романовскому-Гимзе приобретают бледно-розовый цвет, поэтому и называются бледными спирохетами. Подвижны, имеют извитую форму и глубокие и поверхностные фибриллы с двух концов (периплазматические жгутики), которые располагаются между клеточной стенкой и цитоплазматической мембраной. Спор и капсул не имеют, но могут в неблагоприятных условиях образовывать цисты (трепонема скручивается и покрывается плотной оболочкой), переходить в L-форму. По типу дыхания анаэробы или микроаэрофилы; оптимум температуры роста – 35˚С. Устойчивы к низким температурам, чувствительны к высоким: разрушается уже при 55˚С. Чувствительны к растворам ртути, мышьяка, сулемы, антибиотикам.
У возбудителя выявлено 4 антигенных фракции: белковая термолабильная, полисахаридная термостабильная и 2 липидных фракции, одна из них – фосфолипидная – идентична кардиолипиновому антигену сердца быка и имеет диагностическое значение, т.к. вступает в реакцию с антителами, образовавшимися у больного при сифилисе (антигенная мимикрия). При распаде трепонемы выделяют эндотоксин.
Источник инфекции – больной сифилисом человек, особенно имеющий активные проявления свежего сифилиса на коже и слизистых оболочках. Наиболее заразны высыпания с эрозированной (влажной, мокнущей) поверхностью, в отделяемом которых содержится большое количество возбудителя.
Основной путь заражения – прямой (обычно половой) контакт с больным. Возможен также трансплацентарный, трансфузионный (после переливания крови) и контактно-бытовой (заражение через предметы домашнего обихода и т. п.). При врожденном сифилисе заражение происходит внутриутробно – через сосуды плаценты.
Входные ворота – поврежденная кожа и слизистые. Бледные трепонемы распространяются в организме по лимфатической системе, активно размножаются и периодически током крови заносятся в разные органы и ткани, что вызывает те или иные проявления заболевания. С течением времени число бледных трепонем в организме больного уменьшается, однако реакция тканей на возбудителя становится более бурной (сенсибилизация), что обусловливает изменение клинических симптомов на протяжении болезни.
Клиническая картина, патоморфологические изменения. Обычно после заражения наблюдается классическое течение сифилитической инфекции с характерной периодизацией симптомов:
– первичный серонегативный сифилис. После проникновения в ткани спирохеты размножаются, частично гибнут, выделяют антигены и эндотоксин, вызывая местное воспаление. У входных ворот (на слизистой оболочке половых органов) возникает уплотнение, инфильтрат, в центре которого образуется безболезненная язва с твердым дном со скудным серозным отделяемым – «твердый шанкр», увеличиваются и воспаляются паховые лимфоузлы, возникает лимфаденит. Эта стадия длится 5-6 недель. Из лимфоузлов возбудитель проникает в кровь и органы.
– вторичный генерализованный сифилис. Возбудители циркулируют в крови, разрушаются, выделяют эндотоксин; антигены трепонем вызывают образование антител и развитие аллергии, на коже и слизистых оболочках появляются полиморфные аллергические высыпания, развивается полилимфаденит. Это серопозитивный период, когда в организме уже обнаруживаются антитела. Он может продолжаться 2-3 года.
– третичный сифилис. В результате аллергических высыпаний во внутренних органах и нервной системе появляются деструктивные инфекционные поражения в виде гранулем (гумм), которые распадаются с образованием язв и последующим рубцеванием. Из-за общности фосфолипидов трепонем и тканей человека антитела против антигенов возбудителя вызывают аутоиммунные реакции. Без лечения этот период продолжается десятки лет и может перейти в нейросифилис, который сопровождается дегенеративными изменениями в ЦНС и приводит к глубокой инвалидности (спинная сухотка).
Возможно также длительное (многолетнее) бессимптомное течение с развитием в последующем поздних нервных и висцеральных форм заболевания, а также другие формы сифилиса: скрытый серопозитивный сифилис без клинических проявлений; врожденный сифилис, передающийся трансплацентарно плоду от матери; трансфузионный сифилис после переливания крови от инфицированных доноров.
У нелеченых больных выделяют 4 периода приобретенного сифилиса: инкубационный, первичный, вторичный и третичный.
Инкубационный период (от заражения до появления первого клинического симптома – твердого шанкра) длится в среднем 20–40 дней. Возможно как укорочение его (15–7 дней), так и удлинение (3–5 мес). Удлинение инкубационного периода может быть связано с бесконтрольным употреблением антибиотиков по поводу различных заболеваний, а также под влиянием некоторых других факторов. Несмотря на отсутствие клинических симптомов, в инкубационном периоде диссеминация бледных трепонем из места внедрения по лимфатическим, периневральным путям и гематогенно происходит довольно интенсивно и завершается формированием первичной сифиломы – твёрдого шанкра, сопутствующего лимфангита и регионарного склераденита.
Первичный период (от появления твердого шанкра до возникновения первого генерализованного высыпания) длится 6–8 нед. Типичны три симптома: твердый шанкр, регионарный лимфаденит и регионарный лимфангит. Твердый шанкр (от франц. chancre — язва) представляет собой эрозию или язву, возникающую на месте внедрения бледных трепонем (на головке полового члена, на шейке матки, вульве, стенке влагалища, реже в анусе или на слизистой оболочке губ либо полости рта, на пальцах рук у акушеров, патологоанатомов). По образному выражению французов, "при сифилисе первым наказуется то место, которым согрешили". Твердый шанкр имеет небольшие размеры (до мелкой монеты), правильные округлые или овальные очертания, пологие (блюдцеобразные) края, гладкое синюшно-красное дно со скудным отделяемым, плотно-эластический (хрящевидный) инфильтрат в основании. Микроскопически в твердом шанкре обнаруживается подострый или хронический продуктивный воспалительный процесс. В фокусе воспаления эпидермис подвергается некрозу, образуется язва. Воспалительный инфильтрат по краям язвы и в области дна состоит из лимфоидных и плазматических клеток с примесью небольшого числа нейтрофилов и эпителиоидных клеток. По мере изъязвления шанкра на поверхности дефекта с помощью специальных методов можно обнаружить спирохеты. Инфильтрат располагается главным образом вокруг мелких сосудов с признаками эндартериита, в которых наблюдается пролиферация эндотелия, вплоть до полного закрытия просвета. Среди клеток появляются прослойки зрелой соединительной ткани, происходит рубцевание и через 2 – 3 мес. на месте первичного аффекта образуется небольшой, лишенный пигмента рубчик.
Неосложненный твердый шанкр безболезнен, не сопровождается явлениями острого воспаления.
Нередки отклонения от описанной клиники: твердый шанкр может быть очень маленьким или очень крупным (карликовый и гигантский твердый шанкр), дно его может быть покрыто некротической пленкой или коркой (дифтеритический и корковый твердый шанкр). Встречаются множественные (до нескольких десятков) и болезненные (анальные и уретральные) твердые шанкры. Выделяют также атипичные твердые шанкры: индуративный отек (безболезненный плотный отек крайней плоти или половой губы), шанкр-амигдалит (плотный отек миндалины) и шанкр-панариций (симулирует гнойный панариций). Твердый шанкр может осложняться вторичной инфекцией с развитием явлений острого воспаления в его окружности. При внедрении фузоспириллезного симбиоза возникает некроз дна и краев (гангренизация твердого шанкра). Повторная гангренизация (фагеденизм), наблюдающаяся обычно у алкоголиков, приводит к значительному разрушению тканей.
Регионарный лимфаденит проявляется специфическими изменениями ближайших к твердому шанкру лимфатических узлов (чаще паховых). Он возникает через неделю после появления твердого шанкра и может быть как одно-, так и двусторонним. Лимфатические узлы увеличены неравномерно, подвижны, безболезненны, имеют плотно-эластическую консистенцию, никогда не нагнаиваются и не вскрываются, кожа над ними не изменена. Микроскопически на высоте развития первичного комплекса в узлах определяются острый или хронический неспецифический лимфаденит с гиперплазией фолликулов, плазмоцитарные инфильтраты или эпителиально-клеточные гранулемы, десквамация и пролиферация эндотелия синусов и сосудов. В дальнейшем происходит склероз лимфатического узла.
Регионарный лимфангит выявляется не всегда. Его обычно обнаруживают у мужчин (при расположении твердого шанкра на половом члене) в виде плотно-эластичного подвижного безболезненного подкожного тяжа на спинке и у корня полового члена.
Первичный период сифилиса делится на:
• первичный серонегативный сифилис, когда стандартные серологические реакции ещё отрицательны;
• первичный серопозитивный сифилис, когда стандартные серологические реакции становятся положительными, что происходит в среднем через 3–4 недели после возникновения первичной сифиломы.
При отсутствии лечения естественное течение первичного периода завершается общими лихорадочными явлениями, недомоганием, болями в костях, суставах и полиаденитом (умеренное увеличение всех групп лимфатических узлов). Эти симптомы обусловлены генерализацией инфекции и диссеминацией бледных трепонем в органы и ткани.
Вторичный период (от первого генерализованного высыпания до появления третичных сифилидов – бугорков или гумм) длится 3–4 года, характеризуется волнообразным течением, обилием и разнообразием клинических симптомов. Клинически вторичный период сифилиса характеризуется появлением генерализованного высыпания на коже и слизистых оболочках высыпаний – сифилиды вторичного периода, однако могут поражаться все органы и системы.
Различают 5 групп сифилидов вторичного периода: 1) сифилитическая розеола: бледно-розовые округлые нешелушащиеся пятна различной величины, располагающиеся обычно на туловище; 2) сифилитические папулы: синюшно-красные гладкие округлые узелки различного размера, часто изменяющие свою поверхность в зависимости от локализации – эрозивные на слизистых, омозолелые на ладонях и подошвах, вегетирующие в складках заднего прохода и половых органов – так называемые широкие кондиломы; 3) сифилитические пустулы: различной величины и глубины гнойнички на специфическом плотном основании, превращающиеся в язвы или гнойные корки; 4) сифилитическая плешивость: быстро развивающееся диффузное или мелкоочаговое поредение волос на голове без воспалительных изменений кожи; 5) сифилитическая лейкодерма: пятнистая или кружевная гипопигментация кожи шеи. Часто поражается слизистая оболочка зева, где возникают сифилитические ангины (эритематозная, папулезная и пустулезно-язвенная), отличающиеся от банальных ангин резкими границами, отсутствием островоспалительных явлений, лихорадки и болей. При высыпаниях на голосовых связках отмечается охриплость голоса.
Общими для всех сифилидов вторичного периода являются очаговый отек кожи и слизистых оболочек, разрыхление эпителиального покрова, гиперемия сосудов, воспалительная инфильтрация вокруг них, некроз стенок. Сифилиды богаты трепонемами, которые при изъязвлении папул или пустул могут попадать во внешнюю среду, поэтому вторичный период очень заразен.
В редких случаях наблюдаются диффузные периоститы и остеопериоститы с ночными болями в костях (обычно голеней), полиартритические синовиты с гидрартрозами, диффузные или очаговые гепатиты, нефриты, гастриты с неспецифической симптоматикой, полиневриты и менинговаскулярный сифилис.
Первое генерализованное высыпание, идущее на смену заживающему твердому шанкру, бывает наиболее обильным (вторичный свежий сифилис), ему сопутствует выраженный полиаденит. В увеличенных лимфатических узлах отмечаются отек, гиперплазия, очаги некроза, скопления трепонем. Тканевые изменения при вторичном сифилисе отражают реакции повышенной чувствительности немедленного типа.
Сыпь держится несколько недель (реже 2–3 мес.), затем исчезает на неопределенное время, и наступает скрытый (латентный) период заболевания. После заживления сифилидов остаются небольшие безпигментные рубчики, иногда исчезающие. Повторные эпизоды высыпаний (вторичный рецидивный сифилис) чередуются с периодами полного отсутствия проявлений (вторичный латентный сифилис). Сыпь при вторичном рецидивном сифилисе менее обильна, склонна к группировке. В первом полугодии ей сопутствует постепенно разрешающийся полиаденит. Сифилиды вторичного периода обычно не сопровождаются субъективными ощущениями.
Таким образом, вторичный период сифилиса подразделяется на:
• вторичный свежий сифилис, когда на коже и слизистых оболочках впервые появляются обильные и яркие высыпания при наличии первичного склероза или его остатков;
• вторичный скрытый сифилис – период сифилиса без активных проявлений на коже и слизистых оболочках;
• вторичный рецидивный сифилис – период последующих повторных высыпаний.
Вторичный период сифилиса без лечения может продолжаться 3–4 года. Если больной не лечится или лечится недостаточно, то спустя это время наступает третичный период сифилиса, проявляющийся в виде хронического интерстициального воспаления и образования гумм. Тканевые изменения, развивающиеся при этом, отражают реакции гиперчувствительности замедленного типа. В третичном периоде может наблюдаться поражение любого органа, но чаще всего происходит поражение кожи, слизистых оболочек и костей с образованием третичных сифилидов – бугорков и гумм.
Хроническое диффузное интерстициальное воспаление отмечается в печени, легких, стенке аорты, ткани яичек. По ходу сосудов наблюдаются клеточные инфильтраты, состоящие главным образом из лимфоидных и плазматических клеток, в сосудах наблюдается продуктивный эндартериит и лимфангит. В дальнейшем в пораженных органах развивается сифилитический цирроз, который особенно ярко выражен в печени, которая становится дольчатой, бугристой.
Бугорки обычно в большом количестве располагаются в толще кожи и имеют вид полушаровидных плотных гладких образований синюшно-красного цвета, четко отграниченных, величиной с вишневую косточку. Они не дают субъективных ощущений, располагаются обычно группами на любом участке кожи, никогда не сливаются, довольно быстро изъязвляются, а затем заживают, оставляя своеобразные пигментированные по периферии («мозаичные») рубцы. При рецидивах на рубцах новые бугорки никогда не образуются.
Сифилитическая гумма представляет собой очаг сифилитического продуктивно-некротического воспаления. Гуммы могут быть одиночными (солитарные) и множественными. Макроскопически гумма представляет собой безболезненный узел в глубине подкожной клетчатки, в костях, внутренних паренхиматозных органах и нервной системе. По мере роста он достигает величины грецкого ореха, приобретает синюшно-красный цвет, полушаровидную форму, плотно-эластическую консистенцию, а затем изъязвляется в центре с отделением скудной жидкости и образованием некротического стержня. Гомогенное содержимое гумм по консистенции варьирует от клеевидного до каучукоподобного. Микроскопически в наиболее крупных гуммах вокруг некротического центра определяется окружение из палисадных слоев макрофагов и фибробластов, снаружи от которых располагаются лимфоциты и плазматические клетки. Спирохет в гуммах мало, и их весьма трудно обнаружить.
Гуммозная язва безболезненна, имеет плотные валикообразные края и правильные очертания, по заживлении она оставляет пигментированный по периферии гладкий или стянутый к центру («звездчатый») рубец. Гуммы единичны, локализуются обычно на голенях и предплечьях (по ходу большеберцовых и лучевых костей), реже на голове. Их появление обычно провоцируется механической травмой. С течением времени некротические массы гуммы подвергаются рубцеванию, иногда обызвествляются. Гуммы могут осложняться вторичной инфекцией, иногда поражается подлежащая кость.
Поражение слизистых оболочек представлено гуммозными изменениями с аналогичным описанному течением. Чаще всего гуммы локализуются на слизистой оболочке носа и зева, реже на языке. Они часто иррадиируют в подлежащую ткань, приводя к нарушению фонации, глотания, дыхания, разрушению костной части носовой перегородки с последующим формированием седловидного носа.
Течение сифилиса в этом периоде также волнообразное, фазы активных проявлений (третичный активный сифилис) могут сменяться фазами скрытого (или третичного латентного) сифилиса.
Т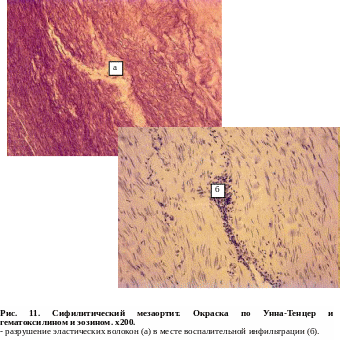 ретичный
период сифилиса может длиться многие
годы. У некоторых больных без лечения
или при его недостаточности через 10–20
лет и более после заражения могут
возникнуть поздние формы сифилиса:
ретичный
период сифилиса может длиться многие
годы. У некоторых больных без лечения
или при его недостаточности через 10–20
лет и более после заражения могут
возникнуть поздние формы сифилиса:
• нейросифилис (сифилис нервной системы) – развивается примерно у 10 % больных третичным сифилисом и может протекать в 3-х формах: менингеальная, паретическая и сухотка спинного мозга;
• висцеросифилис (сифилис внутренних органов) – мезаортит, аневризма аорты, поражение печени, желудка.
Сифилитический мезаортит представлен деструктивными изменениями в средней оболочке аорты, которые могут быть причиной образования аневризм. Изменения в аорте включают в себя также рубцовую деформацию сосуда, рубцовые сужения устьев коронарных артерий и вторичную недостаточность аортальных клапанов, обусловленную деформацией сосуда.
При менингеальной форме (хронический менингит) можно наблюдать и эндаартериит, и периваскулярные плазмоцитарные инфильтраты. Паретический нейросифилис [парез – уменьшение силы и (или) амплитуды произвольных движений, обусловленное нарушениями иннервации мышц], или прогрессирующий паралич является следствием проникновения спирохет в головной мозг. При этом происходит гибель многих клеток мозга. Затем развивается атрофия мозга с прогрессирующей утратой умственных и физических функций, изменениями психики (бред величия и др.) вплоть до тяжелого слабоумия и прогрессивного паралича. Отмечается также нейрогенное нарушение функции зрачков (синдром Аргайлла Робертсона) с сохранением аккомодации и конвергенции, но отсутствием реакции на свет; при этом имеются миоз (сужение) и деформация зрачков. Макроскопически характерно уменьшение массы головного мозга, истончение извилин, атрофия подкорковых узлов и мозжечка. Эпендима желудочков приобретает зернистый вид. При микроскопическом исследовании в ткани мозга обнаруживают воспалительные и дистрофические изменения, гибель нервных клеток с заметным уменьшением количества нейроцитов коры головного мозга, участки демиелинизации, нарушение архитектоники мозговой ткани, пролифераты микроглии и глиоз (разрастание астроцитов с избыточной продукцией глиальных волокон), причем клетки микроглии представлены палочковидными формами. В мягкой оболочке головного и спинного мозга также находят воспалительные изменения. В спинном мозге поражаются задние, реже – боковые столбы.
Спинная сухотка (Tabes dorsalis), результат повреждения задних корешков и задних рогов спинного мозга, проявляется в виде нарушений глубокой чувствительности, сенситивной атаксии (нарушениях координации движений, возникающих при поражении путей глубокой чувствительности), арефлексии, синдроме Аргайлла Робертсона, стреляющих болях в ногах и вегетативных кризах (вазомоторных расстройствах, нарушениях ритмов дыхания и сердечной деятельности). Микроскопически на поперечных срезах задние столбы спинного мозга выглядят истонченными и имеют серую окраску. Обычно дистрофический процесс начинается в верхнепоясничном отделе спинного мозга и касается вначале клиновидных пучков (пучки Бурдаха), а в дальнейшем распространяется на задние столбы; задние корешки спинного мозга истончаются. В задних столбах миелиновые оболочки распадаются, высвобождаются нейтральные жиры, которые поглощаются глиозными элементами, макрофагами и транспортируются в адвентициальные сосудистые пространства. В мягкой мозговой оболочке спинного мозга находят воспалительные изменения. В участках воспаления и в веществе спинного мозга находят бледные трепонемы.
При висцеральном сифилисе вовлекаться в процесс многие внутренние органы (сердце, сосуды, органы пищеварительной, дыхательной систем, молочные железы и др.), но наибольшее значение в клинике висцерального сифилиса имеет поражение сердечно-сосудистой системы). Поражение сердца при висцеральном сифилисе может проявляться в виде гуммозного и хронического межуточного миокардита и заканчивается развитием массивного кардиосклероза. Поражаются артерии разного калибра, возникает продуктивный артериит, заканчивающийся артериосклерозом. Чаще других артерий вовлекается аорта с развитием нередко через 15–20 лет после заражения сифилитического мезаортита. Процесс обычно возникает у мужчин в возрасте 40–60 лет, локализуется в восходящей части и дуге аорты, чаще непосредственно над клапанами. На интиме аорты появляются белесоватые бугристости с рубцовыми втяжениями, придающими аорте вид шагреневой кожи. Микроскопически в стенке аорты обнаруживается воспалительный процесс, распространяющийся со стороны vasa vasorum и адвентиции на среднюю оболочку. Здесь имеются скопления лимфоидных, плазматических клеток, гигантских клеток типа Пирогова – Лангханса, фибробластов, иногда мелкие очажки некроза. Воспалительный инфильтрат разрушает эластические волокна средней оболочки, в ней появляются поля соединительно ткани с обрывками эластических волокон. Прочность стенки аорты уменьшается, просвет ее расширяется – образуется сифилитическая аневризма аорты. Аневризма восходящей части и дуги аорты, увеличиваясь в вентральном направлении, может вызывать узуру грудины и прилежащих частей ребер, выпячиваться через кожу и перфорировать ее. Если присоединяется атеросклероз, то картина специфических изменений затушевывается. В типичных случаях изменения резко обрываются в дуге или в нисходящей части аорты; брюшная аорта поражается очень редко.
Со стенки аорты воспаление может перейти на аортальный клапан и его заслонки. Они становятся белесоватыми, деформируются вследствие грубого рубцевания, характерного для сифилиса, срастаются между собой, что приводит к сифилитическому аортальному пороку. Он нередко комбинируется с аневризмой восходящей части аорты. Возможны и другие осложнения сифилитического мезаортита. Нередко гуммозный инфильтрат переходит на венечные артерии сердца. Вокруг их устьев возникает специфическое воспаление, происходит рубцевание, что приводит к сужению устьев венечных артерий и к коронарной недостаточности.
Традиционное стадийное течение сифилитической инфекции проявляется у значительного числа больных. Однако в последние годы всё чаще стали выявляться больные с асимптомным течением болезни, которая диагностируется только серологически. Сифилис без клинических проявлений с положительными серологическими реакциями подразделяют на:
• ранний скрытый сифилис (до 2 лет после заражения);
• поздний скрытый сифилис (давность болезни более 2 лет).
Врождённый сифилис (syphilis congenita) – сифилис, при котором заражение произошло от больной матери в период внутриутробного развития. Бледные трепонемы проникают в организм плода из пораженной плаценты через пупочную вену или лимфатические щели пуповины. Поражение плода сифилисом чаще происходит в первые три года болезни матери, оно может нарушать течение беременности и приводить к поздним выкидышам, мертворождениям и преждевременным родам.
Различают ранний (до 4 лет) (syphilis congenita praecox) и поздний (после 4 лет) врожденный сифилис (syphilis congenita tarda). Ранний врожденный сифилис дополнительно подразделяют на сифилис плода, врожденный сифилис грудного (до 1 года) и раннего детского возраста (от 1 года до 4 лет). Каждый из периодов и подпериодов имеет свои клинические особенности. Кроме того, выделяют скрытый врождённый сифилис (syphilis congenita latens) - врождённый сифилис, при котором клиническая картина отсутствуют и лабораторные показатели спинномозговой жидкости в норме.
Сифилис плода, развивающийся обычно с 5-го месяца беременности, характеризуется преимущественным поражением внутренних органов и костной системы в виде их диффузной воспалительной мелкоклеточной инфильтрации с последующим разрастанием соединительной ткани, что может серьезно нарушать функции соответствующих органов и приводить к гибели плода. Чаще всего поражаются печень, селезенка и трубчатые кости.
Ранний врождённый сифилис – врождённый сифилис у плода и у детей младше 2 лет, проявляющийся сифилитической пузырчаткой, диффузной папулёзной инфильтрацией кожи, поражением слизистых оболочек, внутренних органов, костной ткани, глаз. Поздний врождённый сифилис – врождённый сифилис у детей старше 2 лет, проявляющийся триадой Гетчинсона, а также поражением кожи, внутренних органов и костей по типу третичного сифилиса.
Врожденный сифилис грудного возраста наряду с общими дистрофическими и лихорадочными симптомами, висцеральным и костными поражениями (гепатит, нефрит, пневмония, остеохондриты и др.) дает весьма обильную и разнообразную сыпь на коже и слизистых оболочках, во многом сходную с сифилидами вторичного периода (различные разновидности сифилитических розеол, папул и пустул). Отдельные сифилиды у грудных детей имеют свои особенности. Папулы даже на коже часто имеют эрозивную, мокнущую поверхность. Папулы в окружности рта сливаются в сплошные экссудативные бляшки, испещренные глубокими радиальными трещинами (диффузные инфильтрации Гохзингера), оставляющими впоследствии характерные лучистые рубцы на коже губ, шеи и подбородка (радиальные рубцы Робинсона – Фурнье)|. Эрозивные папулы на слизистой оболочке носа приводят к образованию корок, препятствующих носовому дыханию, в связи с чем ребенок не может сосать грудь («сифилитический насморк»). Крупные пустулезные высыпания на ладонях, подошвах и других участках конечностей характеризуют сифилитическую пузырчатку.
В легких развивается интерстициальная сифилитическая пневмония («белая пневмония»), ведущая к уплотнению ткани легкого с развитием в нем склеротических изменений, что определяет белесоватый вид легких на разрезе. Поражение печени имеет характер интерстициального гепатита с гибелью гепатоцитов, межуточной круглоклеточной инфильтрацией, образованием милиарных гумм и склерозом. Макроскопически печень коричневатого цвета («кремневая печень»).
В костях нарушается процесс предварительного обызвествления эпифизарного хряща и новообразования костной ткани; он сочетается с воспалительными изменениями в прилежащих к эпифизу отделах кости и сифилитическим эндопериваскулитом. В метафизарных участках трубчатых костей часто возникают остеохондриты; границы кости и хряща имеют вид не ровной, а зазубренной линии. Эти процессы развивается на границе диафиза и нижнего эпифиза бедра, в ребрах и грудине. Нередко остеохондриты трубчатых костей заканчиваются патологическими переломами (псевдопаралич Парро).
В ЦНС возникают сосудистые воспалительные изменения, поражение как вещества мозга, так и мозговых оболочек – сифилитический энцефалит и менингит.
Врожденный сифилис раннего детского возраста характеризуется преимущественным поражением кожи, слизистых оболочек и костей. Высыпания менее обильны, локализованы, сходны с таковыми при вторичном рецидивном сифилисе (часто встречаются широкие кондиломы, сифилитическая алопеция).
Поздний врожденный сифилис чаще проявляется в возрасте 5–17 лет. Его основные симптомы сходны с проявлениями третичного сифилиса. На коже и слизистых оболочках возникают бугорковые и гуммозные изменения. Однако в отличие от третичного сифилиса при позднем врожденном сифилисе имеется совокупность стойких признаков, являющихся результатом приступов сифилиса в грудном возрасте или появляющихся позднее в результате влияния сифилитической инфекции на развивающуюся костную систему и некоторые другие органы. Различают безусловные и вероятные признаки позднего врожденного сифилиса.
К безусловным (патогномоничным) признакам позднего врожденного сифилиса относится только «триада Гетчинсона»: гетчинсоновы зубы (бочкообразные верхние средние резцы с выемкой по свободному краю), паренхиматозный кератит и лабиринтная глухота. Они нередко встречаются одновременно. Изменения в органах сходны с проявлениями приобретенного сифилиса третичного периода. Отличия касаются вилочковой железы, в которой могут встречаться полости, наполненные серозной жидкостью с примесью нейтрофилов и лимфоцитов. Полости окружены валом из эпителиоидных клеток и носят название абсцессов Дюбуа.
Плацента при сифилисе роженицы изменена: ее масса увеличена (до 2250 г вместо 600 г), цвет желтовато-серый, консистенция кожистая. В ней обнаруживаются отек, клеточная инфильтрация, резкая гиперплазия ворсин, иногда в них образуются абсцессы; в стенках сосудов отмечаются воспалительные изменения.
Иммунитет. После заболевания иммунитет нестойкий, нестерильный (только при наличии антигенов спирохет). Его называют шанкерным. При повторном заражении шанкерная стадия отсутствует, развиваются сразу последующие стадии заболевания. Антитела защитной роли не играют. Они способствуют фиксации трепонем в тканях и образованию гранулем. Выражен незавершенный фагоцитоз. В процессе заболевания формируется инфекционная аллергия, сопровождаемая высыпаниями на коже, и вторичный иммунодефицит.
Диагноз сифилиса основывается на клинических проявлениях, результатах конфронтации (обследование предполагаемого источника), обязательном лабораторном исследовании (обнаружение бледных трепонем, положительные серологические реакции). Субстратом для исследований на бледные трепонемы служат отделяемое твердого шанкра, эрозивных и мокнущих папул и содержимое пустулезных сифилидов.
Серологический метод включает в себя несколько реакций:
– ускоренные отборочные реакции – реакция микропреципитации,
– стандартная реакция Вассермана (РСК),
– специфические реакции с трепонемами, в которых определяют специфические антитрепонемные антитела, в частности, реакция иммобилизации бледных трепонем (РИБТ),
– непрямая реакция иммунофлюоресценции,
– реакция иммунного прилипания (РИП),
– РПГА с трепонемным эритроцитарным диагностикумом,
– ИФА с трепонемным антигеном.
Кроме того, используют аллергический метод – вводят внутрикожно аллерген люетин. Через 24-48 часов выявляют гиперемию и инфильтрацию у лиц с ПЧЗТ.
ГОНОРЕЯ – инфекционное заболевание, вызываемое специфическим возбудителем – гонококком,– передающееся преимущественно половым путём и характеризующееся, в основном, поражением слизистых оболочек мочеполовых органов. Наблюдаются также гонококковые поражения слизистой полости рта и прямой кишки, что выявляется после орогенитальных или гомосексуальных контактов.
Этиология, патогенез. Возбудителем гонореи является Neisseria gonorrhoeae - грам-отрицательный диплококк, имеющий форму кофейных зёрен, обращённых своей вогнутой поверхностью друг к другу.
Гонококки обычно располагаются внутриклеточно в протоплазме лейкоцитов, обычно группами, но иногда можно видеть и внеклеточных гонококков. Исследования гонококков в последние годы указывают на изменения их биологических свойств (наличие капсул, фагосом, β-лактамазы, снижение чувствительности к антибиотикам, появление L-форм).
N.gonorrhoeae является факультативным внеклеточным паразитом, который связывается с эпителиальными клетками хозяина и способен преодолевать эпителиальный барьер. Связывание обеспечивается адгезинами или ресничками, которые обладают антигенными различиями, обусловленными внутригеномной рекомбинацией и рекомбинацией, наступающей вслед за встраиванием экзогенной ДНК из лизированных гонококков. Проникновение возбудителя в ткани обеспечивается набором адгезинов, называемых непрозрачными белками внешней мембраны. У этих адгезинов тоже есть генетически обусловленные антигенные различия. Капсульные полисахариды гонококков участвуют в поддержании микробной вирулентности, по мере возможности подавляя фагоцитоз в отсутствие антигонококковых антител. Патогенные нейссерии выделяют протеазу, расщепляющую IgA. Они также освобождают пептидогликаны и эндотоксины, вызывающие продукцию фактора некроза опухоли-α, который может стать причиной шока и недостаточности различных систем.
Источником заражения являются, главным образом, больные хронической гонореей, преимущественно женщины, так как у них хронический процесс протекает почти незаметно, более длительно, труднее диагностируется. Больные острой и подострой гонореей при наличии островоспалительного процесса обычно избегают половых связей. путь передачи заболевания – почти исключительно половой. Внеполовой путь заражения встречается редко (у детей при пользовании общими с больной матерью бельём, губками, полотенцами, на которых сохранился невысохший гонорейный гной). Заражение новорождённого может произойти во время родов при прохождении плода через родовые пути больной матери (гонобленнорея новорожденных).
Клиническая картина, патоморфологические изменения. Инкубационный период 3– 4 дня. По давности заболевания и выраженности клинической картины различают следующие формы гонореи:
– свежая гонорея (давность заболевания до 2-х месяцев): острая, подострая, торпидная (асимптомная). Для последней характерны незначительные клинические проявления при обнаружении у больных возбудителя.
– хроническая гонорея (давность заболевания свыше 2-х месяцев или неустановленная давность заболевания;
– латентная (типично такое состояние, когда гонококки в мазках и посевах не обнаруживаются, симптомы заболевания практически отсутствуют, а женщина является, тем не менее, явным источником заражения).
Возбудитель инфекции поражает преимущественно слизистые оболочки отделов мочеполовой системы, выстланные однослойным эпителием: уретру, выводные протоки бартолиновых желез, цервикальный канал, тело матки, маточную трубу. Процесс может распространяться на парауретральные ходы, покровный эпителий яичников, слизистую оболочку прямой кишки, брюшину малого таза. Воспаление слизистой оболочки влагалища (гонорейный кольпит) возможно при особых состояниях женского организма: в детском возрасте, во время беременности и в период менопаузы. Гематогенное распространение гонококков может иногда обусловить развитие гонококкового сепсиса и появление метастазов в различных органах. При гонококковой бактериемии поражаются суставы, глаза, плевра, эндокард, мышцы, кости, нервы. У новорожденных поражаются глаза, развиваются конъюнктивит, кератит.
острый гонорейный уретрит у мужчин сопровождается отеком наружного отверстия уретры, губки которого становятся слегка вывернуты наружу, а также слизисто-гнойным отделяемым. При отсутствии лечения антибиотиками процесс через разное время затрагивает заднюю уретру, а затем поражает придатки яичек, предстательную железу и семенные пузырьки. В этих органах возникают очаги гнойного воспаления вплоть до абсцессов. Хроническое воспаление может приводить не только к стриктурам уретры, но и мужскому бесплодию. Воспалительный экссудат содержит большое количество фибриногена, быстро выпадающего в фибрин и способствующего тем самым отграничению воспалительного процесса с образованием многочисленных спаек. Распространение инфекции происходит в основном по предсуществующим каналам.
У женщин уретрит выражен слабее покраснение и отечность в области наружного отверстия уретры и слизисто-гнойные выделения, Однако нередко он приводит к бартолиниту (воспалению большой железы преддверия влагалища C.Bartholin). Воспаление всегда начинается с выводного протока железы (каналикулит) и макроскопически выражается в гиперемии области наружных отверстий выводных протоков (гонорейные пятна). При присоединении вторичной инфекции возникает псевдоабсцесс железы с характерной клинической картиной. В воспалительный процесс часто вовлекаются парауретральные ходы. Среди немногочисленных осложнений следует назвать цервицит и сальпингит с последующей рубцовой деформацией маточных труб. Изредка гнойный сальпингит прогрессирует до тубоовариальных абсцессов и даже тазового перитонита. При хроническом уретрите отмечается только утолщение стенок уретры.
Микроскопически при всех гонококковых поражениях прослеживается выраженная экссудативная, обычно гнойная, реакция. Она сменяется формированием грануляционной ткани, плазмоцитарной инфильтрацией, а затем фиброзом.
Иммунитет к гонококку практически не вырабатывается, антитела защитной роли не играют.
Диагностика. Для диагностики заболевания используются бактериологический, бактериоскопический, серологический методы, экспресс-диагностика. Материалом для исследования служит отделяемое из уретры, цервикального канала, а при блефорее – отделяемое конъюнктивы глаза, сыворотка крови.
ТРИХОМОНИАЗ – одно из наиболее распространённых заболеваний мочеполового тракта и пока занимающее первое место среди заболеваний, передаваемых половым путём. Ежегодно на планете вновь заражаются примерно 3 млн. человек.
Этиология. Возбудителем мочеполового трихомониаза является влагалищная трихомонада – Trichomonas vaginalis (семейство Protozoa, класс жгутиковые – Flagellata).
Влагалищная трихомонада представляет собой самостоятельный вид, в естественных условиях обитает только в мочеполовом аппарате человека и не поражает животных. У женщин местом обитания Trichomonas vaginalis является влагалище, у мужчин – предстательная железа и семенные пузырьки. Мочеиспускательный канал может поражаться у обоих полов.
Трихомонада представляет собой типичный одноклеточный паразит, способный повторять рельеф эпителиальной клетки (на которой они паразитируют), проникать между клетками в узкие щели и инвагинировать в клетку хозяина. Способность урогенитальных трихомонад фиксировать на своей поверхности большие количества антитрипсина обеспечивает защиту простейших от разрушительного действия организма. На поверхности они имеют протеолитические ферменты (гиалуронидаза, амилаза, каталаза) и фибронектин – гликопротеид, способствующий прикреплению паразита к лейкоцитам, эпителиальным клеткам, эритроцитам.
Вирулентность урогенитальных трихомонад находится в прямой пропорциональной зависимости от их гемолитической активности.
Урогенитальные трихомонады бывают трёх форм: грушевидной, амебовидной и почкующейся. Тело трихомонады состоит из оболочки, протоплазмы, блефаробласта, ядра, аксостиля, четырёх жгутиков, ундулирующей мембраны, фибрилл. Размножается трихомонада путём продольного деления. Трихомонады не образуют цист или других форм устойчивости, обеспечивающих им сохранение вне человеческого организма.
Трихомонады быстро теряют жизнеспособность вне человеческого организма. Во внешней среде при высушивании трихомонады погибают за несколько секунд, губительное действие на них оказывают температура выше 40°С, прямые солнечные лучи, медленное замораживание, различные антисептики. Трихомонады хорошо растут в анаэробных условиях, оптимум роста их при рН среды 5,5–7,5 и температуре 35–37°С. Трихомонады выделяют во внешнюю среду гиалуронидазу, питаются эндосмотически. Влагалищные трихомонады – аэротолерантные анаэробы.
Путь передачи инфекции – половой; передача инфекции бытовым путём происходит редко. Это определяется способностью возбудителя сохранять жизнеспособность в течение 24 часов в моче, сперме, а также в воде и в течение нескольких часов во влажном чистом белье. Возможность инфицирования женщин трихомониазом при купаниях в реках, плавательных бассейнах, а также в банях, в настоящее время полностью отвергается.
Источник инфекции – больной трихомониазом. Чаще заболевают женщины в возрасте от 16 до 35 лет. Новорожденные, инфицированные T.vaginalis, спонтанно освобождаются от паразита в течение нескольких недель.
Урогенитальные трихомонады проникают в организм постепенно per continuitatem, через межклеточные пространства и затем в субэпителиальную соединительную ткань, а также лимфогенно через множественную сеть лимфатических щелей. Развитие у женщин трихомониаза связано с отсутствием основного компонента нормальной микрофлоры влагалища – кислотообразующей палочки Lactobacillus (описана A. Doederlein). Трихомонады, попадая в уретру, фиксируются на клетках плоского эпителия слизистой оболочки, проникают в железы мочеиспускательного канала и лакуны. Попадая в мочеполовые органы, трихомонады либо обусловливают развитие воспаления, либо не вызывают никаких изменений. Умеренно выраженная воспалительная реакция развивается при наличии большого количества паразитов. Выделяемая трихомонадами гиалуронидаза приводит к значительному разрыхлению тканей и более свободному проникновению в межклеточные пространства токсических продуктов обмена бактерий сопутствующей флоры.
клиническая картина и патоморфологические изменения. В зависимости от длительности заболевания и интенсивности реакции организма на внедрение возбудителя различают свежую (острая, подострая, торпидная (малосимптомный)), хроническую формы трихомониаза и трихомонадоносительство. Для хронической формы характерно торпидное течение и давность заболевания свыше 2-х месяцев). Во время менструации и беременности эта инфекция может обостряться. Наличие трихомонад при отсутствии объективных и субъективных симптомов заболевания позволяет поставить диагноз трихомонадоносительства.
Основными очагами поражения при урогенитальном трихомониазе являются мочеиспускательный канал у мужчин, влагалище и уретра у женщин. У большинства мужчин трихомониаз не имеет симптомов, но все же иногда сопровождается так называемым негонококковым уретритом и даже простатитом. Формирование колониеподобных сообществ T.vaginalis в уретре приводит к учащению и расстройствам мочеиспускания. Клиническая картина острого трихомониаза у женщин характеризуется симптомами вагинита, к которому могут присоединиться вестибулит, уретрит, эндоцервицит, эндометрит.
Макроскопически в пораженных слизистых оболочках определяется очаговая гиперемия, отек с образованием в некоторых случаях мелких пузырьков и папул («земляничная мукоза»). Микроскопически в слизистой оболочке и поверхностном слое подслизистой основы выявляется инфильтрация лимфоцитами, плазматическими клетками и полиморфно-ядерными лейкоцитами. Лишь иногда воспаление имеет выраженный гнойный характер наподобие гонококкового уретрита.
Осложнения при трихомонадных уретритах у мужчин встречаются часто и представлены в виде простатита, везикулита и эпидидимита, которые по клинической картине отличаются от таковых гонорейной этиологии и протекают более бурно. При длительном течении возможно образование множественных стриктур уретры.
Иммунитет. Трихомонадная инфекция не приводит к развитию выраженного иммунитета.
Диагностика. Трихомонады легче всего обнаружить в свежеприготовленном препарате «висячая капля» (капля теплого изотонического раствора хлорида натрия). Забор материала производится из разных очагов (уретра, мочевой пузырь, вульва, вагина, протоки больших вестибулярных желез). В таком препарате неокрашенный паразит хорошо заметен благодаря своей подвижности. В уретральных мазках, окрашенных по Гимзе, трихомонады выявляются гораздо труднее. Для лабораторной диагностики трихомониаза применяются также люминесцентная микроскопия, культуральные, иммунологические методы и экспресс-метод (латекс-агглютинация).
генитальный герпес
При генитальном герпесе, передающимся половым путем, мелкие сгруппированные везикулярные высыпания возникают на слизистых оболочках половых органов и коже паховых зон. До начала высыпаний нередко беспокоит чувство зуда, жжения, болезненности. Герпетические пузырьки, содержащие серозную жидкость, вскрываются, образуя медленно эпителизирующие эрозии и язвы, обрамленные воспалительным инфильтратом. Через 6-9 дней на месте высыпаний остается розовое пятно воспаления, со временем исчезающее. Герпетические высыпания могут сопровождаться явлениями регионарного лимфаденита.
По особенностям клинической картины и течения процесса генитальный герпес делят на острый (первичный), хронический (рецидивирующий) и атипичный.
Острый генитальный герпес у женщин характеризуется типичными герпетическими высыпаниями на коже больших и малых половых губ, промежности, слизистой влагалища, шейки матки, а у мужчин – на коже и слизистой полового члена, мошонки и промежности. Генитальный герпес проявляется гиперемией, отечностью, язвами различной величины, контактными кровотечениями. Длительность заболевания 8-10 дней.
Особую проблему представляет генитальный герпес у беременных женщин в связи с возможностью неонатальной инфекции.
Хронический рецидивирующий генитальный герпес отличается длительным и упорным течением, с частыми обострениями и периодами ремиссии. Эксудативные процессы выражены менее интенсивно, однако заживление язв протекает более длительно.
К атипичным формам герпеса относятся абортивная, отечная и зостериформная. Абортивная форма протекает без образования пузырьков и ограничивается появлением на коже округлых розовых воспалительных пятен с нечеткими границами. Иногда на этих местах ощущается зуд, чувство жжения, но сыпь не появляется. При папулезной форме высыпания имеют форму ярко-розовых узелков величиной с булавочную головку. Отечная форма кожного герпеса характеризуется четко очерченной отечностью тканей без образования везикул. Зостериформный кожный герпес характеризуется образованием элементов высыпаний по ходу нерва и сопровождается невралгией.
Наиболее редко встречаются, но тяжело протекают геморрагически-некротическая и эрозивно-язвенная формы заболеваний. Отличительная особенность этих форм – длительно незаживающие обширные язвенные поверхности. Такая форма герпеса имеет, как правило, внезапное острое начало -подъем температуры до 40°С, появление симптомов интоксикации, вплоть до нарушения сознания. Высыпания занимают обширные поверхности и сопровождаются зудом, жжением, лимфангитом. Высыпания превращаются в пустулы. Нередко в патологический процесс вовлекаются слизистые оболочки и внутренние органы.
Иммунитет. При первичном инфицировании образуются IgM антитела, при рецидивах – IgG и IgA. У инфицированных иммунитет является нестерильным и временным – при снижении иммунитета наступает рецидив инфекции.
Прогноз обычно благоприятный, за исключением генерализованной инфекции, при которой развиваются герпетические энцефалиты, менингоэнцефалиты, пневмонии.
Диагностика герпетической инфекции проводится на основании характерных поражений' кожи и слизистых оболочек. Для подтверждения диагноза используется выделение вируса из содержимого везикул, биологических жидкостей и секретов организма (кровь, слизь, моча, слезная жидкость, спинно-мозговая жидкость), в смывах с тканей и органов, мазках-отпечатках, соскобах. Для диагностики используются методы: цитологический метод (из соскоба из пораженного участка эпителия готовят мазок, окрашивают по Романовскому-Гимзе и обнаруживают многоядерные клетки с внутриклеточными включениями), вирусологический метод (заражают культуры клеток, выявляют ЦПД в виде гигантских многоядерных клеток с включениями, которые разрушаются), серологический метод (определяют нарастание титра АТ в парных сыворотках в ИФА. При первичной инфекции характерно появление IgM, при рецидивах – IgG, IgA), биологический метод, экспресс-метод – РИФ с моноклональными антителами против вируса.
Реакция гибридизации и НКполимеразная цепная реакция применяются для молекулярно-генетической диагностики герпеса.
