
Генетическая инженерия и безопасность
.pdf51
ходанормально раз виты х жиз нес пособ ны х рожденны х животны х б ы лни- ч тожно мал(только одно нормально с ф ормированное животное из 277 зиготс трансплантированны ми я драми – 0,4%). Больш ая ч ас ть трансплантированны х з ароды ш ей погиб лаещ е в утроб е матери, остальны е клоны имели различ ны е патологии. Так, некоторы е из новорожденны х б ы ли ненор-
мально велики, ч то, по мнению |
исс ледователей , б ы ло свя зано с опоздани- |
ем в подс адке раз виваю щ ихс я |
э мб рионов в матку с уррогатной матери. |
Кроме того, клонированная овца Д олли старела в несколько раз б ы стрее своих "нормально рожденны х" родственников. С оглас но одному из наиб о- лее вероя тны х об ъ яс нений б ы с трого старения явля ется гипотез а, ч то оно происходит в силу з апрограммированного огранич ения колич ества делений и продолжительнос ти жиз ни каждой соматич еской клетки вы сш их организ мов. П оодной из версий этоопределя етс я длиной концевы х уч астков плеч хромосом - теломерны х повторов. П ри каждом делении клетки их длина уменьш аетс я, ч то, с оответственно и определя ет ос тавш еес я раз ре- ш енное клетке время жизни. П оскольку в кач ес тве донорской при соз дании Д олли ис пользовалас ь клеткауже вз рос лого животного, которая претерпеладо этого по край ней мере несколько делений , теломеры ее хромосом к тому времени б ы ли несколько укороч ены , ч то и могло определить об щ ий б иологич еский возраст клонированного организма. Кроме того, у овеч ки Д олли б ы ло об наружено прогрессирую щ ее з аб олевание легких, и в 2003 году животное приш лос ь умертвить - в возрасте с еми лет. Э тотэкс - периментещ ераз подтверждаетизвеч ную ис тину о том, ч то природадалеконетакпрос таи однознач на, какэ томожетпоказ атьс я.
В настоя щ ее время перенос я драс оматич ес кой клетки в э нуклеированную з иготу успеш но проведеннамы ш ах я понскими уч ены ми. П роцент вы хода рожденны х мы ш ат составил 2-2,8%. Таким об разом, по край ней мере в некоторы х с луч ая х б ы ладоказанаспособ нос ть я дер соматич еских клетокоб еспеч ивать нормальноераз витиемлекопитаю щ их.
И мею тс я сооб щ ения о клонировании свиньи, коровы , кош ки. О днако, продолжительность жизни клонированны х животны х ниженормы . Так, овеч ка Д олли дотя нула лиш ь до половины с редней продолжительнос ти жизни овец(7 лет). Е еавс тралий с кий “двой ник”– М атильдапогиб лач ерез
два года после рождения , “помеш ав”своему соз дателю |
получ ить гигант- |
ский грант на создание клонированной овеч ьей отары . |
Клонированны е в |
раз лич ны х лаб оратория х мы ш и характериз ую тс я пониженной жизнеспособ ностью и также “вы держиваю т”наэтом свете не б олее половины с редней продолжительности жиз ни, их об уч аемость по сравнению с “исходны м об раз цом”оставля етжелать луч ш его (это квопросу о клонировании гениев! Какб ы вместогениев неполуч илис ь идиоты !).
Н едавними раб отами американских уч ены х доказ ано, ч то у клонированны х таким способ ом млекопитаю щ их примерно 4% генов раб отаю тненормально. С ледовательно, невоз можно ожидать точ ного копирования об раз цов. Более того, такиеаномалии в раб оте генов непременно приведут кразвитию уродств различ ного рода. Кроме всего проч его, условия разви-
52
тия в матке раз ны х матерей б удутразлич атьс я . Э то оз нач ает, ч то в разны х ус ловия х развития зароды ш аодинаковы е гены б удутраб отать по-раз ному. Т.е. вероя тность полного с ходства “клонированны х”животны х б удет не оч ень велика. Н е случ ай но “создатель”Д олли Я н В ильмут вместе с вы - даю щ имс я специалистом по эмб риологии млекопитаю щ их Я ниш ем написали в журнале “Science”з аметку “Н еклон и р уйт елю дей!”. Д ей ствительно, допустим, ч то транс плантировали раз виваю щ иес я я й цеклетки с ч ужеродны ми я драми нескольким сотня м приемны х матерей (ведь процентвы хода низ кий !), ч тоб ы получ ить хотя б ы одну единс твенную живую копию , например, видного политич ес кого дея теля . А ч то б удетс остальны ми з ароды ш ами? В едь б ольш ая ч асть погиб нетв утроб е матери или раз овьетс я в уродов, ч асть которы х, не дай Бог, родится . П редставля ете с еб е – сотни искусс твенно получ енны х ч еловеч еских уродов. И менно поэ тому известны й уч ены й , ч лен-корреспондентРАН Л .И . Короч кин рас сматриваетклонирование лю дей как преступление и вы ступает за принятие Г ос ударственной Д умой моратория наманипуля ции с ч еловеч ескими зароды ш ами.
Для чего п р оводят клон и р ован и е ж и вот н ы х? П оя вление клонов важно для испы тания новы х лекарств, условий развития младенцев. П олная с хожесть организ мов дает воз можность сравнивать влия ние на них раз лич ны х препаратов и внеш них ус ловий (например, оценивать мутагеннос ть различ ны х химич ес ких соединений ). И сс ледования по клонированию животны х имею тважное ф ундаментальное з нач ение. О ни позволя ю т вы я с нить механиз мы диф ф еренцировки клеток в процессе онтогенез а и можно ли э тим процес сом управлять. Э то путь кгенотерапии, искус ственному с озданию органов для трансплантации. Н аконец, такие исс ледования представляю тб ольш ой интерес для размножения транс генны х животны х, которы емогутутеря ть ч ужеродны й генв процессеполовогоразмножения .
П ервы й клон транс генны х сельскохозя й ственны х животны х б ы лполуч ен в 1997 г. наовцах методом пересадки я дер эмб риональны х ф иб роб - ластов, нес ущ их в своем геноме ген ф акторасверты вания крови ч еловека FIX. П ервое раз множение трансгенны х животны х с ис пользованием соматич еского клонирования б ы ловы полнено в 1999 г. накоз ах. И с пользуя ядраэ мб риональны х клеток (CFF6-1) плодакоз, трансгенны х по гену антитромб инаIII ч еловека(rhAT), б ы л получ ен клон из трех трансгенны х животны х, идентич ность которы х доказанаметодом С ауз ерн– б лоттинг.
6. М Е ДИ Ц И Н С К И Е А С ПЕ К ТЫ Г Е Н Е ТИ ЧЕ С К О Й И Н Ж Е Н Е РИ И ЧЕ ЛО В Е К А
М едицинские ас пекты генетич еской инженерии ч еловеказатрагива- ю тв ос новном 2 кругапроб лем – диагностику заб олеваний и генную терапию .
53
6.1. Г еноди агност и ка
Ген оди агн ост и ка – совокупность методов по вы явлению изменений в с труктурегенома. Г енодиагностикаотнос ительно новы й разделдиагностики, получ ивш ий раз витиев последниедес ятилетия .
У с пехи современной медицины во многом завис ятоттого, насколько рано и точ но можно диагнос тировать наиб олее рас пространенны е генетич еские и инф екционны е з аб олевания , атакже новооб разования . Н апример, проф илактику и леч ение лю б ого инф екционного заб олевания з нач и- тельно об легч аетрання я диагностикаи точ ная идентиф икация вы з вавш его его патогенного микроорганизма. Традиционно для проведения диагностич еской процедуры с нач ала вы ращ иваю т культуру потенциально патогенного микроорганизмаи лиш ь затем анализ ирую тс пектрего ф из иологи- ч еских свой ств. Х отя подоб ны е тесты вес ьмаэ ф ф ективны и об ладаю тдос - таточ но вы сокой специф ич ностью , они ч асто занимаю т много времени и я вля ю тся дорогостоя щ ими. Э то относится кидентиф икации и б актерий , и параз итич ес ких микроорганизмов. Кроме того, весьмаогранич енавоз можнос ть вы я вления тех патогенны х микроорганизмов, которы е плохо растут в культуре, либ овооб щ енеподдаю тся культивированию . К их ч ис лу относя тс я, например, об лигатны е внутриклеточ ны е параз иты Chlamydia trachomatis, которы е вы зы ваю тхламидиоз, б олезнь, передаю щ ую ся половы м путем.
Г енная инженерия ввелав практику Д Н К -диагнос тику, основанную навы я влении с пециф ич еских нуклеотидны х пос ледовательностей в б иологич ес ких об раз цах методом гиб ридиз ации (Д Н К -Д Н К, Д Н К-РН К) или полимераз ной цепной реакции (П ЦР). Г иб ридизация нуклетновы х кислот основананаприменении з ондов, использ ую щ ихся для вы я вления комплементарны х пос ледовательностей (искомого уч ас ткаД Н К). И спользование метода полимеразной цепной реакции (П ЦР) для мультипликации тестируемой Д Н К об ес печ иваетвы сокую ч увствительность этих зондов. Зонды применя ю тся : 1) в клинич еской микроб иологии для об наружения генов или нуклеотидны х пос ледовательностей , с пециф ич ны х для воз б удителя инф екционного з аб олевания , определения патогенны х микроорганиз мов – б актерий , вирус ов и простей ш их. С помощ ью этого методаможно об наружить в тканя х единич ны е б актериальны е клетки или ч астицы : хламидии, вирус гепатитаС , возб удителей туб еркулез аи др.; 2) для диагностики наследс твенны х з аб олеваний путем нахождения с пециф ич ес ких из менений в
генах. П реимущ ес тва Д Н К-диагностики – |
б ы строта (воз можность рутин- |
|
ного применения ), |
надежность, вы сокая |
ч увс твительность и с пециф ич - |
нос ть, |
|
|
Ди агност и ка |
наследст венны х заболевани й. М ногооб раз ие ф орм |
|
нас ледственны х б олезней (аих уже из вестно около 5 ты с.), из менч ивость их клинич еских проявлений и ч ас то отсутс твие радикального леч ения делаю тособ енно актуальной разраб отку точ ны х ранних (пре- и постнатальны х) методов диагностики этих б олезней , а также вы я вления нос ителей генов наследс твенны х з аб олеваний . А это прежде всего Д Н К -диагностика
54 |
|
и молекуля рная цитогенетика. Г иб ридиз ационны е з онды способ ны |
вы яв- |
ля ть раз лич ия в тестируемы х пос ледовательностя х, составляю щ их |
даже |
одиннуклеотид. П одоб ны езонды с ущ ествую тдля диагностирования б олее 1000 наследственны х заб олеваний , в том ч исле, ф енилкетонурии, с ерпо- видно-клеточ ной анемии, деф ицита α-антитрипс ина, мы ш еч ной дис тро- ф ии, б олез ни Альцгей мераи др. О дно из наиб олее продвинуты х направлений – Д Н К -диагностика и леч ение муковисцидоз а (кистозного ф иб роз а поджелудоч ной железы ) - самого ч астого наследственного заб олевания в
европеоидны х популя ция х, атакжегемоф илий . |
|
Г иб ридизационны е з онды к минисателлитам, |
метод П ЦР стали э ф - |
ф ективны м с редством в ген ом н ой дакт и лоскоп и и , |
т.е метода вы я вления |
индивидуальны х различ ий и особ енностей у лю дей |
на уровне с труктуры |
Д Н К. Г еномная дактилоскопия ш ироко применя ется в об ласти криминалистики и с удеб но-медицинской экспертиз ы (для идентиф икации лич нос ти). М етод основан на том, ч то Д Н К каждого ч еловекаоб раз ует уникальны й наб ор гиб ридиз ационны х полос. П ри этом в кач естве зондов об ы ч но ис - пользую тминисателлитны е Д Н К ч еловека, которы е не кодирую тникаких б елков и отлич аю тс я вы сокой вариаб ельностью . Анализ амплиф ицированны х с помощ ью П ЦР уч ас тков мтД Н К поз волилидентиф ицировать останки последнегорус скогоцаря Н иколая II и егосемьи.
6.2. Г енная т ерап и я
В настоящ ее время нетспособ ов для исправления деф ектов генети- ч еского материалач еловека, я вляю щ ихся прич иной развития нас ледствен-
ной |
патологии. П ри всех наследственны х заб олеваниях ш ироко применя - |
ется |
симптоматич еское леч ение, с помощ ью которого удаетс я в той или |
иной |
мере сниз ить тя жесть клинич ес кой картины б олез ни. О но вклю ч ает |
применение раз лич ны х лекарственны х препаратов, ф из иотерапевтич еское леч ение, климатолеч ение и др. П ри некоторы х нас ледственны х б олез ня х такое леч ение явля етс я единственно возможны м с пособ ом об легч ения раз -
вивш ей ся с имптоматики. |
|
Больш ие перс пективы в леч ении нас ледственны х з аб олеваний |
ч ело- |
векаоткры ваетген н ая т ер ап и я (ген от ер ап и я), воз можности которой |
сего- |
дня интенс ивно из уч аю т, экспериментируя на раз лич ны х б иологич еских моделях (клетках б актерий , растений , животны х, ч еловекаи др.) и ис пользуя в клинич еской практике.
Ген н ая т ер ап и я – это устранение генетич еских деф ектов (коррекция нас ледственны х патологий ) путем введения в соматич еские клетки полноценны х (ф ункционально активны х) генов вместо (или помимо) поврежденного (мутантного) гена. Э то с пособ ы леч ения различ ны х з аб олеваний , основанны е на введении в организ м ч ужеродной генетич еской инф ормации с целью получ ения терапевтич еского эф ф екта. Т.е. генотерапия направлена на компенс ацию наруш енны х ф ункций клетки на генетич еском уровне. П рич ем, таким способ ом возможно леч ение не только генетич е- ских, но и других неинф екционны х и инф екционны х заб олеваний (рак,
55
С П И Д и т.п.), поэ тому методы генной терапии различ ны . В с луч аегенети-
ческих б олезней генная терапия осущ ествля етс я путем введения нормального гена(трансгена, находя щ егос я в сос тавегенно-инженерной конструкции) в ту ткань, гдеэтотгендолженф ункционировать. Край нежелательно,
чтоб ы введение сопровождалось з амещ ением мутантного аллеля . О днако
технич ески э то пока не удается , и об ы ч но доб авленны е в клетки гены ф ункционирую тнаф онемутантны х в силу с воей доминантности.
Какуже отмеч алось, опис ано около5 ты с . нас ледственны х заб олеваний у ч еловека, нотолькопримернодля ты ся ч и из них най дены и картированы повреждаемы е гены . С оглас но последним данны м, деф екты в 770 генах вы з ы ваю т моногенны е з аб олевания (мы ш еч ная дистроф ия Д ю ш енна, ф енилкетонурия, хорея Г ентингтона, б олез нь Г ош е - лиз осомная б олез нь накопления , гемоф илии А и В и др.). Больш ая ч асть э тих генов клонированаи ведется поиск методов их ис пользования для генной терапии. В том случ ае, когдаб олезнь свя занас отс утс твием или малы м колич еством б елкового продукта (ч то характерно для дей с твия рецесс ивного мутантного гена) ис пользуетс я так наз ы ваемая з аместительная терапия : в клетку вводится неповрежденны й ген и создаю тся условия для его экс прес сии (наря -
ду с экс прессией мутантного гена) с целью |
получ ения достаточ ного коли- |
ч ес тва нормального б елка-продукта. П ри |
корректирую щ ей терапии де- |
ф ектны й ген реально з аменя ется в геноме нормальной копией (например, путем замены пары нуклеотидов, с вя з анной с данны м деф ектом в мутантном гене, на“правильную ”пару).
Больш инс тво |
же генетич еских б олезней я вля ю тся полигенны ми |
(атеросклероз, рак, |
артрит и др.). В этом случ ае предлагаетс я не исправ- |
ля ть генетич еские деф екты , авводить такие гены , которы е ослаб ля ю тпоследс твия этих деф ектов. Н апример, генная терапия некоторы х видов рака раз вивается по линии повы ш ения иммунного ответапо отнош ению краковы м клеткам и по линии индуцирования гиб ели раковы х клетокпутем дос - тавки к ним таких вещ еств, которы е в процесс е метаб олиз ма об разую т токсич ес кие для них молекулы . В с луч ае, когдаопухоль б ы лавы з ванасуперэкс пресс ией онкогенаK-RAS, ее дальней ш ее развитие удалось предотвратить введением в клетки ретровирусного вектора, об ес печ иваю щ его синтез антис мы с ловой РН К , комплементарной к мРН К онкогена. Белок p53 я вляетс я супрессором и подавля ет развитие опухолей , а его деф ектнос ть вы з ы ваетрак. Л еч ение таких б ольны х заклю ч аетс я в введении неповрежденного гена – супрес сора р 53 в опухолевы е клетки (деф ектны е по гену р 53), ч топриводитких гиб ели.
В ирус ны е инф екции могут рассматриватьс я как приоб ретенны е генетич еские з аб олевания , поскольку некоторы е из них (вирус Э нш тей наБарр, вирус гепатита В ) могут вы звать раз витие рака у инф ицированны х индивидуумов. Г енная терапия таких лю дей можетз аклю ч аться во введении в определенны е ткани генов с антивирус ны м эф ф ектом, ч тоб ы предотвратить их онкотрансф ормацию . В ы я вление таких тканей (клеток) определя ет ус пех генной терапии. Н апример, известно, ч то основной миш енью
56 |
я вля ю тся CD4 лимф оциты , |
для вируса иммунодеф ицита ч еловека (В И Ч ) |
|
которы е можно легко вы деля ть из организ ма, |
вводить в них нужны й ген |
(например, антис мы с ловой РН К для вирусной |
мРН К) и возвращ ать об рат- |
но. Цель манипуля ций – предотвратить в клетках развитиевируса(я вление предложеноназ ы вать внутриклеточ ны м иммунитетом).
6.3. М ет оды генной т ерап и и
П ринципиальны й с мы сл генной терапии з аклю ч ается в з амещ ении мутантного б елкаклеток ч еловека (с которы м свя з ано развитие б олезни) нас оответствую щ ий нормальны й б елок, которы й б удетсинтез ироватьс я в таких клетках.
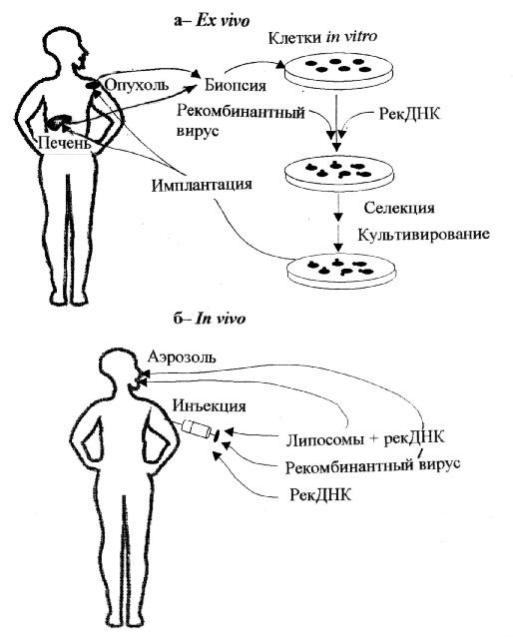
Д ля леч ения з аб олевания на молекулярном уровне применяю т два основны х подхода. 1. Г енная терапия ex vivo - введение “здорового”гена (генов) в вы деленны е из организмаб ольного и культивируемы еin vitro соматич еские клетки (т.е. в клетки-миш ени вне организма) с последую щ ей имплантацией трансф ормированны х клетокоб ратно в организ м (в органы или кровоток). 2. Г енная терапия in vivo - введение генанепосредственно в ткань или органб ольногос генетич еским деф ектом, рисунок17.
Д ля получ ения терапевтич еского эф ф ектанеоб ходимо ввес ти гены в б ольш ое ч ис ло клеток ткани-миш ени, для ч его б олее подходя тметоды ex vivo. Д ля переносагенов ч ащ е вс его использ ую тотносительно легко дос - тупны е клетки: ф иб роб ласты , лимф оциты , клетки печ ени - гепатоциты , каратиноциты , эндотелиальны е и мы ш еч ны е клетки, стволовы е клетки костного моз га. Такие клетки можно из влеч ь из организма, вклю ч ить в них нужную генную конструкцию , провес ти отб ор и культивирование in vitro трансф ормированны х клеток, аз атем вновь ввести их (реимплантировать) в организм б ольного. П ри этом у реципиентане раз виваетс я нежелательного иммунногоответа, нос амапроцедураявля етс я весьмадорогостоя щ ей и трудоемкой . О с ущ ествление э тих раб отвоз можно лиш ь в крупны х специализ ированны х центрах, треб уетб ольш их материальны х з атрати вы соких б иотехнологий . В нас тоя щ еевремя в клиниках экс периментирую тс T- лимф оцитами (остры й комб инированны й иммунодеф ицит, вы званны е де- ф ектом в генеADA), миоб ластами (мы ш еч ная дистроф ия Д ю ш енна: деф ект в гене дистроф ина), ф иб роб ластами (гемоф илия – деф екты в генах ф акто-
ров IX или VIII), клетками эпителия б ронхов (муковисцидоз – |
деф ектв ге- |
не CF-трансмемб ранного ф актора) и гепатоцитами (с емей ная |
гиперхоле- |
стеринемия – деф ектв гене рецепторалипопротеинов низкой |
плотности). |
П рич ем, “здоровы е”гены необ я з ательно вводя тв те клетки, гдеони в норме экспресс ирую тс я. Н апример, ф акторы IX и VIII синтез ирую тс я в гепатоцитах, нов леч еб ны х целях их гены вводя тв ф иб роб лас ты .
В том случ ае, когдаклетки с деф ицитны м геном нельз я из влекать и культивировать, проводя т трансгеноз in vivo (инъ екции в ткань рекД Н К, рекомб инантного вируса, липосом с Д Н К и др.). Э то оч ень перс пективны й подход, расс ч итанны й намас совое леч ение ш ироко рас прос траненны х за-
57
б олеваний , однако покаон апроб ирован только для леч ения мус ковисцидоз а.
Рис унок17. Д вес тратегии генотерапии: введениетерапевтич еских генов в клетки-миш ени внеорганиз ма(а) или внутри организма(б )
[Ры б ч ин, 1999]
Каки есущ ест вую т си ст ем ы п ер ен оса чуж ер одн ы х ген ов? Д ля этой цели испы ты ваю тся плаз мидны е и вирус ны е (ретровирусны е, аденовирус - ны е) векторы (комплекс вирусная Д Н К -ген ч еловека), инъ екция ч истой Д Н К, б омб ардировкамикропуля ми, транс ген в составе липосомного комплекса, транс плантация клетоки др.
П режде ч ем прис тупать кгенной терапии ч еловека, каждая конкретная сис тема(определенны й ген, вектор, ткань, с пособ введения векторав
58
клетки ткани и клетокв организ м) должнаб ы ть апроб ированав аналогич - ны х условия х на животны х. Э то необ ходимо для того, ч тоб ы уб едитьс я, ч то новы й ген можно вводить в клетки определенны х тканей и ч то он сохранитс я достаточ но долго, б удетэ кспрес сироваться в клетках нанеоб ходимом уровнеи неприч инитвреда(клеткеили всему организ му).
6.4. При м еры п ракт и ч ескогоп ри м енени я генной т ерап и и
П ервая успеш ная попы тка применить генотерапию в клинич еской практике б ы ла предпринята в 1990 году в С Ш А для излеч ивания у 4- летнего реб енкаиммунодеф ицита, об условленного мутацией в гене адено-
зиндез аминаз ы (ген |
ADA). П ри этом з аб олевании в крови накапливаетс я в |
||
вы сокой концентрации 2’-дезоксиаденозин, |
оказ ы ваю щ ий |
токсич еское |
|
воздей ствие на Т- |
и B-лимф оциты . П ациенты |
не перенося т контактов с |
|
лю б ой инф екцией |
из -за тотального отсутствия иммунитета. |
У б ольного |
|
реб енкаиз влекали клетки Т-лимф оциты крови, культивировали в проб ирке и при помощ и ретровирус ного вектора вводили неповрежденны й ген (нормальную копию генаADA), кодирую щ ий аденозиндез аминаз у. Реком- б инантны е клетки вы растили до об щ его колич ествав несколько миллиардов и ввели в кровь пациентке. Н апротя жении 10,5 мес я цев пациентке б ы - ло с делано 8 аутологич ны х вливаний транс ф ормированны х лимф оцитов и пос ле полугодового переры вапрограмму реинф уз ии повторя ли кажды е 3- 5- меся цев. У же после первого цикла ч ис ло Т-лимф оцитов нормализ овалос ь, концентрация ADA в циркулирую щ их клетках крови увелич илась с 1 до 20-25% нормального уровня и резко улуч ш илис ь ос новны е иммунны е характеристики. Н апротя жении б олее ч ем 6 мес после прекращ ения мас - сированны х вливаний в кровотоке пациентки устой ч иво с охраня лос ь вы - сокое ч ис ло корректированны х Т-лимф оцитов, ч то поз волило в дальней - ш ем снизить колич ество вводимы х клеток и знач ительно увелич ить промежутокмежду этими процедурами. Э то с об ы тие сч итаетс я “днем рождения генной терапии”. С 1990 г. стализдаваться журнал“Г енная терапия ”.
Х орош ие перс пективы |
с ущ ествую т |
для |
из леч ения генно- |
|
инженерны ми методами лизосомны х б олез ней |
накопления . Н а сегодня ш - |
|||
ний день поддаю тся излеч ению |
с помощ ью трансгенез ауже около 10 б о- |
|||
лезней ч еловека. |
|
|
|
|
Ря д ис следователей |
в раз ны х странах полагаю т, |
ч то с егодня наиб о- |
||
лее реальна генотерапия |
муковисцидоза. Э то тя желое, рецессивно нас ле- |
|||
дуемое з аб олевание (поражаю щ ее в с транах Е вропы одного из 2500 новорожденны х), об условленное деф ектами в гене CFTR (cystic fibrosis transmembrane regulator), которы е приводя ткпоражению э кзокринны х желез и проя вляю тс я ч ащ евсего в видеб ронхолегоч ны х изменений . В прото-
ках некоторы х органов (особ енно в легких и поджелудоч ной |
желез е) с кап- |
ливается слиз ь. О настановится источ ником б актериальной |
инф екции, ко- |
торая с трудом поддаетс я леч ению антиб иотиками. П родолжительнос ть жизни б ольны х мусковисцидозом сос тавля етв нас тоя щ ее время 25-30 лет. Н адея ться наб олее б ы стры й успех генотерапии позволя етдоступность ле-
59
гоч ной ткани для ингаля ций ; тем б олее ч то, по имею щ имся данны м, для терапевтич еского эф ф ектадостаточ но всего 5 - 10% нормально ф ункционирую щ их клеток. С реди воз можны х векторов для доставки корригирую - щ их Д Н К к клеткам и тканям-миш еня м при генотерапии муковис цидоза рас сматриваю тс я вирусны е, плазмидны е и липосомны е конструкции. Н а- пример, для леч ения легоч ной ф ормы муковис цидозалеч еб ны й ген, вклю - ч енны й в липосомы , вводя тв ды хательны е пути в ф орме аэрозоля . О днако
до клинич еских |
ис пы таний предстоит ещ е реш ить непросты е вопрос ы |
вз аимодей с твия |
генетич еских препаратов с клетками, устой ч ивости э ф - |
фектаи т.д.
Внас тоя щ еевремя успеш нораз раб аты ваю тся , в том ч ис леи в наш ей
стране, |
генно-инженерны е подходы леч ения мы ш еч ной |
дистроф ии Д ю - |
ш енна. |
М ы ш еч ная дистроф ия Д ю ш енна – заб олевание, |
сцепленное с Х - |
хромосомой , приводиткранней инвалидности и летальному исходу в воз - расте до20 летодного из кажды х 3500 новорожденны х мальч иков. П рич и- ной з аб олевания я вля ю тся мутации (преимущ ественно делеции) гена(локализ ованного в Х -хромосоме), отвеч аю щ его з ас интез дистроф ина– мы - ш еч ного б елка, играю щ его клю ч евую роль в поддержании с труктурной целостности, об ес печ ении нормальной троф ики и ф ормирования клеточ ного материалапопереч но-полосаты х мы ш ц. О тсутствие дистроф инаприводиткпрогрессирую щ ей дегенерации с келетны х и сердеч ны х мы ш ц. О дин из воз можны х подходов ктерапии этой б олез ни – вос становлениеэкспрес - сии дистроф инапутем транс плантации миоб ластов в мы ш цы . М иоб ласты я вля ю тся предш ественниками клетокс келетны х мы ш ц и расс матриваю тся какклеточ ны й векторб лагодаря своей уникальной с пособ нос ти с ливаться с мы ш еч ны ми волокнами или об разовы вать новы е. М иоб ласты легко вы - деля ю тся из мы ш еч ной ткани, хорош овы ращ иваю тся в культуре, сохраня я при э том с пособ ность кдиф ф еренцировке. С таб ильная э кс прессия введенны х (нормальны х) генов в я драх транс плантированны х миоб ластов наб лю - даетс я до6 мес. О писанположительны й терапевтич еский эф ф ект, когда21 мальч ику в возрасте 6-14 лет, имею щ им э то з аб олевание, трансплантировали в мы ш цы нормальны е миоб ласты , вз я ты е отб ратьев или отцаи вы - ращ енны е в культуре до нужного колич ества. И нъ екции производились в раз ны е мы ш цы об еих нижних конеч нос тей . Ранее неподвижны й реб енок приоб реталспособ ность двигаться !
В опы тах с мы ш ами введенны е в кровоток миоб ласты , содержащ ие генгормонарос тач еловека, вош ли в состав мы ш еч ной ткани и экс прессировали э тотген, ч то позволя етрасс матривать воз можности использования миоб ластов для доставки генов, кодирую щ ие другие гормоны , ростовы е ф акторы , противоопухолевы еагенты .
Д ругой генно-инженерны й подход леч ения мы ш еч ной дистроф ии Д ю ш енна– гендистроф инавводятнепосредс твенно в скелетны емы ш цы с мы ш еч ной дистроф ией путем инъ екции. П роцедурадолжнанеоднократно повторя ться . В екторная Д Н К попадаетв кровь и раз нос ится по вс ему организ му. В опы тах намы ш ах показано, ч то увелич ение колич ествагенадис -
60
троф инапроисходило нетолько в скелетны х мы ш цах, но такжев диаф рагме и в сердце, поражение которы х – однаиз ч асты х прич ин смерти. Г ен дис троф ина э кспрес сируется и оказ ы вает терапевтич еский э ф ф ект. У же ч ерез 20 дней пос ле б аллистич еской трансф екции попереч ны е размеры
мы ш еч ны х волокон (содержащ их дос тавленны й |
ген) приб лижалис ь кнор- |
мальны м. Д ля с ня тия с имптомов з аб олевания |
необ ходимо восстановить |
экспресс ию дистроф инапримернов 20-30% мы ш еч ны х волокнах.
П ри леч ении “с емей ной гиперхолестеринемии”, об ус ловленной мутацией б елка-рецептора, которы й в клетках печ ени должен свя зы вать ч ас - тицу, перенос я щ ую холестерин в плазме крови, у б ольного отсекаю т200-
300 г печ ени. Г епатоциты (клетки печ ени) |
культивирую т и подвергаю т |
трансф ормации в лаб ораторны х условия х. В |
них вводя тнормальны й ген, |
использ уя в кач ествевекторааденовирус или путем б омб ардировки клеток из специальной “генной пуш ки”золоты ми пульками, т.е. ч астицами з олота с нанесенны ми на них ф рагментами Д Н К, вклю ч аю щ ими леч еб ны й ген. Трансф ормированны е гепатоциты вводятб ольному об ратно в печ ень ч ерез
кровеносны е с осуды . С ходная |
процедура ос ущ ествля ется при леч ении |
врожденногоиммунодеф ицита, |
б олезни Г ош е, для некоторы х ф орм рака. В |
пос леднем случ аев клетки дос тавля етс я ген-с упресс оропухоли p-53.
В настоя щ ее время разраб аты ваетс я ря д подходов для леч ения некоторы х опухолей генно-инженерны ми методами. Так, например, для леч е- ния меланом ис пользую тинф ильтрирую щ ие опухоль лимф оциты , в которы евведенгенф акторанекрозаопухоли. П ри введении таких лимф оцитов в пораженны й организ м наб лю дается леч еб ны й э ф ф ект. И мею тс я данны ео воз можности леч ения опухолей головного моз гапри ис пользовании ретровирусны х векторов, которы е перенося тоб ладаю щ ий леч еб ны м э ф ф ектом транс ген только в деля щ иеся клетки опухоли, но не затрагиваю тпри э том
деля щ иеся клетки. |
|
|
В |
международны х документах В с емирной организ ации з дравоохра- |
|
нения , Ю |
Н Е С К О , С оветаЕ вропы и других признается э тич ески допусти- |
|
мой только генотерапия соматич еских, |
но не з ароды ш евы х клеток, по- |
|
скольку прогноз отдаленны х последс твий |
и поб оч ны х эф ф ектов пос ледней |
|
невоз можен. С вою роль должны сы грать и методы вы ращ ивания и ис следования эмб риональногоматериалавнеорганиз ма(in vitro).
В С М И 2001 г. появились сенс ационны е сооб щ ения о рождении в С Ш А первы х генетич ески модиф ицированны х детей . Г енно-инженерны й подход ис пользовандля преодоления врожденногоб есплодия женщ ин, вы - званного деф ектом митохондрий . И звестно, ч то инактивация в рез ультате мутаций митохондриальны х генов я вляется прич иной раз лич ны х патологич ес ких состоя ний – отнаследственной с лепоты и глухоты до диаб етаи старч еского слаб оумия. В се митохондриальны е заб олевания (также, каки сами митохондрии) наследую тся по материнской линии. Г енетич ески мо-
диф ицированны е дети поя вились у об реч енны х наб есплодие матерей |
б ла- |
годаря переносу в их я й цеклетки Д Н К недеф ектны х митохондрий . |
Д ля |
этого в я й цеклетку женщ ины , с традаю щ ей б ес плодием, тонч ай ш ей пипет-
